Абляция печени что это такое простыми словами
Радиочастотная абляция печени
Современные технологии медицины, связанные с лечением рака, ставят перед собой уже новые задачи – не просто лечение, но и уменьшения вредного влияния на здоровые органы и ткани за счет максимально точного воздействия на новообразование (абляция и фотодинамическая терапия). Достигнуть этого можно путем точечной доставки лекарственных средств к пораженным тканям (радио- и химиопрепараты) с дальнейшей эмболизацией сосудов.
Абляция – это способ воздействия на опухоль температурных или химических факторов (возможно их комбинирование), в результате которого происходит деструкция и гибель раковых клеток. Для максимально точного воздействия в новообразование вводится электрод, с помощью которого происходит подача тока с частотой около 400-500 Гц.
Первые клинические испытания абляции рака печени и обоснования радиочастотной термодеструкции прошли в 80-90 годах. По итогам наблюдений отмечались положительные результаты даже в случаях, которые ранее считались безнадежными. Далее была применена радиочастотная абляция (РЧА) рака легких, почек и поджелудочной железы. На начальных этапах применения методики воздействие распространялось на небольшой объем пораженной ткани, до 2 см. Сейчас аппаратура усовершенствована и позволяет за одну процедуру получить деструкцию в пределах 7 см.
Рак печени и РЧА
За 30 лет применения данной методики были сделаны выводы о ее эффективности и разработан список показаний к РЧА:
• Ранее перенесенная радикальная операция на печени при отсутствии метастазов за пределами органа;
• Выявление в печени не более 5 метастазов с посторонним источником. При наличии нейроэндокринного новообразования допустимое количество метастазов печени может возрастать;
• Размер очага до 4 см (большие размеры допускаются при наличии положительных результатов от других способов лечения, например химиотерапии);
• Не полностью излеченная опухоль ранее проводимым лечением;
• Рецидив после эффективно проведенного лечения, в том числе и РЧА;
• Возникновение «подсыпающих» (различных по времени) метастазов после резекции печени или любого другого лечения;
• Новообразования, выявленные с помощью УЗИ или КТ исследований;
• Расстояние между опухолью и магистральными сосудами и желчными протоками более 1 см.
Противопоказания к РЧА
К противопоказаниям в некоторых случаях могут относиться:
• распад опухолевой ткани;
• близкое расположение к желчному пузырю и крупным желчным протокам (может послужить причиной болевого синдрома во время проведения процедуры);
• близкое расположение к диафрагме (также может вызывать возникновение боли различной интенсивности и продолжительности);
• расстояние менее 1 см до крупных сосудов (воротная вена, печеночная артерия), нервных пучков;
• количество метастазов более 5 (за исключением случаев высокодифференцированных опухолей или имеющих продолжительный период роста).
Довольно часто схема лечения, включающая абляцию наиболее крупных узлов с последующей химио- или иммунотерапией, дает хороший результат в случае гормонально активных опухолей нейроэндокринного происхождения.
Результаты РЧА
Основным критерием эффективности локальной деструкции и отдаленной выживаемости является частота полных некрозов. Данный показатель в большой степени зависит от особенностей опухоли и ее размеров и может варьировать от 24 до 98%. Наилучшие результаты были получены при размере опухоли до 2 см. Пропорционально увеличению размера опухоли растет и риск возникновения рецидивов, но это не значит, что необходимо отступать от техники проведения абляции и будет получен отрицательный результат.
Предварительные расчеты объема ткани, подлежащей некрозу, не должны превышать допустимые для сохранения жизнедеятельности и функциональности органа. Для коррекции сроков и объема повторного лечения важную роль играет оценка изменений органа во время проведения первой процедуры, особенностей кровоснабжения органа и вероятности возникновения рецидивов.
Для подбора эффективного метода лечения вы можете обратиться за
— методы инновационной терапии;
— возможности участия в экспериментальной терапии;
— как получить квоту на бесплатное лечение в онкоцентр;
— организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.
Рак печени является крайне опасным и быстро прогрессирующим онкологическим заболеванием. По морфологической структуре опухоли печени подразделяются на 2 основные группы – первичные, то есть изначально возникшие непосредственно в самой печени, и вторичные (метастатические), которые образовались в печени из раковых клеток опухолей других органов и систем через кровоток. Первичный рак печени является довольно редким онкологическим заболеванием, на который приходится менее 1,5% (8 810) от общего числа пациентов обоего пола с первые в жизни установленным диагнозом злокачественного новообразования в России в 2018 году1. Вторичный рак печени напротив диагностируется достаточно часто и до такой степени, что практически у каждого третьего онкологического пациента вне зависимости от расположения первичной опухоли выявляются метастазы в печени, что объясняется функциональными и анатомическими особенностями органа.
Однако по разным объективным причинам хирургическое лечение доступно не более чем для 20% всех пациентов. Это связано как с тяжелой формой заболевания или неоперабельной локализацией опухоли, так и с общим состоянием здоровья пациента, не позволяющим выполнить открытую или лапароскопическую радикальную хирургическую операцию.
В настоящее время в борьбе с онкологическими заболеваниями печени активно используются минимально инвазивные технологии и методы локального лечения, позволяющие существенно продлить жизнь неоперабельным пациентам. К таким методам лечения относятся химиоэмболизация, радиоэмболизация и различные технологии локальной термической абляции. Все эти минимально инвазивные методы могут быть использованы как в качестве самостоятельного метода лечения, так и в комбинации друг с другом, в том числе с хирургией. Мировой и отечественный опыт применения методов локального лечения показывает, что в ряде случаев их эффективность не уступает результатам традиционной хирургии2 при воздействии на ранние формы первичного или метастатического рака печени.
Локальная термическая абляция опухолей не является экспериментальным методом лечения и уже не один десяток лет успешно практикуется при лечении различных онкологических заболеваний. К наиболее часто используемым технологиям локальной термической абляции опухолей печени относятся радиочастотная (РЧА) абляция, микроволновая абляция и криоабляция. Благодаря надежным отдаленным результатам лечения, подтвержденным клиническими испытаниями и исследованиям, и высокой безопасности, в 2016 году все три технологии были включены в клинические рекомендации Европейского сообщества медицинской онкологии ESMO5 по лечению метастатического колоректального рака. В 2018 году радиочастотная и микроволновая абляция были также включены в клинические рекомендации EMSO6 по лечению первичного гепатоцеллюлярного рака.
Микроволновая абляция
Микроволновая (или СВЧ) абляция относится к гипертермическим технологиям внутритканевой термоабляции опухолей, поскольку деструкция и некроз опухолевой ткани возникают под воздействием экстремально высоких температур локально создаваемых в тканях под воздействием микроволнового излучения. При микроволновой абляции в опухолевую ткань вводится специальный инструмент – антенна с излучающей секцией на кончике, которая подключена к микроволновому генератору. Если опухоль крупная или их несколько, то одновременно могут использоваться несколько таких инструментов.
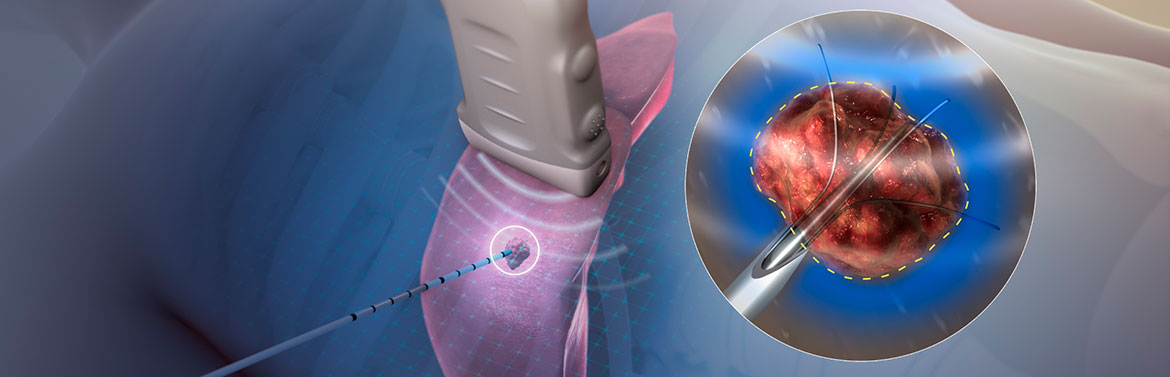
Антенна для микроволновой абляции и введение антенны в опухоль под контролем ультразвука
В большинстве случаев введение антенны в опухоль осуществляется перкутанно, то есть через кожный прокол не требующий хирургических разрезов. Процесс введения инструмента в опухоль с высокой точностью контролируется различными методами лучевой визуализации тканей, например, ультразвуком или компьютерным томографом. В ряде случаев, микроволновая абляция опухоли может также выполняться открытым или лапароскопическим доступом. Выбор доступа определяется от тактики лечения, количества и размеров опухолевых узлов, общего состояния здоровья больного и других факторов. Например, открытым или лапароскопическим доступом микроволновая абляция в большинстве случаев назначается при комбинированном лечении с хирургической резекцией или если по тем или иным причинам проведение операции чрескожным доступом не предоставляется возможным.
После установки антенны в опухоли и подтверждения точности её расположения, антенны подключаются к генератору, который по специальному кабелю (волноводу) передает электромагнитную энергию высокой частоты в диапазоне от 2 400 – 2 500 МГц в опухолевую ткань. Под воздействием электромагнитного излучения молекулы воды, находящиеся в тканях, начинают вращаться с огромной скоростью до 5 миллиардов раз в секунду. В следствие этого под воздействием силы трения кинетическая энергия преобразуется в тепловую, происходит мгновенный нагрев тканей до экстремально высоких температур, превышающих >150 ◦C, приводящих к коагуляционному некрозу и гибели раковых клеток. Таким образом формируется зона абляции, которая постепенно охватывает всю опухолевую ткань.
Генератор для микроволновой абляции. Микроволновая абляция опухоли
При микроволновой абляции высокочастотная энергия фокусируется исключительно в опухоли, здоровые ткани при этом не повреждаются. Дополнительную безопасность от термических ожогов или повреждений смежных органов и тканей обеспечивает непрерывная циркуляция охлаждающей жидкости, температура которой контролируется встроенным в антенну температурным датчиком. Поэтому если температура достигнет критических значений, то подача микроволнового излучения автоматически прервется.
После завершения процесса абляции на коже остается небольшой прокол, не требующий наложения швов. Поскольку процедуры микроволновой абляции являются малоинвазивными, а, следовательно, легко переносятся организмом, то в большинстве случаев из клиники выписывают уже на следующей день после вмешательства. В дальнейшем опухоль наблюдается. При необходимости микроволновую абляцию можно выполнить повторно.
Показания к применению микроволновой абляции
Опухоль печени до абляции. Опухоль печени после абляции – полный некроз и отсутствие признаков роста
Радиочастотная аблация (Radiofrequency ablation _ RFA)
Что такое радиочастотная аблация
Современная аппаратура позволяет точно дозировать воздействие на опухоль и направлять ток так, чтобы не повредить здоровую ткань. Процедуру проводят под контролем УЗИ или компьютерного томографа.
Согласно статистике, число рецидивов рака после радиочастотной аблации не превышает 10%, это ниже, чем после хирургического удаления опухоли (20-30%).
Доступы при РЧА
Для проведения процедуры применяют следующие доступы к опухоли:
Показания РЧА
РЧА применяют при небольших единичных опухолях или метастазах в следующих органах:
Широко используют радиочастотную аблацию при неоперабельных опухолях, или когда больному по состоянию здоровья противопоказана хирургическая операция или химиотерапевтическое лечение.
РЧА эффективна при локализации рака на слизистых оболочках полых органов в начальной стадии.
Противопоказания РЧА
Возможные осложнения РЧА
РЧА более щадящий метод по общему воздействию на организм, чем операция или химиотерапия. Тем не менее, и аблация имеет недостатки, это:
Чтобы избежать осложнений, проводить радиочастотную аблацию нужно после точного определения расположения опухоли и под строгим контролем УЗИ, КТГ или МРТ в условиях специализированного онкоцентра.
Преимущества радиочастотной аблации
Метод РЧА активно применяется для лечения рака последние несколько лет и уже успел завоевать свою достойную нишу, потому что:
Как проводят радиочастотную аблацию при опухолях печени
Посредством небольших разрезов в брюшной стенке либо при операции на брюшной полости в центр опухоли вводят зонд с электродами в форме зубцов. Местное нагревание приводит к расплавлению ткани, расположенной вокруг зонда. Процедура занимает около 10–15 минут. Весь ход процедуры РЧА контролируют с помощью ультразвукового сканирования. В идеале радиочастотную аблацию следует применять при опухолях размером менее 3 см. При более крупных опухолях может потребоваться более одного сеанса.
Радиочастотная абляция и криоабляция опухоли печени
Резекция печени является самым эффективным методом лечения ее злокачественных опухолей, однако она возможна реже, чем в одном из 3-4 случаев. При этом методы локального воздействия имеют гораздо меньше противопоказаний, а эффективность многих из них приближается к хирургической операции. К ним относятся методы термической абляции – радиочастотная абляция (РЧА) и криоабляция.
Методы локального воздействия при опухолях печени
В основе термической абляции лежит создание в опухоли температурного режима, губительного для клеток. При РЧА высокие температуры, вызывающие коагуляционный некроз ткани, достигаются прохождением высокочастотного тока. При криоабляции клеточные структуры тканей разрушаются при заморозке жидким азотом.
Методы термической абляции опухолей печени широко используются во всем мире, так как они:
Радиочастотная абляция или криоабляция опухоли печени?
Радиочастотная абляция и криоабляция дают наилучший результат, если в печени обнаруживается единственный опухолевый узел размером не более 5 см, либо не более 3-х узлов, каждый размером менее 3 см. Оба метода требуют при выполнении контроля УЗИ или КТ. Это необходимо, чтобы правильно позиционировать электрод (при РЧА) или криозонд (при криоабляции), избежать повреждения здоровых тканей, добившись максимальной ликвидации опухоли.
Радиочастотная абляция применяется с 80-х годов прошлого века. Криоабляция была рекомендована Европейским обществом медицинской онкологии (ESMO) для лечения метастатических опухолей печени только в 2016 году, поэтому ее отдаленные результаты еще недостаточно изучены, а опыт специалистов в выполнении значительно меньше, чем в проведении РЧА.
Справедливости ради стоит отметить, что криоабляция безболезненна, позволяет вымораживать очень крупные очаги размером более 10 см, визуализировать создание ледяного конгломерата на всем протяжении процедуры, минимально повреждает соединительнотканные структуры. Однако она имеет и очень существенные недостатки, отсутствующие у метода радиочастотной абляции. Прежде всего, высокий риск:
Мнение эксперта
Главный врач Европейской онкологической клиники в Москве, онколог и хирург с двадцатилетней практикой, кандидат медицинских наук Андрей Львович Пылёв не сомневается, что «радиочастотная абляция, безусловно, и во всех отношениях предпочтительнее криоабляции. РЧА – очень точный и деликатный метод, позволяющий с минимальным риском для пациента полностью удалить опухолевый узел в пределах здоровых тканей. Этого нельзя сказать о криоабляции. Чего стоят только использующиеся при этом массивные криозонды, площадь воздействия которых трудно рассчитать, а также массивные кровотечения, возникающие после размораживания ткани. Неслучайно в мировой практике криоабляция опухолей печени применяется несравнимо реже радиочастотной абляции».
Также Андрей Львович подчеркивает, что решающее значение в том, насколько эффективным и безопасным для пациента будет тот или иной метод локального воздействия при опухолях печени, имеет квалификация и опыт врача. В Европейской онкологической клинике в Москве их применяют лучшие специалисты в области эндоскопической и интервенционной хирургии, используя лучшие модели современного оборудования. Поэтому результаты их применения находятся на уровне статистических показателей ведущих клиник Европы.
Онкологическая клиника в Москве
+7(925)191-50-55
Интраоперационная радиочастотная абляция опухолей печени
Радиочастотная абляция в Европейской клинике
В Европейской клинике хирургии и онкологии, благодаря быстрому освоению самых современных методов диагностики и лечения, показатели выздоровления и выживаемости пациентов очень высокие, а количество осложнений минимально. Учреждение создано для помощи онкологическим больным, которые поступают на разных стадиях развития заболевания.
В большом ряде случаев, диагностируемая опухоль нерезектабельна и приходится изыскивать другие методы воздействия на очаг злокачественного новообразования. Но есть ситуации, когда помимо крупной опухоли есть еще несколько мелких очагов, которые затруднительно удалить традиционным методом, не разрушив полностью нормальную архитектонику органа. В этом случае хорошим подспорьем может быть радиочастотная абляция, которая позволяет выжигать очаг ткани в диаметре 1 см.
Радиочастотная абляция получила распространение не так давно, но спрос на этот метод оперативного вмешательства уже очень велик. Частота рецидивов после проведения радиочастотной абляции в несколько раз меньше, чем после традиционной хирургической резекции опухоли.
Принцип такого подхода заключается в воздействии электрического тока на радиочастоте, что соответствует 450-500 кГц. При этом происходит разогрев ткани до 100ºС и гибель живых клеток. Полезным свойством абляции служит попутная коагуляция сосудов в месте действия тока. Также формируется ишемическая зона некроза вокруг электрода, по которой можно делать разрез без опасения вызвать значительное кровотечение.
После такого термического воздействия опухолевая ткань гибнет и начинает постепенно распадаться с выделением продуктов распада в кровоток и развитием общей интоксикации. Преимущества термокоагуляции заключается в одномоментном уничтожении опухоли и окружающих ее сосудов, что предупреждает гематогенную диссеминацию раковых клеток во время операции.
Врачи Европейской клиники хирургии и онкологии давно освоили и применяют метод радиочастотной абляции как изолированно, так и в комплексе с другим оперативным и консервативным лечением. Наиболее часто этот подход используют при раке печени и метастазах в этот орган при первичной локализации в брюшной полости.
+7(925)191-50-55
г. Москва, Духовской переулок, 22б
Когда применяют радиочастотную абляцию?
Рассматриваемый метод очень хорош для удаления небольших опухолей печени, особенно если их несколько. Из-за небольшого радиуса действия радиочастот вокруг электрода удобно удалять мелкие объекты, не травмируя прилегающие ткани. При этом очаги надежно выжигаются, коагулируя окружающие сосуды. Если есть противопоказания к общей анестезии с интубацией, то радиочастотная абляция будет, кстати, поскольку в этом случае проводят спинальную анестезию или дают простой внутривенный наркоз. Этот метод противопоказан к применению, если опухоль лежит вблизи крупного кровеносного сосуда или рядом с капсулой и тем более в том случае если она проросла капсулу. Выбор радиочастотной абляции может быть определен предпочтением самого пациента, который по тем или иным причинам отказывается от традиционного хирургического вмешательства.
Нежелательно делать абляцию пациенту с кардиостимулятором, с плотным прилеганием к соседним анатомическим структурам (желчному пузырю и т.д.). При тяжелой почечной и печеночной недостаточности, циррозе также избегают подобного вмешательства. Нельзя использовать этот метод при сепсисе, нарушении свертывания крови, кровотечении, быстро рецидивирующем асците, не поддающемуся дренированию и медикаментозной терапии.
Методы радиочастотной абляции можно выполнять при различных уровнях оперативного доступа. Одной такой разновидностью служит чрескожная радиочастотная абляция, при которой разрез, по сути, не делается, а осуществляется транскутанный доступ с проникновением в толщу печеночной ткани непосредственно в опухолевый очаг. При этом в образовавшийся канал вставляют тонкий катетер, через который осуществляют все манипуляции. Такой способ доступа позволяет избежать массивных разрезов и сопутствующих им осложнений: кровотечения, абсцессов, сепсиса и других инфекционных последствий.
Иногда радиочастотную абляцию проводят с лапароскопическим доступом, когда дополнительно вводят эндоскоп в брюшную полость, что позволяет сделать ее ревизию и выявить подозрительные очаги за пределами печеночной ткани.
Также практикуют так называемую интраоперационную абляцию, при которой делается полостной разрез, который дает возможность воочию наблюдать состояние печени и окружающих тканей. При этом можно провести качественную ревизию, но частота гнойно-воспалительных и других осложнений заметно выше, чем при других способах доступа. Интраоперационную абляцию применяю в тех случаях, когда помимо большой опухоли имеется несколько мелких и удалить их традиционным хирургическим путем – будет очень травматично для печени.
Проведение интраоперационной радиочастотной абляции
Перед проведением хирургического вмешательства пациента тщательно обследуют. Необходимо знать расположение опухоли, ее размер, количество, близость к крупным сосудам, капсуле печеночной ткани, следует получить информацию о возможной инвазии в другие анатомические зоны и о наличии метастазов.
Пациент должен сдать обычный в таких случаях перечень анализов, который включает общий анализ крови и мочи, биохимическое исследование, тестирование на маркеры ВИЧ, сифилиса, вирусных гепатитов. Обязательно проверяют коагулограмму, группу крови, резус-фактор. Необходимо снять ЭКГ, получить заключение терапевта, иногда кардиолога и других специалистов по показаниям.
Накануне с пациентом беседует врач-анестезиолог, задача которого выяснить аллергический и соматический анамнез, способность пациента переносить анестезию. Последний прием пищи перед операцией – ужин предыдущего дня. За две недели прекращают прием любых препаратов, препятствующих свертыванию крови. В день операции больной чистит зубы, снимает все протезы из-за необходимости проведения интубации.
Всю операцию делают под общим наркозом. Делают хирургический разрез (продольный или Т-образный), в результате чего открывается возможность провести ревизию органа, оценить его размеры, наблюдать непосредственно опухоль, если она лежит у поверхности капсулы. Проводится хирургическое иссечение крупной опухоли и радиочастотная абляция ее краев с помощью металлических электродов, а также выжигание мелких очагов, если таковые имеются. Опухоль, лежащую в глубине, можно визуализовать и контролировать посредством метода УЗИ.
В последнее время предпочтение отдается лапароскопическому методу, который менее травматичен, имеет очень узкий разрез, что снижает вероятность инфицирования операционной раны в дальнейшем и уменьшает частоту кровотечений. Обычно, если соблюдены все правила асептики и антисептики и операция проведена безукоризненно, проблемы в послеоперационном периоде минимальны. Пациента может беспокоить болевой синдром и повышение температуры, связанной с тем, что при омертвении коагулированного участка ткани, она распадается, а продукты ее деструкции всасываются в кровь, вызывая интоксикацию и пирогенный эффект.
Болевой синдром обычно носит умеренный характер и купируется ненаркотическими анальгетиками. Подавляющее большинство осложнений при такой операции, является общим для всех полостных вмешательств. Обычно это – кровотечения сепсис, образование желчных свищей, ожоги кожи, возникновение печеночной недостаточности и другие. Но, как правило, взвесив, все плюсы и минусы, следует признать, что риск осложнений заметно ниже, чем риск самого онкозаболевания, если не предпринять оперативного вмешательства.
+7(925)191-50-55
г. Москва, Духовской переулок, 22б
+7(925)191-50-55 — европейские протоколы лечения в Москве