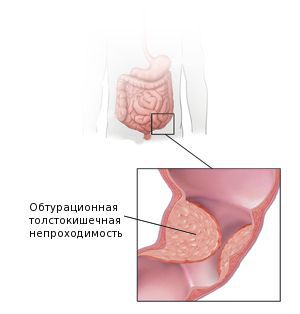
Аденокарцинома прямой кишки low grade что это значит
Высокодифференцированная аденокарцинома прямой кишки
В статье мы расскажем об особенностях строения аденокарцином, симптомах болезни и её лечении.
Что такое высокодифференцированная аденокарцинома прямой кишки
Среди случаев рака прямой кишки опухоли, происходящие из железистого эпителия аденокарциномы, встречаются в 84% случаев. И среди них высокодифференцированная аденокарцинома прямой кишки занимает третье место (около 16%) по частоте возникновения (после умереннодифференцированных и низкодифференцированных аденокарцином).
Особенности строения аденокарцином
Стенка прямой кишки состоит из многих видов клеток различного функционального значения (эпителиальные, мышечные, соединительные). Все эти ткани могут быть источником возникновения злокачественных новообразований. Но нарушения образования и функционирования клеток эпителия, выстилающего изнутри прямую кишку, дает самое большое количество случаев рака. Клетки эпителия, вырабатывающие слизь (железистые клетки) выполняют защитную и секреторную роль. Они вырабатывают “смазку”, облегчающую прохождение каловых масс в кишке, тем самым защищая ее от механических повреждений. При сбое в образовании и обновлении железистых клеток начинается их патологический (ненормальный) рост и деление. При этом работоспособность таких аномальных клеток нарушена, они продуцируют слишком большое количество слизи с измененными свойствами (вязкость, белковый состав) и непрерывно растут. Высокодифференцированные аденокарциномы самые медленнорастущие и благоприятные в отношении прогноза опухоли, так как строение клеток, их образующих, наиболее приближено к строению клеток нормального железистого эпителия (в отличие от умереннодифференцированных и низкодифференцированных аденокарцином).
Клинические проявления аденокарциномы прямой кишки
Каких-либо специфичных признаков аденокарцином прямой кишки нет.
Наиболее характерным для описываемой опухоли является медленный рост, сравнительно ограниченный участок и глубина поражения. Степень выраженности симптомов может быть незначительной, поэтому первоочередное значение приобретает профилактическое пальцевое обследование прямой кишки. Метастазы выявляются в более поздние сроки. Глубина прорастания опухоли в стенку кишки и подлежащие ткани редко бывает глубже 0,6 см. В любом случае со 100% уверенностью определить степень дифференцировки злокачественных клеток сможет только их гистологическое исследование.
Лечение высокодифференцированных аденокарцином прямой кишки
Применяемое хирургическое лечение зависит от многих факторов (площадь поражения, степень вовлечения в процесс подлежащих тканей, наличие метастазов) и проводится после проведения гистологического анализа биоптата. Аденокарциномы с высокой степенью дифференцировки клеток дают наиболее высокие показатели излечения пациентов после операций. Особенно, если лечение было начато в начальных стадиях заболевания. Так как степень поражения близлежащих тканей меньшая, чем при других раках прямой кишки, проводятся операции с резецированием участка кишки в хирургическом отделении университетской клиники МГУ. При этом высока вероятность сохранения сфинктерного аппарата.
Врачи Университетской клиники МГУ им. М.В. Ломоносова в работе
Аденокарцинома кишечника
Стадии заболевания
Если поставлена аденокарцинома кишечника, стадии определяются при помощи разных классификаций. Есть более простая – английская, но в российской практике часто используют ту классификацию, которая была установлена еще во времена СССР. Она предполагает, что аденокарцинома кишечника имеет четыре основных стадии с дополнительными вариантами:
Как и в случае с любым другим раком, аденокарцинома толстого кишечника усложняется по мере повышения стадии, поэтому с каждой ступенью требует все более серьезного лечения.
Факторы риска
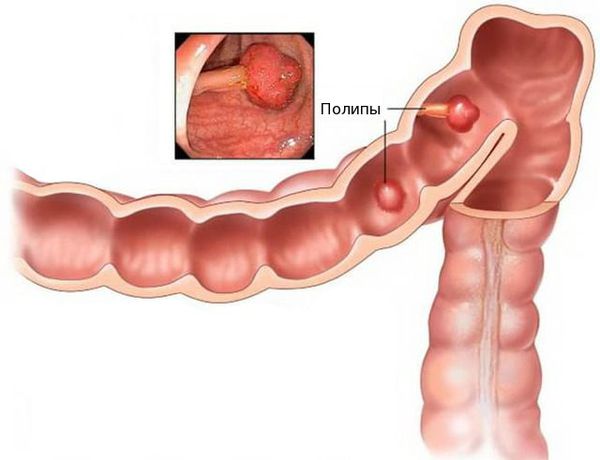
К серьезным факторам риска относятся полипы толстой кишки, из которых нередко развивается аденокарцинома кишечника. На такую трансформацию влияет множество факторов, например, площадь основания самих полипов, их количество. Наиболее опасны множественные образования.
К факторам риска в плане заболеваний относятся и хронические воспаления толстой кишки, в том числе неспецифический язвенный колит. Такое заболевание, если оно длится около 20 лет, практически в 50% случаев приводит к раку. Под угрозой находятся и люди с болезнью Крона, диффузным семейными полипозом толстой кишки, а также наследственностью – если у родственников была аденокарцинома толстого кишечника или же другие виды рака.
Также есть и другие факторы риска:
Все, перечисленное списком, в отличие от конкретных заболеваний, не становится причиной рака напрямую. Это лишь те факторы, из-за которых аденокарцинома толстого кишечника рискует развиться с большей вероятностью.
Симптомы аденокарциномы кишечника
Рак кишечника аденокарцинома не имеет специфических проявлений, поэтому у него будут общие симптомы:
Опасность заключается в том, что аденокарцинома кишечника имеет проявления, которые очень похожи, например, на геморрой. То есть без участия врача и тщательной диагностики обнаружить у себя такую проблему нельзя. Вот почему при обнаружении любых из перечисленных неспецифических симптомов необходимо обращаться к проктологу.
Диагностика
Диагностика такого рака проводится по нескольким направлениям:
Большое значение для выявления такого типа рака имеют скрининговые исследования. Регулярные дополнительные исследования рекомендуются людям старше 50 лет, а также лицам, у которых были обнаружены геморрой, разные воспалительные заболевания толстой кишки, новообразования другого характера. Также в процессе самого исследования важно дифференцировать разные заболевания и правильно поставить диагноз.
Лечение аденокарциномы кишечника
Когда поставлена аденокарцинома кишки, стадии определены и выявлены все особенности заболевания, назначается лечение.
Хирургическое вмешательство
Если поставлен диагноз аденокарцинома, операция требуется во многих ситуациях. Чаще всего, если опухоль поразила не только слизистый, но и подслизистый слой кишки. При небольших размерах опухоли ее удаление производится через задний проход. Также операция делается одномоментно или поэтапно – второй вариант характерен для тех случаев, когда вторжения метастазов довольно обширны и захватывают другие органы.
Лучевая терапия
Данный метод используют перед хирургическим вмешательством, если опухоль выросла через все слои кишки либо обнаружены метастазы. Курс лучевой терапии занимает несколько дней, после чего делается операция. Также есть ситуации, когда данный вид терапии применяется более длительное время с перерывами, а вопрос об операции решается отдельно.
Химиотерапия
Если обнаружена аденокарцинома кишечника на третьей или четвертой стадии, химиотерапия назначается в виде самостоятельного вида лечения или в комплексе с лучевой терапией. «Химию» проводят как до, так и после хирургического вмешательства. В ряде случаев требуется профилактическая химиотерапия.
Если удалена аденокарцинома кишечника, после операции нужно находиться в больнице под наблюдением врачей. А после лечения пациент еще два года наблюдается у врача каждые 6 месяцев, сдает анализы и проходит обследования. Это нужно для того, чтобы избежать рецидивов, вовремя принять необходимые меры.
Прогнозы
Вначале статьи мы уже вкратце упомянули о прогнозах в зависимости от типа рака (см. «Классификация аденокарциномы кишечника»), но немного уточним этот момент. Если поставлена аденокарцинома кишечника, прогноз зависит как от стадии, так и от особенностей, течения самого заболевания. На самых первых этапах, если рак обнаружен вовремя, процент излечения может достигать 97-99% случаев. Ко второй стадии этот показатель снижается примерно на 7%, а начиная с третьей стадии риски сильно возрастают – излечение происходит в 60-70% случаев.
Однако важно помнить: какой бы ни была стадия, всегда есть индивидуальный фактор. При наличии диагноза аденокарцинома кишечника, прогноз может быть не самым благоприятным, а исход более удачным. Очень многое в лечении зависит и от настроя самого пациента, от его окружения.
Профилактические мероприятия
Профилактика в данном случае максимально простая: чтобы избежать проблем с кишечником, приводящих к раку, нужно правильно питаться, соблюдать питьевой режим, обязательно двигаться и следить за весом. Если среди родственников кто-то болел раком, проконсультируйтесь у специалистов. При отсутствии такой наследственности не забывайте о скрининговых исследованиях, начиная с 50 лет.
Бережно и внимательно относиться к своему здоровью, а также вести здоровый образ жизни – лучшая профилактика. Это не гарантирует того, что аденокарцинома никогда не разовьется, но риски такой проблемы будут намного меньше.
Как записаться к специалисту в онкоцентр «София»
Записаться на прием к специалистам онкологического центра «София» можно на сайте – пациенту необходимо внести в соответствующие поля свое имя, номер телефона и адрес электронной почты. Администраторы клиники совершат ответный звонок после обработки полученных данных.
Специалисты информационной службы клиники готовы ответить на любые вопросы и забронировать удобную для пациентов дату визита по телефону +7(495)995-00-34.
Онкологический центр «София» расположен на территории центрального административного округа Москвы по адресу 2-й Тверской-Ямской переулок, дом 10. Удобная локация позволит пациентам быстро добраться до клиники от станций метро «Маяковская», «Новослободская», «Тверская», «Чеховская» и «Белорусская».
Что такое аденокарцинома кишки? Причины возникновения, диагностику и методы лечения разберем в статье доктора Мешечкина В. Г., онколога со стажем в 8 лет.
Определение болезни. Причины заболевания
Аденокарцинома толстой кишки — это самая распространённая форма рака прямой кишки, опухоль развивается в толстой кишке и может метастазировать, как и большинство злокачественных новообразований.
Распространённость аденокарциномы толстой кишки
Факторы риска
Основной фактор риска аденокарциномы толстой кишки — возраст старше 65 лет. Риск развития аденокарциномы толстой кишки также возрастает при наличии некоторых наследственных синдромов:
Благоприятным фоном для злокачественного перерождения клеток являются единичные или множественные полипы толстой кишки. Высокий риск перерождения в раковую опухоль имеют аденоматозные полипы. Отказ от их удаления может привести к развитию аденокарциномы.
Хронические воспалительные заболевания толстой кишки, такие как неспецифический язвенный колит и болезнь Крона, также повышают риск развития аденокарциномы.
К дополнительным факторам риска относят:
Симптомы аденокарциномы кишки
Клинические проявления аденокарциномы толстой кишки зависят от расположения опухоли, её типа, темпа роста и наличия сопутствующей патологии. Ранние формы рака являются случайной находкой, так как могут никак себя не проявлять. Их выявляют при эндоскопическом исследовании кишечника по поводу других заболеваний (например, колита, дивертикулита, холецистита, гастрита и др.) или при полостных или гинекологических операциях — аппендэктомии, миомэктомии и кесаревом сечении.
Наиболее частые симптомы аденокарциномы толстой кишки:
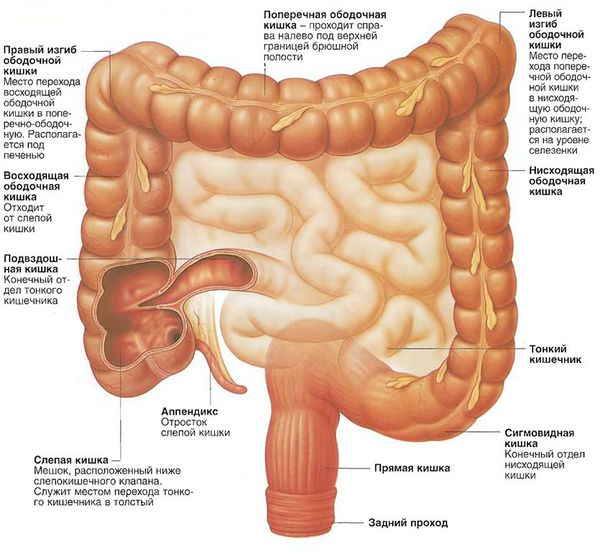
Опухоли левого фланка (сигмовидной и прямой кишки, селезёночного угла, нисходящего отдела) чаще манифестируют с запоров, примеси прозрачной или розоватой слизи и тёмной крови в кале, болезненных позывов, отдающих в промежность.
Поиск причины анемии невыясненной этиологии часто приводит к обнаружению рака правой половины толстой кишки.
Патогенез аденокарциномы кишки
Аденокарцинома — это злокачественная опухоль, возникающая из железистых клеток и способная образовывать метастазы (вторичные очаги опухолевого роста). Чаще всего заболевание развивается на фоне длительно существующих полипов, или разрастаний слизистой.
При хроническом повреждении полипов плотными каловыми массами и воспалении развивается дисплазия эпителия (нарушение деления и дифференцировки клеток), переходящая в рак. У кого-то этот процесс может занять десятки лет, у других развивается за два-три года.
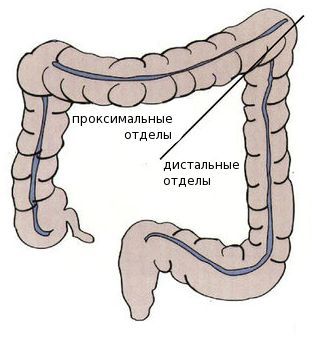
Среди пациентов с раком проксимальных отделов толстой кишки преобладают женщины — вероятно, это связано с наличием гормональных рецепторов эстрогенов в этих отделах. Дистальный рак толстой кишки более характерен для мужчин.
Классификация и стадии развития аденокарциномы кишки
Виды аденокарциномы толстой кишки в зависимости от локализации:
Согласно последней классификации ВОЗ, гистологически выделяют две степени злокачественности аденокарциномы толстой кишки, опираясь на долю железистых структур в составе опухоли: высокую и низкую.
Стадирование новообразований толстой кишки по системе TNM-8 (2017 г.) представлено схемой:
Исходя из этих данных, опухоли присваивают определенную стадию, и далее она уже не меняется. Дальнейшее распространение процесса обозначается как прогрессирование.
Осложнения аденокарциномы кишки
Также среди частых причин осложнений выделяют перфорацию и кровотечение из повреждённой опухоли. Это может явиться первым симптомом заболевания. Часто таких пациентов экстренно оперируют в условиях многопрофильного стационара, а не специализированного учреждения, и только при обследовании органов брюшной полости становится понятна причина перфорации.
Диагностика аденокарциномы кишки
Сбор анамнеза
Помимо описанных выше жалоб, с которыми первично обращаются пациенты, важны данные анамнеза. На первичном осмотре терапевту или онкологу следует отметить наличие наследственных синдромов, ассоциированных с раком толстой кишки, и хронических неспецифических воспалительных процессов толстой кишки, например неспецифического язвенного колита или болезни Крона.
Физикальное обследование
При физикальном обследовании, помимо общего осмотра и пальпации брюшной полости, обязательно проведение ректального пальцевого исследования, выявляющего изменения в области прямой кишки. Это один из самых простых диагностических приёмов, не требующий дополнительной подготовки и оборудования.
Лабораторная диагностика
Лабораторная диагностика включает:
Это анализы необходимы для исключения возможной сопутствующей патологии.
Биопсия
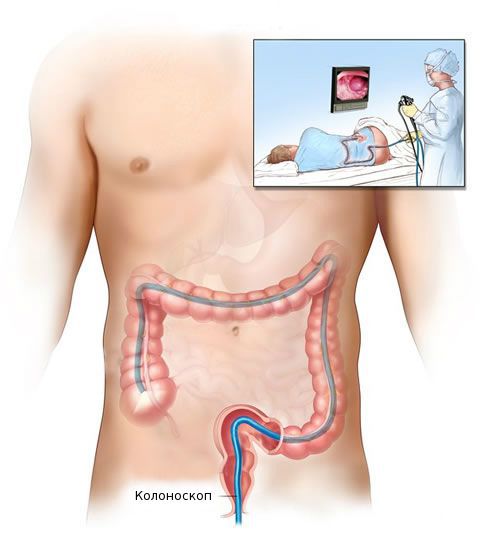
После общеклинического обследования проводят уточняющее исследование (биопсию) для определения гистологической структуры опухоли. Чаще всего биопсия выполняется во время колоноскопии — процедуры, при которой врач с помощи эндоскопа осматривает внутреннюю поверхность толстой кишки.
Ирригоскопия и КТ-колонография
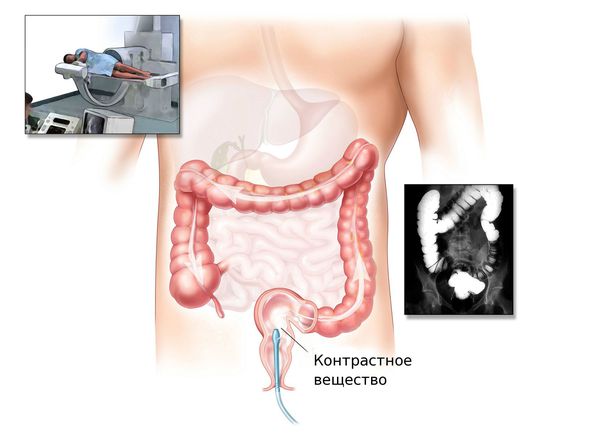
При невозможности проведения колоноскопии врач может назначить ирригоскопию или КТ-колонографию.
Ирригоскопия — это рентгенологический метод обследования толстого кишечника с помощью контрастного вещества, вводимого через прямую кишку.
КТ-колонография — разновидность компьютерной томографии, проводимая при помощи компьютерного томографа.
Компьютерная томография (КТ)
КТ органов грудной клетки и брюшной полости с контрастом — стандарт обследования при раке ободочной кишки. Компьютерную томографию проводят для исключения метастазов в лёгких, лимфоузлах средостения, брюшной полости, канцероматоза (переноса раковых клеток из первичного очага), асцита (скопления жидкости в брюшной полости) и вторичного поражения печени.
Магнитно-резонансная томография (МРТ)
МРТ органов брюшной полости с внутривенным контрастированием применяют для планирования операции на печени при её вторичном поражении.
Для точной оценки размеров опухоли перед операцией и правильного стадирования по TNM проводится МРТ малого таза c применением контраста.
Дополнительно, при наличии болевого синдрома или изменений по КТ, проводится остеосцинтиграфия (ОСГ) — исследование состояния костей скелета.
При подозрении на вторичное поражение головного мозга (исходя из жалоб, осмотра и анамнеза) назначается МРТ головного мозга с внутривенным контрастированием.
Позитронно-эмиссионная томография, совмещённая с компьютерной томографией (ПЭТ/КТ)
ПЭТ-КТ не применяется как рутинный метод при первичной диагностике. Обследование проводят при подозрении на вторичные изменения по данным КТ или МРТ для получения дополнительных данных.
Лечение аденокарциномы кишки
Выбор метода лечения аденокарциномы толстой кишки обусловлен стадией онкологического процесса и наличием или отсутствием соматической патологии.
0-I стадия
На ранних стадиях рака ободочной кишки проводятся органосохраняющие операции, например эндоскопическую резекцию слизистой с удалением в подслизистом слое. При поражении краёв резекции, сосудистой, лимфатической или периневральной инвазии (проникновении раковых клеток в периневрий — слои соединительной ткани, образующие оболочку вокруг пучков нервных волокон), как факторах неблагоприятного прогноза, рекомендуется проведение расширенной операции — повторной резекции краёв.
II–III стадия
При резектабельном (c возможностью удаления) локализованном и местнораспространённом раке ободочной кишки II–III стадий на первом этапе предпочтительно оперативное лечение. Объём хирургического вмешательства определяется индивидуально.
Химиотерапия проводится при поражении лимфатических узлов, прорастании опухолью серозной оболочки и соседних органов, наличии факторов риска.
При распространённом раке ободочной кишки с резектабельными или потенциально резектабельными синхронными метастазами в печени или лёгких выполняют R0-резекцию (в пределах здоровых тканей).
Радиочастотная абляция и стереотаксическая лучевая терапия применяются как дополнительные методы к резекции печени и как самостоятельные методы лечения. Действие радиочастотной абляции основано на нагревании с помощью радиоволн поражённых тканей до высоких температур (90–100 °С).
Стереотаксическая лучевая терапия — это один из видов радиохирургии, который состоит в применении высокоточного излучения, воздействующего на опухоли.
При резектабельных очагах рекомендуется их одномоментное хирургическое удаление.
На послеоперационном этапе при резектабельных метастатических очагах показано проведение адъювантной (следующей за операцией) химиотерапии. Также возможно проведение дооперационной химиотерапии до шести циклов, удаление метастазов и первичной опухоли с дальнейшим продолжением химиотерапии до достижения шестимесячной суммарной продолжительности лечения.
IV стадия
Основная цель лечения на IV стадии заболевания — перевод при помощи химиотерапии нерезектабельных метастазов в резектабельные. Хороший эффект даёт добавление к основному лечению таргетной терапии ( целенаправленно воздействующей на специфические мишени в опухолевых клетках) и иммунотерапии.
При проведении нерадикальной резекции возможно продолжение терапии предоперационной комбинацией химиопрепаратов и моноклональных антител (препаратов, избирательно воздействующих на определённую молекулу, от которой зависит развитие болезни ) до достижения суммарной шестимесячной продолжительности лечения.
При генерализованном раке ободочной кишки с нерезектабельными метастазами применяют комбинацию химиопрепаратов. Возможно добавление таргетных препаратов. Цель лечения — максимально долго контролировать развитие заболевания при сохранении качества жизни.
При проведении химиотерапии каждые 1,5-2 месяца оценивают резектабельность опухоли (по данным КТ, МРТ). При преобладании метастатического поражения печени проводят:
Прогноз. Профилактика
Меры профилактики:
Аденокарцинома прямой кишки low grade что это значит
ФГБОУВО «Московский государственный университет им. М.В. Ломоносова», Москва, Россия
ГУНУ «Факультет фундаментальной медицины МГУ им. М.В. Ломоносова»; ГБОУ ДПО «Российская медицинская академия последипломного образования», Москва
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава РФ; ГБОУ ДПО «Российская медицинская академия последипломного образования», Москва
Новое в классификации злокачественных эпителиальных опухолей толстой кишки. (ВОЗ, 2019, 5-е издание)
Журнал: Архив патологии. 2020;82(3): 38-46
Олейникова Н. А., Мальков П. Г., Данилова Н. В. Новое в классификации злокачественных эпителиальных опухолей толстой кишки. (ВОЗ, 2019, 5-е издание). Архив патологии. 2020;82(3):38-46.
Oleynikova N А, Mal’kov P G, Danilova N V. Changes in the classification of malignant colon epithelial neoplasms. (WHO, 2019, 5th edition). Arkhiv Patologii. 2020;82(3):38-46.
https://doi.org/10.17116/patol20208203138
ФГБОУВО «Московский государственный университет им. М.В. Ломоносова», Москва, Россия
В настоящее время классификация аденокарцином по сравнению с 2010 г. изменилась частично, исключены крибриформная комедоаденокарцинома (код МКБ-О: 8201/3), веретеноклеточная карцинома (8032/3), плоскоклеточная карцинома (8070/3), добавлены карцинома с саркоматозным компонентом (8033/3), дискогезивная (poorly cohesive) карцинома (8490/3) и аденомоподобная карцинома (8262/3). В качестве важных гистологических характеристик в Заключении необходимо указывать наличие лимфатической инвазии, интра- и экстрамуральной сосудистой инвазии, периневральной инвазии, степени злокачественности, «опухолевого почкования» (tumor budding) и характер иммунного окружения. В 5-м издании классификации добавлен большой раздел, посвященный молекулярной диагностике и молекулярным прогностическим факторам колоректального рака. Найдены соответствия между двумя различными классификациями, основанными на двух различных подходах: геномном (по ДНК) и транскриптомном (по РНК). В соответствии с геномной классификацией выделены две большие группы колоректального рака: гипермутационные и негипермутационные, которые соответствуют молекулярным путям с развитием микросателлитной и хромосомной нестабильности соответственно. Раздел нейроэндокринных опухолей существенных изменений не претерпел. Не рекомендовано использовать термин «карциноид» для обозначения нейроэндокринной опухоли G1, т.е. термин «карциноид» исключен.
ФГБОУВО «Московский государственный университет им. М.В. Ломоносова», Москва, Россия
ГУНУ «Факультет фундаментальной медицины МГУ им. М.В. Ломоносова»; ГБОУ ДПО «Российская медицинская академия последипломного образования», Москва
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава РФ; ГБОУ ДПО «Российская медицинская академия последипломного образования», Москва
Новая классификация опухолей толстой и прямой кишки WHO 2019, 5-е издание [1] выглядит довольно стройной, чрезвычайно краткой и включает только эпителиальные новообразования, разделенные на две группы: доброкачественные и злокачественные новообразования. Наша публикация посвящена классификации злокачественных новообразований (табл. 1). Ранее входившие в классификацию мезенхимальные опухоли и лимфомы из классификации исключены и вынесены в отдельный раздел.

Примечание. *NOS — not otherwise specified (без дополнительных уточнений).
Частота возникновения колоректального рака стремительно растет и регистрируется преимущественно в странах с высоким доходом, причем отмечается тенденция к развитию заболевания в молодом возрасте. В 2018 г. заболеваемость колоректальным раком занимала 2 место в мире у женщин и 3 место у мужчин [1].
Аденокарциномы
Морфологическая классификация аденокарцином по сравнению с 2010 г. изменилась частично, исключены крибриформная комедоаденокарцинома (8201/3), веретеноклеточная карцинома (8032/3), плоскоклеточная карцинома (8070/3), добавлены карцинома с саркоматозным компонентом (8033/3), дискогезивная (poorly cohesive) карцинома (8490/3) и аденомоподобная карцинома (8262/3).
Карцинома с саркоматозным компонентом. Характеризуется недифференцированными фокусами с наличием саркомоподобных признаков, таких как веретеноклеточный компонент или рабдоидные фигуры. Прогноз крайне неблагоприятный. Как правило, опухоли имеют большой размер, рабдоидные клетки с яркими внутрицитоплазматическими рабдоидными тельцами. Опухолевые клетки часто разрознены и заключены в миксоидный матрикс. Могут встречаться плеоморфные гигантские или веретеновидные клетки наряду с фокусами железистой дифференцировки. Характерно отсутствие ядерного окрашивания при иммуногистохимическом определении SMARCB1 (INI1).
Аденомоподобная карцинома. Ранее называлась «ворсинчатая», или «инвазивная папиллярная аденокарцинома», представляет собой инвазивную аденокарциному, в которой более 50% «инвазивных зон» (дословный перевод) похожи на ворсинчатые структуры аденомы с дисплазией low-grade. Характеризуется высокой частотой мутаций в гене KRAS и благоприятным прогнозом. Диагноз с помощью биопсии труден.
Зубчатая аденокарцинома. Критерии постановки диагноза не изменились. Частота встречаемости 10—15% от всех колоректальных раков. Морфология опухоли должна быть похожа на зубчатые образования с наличием зубчатого просвета, возможен муцинозный компонент. Опухолевые клетки имеют низкое ядерно-цитоплазматическое соотношение. Критерии этого подтипа весьма условны, поскольку при различных степенях дифференцировки и выраженности клеточной атипии оценить наличие зубчатого просвета и его «истинность» крайне затруднительно. Однако по сравнению с предыдущим изданием принципиально новых диагностических критериев или маркеров не добавлено.
Дискогезивная (poorly cohesive) аденокарцинома. Описание и критерии постановки не приведены, несмотря на ее наличие в классификации. Учитывая общий с перстневидно-клеточной аденокарциномой код МКБ-О (8490/3), отсутствие критериев нельзя считать критичным, однако с практической точки зрения неясно, в каких случаях пользоваться данной рубрикой. Такие опухоли ранее описаны при раке желудка, для колоректального рака этот подтип введен впервые. Смеем предположить, что критерии для толстой кишки те же, что и для желудка: изолированные или сгруппированные в мелкие кластеры опухолевые клетки, которые могут быть не только перстневидными, но и напоминать гистиоциты, лимфоциты, плеоморфные с резко атипичным ядром или ярко выраженной эозинофильной цитоплазмой и выраженной стромальной реакцией.
Аденоплоскоклеточная карцинома по-прежнему осталась в классификации и описана как редкий (частота менее 0,1%) тип, сочетающий в себе признаки аденокарциномы и плоскоклеточной карциномы (рис. 1).

Окраска гематоксилином и эозином, об. ×20.
Авторы по-прежнему настоятельно рекомендуют оценивать степень злокачественности по двухступенчатой шкале — low- и high grade по самому злокачественному компоненту, а не по степени дифференцировки опухоли (G1, G2, G3). Основные востребованные критерии колоректального рака [1]:
‒ степень дифференцировки: Low/High;
‒ глубина инвазии (по TNM);
‒ наличие (лимфо)васкулярной инвазии: интрамуральная сосудистая, экстрамуральная сосудистая инвазия, лимфатическая инвазия;
‒ периневральный рост: есть / нет;
‒ край резекции (проксимальный, дистальный, хирургический): позитивный, негативный, расстояние в сантиметрах;
‒ качество образцов краев резекции;
‒ количество выявленных лимфатических узлов;
‒ количество лимфатических узлов с метастазами;
‒ наличие ответа на терапию: есть (частичный или полный) / нет;
‒ микросателлитный статус/наличие белков системы репарации ДНК (MLH1, MSH2, MSH6,м PMS2): микросателлитно-стабильная, микросателлитно-нестабильная; окрашивание с белками системы репарации ДНК отсутствует или присутствует;
‒ статус опухолевого почкования;
‒ наличие/отсутствие соответствующих мутаций.
В качестве важных гистологических характеристик в Заключении необходимо указывать наличие лимфатической инвазии, интра- и экстрамуральной сосудистой инвазии, периневральной инвазии, степени злокачественности, опухолевого почкования (tumor budding) и характер иммунного окружения [2]. Все эти параметры, за исключением последнего, ассоциированы с плохим прогнозом, а иммунное окружение — с благоприятным (табл. 2). Также важно отмечать наличие позитивных/негативных краев резекции (проксимального, дистального и края резекции клетчатки) — считается положительным, если расстояние между опухолью и краем резекции менее 1 мм. В стадировании колоректального рака принципиальных изменений не выявлено, кроме введения новой подрубрики M1c — наличие метастазов на брюшине независимо от поражения соседних органов (ранее эти случаи кодировались M1b).

Примечание. *HR — hazard ratio — соотношение рисков,**CI — confidence interval — доверительный интервал.
В новую классификацию введены дополнительные характеристики опухоли: опухолевое почкование (tumor budding) и иммунное микроокружение. В тексте 5-го издания подробных инструкций к определению данных параметров не приводится, однако указаны ссылки на релевантные источники, которые рекомендуется использовать.
Консенсус «International Tumor Budding Consensus Conference» в марте 2015 г. в Бостоне [3] определил опухолевое почкование (tumor budding) как единичные клетки или как кластеры не более чем из 4 клеток (5 клеток и более именуются плохо дифференцированными кластерами), которые находятся в инвазивном крае опухоли и расцениваются как независимый прогностический фактор колоректального рака. Отмечено, что опухолевое почкование должно быть оценено на препаратах, окрашенных гематоксилином и эозином, при всех возможных вариантах, за исключением случаев с выраженным перитуморальным воспалением и фрагментацией желез; в некоторых случаях следует проводить иммуногистохимическое типирование. В дооперационных биопсиях следует использовать метод горячей точки (hotspot 1 ). В операционном материале может быть использован как метод hotspot, так и подсчет на 10 полях зрения. Инвазивный край с формированием опухолевых почек (budding) и плохо дифференцированных кластеров в общую оценку степени злокачественности опухоли не включаются, так как являются отдельным прогностическим фактором.

Метод определения количества опухолевых почек «hotspot» включает в себя следующие этапы (рис. 2):
1) выбор микропрепарата с наибольшей глубиной инвазии;
2) обзорный просмотр препарата при об. ×10 для определения горячей точки, hotspot — на 10 полях зрения вдоль инвазивного края в операционном материале (см. рис. 2, а) и на всех полях зрения вдоль инвазивного края при pT1-эндоскопическом материале (см. рис. 2, б);

Описание рисунков приводится в тексте.
3) подсчет опухолевых почек в выбранной области (hotspot) при об. ×20 (рис. 3);
4) нормализация опухолевых почек по формуле с учетом коэффициента пересчета из табл. 3.

Окраска гематоксилином и эозином, об. ×20.
Формула подсчета опухолевых почек:
где Bd — budding, опухолевые почки на площадь 0,785 мм 2 ; N — количество почек, подсчитанное при об. ×20; F — коэффициент пересчета (см. табл. 3).
Полученное значение Bd стандартизовано:
Bd1 2 2 (Low grade) — 0—4 почки;
Bd2 (Intermediate) — 5—9 почек;
Bd3 (High grade) — 10 почек и более.
В некоторых гистологических подтипах колоректального рака (муцинозном, перстневидно-клеточном, медуллярном и микропапиллярном) оценку опухолевых почек следует проводить с осторожностью:
— в муцинозных и перстневидно-клеточных карциномах опухолевые почки, расположенные в озерах слизи, считать не следует;
— в медуллярной карциноме в зоне выраженного воспалительного инфильтрата разрозненные опухолевые клетки не отличаются от истинных опухолевых почек, поэтому считать их следует с большой осторожностью;
— в микропапиллярной карциноме не следует в подсчет опухолевых почек включать плохо дифференцированные кластеры (5 клеток и более);
— во всех типах аденокарцином фрагментация желез в зоне выраженного (часто нейтрофильного) воспалительного инфильтрата также может быть с трудом отличима от опухолевых почек.
В случаях, когда точное количество опухолевых почек не может быть посчитано, в Заключении следует писать: «опухолевые почки не могут быть оценены», с последующим пояснением. В материале резекций прямой кишки по поводу рака после неоадъювантной терапии опухолевые почки не следует считать, поскольку в этих случаях их прогностическое значение не доказано.
Опухолевое почкование имеет доказанное прогностическое значение в трех ситуациях:
1) в случаях эндоскопических резекций pT1-раков, когда опухолевое почкование ассоциировано с метастазами в лимфатические узлы, показана хирургическая резекция;
2) у пациентов со II стадией, когда опухолевое почкование ассоциировано с короткой безрецидивной выживаемостью, целесообразна адъювантная терапия;
3) при оценке статуса опухолевого почкования в пред- операционной биопсии, что может помочь пациенту в выборе неоадъювантной терапии и потенциально предсказать регрессию опухоли.
Наличие иммунного микроокружения ассоциировано с лучшим прогнозом и микросателлитной нестабильностью (как независимым от прогноза фактором). Иммунное окружение следует оценивать по опухольинфильтрирующим лимфоцитам и тканевой реакции, подобной болезни Крона (Crohn) [2]:
— тканевая реакция, подобная болезни Крона, — более 3 лимфоидных фолликулов в фокусе выраженной воспалительной реакции;
— опухольинфильтрирующие лимфоциты (TILs) — наличие лимфоцитов (но не гранулоцитов) строго между опухолевыми клетками, считается на 5 полях зрения при об. ×40, среднее значение TILs вычисляется как общее количество лимфоцитов, деленное на 5.
Показано, что среднее число более 2 TILs в поле зрения и выраженная тканевая реакция, подобная болезни Крона, являются независимыми благоприятными прогностическими факторами. Другая известная схема подсчета TILs, основанная на рекомендациях International TILs Working Group, была предложена Y. Iseki и соавт. [6], однако в официальной классификации она не упоминается.
Для оценки опухолевого ответа на терапию предлагается использовать любую из нижеприведенных шкал оценки (табл. 4).

Примечание. AJCC — American Joint Committee on Cancer; MSKCC — Memorial Sloan Kettering Cancer Center; * — в оригинальной работе — пищеводная стенка.
Диагностическая молекулярная патология
В 5-м издании классификации добавлен большой раздел, посвященный молекулярной диагностике и молекулярным прогностическим факторам колоректального рака. Найдены соответствия между двумя различными классификациями, основанными на двух различных подходах: геномном (по ДНК) и транскриптомном (по РНК).
В соответствии с геномной классификацией выделены две большие группы колоректального рака: гипермутационные и негипермутационные, которые соответствуют молекулярным путям с развитием микросателлитной и хромосомной нестабильности соответственно.
Гипермутационные раки (около 15%) имеют высокую частоту мутаций и часто ассоциированы с MSI из-за гиперметилирования промотера гена MLH1 или инактивации ДНК через механизм MMR (13%). Почти все опухоли имеют CpG-фенотип и множество неактивных (silenced) генов из-за гиперметилирования промотера. Малое число опухолей является наследственными и относится к синдрому Линча (Lynch) или соматическим мутациям в MMR. Около 2—3% раков относят к ультрамутационным с чрезвычайно высоким уровнем мутаций, характерной заменой нуклеотидов (C→А), приводящей к наличию мутации, инактивирующей корректирующую функцию экзонуклеазного домена ДНК-реплицирущего фермента POLE (или реже POLD1), что, в свою очередь, приводит к ошибкам при спаривании оснований во время репликации ДНК. Ультрамутационные и гипермутационные часто объединяют в единую группу, поскольку показана достоверно более высокая частота мутаций по сравнению с негипермутационными раками.
Негипермутационные раки (85%) микросателлитно-стабильны и имеют низкую частоту мутаций, однако в них наблюдается высокая частота изменений (увеличение/уменьшение) числа копий соматических генов (SCNA, somatic copy-number alteration) на уровне плеча хромосомы. Гены, которые часто мутированы в негипермутированных раках, — APC (80%), TP53 (60%), KRAS (45%), а также другие (табл. 5).

Чаще всего данные изменения (табл. 6) находят отражения в WNT-, MAPK- и PI3K-сигнальных путях и в инактивации TGF-β- и p53-ингибиторных путей, что может служить основой для таргетной терапии. WNT-сигнальный путь активируется в 97% гипермутационных раков и в 93% негипермутационных.
Впервые достигнут консенсус по молекулярным подтипам колоректального рака (рис. 4). На основании транскриптомного профиля выделены четыре подтипа (consensus molecular subtype, CMS). Почти все гипермутационные (по генетической классификации) раки относятся к первой категории (CMS1, MSI-immune, 14%). Эти раки характеризуются частыми мутациями гена BRAF, метиляторным фенотипом, низкими SCNA, выраженным иммунным ответом — инфильтрацией CD8+ лимфоцитами, что обусловливает потенциальный ответ на ингибиторы контрольных точек иммунного ответа. Остальные микросателлитно-стабильные раки делятся на три подтипа: CMS2 (канонические, 37%), CMS3 (метаболические, 13%) и CMS4 (мезенхимальные, 23%). Тем не менее около 13% всех колоректальных раков не укладываются в достигнутый консенсунс, представляют собой раки с переходным фенотипом или внутриопухолевой гетерогенностью и отнесены к неклассифицируемому подтипу (см. рис. 4).

Выделены биомаркеры с установленным предикторным значением и биомаркеры с частично установленным предикторным значением или находящиеся в стадии разработки (см. табл. 6).

Биомаркеры с установленным предикторным значением
RAS-гены, к которым относятся KRAS и NRAS, имеющие терапевтическое значение. По международным рекомендациям подлежат анализу 12, 13, 59, 61, 117 и 146-й кодоны генов KRAS и NRAS, поскольку они коррелируют с устойчивостью к моноклональным антителам к внеклеточному домену EGFR (HER1). Эти антитела (цетуксимаб и панитумумаб) предотвращают димеризацию EGFR и последующее развитие онкогенных сигнальных путей. Почти 50% колоректальных раков имеют мутации гена KRAS и устойчивы к анти-EGFR-терапии, однако оставшиеся 40—60% опухолей с геном KRAS дикого типа хорошо отвечают на данную терапию.
BRAF. Мутации гена BRAF (чаще в районе 600-й аминокислоты, V600E) сопряжены с неблагоприятным прогнозом, используются для исключения синдрома Линча. Есть данные об отсутствии эффекта от анти-EGFR-терапии у пациентов с мутацией V600E.
Микросателлитная нестабильность. Наличие микросателлитной нестабильности — ключевой момент при синдроме Линча. Микросателлитная нестабильность, ассоциированная с геном BRAF дикого типа, является предиктором хорошего прогноза. С терапевтических позиций микросателлитная нестабильность снижает эффект от химиотерапии фторурацилом и является основанием для назначения иммунотерапии опухоли, в том числе блокаторов PD-L1, особенно в тех случаях, когда традиционная терапия не оказала эффекта.
Биомаркеры с частично установленным предикторным значением или находящиеся в стадии разработки
Успех PD-1/PD-L1-ингибиторов в лечении микросателлитно-нестабильных раков является обнадеживающим, однако имеет много ограничений в биологии и стадии опухоли.
Ген PIK3CA кодирует каталитическую субъединицу PI3K и подвержен мутациям в 10—20% случаев колоректального рака, которые затрагивают преимущественно экзоны 9 и 20. В колоректальных раках с геном RAS дикого типа мутации гена PIK3CA ассоциированы с неблагоприятным прогнозом и плохим ответом на терапию моноклональными антителами к EGFR. С другой стороны, мутация PIK3CA сопряжена с успешной адъювантной терапией ацетилсалициловой кислотой.
c-Met, рецепторная тирозинкиназа часто гиперэкспрессируется в гастроинтестинальных опухолях; аберрантная экспрессия, активация, амплификация и мутация гена MET наблюдаются в некоторых группах колоректального рака и могут являться потенциальными предиктивными маркерами к терапии ингибиторами c-Met.
«Жидкостная биопсия» — анализ периферической крови пациента. Может быть использована в диагностике метастатического колоректального рака и для определения предиктивных маркеров противоопухолевой терапии. Среди всех потенциальных тестов (обнаружение циркулирующих опухолевых клеток, экзосом, внеклеточной ДНК) выявление мутаций в генах (K)RAS и BRAF-мутаций сейчас доступно в некоторых центрах и с большой вероятностью станет широко распространено в ближайшем будущем.
Любопытно отсутствие упоминания о маркерах стволовых клеток и опухолевого микроокружения, которые являются активно развивающимися областями в онкологии и которым посвящено большое количество публикаций.
Нейроэндокринные опухоли. Раздел нейроэндокринных опухолей существенных изменений не претерпел и включает:
‒ нейроэндокринную опухоль (NET);
‒ нейроэндокринную карциному (NEC);
‒ смешанную нейроэндокринную/ненейроэндокринную карциному (8154/3), которая ранее именовалась как смешанная аденонейроэндокринная карцинома (8244/3).
Нейроэндокринные опухоли чаще развиваются в прямой кишке, отмечается незначительное увеличение заболеваемости в 1,5 раза за последние 20 лет. Не рекомендовано использовать термин карциноид для обозначения нейроэндокринной опухоли G1, т.е. термин карциноид исключен. Добавлена новая подрубрика — нейроэндокринная опухоль G3 с кодом, идентичным нейроэндокринной опухоли G2 (8249/3), однако критерии еще не определены.
Заключение
Классификация аденокарцином толстой кишки по сравнению с 2010 г. изменилась частично, исключены крибриформная комедоаденокарцинома, веретеноклеточная карцинома, плоскоклеточная карцинома, добавлены карцинома с саркоматозным компонентом, дискогезивная (poorly cohesive) карцинома и аденомоподобная карцинома. Введены дополнительные характеристики опухоли — опухолевое почкование (tumor budding) и иммунное микроокружение, имеющие прогностическое значение. На основании секвенирования генома выделены гипермутационные и негипермутационные раки и на основании транскриптомного профиля CMS1 (раки с MSI, 14%), CMS2 (канонические, 37%), CMS3 (метаболические, 13%), CMS4 (мезенхимальные, 23%), а также неклассифицируемый подтип (около 13%).
Работа выполнена в рамках госзадания ФГБОУ ВО МГУ им. М.В. Ломоносова с использованием оборудования, приобретенного по Программе развития ФГБОУ ВО МГУ им. М.В. Ломоносова до 2020 г.
1 Зона с максимально выраженным процессом, опухолевым почкованием.