Акб в смартфоне что
Анатомия мобильного аккумулятора
Содержание
Содержание
Тысячи мобильных гаджетов нуждаются в бесперебойных поставках энергии в свои маленькие тела. Энергоносителем для таких устройств выступают аккумуляторы, запасающие электричество в ячейках. В отличие от обычных батареек, они способны выдержать до 15 000 циклов заряда-разряда.
Устройство аккумулятора
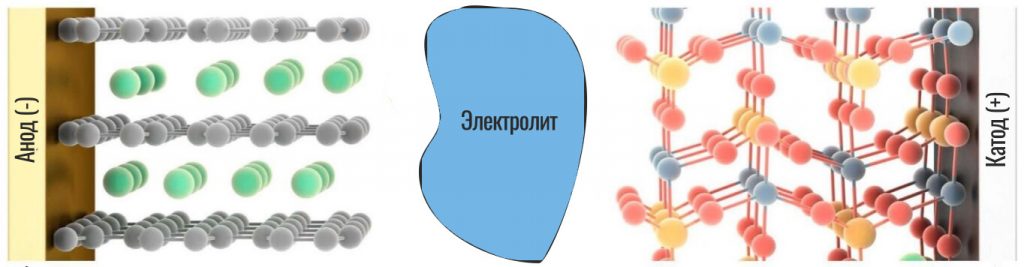
Классическая батарея — банка с положительно заряженным графитовым анодом и отрицательно заряженным катодом, между которыми находится пористая прокладка, покрытая активным веществом — электролитом. Электрический заряд хранит в себе положительно заряженные ионы, выстраивающиеся в кристаллическую решетку токопроводящего электролита. При зарядке, ток гонит ионы к аноду, при разрядке они меняют свое направление, отправляясь обратно к катоду.
Сейчас выделяют три основных типа перезаряжаемых батарей: металл-гидроидные (Ni-MH), никель-кадмиевые (Ni-Cd) и литий-ионные (Li-ion).
Ni-cd и Ni-MH злопамятные. Они запоминают, что их уже зарядили, и теряют часть емкости при новой попытке заправить их под завязку — процесс получил название «эффект памяти». Именно из-за этого особой популярности у переносных устройств они не завоевали.
В свою очередь литиевые подразделяются на кобальтовые, марганцевые и титанатные. Именно о них мы и поговорим в данном блоге, ведь только Li-ion оптимально зарекомендовали себя среди мобильных устройств.
Литиевое семейство
LiCoO2 — химическое соединение литий-кобальта, которое отличается высокой энергоемкостью с номинальным напряжением в 3,6 В и пиковым — 4,2 В. Легкие, емкие, быстро заряжаются и гарантированно обеспечивают стабильную работу шуруповерта, ноутбука, телефона на протяжении до 1000 перезарядок. Единственный минус — высокая цена кобальта, из которого делают катод.
LiMn2O4 — литий-марганцевые батареи имеют более высокое напряжение при сниженном жизненном цикле — 700 перезарядов. Применяются в энергоемких гаджетах.
LiNiMnCoO2— удачный результат симбиоза, получивший неоспоримое преимущество. Литий-никель-марганец-кобальтовые аккумуляторы могут перезаряжаться до 2000 раз, в каждой банке до 2800 мА·ч. Используются для создания источников питания для автомобилей, гироскутеров.
Li4Ti5O12 — литий-титанатный конкурент вышеописанного аккумулятора. Заряжается в 5 раз быстрее, но выдает низкий ток и не так энергоэффективен. Размер батареи на 200-300% больше LiNiMnCoO2 при равном объеме, из-за этого не может применяться в носимых устройствах. Литий- титанатные аноды испускают дух только после 15 000 циклов и эффективно противостоят холоду, поэтому их используют в Московских электробусах.
Li-pol — литий-полимерные аккумуляторы на 25% энергоэффективнее, но при этом быстрее деградируют, способны перезаряжаться около 1000 раз. Полимер позволяет делать батарею гибкой, благодаря этой технологии появилось большое количество сгибаемых портативных устройств.
Отрицательная черта всего семейства литий-ионных батарей — чувствительность к сильным токам и страх перед полной разрядкой. Под высокой нагрузкой они теряют часть «жизненных сил» и быстрее выходят из строя. Решают эту проблему контроллеры заряда, следящие за силой тока и нагревом батарейки. Чем полней коробочка, тем жарче внутри, именно поэтому быстрая зарядка работает только до 50%, затем интенсивность заполнения емкости снижается. Подробнее можно ознакомиться здесь.
Проблема недержания
Отработав несколько сотен циклов, батарея начинает деградировать, частично теряя способность удерживать заряд. Процесс заполнения батареи энергией похож на накачку водонапорной башни. Чтобы поднять жидкость вверх, потребуется энергия, назад вода бежит своим ходом. Тоже происходит и с ионами, чтобы оторвать их от катода, требуется ток, от анода они убегают самостоятельно.
Тепло и мороз
Высокие температуры, равно как и мороз, негативно влияют на поведение накопителя. Набившись стайкой в банку, ионы провоцируют повышение градуса по Цельсию. Каждый раз, когда аккумулятор «жарится» под нагрузкой или при зарядке, часть ионов слипается, лишаясь возможности двигаться и передавать энергию.
Холод тоже негативно влияет на способность батареи к удержанию энергии и способен нанести необратимый урон. Почему аккумуляторы теряют стойкость на морозе и как уберечь свой гаджет от быстрой потери заряда, вы можете прочитать в блоге на эту тему.
Кислая проблема
С точки зрения химии в батарее происходит окислительно-восстановительный процесс, его проявление иногда заметно на поверхности батарей, покрывшихся белым/зеленым порошком — окисью. Катод и анод предают энергию через коллектор тока, связанный с ними клейким материалом. Со временем «сцепка» осыпается из-за циклов нагрева и охлаждения, обнажая алюминиевую ножку коллектора. Анод передает эстафету коррозии коллектору, который по своей ножке поднимает окись вверх. Катод состоит из графита, который может покрыться налетом, но передать окись металлу не способен. Иногда к ним присоединяется электролит, выливающийся из-за повреждения банки, слишком разросшимся кристаллом — это процесс сопровождается вздутием. Батарея — должна быть герметична, если окись вышла посмотреть, что делается в большом мире, внутри полный аут, остается только выкинуть.
Что в итоге?
Идеальных аккумуляторов не существует, более чем за 100 лет производства инженеры разработали десятки видов накопителей энергии, но не смогли создать универсального. Подбирая аккумулятор, необходимо ориентироваться на конкретные задачи, выбирая между объемом и мощностью.
Что такое аккумулятор в телефоне: рассказываем и показываем
Что такое аккумулятор в телефоне никто особо не задумывается. А между тем, благодаря этому изобретению, телефон может по праву считаться «мобильным».
Нет нужды постоянно сидеть у электрической розетки, либо же выбрасывать баснословные деньги на бесконечную замену стандартных батареек.
Что такое аккумуляторная батарея
Аккумулятор электрического тока – это накопитель энергии, принцип его работы достигается благодаря обратимости внутренних химических процессов.
Данные процессы обеспечивают его многократный «заряд-разряд».
Другими словами, это автономный источник электропитания для всевозможных электротехнических устройств, в т.ч. для телефонов, смартфонов и планшетов.
Аккумуляторная батарея получена путем объединения нескольких аккумуляторов в единую электрическую цепь.
Аккумулятор нуждается в периодической подзарядке, чтобы пополнять уровень химической энергии, которая постепенно расходуется.
Заряжать такую батарею можно не только от классической электророзетки.
Допускается использование любых альтернативных источников постоянного ограниченного тока с напряжением, которое выше, чем напряжение в самой батарее.
То есть, есть возможность «меньшее» заряжать «большим».
Какие бывают аккумуляторы в устройстве
Тип батареи зависит от материала электродов и состава электролита, используемых при его производстве.
При создании батареи для современных телефонов используются два типа:
Характеристика многочисленных подтипов зависит от химического состава входящих компонентов. Состоит из электродов (катодного материала на алюминиевой фольге и анодного материала на медной фольге).
Обладает большой емкостью и низким саморазрядом.
Данный тип батарей имеет массу преимуществ (низкий саморазряд, компактность, гибкость, отсутствие эффекта памяти, неприхотливость к температурным условиям).
Батарея смартфона. Часть 1. Как она работает и как правильно заряжать свой телефон
Этой статьей мы начинаем серию увлекательных материалов, посвященных аккумулятору смартфона. На первый взгляд слова «увлекательный» и «аккумулятор» не имеют логической связи. Однако, прочитав эту статью до конца, вы убедитесь в обратном!
Проблема с подобного рода статьями заключается в том, что советы по поводу «правильной» зарядки дает каждый второй пользователь смартфона и нередко можно увидеть прямо противоположную информацию.
Кто-то говорит, что можно без проблем оставлять смартфон на зарядке на всю ночь или разряжать телефон до нуля, ведь система управления питанием не допустит критического падения или превышения напряжения внутри аккумулятора. Другие с этим в корне не согласны, приводя в качестве аргументов личный печальный опыт.
В этой серии мы затронем все вопросы, начиная от принципа работы аккумулятора и заканчивая быстрыми и беспроводными зарядками. В первой части поговорим о том, как вообще работает аккумулятор, откуда там появляется ток и куда он девается, а также ответим на некоторые важные практические вопросы.
Загадочная «баночка с энергией» или как работает аккумулятор смартфона
Многие люди представляют себе аккумулятор телефона в виде небольшой баночки, в которую по проводу из розетки «заливается» ток. Набрали полную батарейку электронов — теперь можем в течение дня расходовать эту энергию на подпитку дисплея, динамиков, процессора и других компонентов смартфона. Закончились электроны в батарейке — телефон разрядился и нужна новая порция электронов.
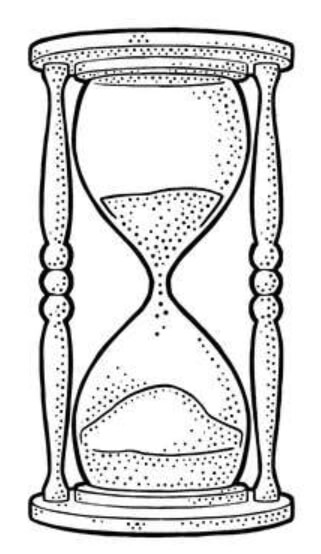
Выглядит эта картина вполне логично, но не совсем верно. В реальности аккумулятор больше похож на закрытые песочные часы, только вместо песка у нас «засыпаны» электроны:
Когда верхний «сосуд» с электронами опустошится, нужно будет зарядить смартфон, то есть, как-то перевернуть часы, чтобы электроны снова посыпались вниз. Зарядка «переворачивает часы», забирая «песок» с нижней части аккумулятора и пересыпая его в «верхнюю» чашу, чтобы электроны снова могли двигаться в нужном направлении.
Мы все прекрасно понимаем, почему песок сыпется вниз. Это происходит под действием силы тяжести. Если бы часы лежали на боку, песок не пересыпался бы с одного сосуда в другой. Теперь представим, что часы лежат на столе (для простоты уберем лишние детали), но электроны «часов» почему-то продолжают «пересыпаться» с одной части в другую:
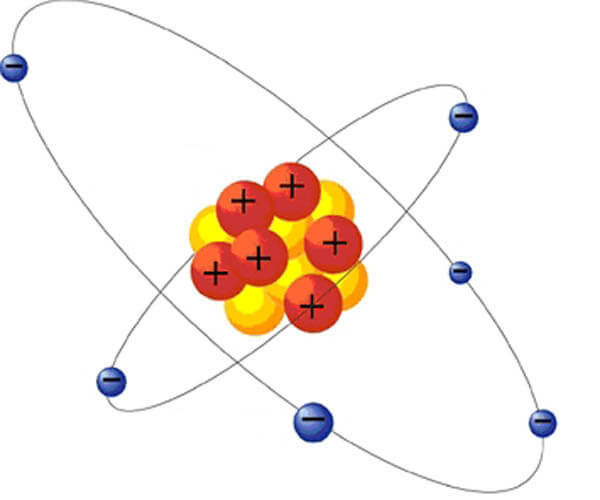
Как это происходит!? Для ответа на этот вопрос давайте вспомним, что вообще такое электрон. Всё, что нас окружает, состоит из атомов. Атомы, в свою очередь, состоят из ядра, вокруг которого, словно планеты вокруг солнца, вращаются электроны (на самом деле, это примитивная и устаревшая модель, так как электроны не летают по орбитам, да и орбит никаких нет, но для нашего разговора такая модель сгодится):
Электроны (синие шарики со знаком минус) — это отрицательно заряженные частицы, а внутри ядра находятся положительно заряженные (протоны) и нейтрально заряженные (нейтроны) частицы. Опять
Если количество электронов (-) и протонов (+) одинаково, атом считается электрически нейтральным. Если больше электронов (-), тогда атом обладает отрицательным зарядом, а если больше протонов (+), тогда атом обладает положительным зарядом.
Так вот, разноименные заряды (плюс и минус) всегда притягиваются друг ко другу, а одноименные (плюс-плюс или минус-минус) — отталкиваются. И не нужно пугаться слов «положительный» и «отрицательный» заряд. Это просто названия, не имеющие под собой никакого основания. Раньше такие заряды назывались «стеклянными» и «смоляными». Затем их решили называть «положительными» и «отрицательными». Главный смысл — показать, что заряды бывают двух типов и они между собой как-то взаимодействуют.
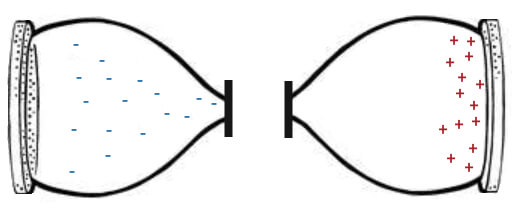
Теперь немножко подправим наши часы, сделав их более похожими на батарейку смартфона. Для этого изолируем две чаши и в одну из них поместим отрицательные заряды, а в другую — положительные:
Слева находится множество отрицательных электронов, а справа — положительных ионов. Ион — это просто другое название для атома, который потерял или получил электрон. В нашем случае, он потерял электрон («минус») и заряжен положительно. Получается, слева избыток электронов, а справа — их недостаток.
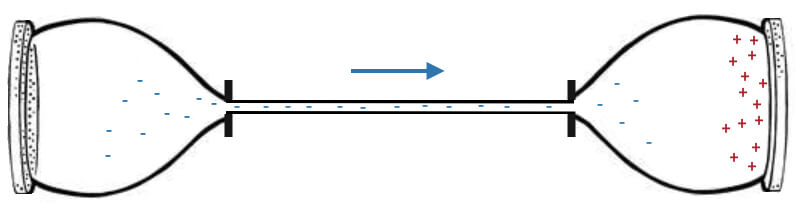
Но в природе все стремится к равновесию, атомы «хотят» быть нейтральными. То есть, количество положительных зарядов должно соответствовать количеству отрицательных зарядов. Если мы соединим обе чаши проводником (проводом), электроны слева моментально начнут движение по этому проводу в правую чашу:
И в этот момент в проводе возникнет электрический ток, так как ток — это и есть движение электронов в одном направлении. Теперь можно этот провод провести через все компоненты смартфона. Электроны, проходя от отрицательной «чаши» к положительной, будут давать электрический ток. Соответственно, будет работать экран, динамики и другие компоненты.
Теперь представьте, что чаша слева — это одна сторона аккумулятора (минус), а чаша справа — другая (плюс) и ток течет от отрицательной стороны батарейки к положительной. Но наступит момент, когда количество электронов выровняется. Больше нет «плюса» и «минуса», так как атомы везде стали нейтральными, все лишние электроны присоединились к ионам и телефон полностью разрядился.
Если бы это была обычная батарейка, толку от нее больше не было бы. Но так как это аккумулятор, можно попытаться снова разделить атомы на положительные ионы и отрицательные электроны, собрав «минусы» на одной стороне аккумулятора, а «плюсы» — на другой. И весь процесс запустится по кругу.
Что такое амперы и вольты?
Вернемся к потоку электронов. Чем большее их количество протекает по проводу за 1 секунду, тем выше сила тока, то есть, тем больше ампер выдает аккумулятор. Заряд одного электрона ничтожно мал, соответственно, нужно очень много электронов, чтобы силы тока было достаточно для питания смартфона. Амперы — это и есть наш ток. Если не будет ампер, значит, нет и электронов, которые бы двигались в одном направлении. Соответственно, нет и электричества. Если говорить точно, тогда 1 ампер — это поток из 6240 квадриллионов электронов, протекающих за 1 секунду.
Теперь возьмем батарейку смартфона, на одной стороне которой собралось много отрицательных частиц (со знаком «минус»), а на другой — положительных (со знаком «плюс»). В результате мы получаем два потенциала, один из которых «хочет» избавиться от лишних электронов. Их слишком много, им мало места, они выталкивают друг друга (электроны с одинаковым зарядом отталкиваются). А на втором конце наблюдается сильная недостача электронов и атомы пытаются их притянуть. Так вот, разница между такими потенциалами («плюс» и «минус») называется напряжением и измеряется в вольтах. Чем больше с одной стороны свободных электронов и сильнее их недостача с другой стороны, тем выше напряжение.
Если сравнить течение тока с водой в трубке, тогда сила тока (амперы) — это количество воды в трубке, а напряжение (вольты) — это давление, с которым мы толкаем воду. Соответственно, сколько бы воды не было в трубке, если мы не можем ее протолкнуть — никакого тока не будет. Верно и обратное — если воды очень и очень мало, то с каким бы давлением мы не пытались ее вытолкнуть, большой мощности не будет. То есть, эта вода будет бесполезной, так как она не сможет сделать никакой полезной работы, например, вращать водяную мельницу. Нужно не только много воды, но и хорошее давление.
Итак, только что мы рассмотрели базовый принцип работы батарейки. Электроны из одной части аккумулятора по проводам перетекают в другую часть. Только на нашей картинке обе части находились на расстоянии друг от друга, а внутри смартфона — это цельная конструкция. Просто электроны не могут попасть с одной стороны (минус) на другую (плюс) напрямую, так как между ними стоит «барьер». Соответственно, нужно между этими частями «проложить мостик», по которому электроны моментально начнут движение. Таким мостиком является проводка внутри смартфона.
Принцип работы литий-ионного (Li-ion) аккумулятора
Все смартфоны уже давно используют исключительно один тип аккумуляторов — это литий-ионные батареи (Li-Ion). О них и поговорим подробнее.
Кто-то может возразить и сказать, что в его смартфоне установлен литий-полимерный (Li-Po или LiPo) аккумулятор, который гораздо лучше литий-ионного. В доказательство можно привести тысячи статей на всевозможных сайтах, включая самые авторитетные. Однако в реальности, «литий-полимерный» аккумулятор — это не более, чем маркетинговая уловка, не имеющая никакого отношения к твердотелым аккумуляторам. Подробнее об этом я упомяну чуть позже. На этом этапе будет непонятной разница между литий-ионной и литий-полимерной батарейкой.
Итак, главным действующим лицом в литий-ионных аккумуляторах, как следует из названия, является литий, а точнее, его ионы. У лития всего 1 электрон на внешней оболочке атома (то есть, на самой дальней и нестабильной орбите). Соответственно, такой электрон очень легко может оторваться, превратив атом в положительно заряженный ион (вспоминаем, электрон — это отрицательная частица и если ее оторвать, атом станет положительным). По этой причине литий в чистом виде легко вступает в реакцию.
Но если атом лития станет частью оксида металла (соединение химических элементов), тогда он будет достаточно стабильным. Схематически это можно отобразить так:
Свободные атомы лития (зеленые шарики) очень нестабильные и могут вступать в реакцию, теряя электрон, а те, что в структуре оксида металла (в основном используется кобальт) — достаточно стабильные. Когда атом лития нестабилен, он, как и все мы, стремится к стабильности, возвращаясь на место в оксид металла.
Теперь вспоминаем устройство батарейки. Литий-ионный аккумулятор состоит из двух «камер» или частей. Одна из них будет отрицательной (называется Анод), а вторая положительной — Катод. Как и в нашем примере, электроны из Анода (-) должны попасть в Катод (+). Но сделать это напрямую внутри аккумулятора они не могут, так как между анодом и катодом находится жидкий электролит (переносчик положительных зарядов).
В современных аккумуляторах, кажется, что нет никакой жидкости внутри. Но это только так кажется. Многие современные аккумуляторы используют полимер, смоченный электролитом или же специальный пористый разделитель (сепаратор) из полимера, пропитанного электролитом. Но это всё тот же жидкий электролит, просто немного в другом виде. А существуют настоящие литий-полимерные аккумуляторы, у которых сам полимер проводит литий, то есть, там вообще нет никакого жидкого электролита. Такие аккумуляторы не используются в смартфонах.
Итак, посмотрим на схему нашего аккумулятора:
Мы видим здесь две части батареи: минус (слева) и плюс (справа). Они разделены по центру сепаратором, пропитанным электролитом. В левой части (в аноде) между слоями графита размещаются атомы лития. Кристаллическая решетка графита позволяет легко задерживать атомы лития между слоями. То есть, литий в нем, как бы, «застревает» (это явление называется интеркаляцией). Сам графит не вступает ни в какие реакции, он просто служит своеобразными «полочками», на которых можно удобно разместить все ионы.
Справа от электролита (в катоде) находится оксид кобальта, который вступает в реакцию с литием.
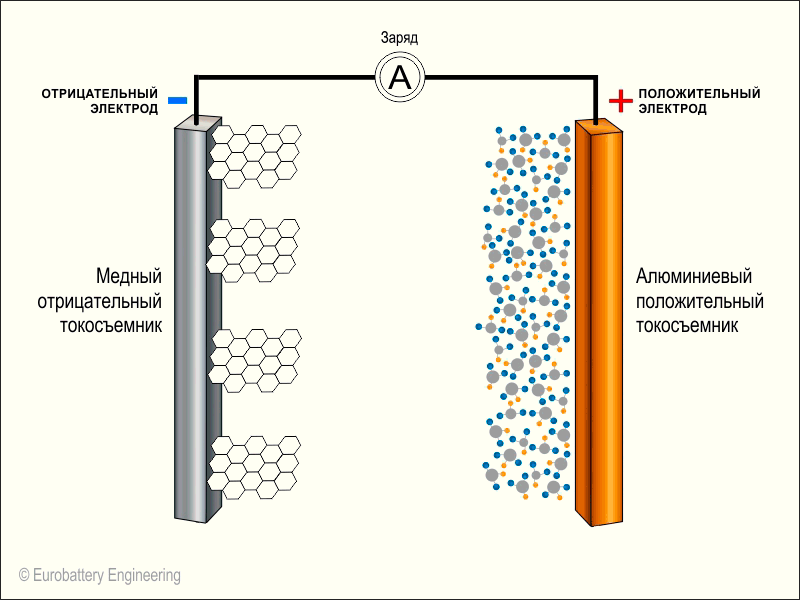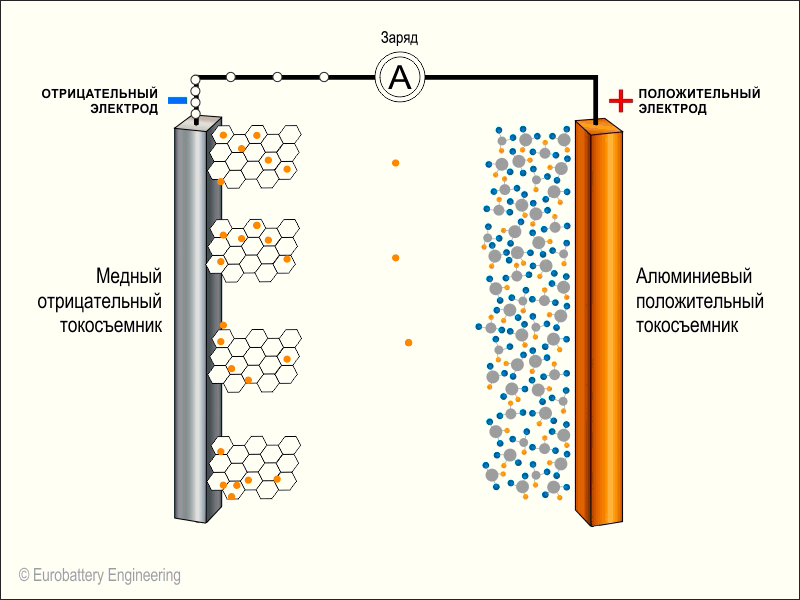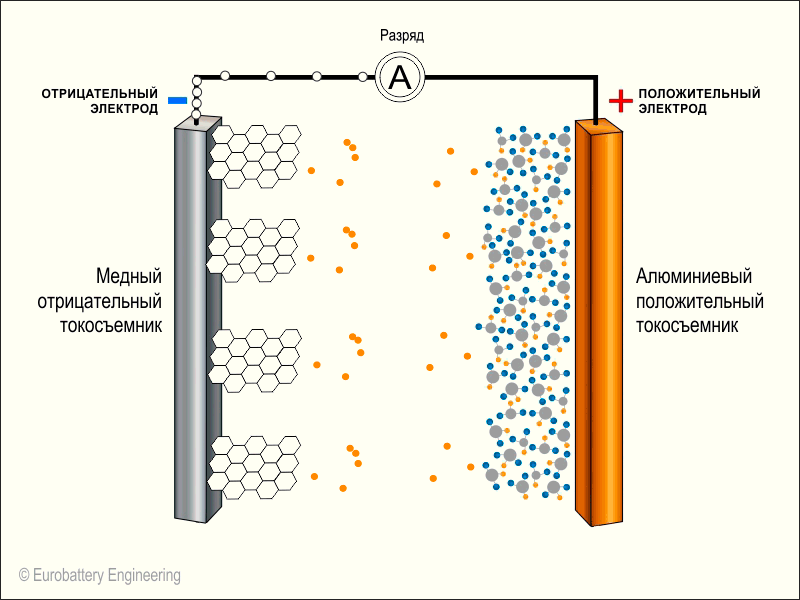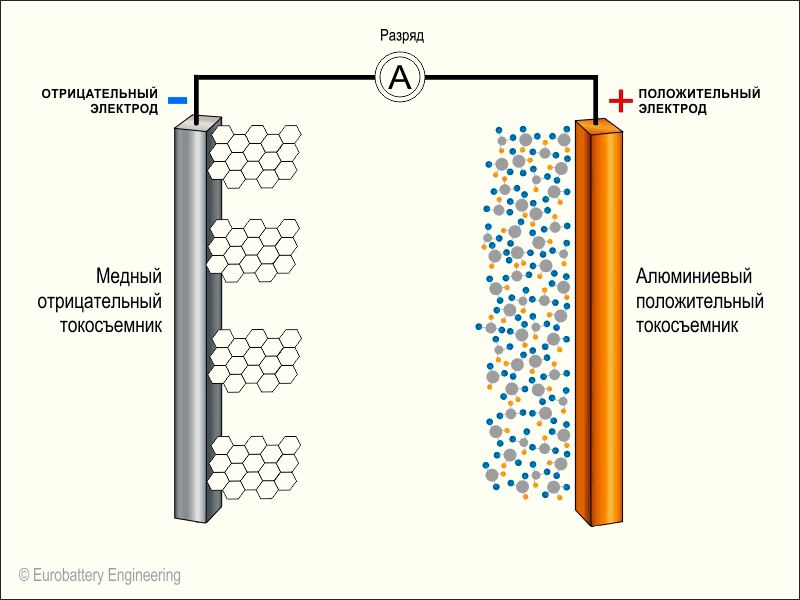
Разрядка телефона
Атомы кобальта на катоде (плюсе) из-за химической реакции потеряли электроны и их заряд стал еще более положительным. В результате они хотят вернуть свои электроны, чтобы нейтрализовать заряд. А как мы помним, на аноде (минусе) в графите «застряло» много лития, который без проблем отдаст свой электрон.
Но эти электроны не могут пройти через электролит, чтобы соединиться с кобальтом (оксидом металла).
Аккумулятор подключается плюсом и минусом к контактам смартфона. Дорожка от одного контакта (-) проходит через все компоненты смартфона и доходит до второго контакта (+). Она и соединяет две части батареи.
Как только между анодом и катодом появляется путь, электроны на аноде отрываются от лития и устремляются по нему, чтобы примкнуть к положительно заряженному кобальту. А литий в это же время свободно проходит через электролит и встраивается в оксид кобальта.
По дороге электроны «заходят» во все компоненты смартфона, которые встречаются им по пути и заставляют их работать.
Еще раз хочу обратить внимание на то, что электроны не «тратятся», как, например, топливо. Электрон вышел из точки А и пришел в точку Б, а если по пути встретилась лампочка, то еще и ее «зажег», но сам при этом никуда не испарился.
Зарядка телефона
Когда весь литий перейдет через электролит от анода к катоду, больше не останется электронов, которые бы могли путешествовать по внешнему проводу (по электрической цепи). Теперь нам нужно провернуть обратный процесс, а именно, «перетянуть» литий из катода в анод.
Для этого мы прикладываем внешний источник питания «плюсом» к катоду батарейки (+) и «минусом» к аноду батарейки (-). Так как напряжение внешнего источника выше напряжения батарейки, происходит химическая реакция. От кобальта отрываются электроны и уходят в «розетку». При этом атомы лития также вылетают из оксида металла.
В то же время от блока питания на «минус» батарейки залетают электроны и эта часть аккумулятора становится всё более и более отрицательно заряженной. В результате положительные ионы лития проходят через электролит и на аноде (в графите) встречаются с электронами.
Теперь весь литий снова на аноде и когда зарядка будет прекращена, начнется обратный процесс — электроны устремятся к положительному кобальту через весь смартфон, а литий следом — через электролит:
На этой иллюстрации вместо буквы А в кружочке и находятся компоненты нашего смартфона. Также на анимации не показан электролит по центру. Оранжевые кружочки — это положительные ионы лития, а белые кружочки — это электроны.
Так можно ли полностью разряжать свой смартфон или оставлять его на зарядке на всю ночь?
Вы можете делать все, что вашей душе угодно. Но стоит помнить, что у любого действия есть свои последствия. Это может прозвучать очевидно, но именно заряд/разряд смартфона и сокращает его емкость. По этой причине существует такое понятие как цикл разряда/заряда.
Я думаю, вы не раз слышали о том, что смартфоны рассчитаны на определенное количество циклов заряда/разряда, например, 500 полных циклов. Apple на своем сайте заявляет, что если полностью зарядить iPhone до 100%, после чего разрядить его до 0%, тогда через 500 таких зарядок/разрядок, емкость аккумулятора снизится до 80%. В случае с Apple Watch количество циклов увеличено до 1000.
Многие пользователи знают об этом и всё пытаются понять, как злобный производитель подсчитывает эти циклы, снижая емкость их аккумулятора. Кто-то старается выяснить, что считается полным циклом и как можно обмануть смартфон, разряжая его не совсем до нуля или заряжая не совсем до 100%.
На самом же деле, никто не считает циклы, чтобы специально испортить батарейку. Понятие полных/неполных циклов заряда введено для удобства. А портит батарейку именно заряд/разряд.
Понимая все, что мы разобрали в статье, посмотрим, кто же портит наш аккумулятор. Итак, при зарядке литий проходит через электролит от плюса к минусу, то есть, от катода к аноду.
Теперь, когда начинается разрядка смартфона, обратно вернутся не все ионы лития. Кто-то из них погибнет по пути домой. Возвращаясь через электролит, на внешней границе происходит реакция, в которой участвуют органические вещества электролита, сам литий и его электроны. В результате такой реакции образуется тонкая пленочка на аноде под названием SEI (Solid Electrolyte Interface).
С одной стороны, она и защищает слой электролита от бомбардировки электронами, которые стремятся пройти через электролит вслед за ионами лития, но не могут. С другой же стороны, на ее образование уходит часть атомов лития. То есть, самого лития становится меньше. А значит, уменьшается и емкость батарейки. И с каждым новым циклом заряда/разряда этот слой (SEI) становится все толще. Рано или поздно это приведет к созданию барьера, через который литий уже не сможет переходить к графиту анода.
На катоде тоже происходит реакция — окисление электролита. Чем выше напряжение — тем быстрее это происходит. Соответственно, собирать большое количество лития на одном из полюсов и держать его в таком состоянии, приводит к более быстрой деградации аккумулятора.
Получается, когда вы ставите смартфон на ночь на зарядку, конечно же, BMS (система управления батареей) не позволит аккумулятору «перезарядиться», то есть, получить большее напряжение, чем он способен выдержать. И проблема совершенно не в этом.
Всю ночь аккумулятор вашего смартфона будет находиться в состоянии, при котором деградация батареи будет максимально ускоряться. То же касается и падения заряда ниже 15-20%. В этом случае, мы получаем ту же ситуацию, что и с полностью заряженным аккумулятором, только наоборот. На ускорение вредных процессов влияет также и температура батареи.
Таким образом, для максимального срока службы литий-ионного аккумулятора нужно не только не оставлять свой смартфон на зарядке на всю ночь, но и не заряжать его вовсе до 100%, как и не разряжать ниже 20%. Гораздо лучше для батареи зарядить смартфон дважды в день (от 30 до 80%), нежели один раз в сутки ставить его на зарядку на всю ночь. Аккумулятор прослужит дольше, даже если вы будете заряжать его 4 раза в день от 40 до 70%, нежели проходить полный цикл заряда/разряда.
К слову, бывают случаи, когда человек использует свое устройство очень редко, например, зеркальную камеру. И в связи с этим хочет максимально эффективно хранить батарейку, чтобы она не теряла емкость. В таком случае, лучше всего разрядить аккумулятор до 40% и поместить его в полиэтиленовый пакет. А сам пакет с батареей хранить в холодильнике (не морозилке) при температуре от 0 до 3°C.
Ниже в таблице вы можете увидеть зависимость деградации аккумулятора от уровня его заряда и температуры хранения через 1 год:
| Температура | 40%-уровень заряда | 100%-уровень заряда |
| 0°C | 98% | 94% |
| 25°C | 96% | 80% |
| 40°C | 85% | 65% |
| 60°C | 75% | 60% через 3 мес. |
Надеюсь, вам понравилась первая часть из нашей новой серии, а во второй мы поговорим о беспроводной зарядке.
Алексей, главный редактор Deep-Review
P.S. Не забудьте подписаться в Telegram на первый научно-популярный сайт о мобильных технологиях — Deep-Review, чтобы не пропустить очень интересные материалы, которые мы сейчас готовим!
Как бы вы оценили эту статью?
Нажмите на звездочку для оценки
Внизу страницы есть комментарии.
Напишите свое мнение там, чтобы его увидели все читатели!
Если Вы хотите только поставить оценку, укажите, что именно не так?