Аккумулятор li ion что это значит
Литий-ионный аккумулятор (Li-ion)
В настоящее время литий-ионный аккумулятор используется абсолютно во всей домашней и портативной электронике.

Можно без преувеличения сказать: без портативных источников питания, мир современной техники был бы намного беднее. Все разнообразие карманных электронных гаджетов, приборов, смартфонов, гироскутеров, электромобилей наконец, стало возможным благодаря литий-ионным аккумуляторам.
Принцип работы литий-ионного аккумулятора
Давайте рассмотрим литий-ионный аккумулятор. Как видите, он состоит из нескольких слоев с различным химическим составом.

В основе работы литий-ионного аккумулятора лежит, так называемый, электрохимический потенциал. Суть его в том, что металлы стремятся «отдавать» свои электроны. Как видно на рисунке ниже, наибольшая способность к отдаче электронов – у лития, а наименьшая – у фтора. Если такой атом отдает свой электрон, то он становится положительным ионом.
Первая в истории электрическая батарейка, созданная более 200 лет назад Алессандро Вольтой, работала как раз на принципе электрохимического потенциала. Вольта взял два металла с разными электрохимическими потенциалами (цинк и серебро) и получил электрический ток. В честь его открытия такую «батарейку» назвали Вольтовым столбом.
В 1991 г. Sony выпустила первый коммерчески успешный литий-ионный аккумулятор.
В литий-ионных элементах используется металл с наибольшей способностью отдавать электроны – литий. У лития всего один электрон на внешней орбите, и он постоянно стремится его «потерять».
Из-за этого литий считается чрезвычайно химически активным металлом. Он реагирует даже с водой и воздухом. Но активен только чистый литий, а вот его оксид, напротив, очень стабилен.
Это свойство лития как раз используется при создании литий-ионных аккумуляторов.
Допустим, мы каким-то образом отделили атом лития от оксида. Этот атом будет крайне нестабилен и сразу превратится в положительный ион, потеряв электрон.
Однако в составе оксида литий гораздо более стабилен, чем одинокий атом лития. Если мы сможем каким-то образом обеспечить движение по двум отдельным путям для электрона и для положительного иона лития, то ион самостоятельно достигнет оксида и встанет там на свое место. При этом мы получим электрический ток благодаря движению электрона.
Итак, можно получить электрический ток из оксида лития, если сначала отделить атомы лития от оксида и затем направить потерянные ими электроны по внешней цепи. Рассмотрим, как эти две задачи решаются в литий-ионных элементах.
Строение литий-ионного аккумулятора
Помимо оксида лития, элементы содержат также электролит и графит. В графите связь между слоями гораздо слабее, чем между атомами внутри слоев, поэтому графит имеет слоистую структуру. (Переходи и смотри подробно про строение атома)

Электролит, помещенный между оксидом лития и графитом, служит барьером, пропускающим сквозь себя только ионы лития. Электроны же не могут проникать сквозь электролит и отскакивают от него, как теннисный мячик об стенку. В качестве электролита используется органическая соль лития, которая наносится на слой разделителя (о разделителе ниже в статье).

Процесс заряда и разряда литий-ионного аккумулятора
Итак, у нас есть разряженный аккумулятор

Давайте же его зарядим. Для этого нам нужен какой-либо источник питания. Что произойдет в этот момент на самом литий-ионном аккумуляторе? Положительный полюс начнет притягивать электроны, «вытаскивая» их из оксида лития.

Поскольку электроны не могут проникать через электролит, то они движутся по внешней цепи через источник питания.
и в конце концов достигают графита
где очень удобно располагаются в слоях графита.
В этот же самый момент положительные ионы лития притягиваются отрицательным полюсом, проходя сквозь электролит и также попадают в графит, размещаясь между его слоями.
Когда все ионы лития достигнут графита и будут «захвачены» его слоями, батарея будет полностью заряжена.
Такое состояние батареи неустойчивое. Это можно представить как шар, который находится на самой верхушке холма и в любой момент может скатиться.
Вот мы и достигли первой цели: электроны и ионы лития отделены от оксида. Теперь надо как-то сделать так, чтобы электроны и ионы двигались разными путями. Как только мы подключим какую-либо нагрузку к нашему заряженному литий-ионному аккумулятору, то начнется обратный процесс. В этом случае ионы лития через электролит пожелают вернуться в свое изначальное состояние.
Поэтому они начнут двигаться обратно сквозь электролит, а электроны побегут через внешнюю цепь, то есть через нагрузку.

Так как электрический ток — это не что иное, как упорядоченное движение заряженных частиц, то в цепи лампочки накаливания возникнет электрический ток, который заставит эту самую лампочку светиться.
Как только все электроны «убегут» из графита, то батарея полностью разрядится. Чтобы ее снова зарядить, достаточно поставить аккумулятор «на зарядку».

При этом графит сам по себе не участвует в химических реакциях – он лишь служит «складом» для ионов и электронов лития.
Слой разделителя в литий-ионном аккумуляторе
Если внутренняя температура элемента по какой-то причине начнет расти, жидкий электролит высохнет, и произойдет короткое замыкание между анодом и катодом. В результате элемент может загореться или даже взорваться.
Чтобы этого не произошло, между электродами помещается дополнительный изолирующий слой, называемый разделителем. Разделитель проницаем для ионов лития благодаря наличию микропор. Электроны он не пропускает.

Из чего делают литий-ионный аккумулятор
В реальных литий-ионных аккумуляторах графит и оксид лития наносятся в виде покрытия на медную и алюминиевую фольгу. Ниже на рисунке мы видим, что на тонком листе меди у нас располагается графит, а на тонком листе алюминия — оксид лития.
Минус аккумулятора снимается с медной фольги, а плюс — с алюминиевой.
ну а между ними располагается еще разделитель, пропитанный электролитом
Для того, чтобы уменьшить объем, все эти три слоя сворачивают в «рулончик».

образуя при этом всем нам знакомую литий-ионную цилиндрическую батарейку
Литий-ионные аккумуляторы в автомобиле Tesla
Вообразите мир, в котором все машины оснащены электродвигателями, а не двигателями внутреннего сгорания. Электромоторы превосходят ДВС практически по всем техническим показателям, да к тому же намного дешевле и надежнее. У ДВС есть существенный недостаток: он выдает достаточный крутящий момент лишь в узком диапазоне скоростей. В общем, электродвигатель – однозначно лучший выбор для автомобиля. Об этом мы писали еще в статье про автомобиль Тесла.

Но есть одно «узкое место», из-за которого электрическая революция в автопроме постоянно откладывается — это источники питания. Долгое время громоздкие, тяжелые, недолговечные и ненадежные аккумуляторы электромобилей никак не могли составить конкуренцию полному баку бензина. Но все изменилось, когда на рынок вышел производитель электромобилей Тесла.
Именно литий-ионные аккумуляторы использует компания Тесла для своих электрокаров.
Стандартный элемент выдает напряжение 3,7 – 4,2 В. Множество таких элементов, соединенных последовательно и параллельно, образуют модуль.

Литий-ионные элементы при работе выделяют много тепла. При этом высокая температура снижает срок службы и эффективность самих элементов. Для контроля температуры, а также их уровня заряда, защиты от перезаряда и общего состояния элементов питания, служит специальная система управления батареями (Battery management system, сокращенно BMS). В батареях Tesla используется спиртовая система охлаждения. BMS регулирует скорость движения спирта в системе, поддерживая оптимальную температуру батарей.

Еще одна важнейшая функция BMS – защита от перезаряда. Допустим, есть три элемента с разной емкостью. Во время зарядки элемент с большей емкостью зарядится сильнее двух остальных. Чтобы этого не допустить, BMS использует так называемое выравнивание заряда элементов (cell balancing). При этом все элементы заряжаются и разряжаются равномерно и защищены от чрезмерного или недостаточного заряда.
И в этом преимущество Tesla над технологией аккумуляторов Nissan. У Nissan Leaf серьезная проблема с охлаждением аккумулятора из-за большого размера элементов и отсутствия системы активного охлаждения.

У конструкции с множеством маленьких цилиндрических элементов есть и еще одно преимущество: при большом расходе энергии нагрузка распределяется равномерно между всеми элементами. Если бы вместо множества маленьких элементов был один огромный элемент, из-за постоянных нагрузок он очень быстро бы пришел в негодность. Tesla сделала ставку на маленькие цилиндрические элементы, технология производства которых уже хорошо отработана. Более подробно про батарейный модуль Тесла читайте в этой статье.
Защитный SEI-слой
Во время первой зарядки внутри литий-ионного элемента происходит одно замечательное явление, спасающее элемент от скорой «смерти». Неожиданной проблемой оказались электроны, находящиеся в слое графита. При контакте с электролитом они начинают разрушать его. Но одно случайное открытие позволило не допустить контакт электронов с электролитом. При первой зарядке элемента, как мы уже говорили, ионы лития движутся сквозь электролит. В процессе этого движения молекулы растворенного в электролите вещества покрывают ионы. Достигнув графитового слоя, ионы лития вместе с молекулами раствора электролита реагируют с графитом, образуя так называемая промежуточную фаза твердого электролита (solid electrolyte interphase, или SEI-слой). Этот слой предотвращает контакт электронов с электролитом, предохраняя электролит от разрушения.
Вот так проблема случайным образом решилась сама собой. Хотя эффект SEI был открыт случайно, в последующие два десятилетия ученые целенаправленно улучшали процесс, подбирая наиболее эффективную толщину и химический состав.
Заключение
Сегодня уже удивительно, что еще два десятка лет назад в электронных гаджетах не применялись литий-ионные аккумуляторы. Индустрия литий-ионных аккумуляторов развивается с фантастической скоростью: ожидается, что в ближайшие несколько лет их рынок достигнет 90 млрд. долларов. Современные литий-ионные батареи способны выдержать примерно 3000 циклов зарядки-разрядки – это уже приличный показатель, но еще есть, куда расти. Лучшие умы во всем мире трудятся над тем, чтобы повысить их долговечность до 10 000 циклов. В этом случае аккумулятор электромобиля не придется заменять целых 25 лет. Миллионы долларов вкладываются в исследования, которые позволят заменить графит на кремний в качестве «хранилища» в литий-ионных элементах. Если это удастся сделать, их емкость возрастет более чем в пять раз! В настоящее время мир переходит уже на литий-полимерные аккумуляторы, которые показали себя чуточку лучше, чем литий-ионные.
Литий-ионные и литий-полимерные аккумуляторы
Инженерная мысль непрерывно развивается: ее стимулируют постоянно возникающие проблемы, требующие для своего решения разработки новых технологий. В свое время на смену никель-кадмиевым (NiCd) аккумуляторам пришли никель-металлгидридные (NiMH), а сейчас место литий-ионных (Li-ion) пытаются занять литий-полимерные (Li-pol) аккумуляторы. NiMH аккумуляторы в какой-то степени потеснили NiCd, но в силу таких неоспоримых достоинств последних, как способность отдавать большой ток, низкая стоимость и длительный срок службы, не смогли обеспечить их полноценной замены. А вот как обстоит дело с литиевыми аккумуляторами? Каковы их особенности и чем отличаются Li-pol аккумуляторы от Li-ion? Попробуем разобраться в этом вопросе.
Как правило, все мы при покупке мобильника или портативного компьютера не задумываемся о том, какой аккумулятор у них внутри и чем вообще различаются эти устройства. И только потом, столкнувшись на практике с потребительскими качествами тех или иных аккумуляторов, начинаем анализировать и выбирать. Тем, кто спешит и желает сразу получить ответ на вопрос, какой аккумулятор является оптимальным для сотового телефона, я отвечу коротко — Li-ion. Дальнейшая информация предназначена для любознательных.
Для начала небольшой экскурс в историю.
Первые эксперименты по созданию литиевых батарей начались в 1912 году, но только спустя шесть десятилетий, в начале 70-х годов, они впервые были внедрены в бытовые устройства. Причем, подчеркну, это были именно батареи. Последовавшие вслед за этим попытки разработать литиевые аккумуляторы (перезаряжающиеся батареи) оказались неудачными из-за проблем, связанных с обеспечением безопасности их эксплуатации. Литий, самый легкий из всех металлов, имеет наибольший электрохимический потенциал и обеспечивает самую большую плотность энергии. Аккумуляторы, использующие литиевые металлические электроды, характеризуются и высоким напряжением, и превосходной емкостью. Но в результате многочисленных исследований в 80-х годах было выяснено, что циклическая работа (заряд — разряд) литиевых аккумуляторов приводит к изменениям на литиевом электроде, в результате которых уменьшается тепловая стабильность и появляется угроза выхода теплового состояния из-под контроля. Когда это происходит, температура элемента быстро приближается к точке плавления лития — и начинается бурная реакция с воспламенением выделяющихся газов. Так, например, большое количество литиевых аккумуляторов для мобильных телефонов, поставленных в Японию в 1991 году, было отозвано после нескольких случаев их воспламенения.
Из-за свойственной литию неустойчивости исследователи обратили свой взор в сторону неметаллических литиевых аккумуляторов на основе ионов лития. Немного проиграв при этом в плотности энергии и приняв некоторые меры предосторожности при заряде и разряде, они получили более безопасные так называемые Li-ion аккумуляторы.
Плотность энергии Li-ion аккумуляторов обычно вдвое превышает плотность стандартных NiCd [1], а в перспективе, благодаря применению новых активных материалов, предполагается еще больше увеличить ее и достигнуть трехкратного превосходства над NiCd. В дополнение к большой емкости Li-ion аккумулятор при разряде ведет себя аналогично NiCd (форма их разрядных характеристик подобна и отличается лишь напряжением).
На сегодняшний момент существует множество разновидностей Li-ion аккумуляторов, причем можно долго говорить о преимуществах и недостатках того или иного типа, но отличить их по внешнему виду невозможно. Поэтому отметим только те достоинства и недостатки, которые свойственны всем типам этих устройств, и рассмотрим причины, вызвавшие появление на свет литий-полимерных аккумуляторов.
Технология изготовления Li-ion аккумуляторов постоянно улучшается. Она обновляется приблизительно каждые шесть месяцев, и понять, как «ведут себя» новые аккумуляторы после длительного хранения, трудно.
Словом, всем был бы Li-ion аккумулятор хорош, если бы не проблемы с обеспечением безопасности его эксплуатации и высокая стоимость. Попытки решения этих проблем и привели к появлению литий-полимерных (Li-pol или Li-polymer) аккумуляторов.
Основное их отличие от Li-ion отражено в названии и заключается в типе используемого электролита. Первоначально, в 70-х годах, применялся сухой твердый полимерный электролит, похожий на пластиковую пленку и не проводящий электрический ток, но допускающий обмен ионами (электрически заряженными атомами или группами атомов). Полимерный электролит фактически заменяет традиционный пористый сепаратор, пропитанный электролитом.
Такая конструкция упрощает процесс производства, характеризуется большей безопасностью и позволяет выпускать тонкие аккумуляторы произвольной формы. К тому же отсутствие жидкого или гелевого электролита исключает возможность воспламенения. Толщина элемента составляет около одного миллиметра, так что разработчики оборудования свободны в выборе формы, очертаний и размеров, вплоть до внедрения его во фрагменты одежды.
Но пока, к сожалению, сухие Li-polymer аккумуляторы обладают недостаточной электропроводностью при комнатной температуре. Внутреннее сопротивление их слишком высоко и не может обеспечить величину тока, необходимую для современных средств связи и электропитания жестких дисков переносных компьютеров. В то же время при нагревании до 60 °C и более электропроводность Li-polymer увеличивается до приемлемого уровня, однако для массового использования это не годится.
Исследователи продолжают разработку Li-polymer аккумуляторов с сухим твердым электролитом, работающим при комнатной температуре. Подобные аккумуляторы, как ожидается, станут коммерчески доступными к 2005 году. Они будут стабильными, допускать 1000 полных циклов заряда-разряда и иметь более высокую плотность энергии, чем сегодняшние Li-ion аккумуляторы
Тем временем некоторые виды Li-polymer аккумуляторов в настоящее время используются в качестве резервных источников питания в жарком климате. Например, часть производителей специально устанавливает нагревающие элементы, поддерживающие благоприятную для аккумулятора температуру.
Вы спросите: как же так? На рынке вовсю продают Li-polymer аккумуляторы, изготовители комплектуют ими телефоны и компьютеры, а мы тут говорим, что для коммерческой эксплуатации они пока не готовы. Все очень просто. В данном случае речь идет об аккумуляторах не с сухим твердым электролитом. Для того чтобы повысить электропроводность небольших Li-polymer аккумуляторов, в них добавляют некоторое количество гелеобразного электролита. И большинство Li-polymer аккумуляторов, используемых сегодня для мобильных телефонов, фактически являются гибридами, поскольку содержат гелеобразный электролит. Правильнее было бы их называть литий-ионными полимерными. Но большинство изготовителей в рекламных целях маркируют их просто как Li-polymer. Остановимся подробнее на этом типе литий-полимерных аккумуляторов, поскольку на данный момент именно они представляют наибольший интерес.
Итак, в чем различие между Li-ion и Li-polymer аккумулятором с добавкой гелеобразного электролита? Хотя характеристики и эффективность обеих систем во многом сходны, уникальность Li-ion полимерного (можно его и так назвать) аккумулятора заключается в том, что в нем все же используется твердый электролит, заменяющий пористый сепаратор. Гелевый электролит добавляется только для увеличения ионной электропроводности.
Технические трудности и задержка в наращивании объемов производства задержали внедрение Li-ion полимерных аккумуляторов. Это вызвано, по мнению некоторых экспертов, желанием инвесторов, вложивших большие деньги в разработку и массовое производство Li-ion аккумуляторов, получить свои инвестиции обратно. Поэтому они и не спешат переходить на новые технологии, хотя при массовом производстве Li-ion полимерные аккумуляторы будут дешевле литий-ионных.
А теперь об особенностях эксплуатации Li-ion и Li-polymer аккумуляторов.
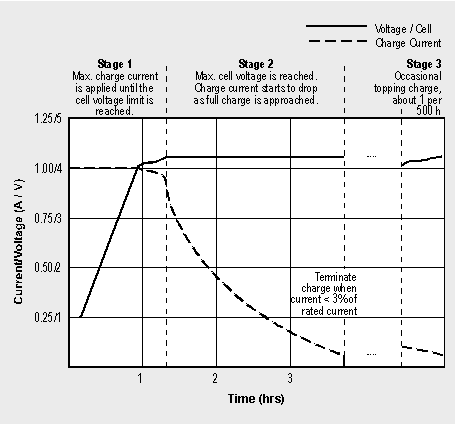
Их основные характеристики очень похожи. О заряде Li-ion аккумуляторов достаточно подробно рассказано в статье [2]. В добавление приведу лишь график (Рис.1) из [3], иллюстрирующий стадии заряда, и небольшие пояснения к нему.
Время заряда всех Li-ion аккумуляторов при начальном зарядном токе в 1С (численно равном номинальному значению емкости аккумулятора) составляет в среднем 3 часа. Полный заряд достигается при напряжении на аккумуляторе, равном верхнему порогу, и при уменьшении тока заряда до уровня, примерно равного 3% от начального значения. Аккумулятор во время заряда остается холодным. Как видно из графика, процесс заряда состоит из двух стадий. На первой (час с небольшим) напряжение растет при почти постоянном начальном токе заряда в 1С до момента первого достижения верхнего порога напряжения. К этому моменту аккумулятор заряжается примерно на 70% от своей емкости. В начале второго этапа напряжение остается почти постоянным, а ток уменьшается до тех пор, пока не достигнет вышеуказанных 3%. После этого заряд полностью прекращается.
Если требуется поддерживать аккумулятор все время в заряженном состоянии, то подзаряд рекомендуется проводить через 500 часов, или 20 дней. Обычно его проводят при уменьшении напряжения на выводах аккумулятор до 4.05 В и прекращают при достижении 4.2 В
Несколько слов о температурном диапазоне при заряде. Большинство разновидностей Li-ion аккумуляторов допускают заряд током в 1С при температуре от 5 до 45 °C. При температуре от 0 до 5 °C рекомендуется заряжать током в 0.1 С. Заряд при минусовой температуре запрещен. Для заряда оптимальна температура от 15 до 25 °C.
Зарядные процессы в Li-polymer аккумуляторах почти идентичны вышеописанным, поэтому потребителю совершенно ни к чему знать, какой их двух типов аккумуляторов у него в руках. И все те зарядные устройства, которые он использовал для Li-ion аккумуляторов, годятся для Li-polymer.
А теперь об условиях разряда. Обычно Li-ion аккумуляторы разряжают до значения 3.0 В на элемент, хотя для некоторых разновидностей нижний порог составляет 2.5 В. Производители оборудования с питанием от аккумуляторов, как правило, разрабатывают устройства с порогом выключения 3.0 В (на все случаи жизни). Что это означает? Напряжение на аккумуляторе при включенном телефоне постепенно уменьшается, и как только оно достигнет 3.0 В, аппарат предупредит вас и выключится. Однако это совсем не означает, что он перестал потреблять энергию от аккумулятора. Энергия, пусть незначительная, требуется для определения нажатия клавиши включения телефона и некоторых других функций. Кроме того, энергию потребляет собственная внутренняя схема управления и защиты, да и саморазряд, хоть и небольшой, но все же характерен даже для аккумуляторов на основе лития. В результате, если оставить литиевые аккумуляторы на длительный срок без подзарядки, напряжение на них упадет ниже 2.5 В, что очень плохо. В этом случае возможно отключение внутренней схемы управления и защиты, и не все зарядные устройства смогут зарядить такие аккумуляторы. Кроме того, глубокий разряд отрицательно сказывается на внутренней структуре самого аккумулятора. Полностью разряженный аккумулятор должен заряжаться на первом этапе током всего в 0.1C. Словом, аккумуляторы скорее любят находиться в заряженном состоянии, чем в разряженном.
Несколько слов о температурных условиях при разряде (читай во время работы).
Как правило, Li-ion аккумуляторы лучше всего функционируют при комнатной температуре. Работа в более теплых условиях серьезно сокращает срок их службы. Хотя, например, свинцово-кислотный аккумулятор имеет самую высокую емкость при температуре более 30 °C, но длительная эксплуатация в таких условиях сокращает жизнь аккумулятора. Точно так же и Li-ion лучше работают при высокой температуре, которая поначалу противодействует увеличению внутреннего сопротивления аккумулятора, являющемуся результатом старения. Но повышенная энергоотдача коротка, поскольку повышение температуры, в свою очередь, способствует ускоренному старению, сопровождаемому дальнейшим увеличением внутреннего сопротивления.
Исключение составляют на данный момент только литий-полимерные аккумуляторы с сухим твердым полимерным электролитом. Для них жизненно необходима температура от 60 °C до 100 °C. И такие аккумуляторы заняли свою нишу на рынке резервных источников в местах с жарким климатом. Они помещаются в теплоизолированный корпус со встроенными элементами нагревания, питающимися от внешней сети. Li-ion полимерные аккумуляторы в качестве резервных, как считают, превосходят по емкости и долговечности VRLA аккумуляторы, особенно в полевых условиях, когда управление температурой невозможно. Но их высокая цена остается сдерживающим фактором.
Важно не забывать, что, хотя аккумулятор и может работать при низких температурах, это совсем не означает, что он может быть также заряжен в этих условиях. Восприимчивость к заряду у большинства аккумуляторов при очень низких температурах чрезвычайно ограничена, и ток заряда в этих случаях должен быть уменьшен до 0.1C.
В заключение хочу отметить, что задать вопросы и обсудить проблемы, связанные с Li-ion, Li-polymer, а также другими типами аккумуляторов, можно на форуме [4] в подфоруме по аксессуарам.
При написании статьи использованы материалы [3], любезно предоставленные г-ном Isidor Buchmann, основателем и главой канадской компании Cadex Electronics Inc. [5].
Более подробная информация на русском языке об аккумуляторах для мобильной техники связи, компьютеров и других портативных приборов, советы по эксплуатации и обслуживанию приведены в [6].