Аксиальный спондилоартрит что это
Аксиальный спондилоартрит
Если сравнить частоту ревматических заболеваний у мужчин и женщин, то гендерное неравенство станет очевидно: женщин большинство. Но есть одно заболевание, которое значительно чаще встречается у мужчин. А при развитии у женщин оно будет протекать значительно легче.
С чем же так «повезло» мужчинам?
Прежде чем пойти дальше скажем пару слов об этих самых спондилоартритах, так как здесь есть заблуждения!
Самое главное, спондилоартрит НЕ РАВНО болезни Бехтерева!
Спондилоартриты – это группа воспалительных заболеваний, для которых характерно поражение позвоночника и/или суставов. Они объединены по механизмам их развития и похожим клиническим проявлениям. Делится эта группы на две подгруппы – аксиальный и периферический спондилоартрит. Разница в том, что при первом поражается только крестцово-подвздошные суставы и/или позвоночник, а при втором – может поражать также суставы верхних и нижних конечностей.
Кроме того, подгруппа аксиального спондилоартрита делится на анкилозирующий спондилит (это и есть болезнь Бехтерева) и не рентгенологический аксиальный спондилоартрит. Разница между ними – наличие /отсутствие поражения крестцово-подвздошных суставов на рентгенографии. Рентгенологические изменения происходят очень медленно, иногда для появления признаков «сращения» должно пройти 7-8 лет, поэтому до сих пор идут горячие споры о том, являются ли эти две формы стадиями одного процесса, или разными заболеваниями из одной группы.
Для лучшего понимания ниже будем говорить о группе аксиального спондилоартрита (АС).
Причины заболевания
Точная причина заболевания неизвестна. Спондилоартриты в отличие от ревматоидного артрита, относятся в большей степени не к аутоиммунным, а к гипервоспалительным заболеваниям. Они редко вызывают системные воспалительные реакции, а поражают определённые органы и ткани – суставы, кожу, кишечник, глаза.
Однако, когда заболевание уже проявило себя, не ищите эти таинственные микробы – скорее всего организм уже давно избавился от них, а воспаление будет продолжаться.
Мужчины страдают чаще, дебют приходится на возраст младше 45 лет. Возможно развитие АС в детском возрасте с переходом во взрослое состояние, который обычно протекает достаточно тяжело.
Симптомы
Боль может быть неявной, по типу дискомфорта или ощущения тяжести, часто сопровождается утренней скованностью (тугоподвижностью), может отдавать в ягодицы, но очень часто боль вынуждает просыпаться пациента в 4-5 часов утра.
Симптомы обычно прогрессируют очень медленно (годами и даже – десятилетиями), и пациенты часто наблюдаются с диагнозом «остеохондроз». Насторожить врача или пациента должен непреходящий характер болей, молодой возраст (до 45 лет) и отсутствие улучшения после отдыха.
Вместе с кальцифицикацией связок позвоночника это создает на рентгенограмме характерную картину «бамбуковой палки», а при внешнем осмотре врач наблюдает «позу просителя»: позвоночные изгибы сглажены, голова пациента наклонена вперёд, боковые движения в позвоночнике возможны только при повороте всего туловища. Такого пациента врачу-ревматологу видно «издалека», но, к сожалению, в этой стадии возможности терапии крайне ограничены. Поэтому современные диагностические критерии направлены на возможно более раннюю диагностику АС.
«Классическим» инструментальным исследованием является рентгенография таза, на которой выявляется двусторонний сакроилиит – воспаление крестцово-подвздошных суставов. Но симптомы на рентгенографии появляются не ранее, чем через 4-5 лет, поэтому для ранней диагностики, как залоге эффективного лечения, применяется метод МРТ. В случае, если сакроилииит выявляется на МРТ, а на рентгенографии его нет, он называется нерентгенологический. Основной признак сакроилиита – отек костного мозга в зоне, прилежащей к крестцово-подвздошным суставам.
Другие традиционные воспалительные изменения – повышение СОЭ и С-реактивного белка можно наблюдать только у 30% пациентов с АС, поэтому нормальные показатели этих анализов не исключают и не подтверждают наличие заболевания.
Еще одним проявлением со стороны опорно-двигательного аппарата может быть дактилит (в переводе-«воспаление пальца»), хотя воспаляются только сухожилия, но не суставы. При этом палец приобретает вид сосиски. Непосредственно воспаление суставов – артриты: чаще асимметричные с большим вовлечением нижних конечностей, также являются тем симптомом, который сориентирует врача на поиск HLA B-27. Кстати, если «мозаика» у конкретного пациента сложится так, что будут воспалены только периферические суставы без вовлечения позвоночника, то заболевание приобретет название «периферический спондилоартрит».
Иногда проявлением заболевания становится передний увеит – воспаление передней камеры глаза. Симптомы: выраженная боль и покраснение глаза, слезотечение, нарушение зрения (помутнение), светобоязнь. Сочетанием с АС может быть поражение кишечника, сопровождающееся болями в животе, послабленным или жидким стулом, в котором могут быть примеси слизи или крови. При колоноскопии может быть диагностирована болезнь Крона или язвенный колит. Еще одним органом-мишенью для HLA B-27 может стать кожа, поэтому врач непременно спросит про наличие псориаза.
Таким образом, сочетание жалоб и анамнеза пациента, проведение специфических тестов, анализ инструментальных и лабораторных данных позволяет врачу поставить диагноз АС и начать терапию.
Лечение
Пациенту необходимо получить от врача максимум информации и строго следовать клиническим рекомендациям. Несмотря на то, что список групп препаратов, влияющих на течение заболевания невелик, вполне возможно избежать анкилоза позвоночника и развития внесуставных осложнений со стороны других органов и систем. Очень важная роль отводится ежедневной гимнастике, которая показана абсолютно всем вне зависимости от активности заболевания и развития анкилоза. Её цель – замедление прогрессирование, профилактика и лечение деформаций, улучшение общего самочувствия. Основные упражнения – растяжение позвоночника и укрепление околопозвоночных мышц.
Если оценивать арсенал препаратов, доказанных в отношении АС (Внимание! Сейчас мы говорим только про позвоночник), то существует два основных класса лекарств.
В первую очередь, это нестероидные противовоспалительные препараты (НПВП). Они должны быть назначены пациенту сразу после установления диагноза, независимо от стадии заболевания, должны приниматься длительно и без перерывов, и способны не просто уменьшать боль, но и замедлять прогрессирование АС.
Иначе говоря, срастание позвонков между собой происходит в четыре раза медленнее по сравнению с теми пациентами, кто использовал НПВП только «по требованию». Подбор НПВП осуществляется лечащим врачом с учётом многих факторов, в том числе сопутствующих заболеваний пациента, особенностей назначения препарата и его возможных побочных эффектов.
Генно-инженерная терапия – это блокаторы ФНО-α (инфликсимаб, голимумаб, адалимумаб, цертолизумаба пэгол, этанерцепт) и антитела к интерлейкину-17 (секукинумаб, нетакимаб). Эффективны на любой стадии развития АС (но на ранней больше, чем на поздней) и для снижения активности, и для профилактики деформаций. Как правило, назначаются в том случае, если эффект от НПВП недостаточный. С учетом наличия нескольких препаратов из группы генно-инженерной терапии у врача появляются возможности «переключать» пациента на другой лекарственный препарат в случае неэффективности первого.
В том случае, если возникают внесуставные поражения глаз, кишечника или кожи, то арсенал врача в плане эффективной терапии расширяется еще больше.
Тяжелые осложнения возникают либо при позднем обращении пациента, либо при игнорировании им рекомендованного лечения.
В наше время терапия позволяет избежать быстрого и выраженного прогрессирования анкилозирующего спондилита и сделать классическую «позу просителя» достоянием истории
Аксиальный спондилит причины, симптомы, методы лечения и профилактики
Аксиальный спондилит — разновидность патологического синдрома без четкой клинической картины. На рентгенографии не диагностируется. Поражается исключительно позвоночник больного, патология не воздействует на суставы и другие органы. Характеризуется хроническим течением. Для лечения аксиального спондилита требуется обратиться к вертебрологу.
Причины аксиального спондилита
Точные провоцирующие факторы патологического синдрома установить не удалось. Врачи предполагают, что риск возникновения аксиальной формы спондилита связан с генетическим фактором. Также вероятность прогрессирования патологии увеличивается после инфекционных заболеваний мочеполовой системы или инфекций желудочно-кишечного тракта.
Статью проверил
Дата публикации: 24 Марта 2021 года
Дата проверки: 24 Марта 2021 года
Дата обновления: 21 Декабря 2021 года
Содержание статьи
Симптомы аксиального спондилита
На начальной стадии заболевания ярко выраженные симптомы отсутствуют. В дальнейшем развиваются болезненные ощущения в пораженной области, которые могут распространяться по всему позвоночнику. В других системах организма могут развиваться воспаления инфекционного типа, например, поражение желудочно-кишечного тракта.
Методы диагностики
Диагностика подразумевает комплексное обследование организма. Врач проводит осмотр пациента, назначаются: функциональные пробы, рентгенографическое обследование, анализы крови. По усмотрению доктора пациенту потребуется пройти компьютерную томографию. В сети клиник ЦМРТ мы используем такие методы для диагностики аксиального спондилита:
Спондилоартриты: трудности диагностики и возможности современных методов высокотехнологичной помощи
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
В диагностике ревматических заболеваний решающее значение имеют подробно собранные жалобы, анамнез заболевания, лабораторные и инструментальные методы исследования. От своевременно поставленного диагноза зависит правильность тактики ведения и назначаемого лечения, что обеспечивает замедление прогрессирования болезни и позволяет достичь эффективного контроля над заболеванием в динамике. В статье представлено описание клинического наблюдения поздней диагностики анкилозирующего спондилита (АС) у молодого пациента 34 лет с явлениями тяжелого коксита. Заболевание дебютировало появлением боли в левом тазобедренном суставе (ТБС). В течение двух лет пациент находился под наблюдением с диагнозом реактивного артрита неуточненной этиологии с системными проявлениями. Несмотря на проводимую терапию (преднизолон, сульфасалазин), отмечалось прогрессирование суставного синдрома.. После дополнительного обследования критериально установлен диагноз АС высокой активности (ASDASCRP — 3,03, BASDAI — 3,6), с внеаксиальными (двусторонний коксит) проявлениями, HLA-В27-позитивный. Осложнение: двусторонний коксартроз III стадии с преимущественным поражением левого ТБС с выраженным болевым синдромом. Для достижения быстрого эффекта и уменьшения прогрессирования заболевания был назначен ингибитор ФНО-α. В результате лечения достигнута низкая активность заболевания, что позволило успешно выполнить тотальное эндопротезирование левого ТБС.
Ключевые слова: анкилозирующий спондилит, коксит, коксартроз, эндопротезирование тазобедренного сустава, генно-инженерная биологическая терапия, ингибитор ФНО-α, преднизолон.
Для цитирования: Вахлевский В.В., Свинцицкая И.С., Тыренко В.В. Спондилоартриты: трудности диагностики и возможности современных методов высокотехнологичной помощи. РМЖ. 2021;7:70-73.
Spondyloarthritis: diagnostic challenges and possibilities of modern methods of high-tech medical care
V.V. Vakhlevsky, I.S. Svinitskaya, V.V. Tyrenko
S.M. Kirov Military Medical Academy, St. Petersburg
In the diagnosis of rheumatic diseases, detailed complaints, medical history, laboratory and instrumental research methods are crucial. The correctness of the treatment tactics and patient management depends on the timely diagnosis, which ensures retardation in the disease progression and allows achieving effective disease control in dynamics. The article describes a clinical case of lately diagnosed ankylosing spondylitis (AS) in a 34-year-old young patient with severe coxitis. The disease onset started with the pain occurrence in the left hip joint (HJ). For two years, the patient was under follow-up with a diagnosis of reactive arthritis of unspecified etiology with systemic manifestations. Despite the ongoing therapy (prednisolone, sulfasalazine), the articular syndrome progression was noted. After an additional examination, the diagnosis of high-activity AS (ASDASCRP — 3.03, BASDAI — 3.6), with non-axial (bilateral coxitis) manifestations, HLA-B27-positive was established criterion-wise. Complication: stage III bilateral coxarthrosis with a predominant lesion of the left HJ with severe pain syndrome. To achieve a rapid effect and reduce the disease progression, a TNF-α inhibitor was prescribed. As a result of treatment, disease low activity was achieved, which made it possible to successfully perform total left HJ replacement.
Keywords: ankylosing spondylitis, coxitis, coxarthrosis, hip replacement, genetically engineered biological therapy, TNF-α inhibitor, prednisolone.
For citation: Vakhlevsky V.V., Svinitskaya I.S., Tyrenko V.V. Spondyloarthritis: diagnostic challenges and possibilities of modern methods of high-tech medical care. RMJ. 2021;7:70–73.
Введение
Согласно современным представлениям спондилоартриты относятся к неоднородной группе заболеваний, объединенных общими патогенетическими механизмами и схожими симптомами. В соответствии с современной классификацией выделяют периферический спондилоартрит и аксиальный спондилоартрит, который, в свою очередь, подразделяется на нерентгенологический аксиальный спондилоартрит и анкилозирующий спондилит (АС) [1].
Анкилозирующий спондилит — хроническое иммуновоспалительное заболевание из группы спондилоартритов, характеризующееся обязательным поражением крестцово-подвздошных суставов (КПС) и/или позвоночника с потенциальным исходом их в анкилоз, с частым вовлечением в патологический процесс энтезисов и периферических суставов [1].
В диагностике ревматических заболеваний решающее значение имеют тщательно собранные жалобы, анамнез заболевания, данные объективных методов исследования.. Особое внимание следует уделять характеру болевого суставного синдрома. Так, при ревматических заболеваниях в большинстве случаев болевой синдром имеет воспалительный характер, в то время как для дегенеративно-дистрофических процессов характерна боль механического характера. Характеристика болевого синдрома чрезвычайно важна при дифференциальной диагностике спондилоартритов и дегенеративно-дистрофического поражения позвоночника (остеохондроза). После выявления признаков спондилоартрита его целесообразно рассматривать как недифференцированный и в дальнейшем действовать в соответствии с клиническими рекомендациями.
Диагностика АС преимущественно основывается на характерных жалобах пациента, таких как боль «воспалительного» характера в нижней части спины и других отделах позвоночного столба согласно критериям ASAS (2009), и подтвержденном лучевыми методами исследования двустороннем сакроилиите [2]. При этом такие лабораторные показатели, как СОЭ и уровень С-реактивного белка (СРБ), не имеют самостоятельного диагностического значения, но необходимы для оценки прогноза заболевания и выбора тактики ведения пациента [2, 3].
Немаловажное значение в диагностике как нерентгенологического аксиального спондилоартрита, так и АС имеют внеаксиальные проявления заболевания: периферические асимметричные моноолигоартриты, энтезиты, увеиты, дактилиты [2].
Поражение периферических суставов в дебюте АС имеет неблагоприятный прогноз, и одним из его грозных факторов при АС является коксит, приводящий к развитию осложнения в виде коксартроза, как правило, с выраженным болевым синдромом, с нарушением функции тазобедренного сустава (ТБС), что в дальнейшем требует проведения эндопротезирования.
Комплексный подход к диагностике АС и его осложнений на ранних этапах заболевания позволяет в кратчайшие сроки определить тактику ведения пациента, способствуя снижению уровня инвалидизации и повышению качества жизни пациента.
Независимо от активности заболевания, наличия осложнений безальтернативным является длительный прием различных групп НПВП как в сочетании с генно-инженерными биологическими (ингибиторы фактора некроза опухоли α (иФНО-α), ингибиторы интерлейкина-17А) и синтетическими таргетными препаратами (ингибиторы янус-киназ), так и без них [3–6]. В то же время длительное применение системных кортикостероидов не рекомендовано при лечении АС независимо от наличия внеаксиальных проявлений и характера развившихся осложнений [7].
В лечении периферических артритов следует использовать сульфасалазин (в дозе до 3 г/сут) с оценкой эффективности терапии не менее чем через 3 мес. [8, 9]. При сохранении высокой активности заболевания на фоне приема НПВП и сульфасалазина в максимально переносимых дозах рекомендовано как можно раньше назначать терапию иФНО-α или ингибиторами ИЛ-17. Эффективность генно-инженерной биологической терапии выше на ранней стадии болезни и при ее высокой активности.
Следует отметить, что у пациентов с достоверным диагнозом АС при наличии быстропрогрессирующего коксита рекомендовано инициировать терапию генно-инженерными биологическими препаратами без учета активности болезни [10, 11].
Представляем клиническое наблюдение пациента с АС с двусторонним кокситом, потребовавшим выполнения тотального эндопротезирования ТБС.
Клиническое наблюдение
Пациент Ч., 34 года. Наблюдается в клинике факультетской терапии с декабря 2020 г. Поступил с жалобами на боль в левом ТБС в покое, усиливающуюся при движении, боль в правом плечевом суставе, общую слабость.
Из анамнеза известно, что в 2018 г. впервые появилась боль в левом ТБС. По данному поводу лечился и обследовался в терапевтическом отделении с диагнозом: реактивный артрит неуточненной этиологии с системными проявлениями (снижение массы тела, анемия), полиартрит, острое течение, 3-й степени активности. Из инструментальных исследований выполнена рентгенография левого ТБС — патологии не выявлено (из выписного эпикриза), по остальным исследованиям сведения отсутствуют. Проводилось лечение: преднизолон 40 мг/сут, диклофенак 150 мг/сут, азитромицин 500 мг/сут № 3 — с положительным эффектом. В дальнейшем по рекомендации врача снизил суточную дозу преднизолона до 2,5 мг. При попытке полной его отмены проявления артрита возобновились.. В динамике, несмотря на соблюдение рекомендаций (прием преднизолона, сульфасалазина 2 г/сут), рецидивировал болевой суставной синдром в ТБС, больше слева, появилась боль в плечевых суставах, стал отмечать уменьшение мышечной массы левой нижней конечности. Последняя госпитализация в терапевтическое отделение была 26.10.2020 с диагнозом: основным — реактивный артрит неуточненной этиологии, полиартрит, острое течение, 3-й степени активности; двусторонний сакроилиит; функциональная недостаточность сустава II; сопутствующим — остеоартроз правого тазобедренного сустава 2-й степени, левого тазобедренного сустава 3-й степени.
Проведено обследование, по результатам которого выявлена высокая острофазовая активность заболевания: в клиническом анализе крови — гемоглобин 124–130 г/л, лейкоциты 10,4–14×10 9/ л, СОЭ 47–60 мм/ч, в биохимическом анализе крови — СРБ 48 мг/л, фибриноген 9,1 г/л. Также выявлены антитела (IgА) к Ureaplasma urealyticum.
По данным МРТ тазобедренных суставов (30.10.2020) выявлены изменения, характерные для двустороннего далеко зашедшего коксита с явлениями деструкции ТБС, более выраженные слева: суставная щель значительно неравномерно сужена, головка левой бедренной кости умеренно деформирована за счет уплощения суставной поверхности, по краю крыши вертлужной впадины и головки бедренной кости определяются краевые остеофиты, кортикальная пластинка по суставным поверхностям головки бедренной кости и вертлужной впадины — с наличием глубоких эрозий. Структура костного мозга головки и шейки левой бедренной кости, а также прилежащих отделов вертлужной впадины — с зонами отека трабекулярной костной ткани. Гиалиновый хрящ неравномерно истончен, визуализируется фрагментарно. В полости сустава незначительное количество выпота, синовиальная оболочка неравномерно утолщена.. Справа: хрящевой компонент истончен, МР-сигнал от него снижен, по краю крыши вертлужной впадины и головки бедренной кости определяются краевые остеофиты. Структура костного мозга головки и шейки левой бедренной кости, а также прилежащих отделов вертлужной впадины — с зонами отека трабекулярной костной ткани. Кортикальная пластинка по суставным поверхностям головки бедренной кости и вертлужной впадины — с наличием немногочисленных эрозивных дефектов.. Заключение: МР-картина остеоартроза тазобедренных суставов, справа — II стадии, слева — III стадии (снимки пациентом не представлены).
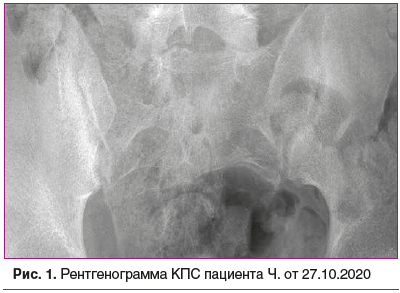
Также выполнена рентгенография КПС (27.10.2020).
На рентгенограмме (рис. 1) определяется чередование участков расширения и сужения рентгеновской суставной щели, неровность контуров КПС с обеих сторон. Выраженный субхондральный склероз подвздошной кости.. Заключение: двусторонний сакроилиит.
Проведенное лечение: преднизолон 40 мг/сут, сульфасалазин 2 г/сут — без эффекта.
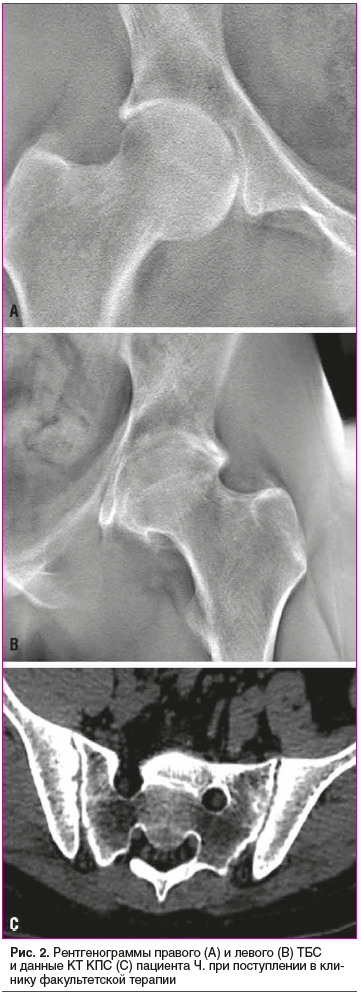
При поступлении в клинику факультетской терапии Военно-медицинской академии имени С.М. Кирова в ноябре 2020 г. дополнительно выполнена рентгенография ТБС (рис. 2, А, В).
Выявлено значительное сужение суставной щели, уплощение крыши вертлужной впадины, наличие глубоких эрозий в кортикальной пластинке по суставным поверхностям головки бедренной кости и вертлужной впадины.
Также пациенту выполнена КТ КПС (рис. 2, С). На представленных томограммах визуализируется чередование участков расширения и сужения рентгеновской суставной щели, а также множественные эрозии подвздошной кости с обеих сторон.
По результатам обследования критериально установлен диагноз: анкилозирующий спондилит, развернутая стадия, активность высокая (ASDASCRP — 3,03, BASDAI — 3,6), с внеаксиальными (двусторонний коксит) проявлениями, HLA-В27-позитивный, функциональный класс 2. Осложнение: двусторонний коксартроз III стадии с преимущественным поражением левого тазобедренного сустава с выраженным болевым синдромом. Комбинированная контрактура тазобедренных суставов.
В связи с неэффективностью комбинированной терапии НПВП и БПВП (сульфасалазин в дозе 2–3 г/сут в течение 3 мес.), быстропрогрессирующим кокситом, высокой активностью заболевания пациенту инициирована генно-инженерная биологическая терапия. Для достижения быстрого эффекта и уменьшения прогрессирования заболевания выбран иФНО-α цертолизумаба пэгол в виде двух инъекций по 200 мг в первый день, на 2-й
и на 4-й неделе лечения, в дальнейшем по 400 мг 1 р/мес. подкожно.
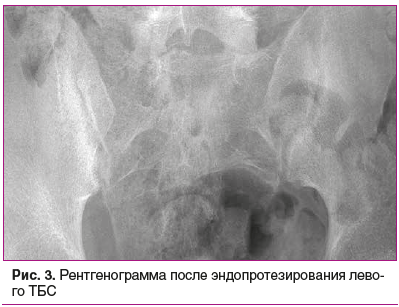
Посредством проводимой терапии в январе 2021 г. удалось достигнуть низкой активности заболевания (ASDASCRP — 0,97, BASDAI — 2,8). После достижения низкой активности заболевания в феврале 2021 г. пациенту успешно проведено эндопротезирование левого ТБС (рис. 3).
В настоящее время, согласно данным контрольного обследования, признаков прогрессирования заболевания не выявлено, клинически значительно уменьшились спондилоалгии в поясничном отделе позвоночника, увеличился объем движений в левом ТБС, острофазовая активность снизилась, продолжено динамическое наблюдение.. С учетом тяжелого поражения (анкилоз) правого ТБС в ближайшее время планируется оперативное вмешательство — тотальное эндопротезирование пораженного сустава.
Обсуждение
В рамках представленного клинического наблюдения хотелось бы акцентировать внимание на важности как можно более ранней диагностики данной патологии и своевременного назначения противовоспалительной базисной иммуносупрессивной и генно-инженерной биологической терапии, которая данному пациенту в дебюте заболевания не назначалась. Этот факт в последующем повлиял, вероятно, на быстрое прогрессирование болезни с формированием анкилоза обоих ТБС.. В конечном итоге потребовалось применение высокотехнологичных дорогостоящих методов лечения (генно-инженерная биологическая терапия, тотальное эндопротезирование суставов) с целью купирования острофазовой активности заболевания, болевого синдрома, восстановления утраченных функций ТБС. Вероятно, при более ранней диагностике данного заболевания удалось бы избежать применения тяжелого оперативного вмешательства, а также значительно уменьшить материальные затраты на лечение..
Выводы
Несвоевременное установление правильного диагноза АС приводит к быстрому прогрессированию заболевания и инвалидизации лиц молодого возраста.
Использование современных высокотехнологичных методов лечения (генно-инженерная биологическая терапия) при отсутствии эффекта от стандартной базисной терапии в сочетании с глюкокортикостероидами позволяет в сокращенные сроки замедлить прогрессирование болезни и достичь эффективного контроля над заболеванием в динамике.
Своевременно выполненное на данном этапе эндопротезирование тазобедренного сустава [12] позволило значительно улучшить качество жизни молодого пациента.