Аллергический ринит что принимать
Лечение аллергического ринита
Аллергический ринит (АР) относится к широко распространенным заболеваниям [1, 3]. За последние десятилетия во всех экономически развитых странах отмечено увеличение числа больных АР. По данным эпидемиологических исследований, проведенных в разных
Аллергический ринит (АР) относится к широко распространенным заболеваниям [1, 3]. За последние десятилетия во всех экономически развитых странах отмечено увеличение числа больных АР. По данным эпидемиологических исследований, проведенных в разных странах, распространенность АР составляет от 1 до 40%. В большинстве европейских стран 10—25% населения страдают аллергическим ринитом [8, 16, 17]. Эпидемиологические исследования, проведенные в разных регионах России, показали, что частота АР колеблется от 12 до 24% [4, 6]. Следует отметить, что многие больные не квалифицируют АР (особенно интермиттирующие формы) как заболевание и не обращаются к врачам. Тем не менее АР относится к 10 заболеваниям, по поводу которых пациенты наиболее часто обращаются за медицинской помощью [13], и представляет серьезную проблему для здравоохранения в целом [12].
АР — это заболевание, которое характеризуется аллергическим (IgE-опосредованным) воспалением слизистых оболочек носа и проявляется чиханием, зудом в полости носа, выделениями из носа и затруднением носового дыхания.
Аллергическое воспаление формируется после контакта с аллергенами. В таблице 1 приведены некоторые наиболее распространенные аллергены.
Плазматические клетки синтезируют специфические IgE-антитела, которые в дальнейшем связываются с особыми рецепторами на мембране тучных клеток и базофилов. При повторном попадании аллергена в сенсибилизированный организм происходят соединение аллергена с соответствующими аллерген-специфическими IgE-антителами, активация тучных клеток и высвобождение из них биологически активных веществ, в первую очередь гистамина, лейкотриенов, простагландинов. Ранняя фаза аллергической реакции развивается в течение нескольких минут после воздействия аллергена, клинически проявляется зудом в полости носа, чиханием, ринореей. Через 4—6 ч после начала экспозиции аллергена в результате сложного каскада реакций, миграции клеток аллергического воспаления в ткани, формируется поздняя фаза. В патогенезе поздней фазы аллергического воспаления ведущая роль принадлежит эозинофилам. К симптомам хронического аллергического воспаления относятся заложенность носа, нарушение обоняния, гиперреактивность [2, 9, 15].
Классификация АР
Традиционно АР подразделяют на сезонный (САР), круглогодичный (КАР) и профессиональный. У больных САР заболевание обусловлено аллергией к пыльце растений, у больных КАР — аллергией к бытовым аллергенам; формулировка диагноза включает указание на спектр аллергенов, выявленных у больного, и тяжесть симптомов. Данная классификация удобна и достаточно информативна. Диагноз «САР, аллергия к пыльце ольхи и березы» отражает сроки возникновения симптомов ринита (в данном случае это конец апреля-май), длительность заболевания (около трех недель), а также, косвенно, рекомендации по исключению перекрестно реагирующих продуктов питания (яблоки, морковь, лесные орехи). Данная классификация соответствует МКБ 10-го пересмотра.
В 2001 г. была предложена новая классификация АР (см. таблицу 2). По частоте возникновения симптомов выделяют интермиттирующий и персистирующий АР, по тяжести — легкий и среднетяжелый/тяжелый [8].
Лечение больных АР включает [5, 11]:
Уменьшение контакта или устранение причинного аллергена
Тяжесть течения АР непосредственно связана с концентрацией аллергенов в окружающей среде. У больных с аллергией к клещам домашней пыли симптомы АР усиливаются во время уборки в квартире; у пациентов с аллергией к эпидермальным аллергенам — при контакте с кошкой или собакой. Больные с аллергией к пыльце березы в холодное время года забывают о своем заболевании, но каждый год в период цветения березы у них вновь отмечаются симптомы АР. Уменьшение контакта с причинно-значимым аллергеном является первым и необходимым шагом в лечении больных АР. Особенно важно соблюдать элиминационный режим в тех случаях, когда имеются серьезные ограничения в проведении фармакотерапии. Это, в первую очередь, относится к беременным женщинам и людям с тяжелой сопутствующей патологией. В большинстве случаев добиться полного исключения контакта с аллергеном невозможно, однако благодаря скрупулезному выполнению рекомендаций облегчается течение заболевания, снижается потребность в лекарствах.
Мероприятия, направленные на элиминацию бытовых аллергенов
Мероприятия, направленные на элиминацию пыльцевых аллергенов
Фармакотерапия АР
При лечении АР используются следующие основные группы препаратов:
Место каждого препарата определяется его действием на разные звенья патогенеза, симптомами заболевания и их тяжестью, а также возрастом больного и наличием у него заболеваний, ограничивающих назначение тех или иных лекарственных средств [2, 8].
В лечении АР важное место принадлежит антигистаминным (АГ) препаратам, что определяется ролью гистамина в формировании клинических проявлений заболевания. Механизм их действия основывается на предупреждении патологических эффектов гистамина, который высвобождается из тучных клеток и базофилов в ранней фазе аллергической реакции [23, 24, 25].
При приеме АГ-препаратов у больных значительно уменьшаются такие симптомы аллергического ринита, как зуд в носу, чихание, ринорея. Эффективны эти препараты и при сопутствующем аллергическом конъюнктивите.
Хорошо известны преимущества и недостатки блокаторов Н1-рецепторов первого и второго поколений. Седативный эффект, свойственный первой генерации антигистаминных препаратов, существенно ограничивает их применение. Особенно важно это помнить при назначении данных лекарственных средств больным, чья профессиональная деятельность требует концентрации внимания, быстрого принятия решений, а также студентам и школьникам — в связи со снижением способности к обучению, восприятию новых знаний. С осторожностью АГ-препараты первой генерации следует назначать больным глаукомой, гипертрофией простаты, при тяжелых поражениях печени. Учитывая конкурентную блокаду Н1-рецепторов антигистаминными препаратами первой генерации, для достижения клинического эффекта требуется назначение относительно более высоких доз при увеличении кратности приема до трех-четырех раз в сутки.
Новые АГ-препараты обладают значительными преимуществами по сравнению с препаратами первого поколения. Их характеризует высокая специфичность и сродство к Н1-рецепторам гистамина, а также низкая способность к проникновению через гематоэнцефалический барьер; другими словами, эти препараты лишены большинства недостатков, характерных для ранних АГ- средств. Их характеризует быстрое начало и длительное (24 ч) действие, отсутствие либо минимальный седативный эффект; к ним не развивается привыкание (тахифилаксия), поэтому возможен длительный прием одного препарата без снижения его клинической эффективности.
Разработаны топические Н1-блокаторы в форме назального спрея и глазных капель. Топические антигистаминные препараты характеризуются быстрым началом действия и минимальными нежелательными эффектами.
Современные топические глюкокортикостероиды (ТГКС) для интраназального введения являются высокоэффективными средствами лечения АР. Они обладают выраженным противовоспалительным действием и оказывают влияние как на раннюю, так и на позднюю фазы аллергического воспаления. Проведенные исследования показали, что ТГКС по эффективности превосходят АГ-препараты и оказывают более выраженный терапевтический эффект в отношении всех симптомов АР. Следует особо подчеркнуть, что назальные ГКС наиболее действенны у больных с затруднением носового дыхания и нарушением обоняния [2, 14, 18].
Интересные данные были получены в ходе исследования, проведенного в странах Западной Европы. Оценивалась эффективность двух терапевтических подходов к лечению САР. Больные первой группы (224 пациента) получали лечение в соответствии с рекомендациями Международного консенсуса по АР, больным второй группы (241 человек) терапия назначалась по усмотрению врача. В результате в первой группе лечение оказалось более эффективным. Более выраженное облегчение всех симптомов АР и улучшение качества жизни были связаны с высокой частотой назначения топических ГКС у больных со среднетяжелым и тяжелым течением болезни — 84%. Во второй группе лечение АР, в соответствии с Международным консенсусом, было назначено только 20% больным. У наибольшего числа больных применялись АГ-препараты второй генерации, вне зависимости от тяжести симптомов. Топические ГКС назначались изолированно или в комбинации с другими препаратами только в 32% случаях [7].
Таким образом, исследование подтвердило высокую клиническую эффективность рекомендаций по лечению АР и еще раз продемонстрировало, что топические глюкокортикостероиды являются препаратами первого выбора у больных АР средней и высокой степени тяжести.
Препараты кромогликата натрия относятся к средствам, обладающим низкой противовоспалительной активностью. Наиболее широкое применение они нашли в педиатрии — в связи с высокой степенью безопасности.
Топические сосудосуживающие препараты (деконгестанты) быстро и эффективно восстанавливают носовое дыхание при АР, не оказывая положительного влияния на патогенетические механизмы болезни. В связи с быстрым облегчением носового дыхания деконгестанты очень удобны для больных, однако их прием быстро приводит к развитию тахифилаксии, больным постоянно требуется все большая доза лекарства для достижения эффекта. Назначение деконгестантов возможно при выраженной заложенности носа в течение очень короткого промежутка времени. Длительное, более 7—10 дней, лечение сосудосуживающими препаратами только усугубляет отек слизистой носа, приводит к развитию медикаментозного ринита.
Основной задачей лекарственной терапии АР является достижение полного (оптимального) контроля над симптомами заболевания. Исходя из этого, лечение строится с учетом тяжести и частоты возникновения симптомов ринита.
Течение АР определяется как легкое в тех случаях, когда симптомы АР не влияют на сон и дневную активность больного, а также на профессиональную деятельность и учебу.
При среднетяжелой форме заболевания нарушаются сон и повседневная активность больного, ухудшается качество жизни.
Тяжелая форма АР подразумевает наличие у больного мучительных симптомов, которые не дают возможности нормально спать, работать, заниматься спортом, отдыхать.
Тактика ведения больных с интермиттирующим и персистирующим АР представлена на рисунках 1 и 2.
 |
| Рисунок 1. Лечение персистирующего (преимущественно круглогодичного) аллергического ринита |
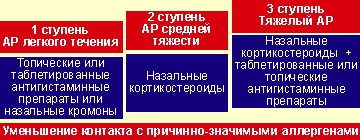 |
| Рисунок 2.Лечение итермиттирующего (преимущественно сезонного) аллергического ринита |
После проведения мероприятий, направленных на уменьшение контакта с аллергенами и достижения клинического эффекта в результате рациональной фармакотерапии, необходимо рассмотреть возможность проведения больным аллерген-специфической иммунотерапии.
Аллерген-специфическая иммунотерапия
Особое место в лечении больных АР занимает аллерген-специфическая иммунотерапия (АСИТ). Она представляет собой введение в возрастающих дозах в организм больного того аллергена, к которому у больного имеется повышенная чувствительность. Этот метод впервые применили Нун и Фриман в 1911 г. для лечения поллиноза. Учеными было показано, что в результате инъекции больному поллинозом экстракта пыльцы трав до сезона цветения растений было отмечено ослабление или полное исчезновение симптомов болезни в период цветения растений. В настоящее время многочисленные исследования подтверждают достоверность этих первых опытов [10, 15, 19].
АСИТ — это высокоэффективный и единственный из существующих методов лечения аллергических заболеваний, влияющих на характер реакции организма на аллерген. Под воздействием лечения происходит изменение соотношения Т-клеток в сторону активации Тh-1 и угнетения Тh-2, подавление продукции IL-4 и в конечном итоге — синтеза IgE.
В результате АСИТ существенно уменьшаются клинические симптомы АР, снижается потребность в медикаментах, наступает длительная ремиссия заболевания. Важным преимуществом АСИТ является профилактический эффект — своевременно начатое и последовательно проводимое лечение предупреждает формирование бронхиальной астмы [16, 20, 22, 24].
АСИТ проводится несколькими методами: парентеральным, сублингвальным, интраназальным. Вопрос о возможности назначении АСИТ, способе введения аллергена и схеме терапии в каждом конкретном случае решает врач аллерголог. Лечение обычно бывает длительным — от трех до пяти лет — и проводится только в специализированных аллергологических кабинетах, а также аллергологических отделениях стационаров.
Литература
И. В. Сидоренко, доктор медицинских наук
ММА им. И. М. Сеченова, Москва
Лечение аллергического круглогодичного ринита антигистаминными препаратами
Люди каждый день сталкиваются с аллергенами, способными вызывать ринорею, чихание, заложенность носа — симптомы ринита. Аллергический ринит сегодня рассматривается как наиболее распространенное заболевание в структуре аллергопатологии. Известно, что част
Люди каждый день сталкиваются с аллергенами, способными вызывать ринорею, чихание, заложенность носа — симптомы ринита. Аллергический ринит сегодня рассматривается как наиболее распространенное заболевание в структуре аллергопатологии. Известно, что частота встречаемости аллергического ринита в общей популяции составляет от 10 до 25% и характеризуется устойчивым ростом [4]. Это означает, что ежедневно миллионы людей вынуждены использовать медикаментозные препараты для купирования беспокоящих их симптомов. Хотя современные противоаллергические средства позволяют эффективно контролировать течение болезни, однако они способны вызывать также различные нежелательные реакции. В связи с этим очень важен правильный выбор медикаментов для лечения аллергического ринита, особенно при круглогодичном течении этого заболевания.
Круглогодичный аллергический ринит (КАР) — это заболевание, диагностика, а также подбор безопасной и эффективной терапии которого сопряжены с рядом проблем. Большинство пациентов с КАР обращаются за квалифицированной медицинской помощью через 5–10 лет от начала заболевания. В течение этого времени многие из них используют сосудосуживающие капли, прибегают к хирургическим вмешательствам. По данным исследователей из Великобритании и Нидерландов (W. J. Fokkens, G. K. Scadding, 2004), до 20% аденотомий проводится пациентам, страдающим КАР. Между тем при отсутствии, а также неадекватном лечении КАР возрастает риск развития средних отитов, синуситов, бронхиальной астмы [9].
В настоящее время, согласно международным консенсусам и рекомендациям, для лечения КАР используют препараты кромогликата натрия, назальные кортикостероиды и антигистаминные средства, применению которых и посвящена эта статья.
Широкое использование антагонистов Н1-рецепторов в качестве противоаллергических средств объясняется важнейшей ролью гистамина в патогенезе большинства симптомов аллергических заболеваний [1]. Хотя клинические проявления аллергического ринита обусловлены тем или иным набором медиаторов аллергии, только гистамин через стимуляцию Н1-рецепторов участвует практически во всех симптомах. Исключение составляет лишь поздняя фаза аллергического ответа — поддержание аллергического воспаления и связанная с этим гиперреактивность слизистых (см. табл.).
Более 60 лет назад первые антигистаминные препараты стали доступны для клинического использования. С тех пор они представляют собой наиболее востребованную группу противоаллергических фармацевтических средств, широкое применение которых научно обоснованно [2]. Антагонисты Н1-рецепторов — это азотистые основания, содержащие алифатическую боковую цепь замещенного этиламина (как и в молекуле гистамина), которая является важнейшей для проявления противогистаминной активности. Боковая цепь присоединена посредством атома азота, углерода или кислорода к одному или двум циклическим или гетероциклическим кольцам. Классические Н1-антагонисты, или первое поколение антигистаминных препаратов (дифенгидрамин, хлоропирамин, клемастин, прометазин, мебгидролин, диметинден, ципрогептадин и др.), являются конкурентными блокаторами Н1-рецепторов, и потому связывание их с рецептором происходит быстро и носит обратимый характер. В связи с этим для достижения основного фармакологического действия требуются высокие дозы таких антагонистов, при этом чаще и интенсивнее проявляются их побочные свойства. Кроме того, кратковременность действия этих препаратов требует их многократного применения в течение суток. Антигистаминные препараты первого поколения в терапевтических дозах оказывают блокирующее действие и на рецепторы других медиаторов (холинорецепторы, адренорецепторы), что объясняет связанные с их применением нежелательные побочные эффекты, в частности негативное воздействие на сердечно-сосудистую систему, зрение, мочевыводящую систему, желудочно-кишечный тракт, центральную нервную систему [7].
Вместе с тем Н1-антагонисты первого поколения, во всяком случае в ближайшее время, останутся в арсенале лекарственных средств широкого клинического применения. Это связано, во-первых, с накопленным богатым опытом использования этих препаратов и, во-вторых, как ни странно, с побочными действиями, которые в определенной клинической ситуации могут оказаться желательными (наличие, в частности, антисеротониновой активности, седативного или местно-анестезирующего действия). В-третьих, это объясняется наличием инъекционных лекарственных форм, абсолютно необходимых для лечения острых и неотложных аллергических состояний. В-четвертых — относительно более низкой стоимостью по сравнению с препаратами последнего поколения. Кроме того, появившиеся в последнее время сведения позволяют расширить клинические показания для использования препаратов первого поколения. Так, они оказались эффективными (по-видимому, за счет своего действия на М-холинорецепторы, приводящего к подсушиванию слизистых и подавлению рефлекса чихания) и у пациентов с ринитами при риновирусных инфекциях, у которых они уменьшают выделение слизи, частоту чиханий и несколько подавляют заложенность носа. Это показано на примере бромфенирамина, клемастина и хлоропирамина [5, 12].
Тем не менее, в силу вышесказанного, возникла необходимость создания противогистаминных препаратов, которые имели бы высокое сродство к Н1-рецепторам и обладали бы высокой избирательной активностью, не затрагивая рецепторов других медиаторов. Эта цель была достигнута в конце 70-х годов прошлого века, когда были созданы антагонисты Н1-рецепторов нового поколения (терфенадин, цетиризин, астемизол, лоратадин, эбастин и некоторые другие), которые соответствовали заданным фармакологическим свойствам, надежно блокировали Н1-рецепторы и могли использоваться однократно в сутки. Многие Н1-антагонисты последнего поколения связываются с рецепторами неконкурентно. Такие соединения с трудом вытесняются с рецептора, чем объясняется продолжительное действие таких препаратов. Препараты второго поколения, в отличие от своих предшественников, не имели побочных эффектов, в частности не оказывали или оказывали крайне незначительное седативное воздействие. Эти средства вошли в широкую практику врачей-аллергологов и других специалистов, стали весьма популярны во всем мире, в том числе в нашей стране [6]. Широко известен в России лоратадин, представленный в аптечной сети под разными торговыми названиями (кларитин, кларотадин, кларисенс, кларидол и др.). Этот препарат назначается однократно в дозе 10 мг/сут, не оказывает побочных кардиотоксических эффектов и не вызывает седации, он разрешен к применению с раннего детского возраста в связи с широким профилем безопасности. Но лоратадин, как и некоторые другие средства второго поколения антигистаминных средств, имеет некоторые ограничения, связанные с его применением в сочетании с другими препаратами (макролиды, кетоконазол и некоторые другие).
Именно поэтому встал вопрос о необходимости совершенствования и этой группы препаратов. Большинство из них представляют собой пролекарства, т. е. при поступлении в организм человека подвергаются метаболизму и лишь конечные продукты оказывают основное фармакологическое действие — осуществляют блокаду Н1-рецепторов. Если по какой-либо причине метаболизм лекарственного средства оказывается нарушен, происходит накопление исходного продукта, который может обладать нежелательными эффектами. Именно это произошло с терфенадином и астемизолом, которые при превышении рекомендованных терапевтических доз или нарушении метаболизма, вследствие поражения печени, либо при сопутствующем приеме препаратов, угнетающих активность ферментов, участвующих в превращении указанных пролекарств в конечные метаболиты, вызывали нарушения сердечного ритма, в некоторых случаях заканчивавшиеся смертельным исходом.
Оптимальным направлением работы по улучшению профиля антигистаминных препаратов явилось создание лекарственных средств на основе фармакологически активных конечных метаболитов препаратов второго поколения. Они должны были сохранить все преимущества своих предшественников и при этом не оказывать побочных действий на сердечно-сосудистую систему, а также не взаимодействовать с препаратами, угнетающими систему цитохрома Р450.
Первым антигистаминным средством, крайне незначительно подвергающимся метаболизму, был цетиризин (аналергин, зиртек, зодак, летизен, цетрин). Следы метаболита цетиризина появляются в плазме через 10 ч. Период полуэлиминации цетиризина у взрослых после однократного приема 10 мг препарата составляет 7–11 ч. У пожилых людей этот показатель несколько выше, что связано с особенностью функционирования почек. Для цетиризина характерны низкий объем распределения и высокая способность проникновения в кожу. При курсовом лечении постоянная концентрация в плазме достигается в течение 3 сут, а при дальнейшем применении не наступает аккумуляции препарата и не изменяется скорость элиминации.
Создание фексофенадина (телфаст, фексадин, фексофаст) было примером целенаправленного получения неметаболизируемого Н1-антагониста на основе конечного фармакологически активного метаболита терфенадина. Этот препарат быстро абсорбируется из желудочно-кишечного тракта, выводится в неизмененном виде с желчью через желудочно-кишечный тракт и с мочой через почки. Период полуэлиминации соответствует 11–15 ч. Поскольку это лекарственное средство не метаболизируется в организме, возможно его одномоментное применение с другими препаратами, тормозящими оксигеназную активность CYP3А4 системы цитохрома Р450 (макролидами, кетоконазолом и др.). Нарушение функциональной активности печени и почек не сказывается на переносимости фексофенадина; кроме того, он хорошо переносится пациентами разных возрастных групп.
В последние годы на фармацевтическом рынке России появился еще один препарат, являющийся хотя и не конечным, но фармакологически активным метаболитом лоратодина, — дезлоратадин (эриус), который используется в меньшей дозе (5 мг/сут), чем его предшественник (лоратадин). Дезлоратадин обладает всеми достоинствами антигистаминных средств последнего поколения, доказаны его эффективность при аллергическом рините и высокий уровень безопасности, что позволяет рекомендовать препарат к применению и в педиатрической практике.
Эбастин (кестин) представляет собой не рацемическую смесь (как большинство системных антигистаминных препаратов), а является единственным соединением. Через 2,5 ч после однократного приема 10 мг эбастина пиковая концентрация каребастина (фармакологически активного метаболита) в плазме крови соответствует 0,12 мг/л. Прием пищи не влияет на скорость наступления клинического эффекта, при этом абсорбция эбастина из желудочно-кишечного тракта несколько ускоряется. Основной путь экскреции каребастина — через почки, в меньшей степени — с калом. Конечный период полувыведения — 13–15 ч; он сопоставим у молодых и у пожилых лиц, что позволяет принимать препарат без коррекции дозы в зависимости от возраста. Нарушение функции печени и почек оказывает минимальное влияние на фармакокинетику каребастина. В дозах (60 мг/сут), в 3–6 раз превышающих терапевтические, эбастин не оказывает заметного действия на интервал QT. Не обнаружено взаимодействия каребастина с этанолом и диазепамом, что избавляет пациента от необходимости менять образ жизни или корректировать проводимое по поводу других заболеваний лечение. Терапевтический эффект препарата может быть повышен путем увеличения дозы с 10 до 20 мг/сут при однократном приеме. При этом сохраняется хорошая переносимость препарата, отсутствуют нежелательные явления. Эбастин эффективно угнетает не только ринорею, но и заложенность носа, т. е. симптом, который обычно с трудом поддается коррекции противогистаминными препаратами.
Опыт широкого медицинского применения антигистаминных препаратов нового поколения не только подтвердил их безопасность и терапевтическую эффективность, но и позволил обнаружить важные противоаллергические свойства, которые не могут быть объяснены только блокадой Н1-рецепторов. Так, оказалось, что у пациентов с аллергическим ринитом на фоне приема этих средств уменьшается заложенность носа — симптом, который не поддается угнетению антигистаминными препаратами первого поколения, т. е. Н1-блокаторы второго поколения (цетиризин, эбастин, фексофенадин, дезлоратадин) способны подавлять не только раннюю, но и позднюю фазы аллергического ответа. Несколькими группами исследователей было показано, что эти медикаменты тормозят активность разных клеток, вовлекаемых в аллергическую реакцию, тем самым угнетая образование и секрецию из них молекулярных посредников (медиаторов) аллергии [1]. Очень важно, что данные лекарственные средства в концентрациях, сопоставимых с таковыми в плазме крови человека при принятии средней терапевтической дозы, не теряют вышеописанных свойств.
Улучшение фармакологических свойств новых Н1-антагонистов обосновывает расширение клинических показаний для их использования. Так, с появлением антигистаминных средств второго поколения были устранены препятствия для их применения при бронхиальной астме. Дело в том, что препараты первого поколения, имеющие невысокую избирательность по отношению к рецепторам, вызывают сухость слизистых и ухудшают отхождение и без того вязкой мокроты у таких больных. Н1-антагонисты, не имеющие такого побочного действия, начали использоваться у пациентов с бронхиальной астмой для лечения ринита и других аллергических проявлений. С одной стороны, стали вновь предприниматься попытки лечения собственно астмы антигистаминными препаратами, а с другой — ученым удалось доказать, что адекватное лечение аллергического ринита сопровождается улучшением течения бронхиальной астмы, включая снижение потребности в использовании бронхолитических средств. Выбирая средство для лечения пациента, страдающего аллергическим ринитом, врач обязательно учитывает такой фактор, как индивидуальная чувствительность к фармакологическому действию одного и того же вещества [3]. С одной стороны, подбор оптимального для данного пациента препарата всегда осуществляется индивидуально, с другой — этим определяется необходимость присутствия на фармацевтическом рынке большого числа препаратов сходного действия. Для Н1-антагонистов это особенно важно, так как в случае лечения заболеваний круглогодичного течения, к которым относится аллергический ринит с повышенной чувствительностью к бытовым, эпидермальным, грибковым аллергенам, принимать эти лекарства приходится на протяжении длительного времени.
При круглогодичном аллергическом рините используются и местные топические антигистаминные средства, такие, как аллергодил (второе поколение), виброцил, санорин-аналергин.
С учетом вышеизложенного следует подчеркнуть, что для лечения аллергического ринита круглогодичного течения необходимо использовать неседативные антигистаминные средства второго поколения, обладающие высоким терапевтическим индексом, позволяющие при необходимости лабильно изменять дозу препарата без риска развития серьезных нежелательных явлений.
Литература
И. С. Гущин, доктор медицинских наук, профессор, член-корреспондент РАМН
О. М. Курбачева, кандидат медицинских наук
ГНЦ Институт иммунологии МЗ РФ, Москва

