Аллергия на хлоропирамин что делать
ХЛОРОПИРАМИН
Лекарственная форма: ТАБ
Производители
Инструкция по применению
Состав
Состав на 1 таблетку:
Описание
круглые плоские таблетки белого или почти белого цвета, без или почти без запаха, с крестообразной риской с одной стороны и фасками с двух сторон.
Фармакотерапевтическая группа
Фармакодинамика
Блокатор H1-гистаминовых рецепторов, оказывает аптигистаминное и м-холиноблокирующее действие, обладает противорвотным эффектом, умеренной спазмолитической и периферической холиноблокирующей активностью
Фармакокинетика
Показания
Крапивница, сывороточная болезнь, сезонный и круглогодичный аллергический ринит, конъюнктивит, контактный дерматит, кожный зуд, острая и хроническая экзема, атопический дерматит, пищевая и лекарственная аллергия, аллергические реакции на укусы насекомых. Ангионевротический отек (в качестве вспомогательного средства).
Противопоказания
Повышенная чувствительность к хлоропирамину и другим компонентам препарата, беременность, период лактации, детский возраст до 3-х лет, непереносимость лактозы, дефицит лактазы или глюкозо-галактазиая мальабсорбция, приступ бронхиальной астмы.
С осторожностью
Закрытоугольная глаукома, задержка мочи, гиперплазия предстательной железы, нарушение функции печени и/или почек, язвенная болезнь желудка в стадии обострения, сердечно-сосудистые заболевания, пожилые пациенты, истощенные пациенты, дыхательная недостаточность, одновременный прием ингибиторов моноаминооксидазы (МАО) и других лекарственных средств, угнетающих центральную нервную систему.
Беременность и лактация
Хлоропирамин противопоказан при беременности.
При необходимости применения препарата в период лактации следует решить вопрос о прекращении грудного вскармливания
Способы применения и дозы
Внутрь, во время еды, не разжевывая и запивая достаточным количеством воды.
Пациенты с нарушением функции почек: может потребоваться изменение режима приема препарата и снижение дозы в связи с тем, что активный компонент в основном выделяется через почки.
Продолжительность курса лечения зависит от симптомов заболевания, его длительности и течения.
Побочные эффекты
— Со стороны центральной нервной системы (ЦНС): сонливость, слабость, утомляемость, головокружение, головная боль, нервное возбуждение, тремор, эйфория, нарушения координации движений, судороги, энцефалопатия.
— Со стороны органов желудочно-кишечного тракта: дискомфорт в животе, боль в верхней части живота, сухость слизистой оболочки полости рта, тошнота, рвота, диарея, запор, потеря или повышение аппетита.
— Со стороны сердечно-сосудистой системы: снижение артериального давления, тахикардия, аритмия.
— Со стороны органа зрения: нечеткость зрительного восприятия, глаукома, повышение внутриглазного давления.
— Со стороны кроветворения: лейкопения, агранулоцитоз, гемолитическая анемия и другие патологические изменения клеточного состава крови.
— Прочее: затрудненное мочеиспускание, задержка мочи, мышечная слабость, фотосенсибилизация, аллергические реакции.
При возникновении побочных действий необходимо прекратить прием препарата и срочно обратиться к врачу.
Передозировка
Взаимодействие
Ингибиторы МАО могут усиливать и продлевать антихолинергическое действие хлоронирамина. Усиливает действие лекарственных средств для общей анестезии, снотворных, седативных, транквилизаторов, анальгетиков (в т.ч. опиоидных), местных анестетиков, атропина, симнаголитиков, барбитуратов, М-холиноблокаторов. Одновременное применение с этанолом не рекомендуется (риск тяжелого угнетения ЦНС). Трициклические антидепрессанты усиливают м-холиноблокирующее и угнетающее действие на ЦНС. Кофеин уменьшает угнетающее действие на ЦНС. Антигистаминные средства могут препятствовать проявлению реакции при постановке кожных аллергологических проб, поэтому за несколько дней до планируемого проведения теста прием препаратов этого типа следует прекратить. Хлоропирамин может маскировать признаки осложнений, вероятных при лечении ототоксическими препаратами в случае их одновременного применения.
Особые указания
При сочетании с ототоксическими препаратами хлоропирамин может маскировать ранние признаки ототоксичности. Заболевание печени и почек могут потребовать изменения (снижения) дозы препарата. Прием препарата на ночь может усиливать симптомы рефлюкс- эзофагита. Недопустимо одновременное употребление этанола (алкогольных напитков). Длительный прием антигистаминных препаратов может привести к нарушениям кроветворения (лейкопения, агранулоцитоз, тромбоцитопения, гемолитическая анемия). Если во время длительного приема препарата наблюдается необъяснимое повышение температуры тела, ларингит, бледность кожных покровов, желтуха, образование язв во рту, появление гематом, необычные и длительно продолжающиеся кровотечения, необходимо провести анализ для определения числа форменных элементов крови. Если результаты анализа указывают на изменение формулы крови, прием препарата прекращают.
Влияние на способность управлять трансп. ср. и мех.
Хлоропирамин, особенно в начальном периоде лечения, может вызвать сонливость, утомляемость и головокружение. Поэтому в начальном периоде, длительность которого определяется индивидуально, запрещается вождение транспортных средств или выполнение работ, связанных с повышенным риском несчастных случаев. После этого степень ограничения на вождение транспорта и работу с механизмами врач должен определять для каждого пациента индивидуально.
Терапия острых аллергических состояний на догоспитальном этапе
К острым аллергическим заболеваниям относят анафилактический шок, обострение (приступ) бронхиальной астмы, острый стеноз гортани, отек Квинке, крапивницу, обострение аллергического конъюнктивита и/или аллергического ринита. Считается, что аллергическими
К острым аллергическим заболеваниям относят анафилактический шок, обострение (приступ) бронхиальной астмы, острый стеноз гортани, отек Квинке, крапивницу, обострение аллергического конъюнктивита и/или аллергического ринита. Считается, что аллергическими заболеваниями страдает в среднем около 10% населения земного шара. Особую тревогу вызывают данные ННПО скорой медицинской помощи, согласно которым за последние 3 года число вызовов по поводу острых аллергических заболеваний в целом по РФ возросло на 18%.
Основные причины возникновения и патогенез
Патогенез аллергических реакций на сегодняшний день достаточно полно изучен и подробно описан во многих отечественных и зарубежных монографиях по аллергологии и клинической иммунологии. Центральная роль в реализации иммунопатологических реакций принадлежит иммуноглобулинам класса Е (IgE), связывание которых с антигеном приводит к выбросу из тучных клеток медиаторов аллергии (гистамина, серотонина, цитокинов и др.).
Наиболее часто аллергические реакции развиваются при воздействии ингаляционных аллергенов жилищ, эпидермальных, пыльцевых, пищевых аллергенов, лекарственных средств, антигенов паразитов, а также при укусах насекомых. Лекарственная аллергия чаще всего развивается при применении анальгетиков, сульфаниламидов и антибиотиков из группы пенициллинов, реже цефалоспоринов (при этом следует учитывать риск перекрестной сенсибилизации к пенициллину и цефалоспоринам, составляющий от 2 до 25%). Кроме того, в настоящее время возросло число случаев развития латексной аллергии.
Клиническая картина, классификация и диагностические критерии
С точки зрения определения объема необходимой лекарственной терапии на догоспитальном этапе оказания помощи и оценки прогноза острые аллергические заболевания можно подразделить на легкие (аллергический ринит — круглогодичный или сезонный, аллергический конъюнктивит — круглогодичный или сезонный, крапивница), средней тяжести и тяжелые (генерализованная крапивница, отек Квинке, острый стеноз гортани, среднетяжелое обострение бронхиальной астмы, анафилактический шок). Классификация и клиническая картина острых аллергических заболеваний представлены в табл. 1.
При анализе клинической картины аллергической реакции врач СМП должен получить ответы на следующие вопросы (табл. 2).
При начальном осмотре на догоспитальном этапе следует оценить наличие стридора, диспноэ, свистящего дыхания, одышки или апноэ; гипотензии или синкопе; изменений на коже (высыпаний по типу крапивницы, отека Квинке, гиперемии, зуда); гастроинтестинальных проявлений (тошноты, болей в животе, диареи); изменений сознания. Если у больного отмечаются стридор, выраженная одышка, гипотензия, аритмия, судороги, потеря сознания или шок, то данное состояние рассматривается как угрожающее жизни.
Лечение острых аллергических заболеваний
При острых аллергических заболеваниях на догоспитальном этапе неотложная терапия строится по следующим направлениям:
Прекращение дальнейшего поступления в организм предполагаемого аллергена.
Например, в случае реакции на лекарственный препарат, введенный парентерально, или при укусах насекомых — наложение жгута выше места инъекции (или укуса) на 25 мин (каждые 10 мин необходимо ослаблять жгут на 1-2 мин); к месту инъекции или укуса прикладывается лед или грелка с холодной водой на 15 мин; обкалывание в 5-6 точках и инфильтрация места инъекции или укуса 0,3-0,5 мл 0,1%-ного раствора адреналина с 4,5 мл изотонического раствора хлорида натрия.
Противоаллергическая терапия (антигистаминными препаратами или глюкокортикостероидами).
Введение антигистаминных препаратов (блокаторов Н1-гистаминовых рецепторов) показано при аллергическом рините, аллергическом конъюнктивите, крапивнице. Выделяют классические антигистаминные препараты (например, супрастин, димедрол) и препараты нового поколения (семпрекс, телфаст, кларотадин и др.). Необходимо отметить, что для классических антигистаминных препаратов в отличие от препаратов нового поколения характерно короткое время воздействия при относительно быстром наступлении клинического эффекта; многие из этих средств выпускаются в парентеральных формах. Антигистаминные препараты нового поколения лишены кардиотоксического действия, конкурентно влияют на гистамин, не метаболизируются печенью (например, фармакокинетика семпрекса не меняется даже у больных с нарушенными функциями печени и почек) и не вызывают тахифилаксии. Эти препараты обладают длительным воздействием и предназначаются для приема внутрь.
При анафилактическом шоке и при отеке Квинке (в последнем случае — препарат выбора) внутривенно вводится преднизолон (взрослым — 60-150 мг, детям — из расчета 2 мг на 1 кг массы тела). При генерализованной крапивнице или при сочетании крапивницы с отеком Квинке высокоэффективен бетаметазон (дипроспан в дозе 1-2 мл внутримышечно), состоящий из динатрия фосфата (обеспечивает быстрое достижение эффекта) и дипропионата бетаметазона (обусловливает пролонгированное действие). Для лечения бронхиальной астмы, аллергического ринита, аллергического конъюнктивита разработаны топические формы глюкокортикостероидов (флутиказон, будесонид). При отеке Квинке для предупреждения влияния на ткани гистамина необходимо комбинировать антигистаминные препараты нового поколения (семпрекс, кларитин, кларотадин) с глюкокортикостероидами (ГКС).
Побочные эффекты системных ГКС — артериальная гипертензия, повышенное возбуждение, аритмия, язвенные кровотечения. Побочные эффекты топических ГКС — осиплость голоса, нарушение микрофлоры с дальнейшим развитием кандидоза слизистых, при применении высоких доз — атрофия кожи, гинекомастия, прибавка массы тела и др. Противопоказания: язвенная болезнь желудка и 12-перстной кишки, тяжелая форма артериальной гипертензии, почечная недостаточность, повышенная чувствительность к глюкокортикоидам в анамнезе.
Симптоматическая терапия.
При развитии бронхоспазма показано ингаляционное введение b2-агонистов и других бронхолитических и противовоспалительных препаратов (беродуала, атровента, вентолина, пульмикорта) через небулайзер. Коррекцию артериальной гипотонии и восполнение объема циркулирующей крови проводят с помощью введения солевых и коллоидных растворов (изотонического раствора хлорида натрия — 500-1000 мл, стабизола — 500 мл, полиглюкина — 400 мл). Применение вазопрессорных аминов (допамина — 400 мг на 500 мл 5%-ной глюкозы, норадреналина — 0,2-2 мл на 500 мл 5%-ного раствора глюкозы, доза титруется до достижения уровня систолического давления 90 мм рт. ст.) возможно только после восполнения ОЦК. При брадикардии допускается введение атропина в дозе 0,3-0,5 мг подкожно (при необходимости инъекцию повторяют каждые 10 мин). При наличии цианоза, диспноэ, сухих хрипов показана также кислородотерапия.
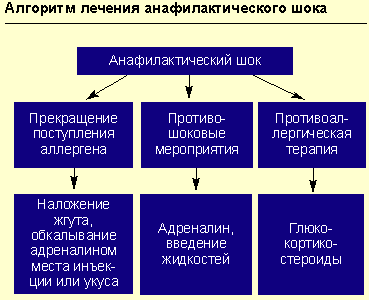
Противошоковые мероприятия (см. рисунок).
При анафилактическом шоке больного следует уложить (голова ниже ног), повернуть голову в сторону (во избежание аспирации рвотных масс), выдвинуть нижнюю челюсть (при наличии съемных зубных протезов их нужно удалить).
Адреналин вводят подкожно в дозе 0,1-0,5 мл 0,1%-ного раствора (препарат выбора), при необходимости инъекции повторяют каждые 20 мин в течение часа под контролем уровня АД. При нестабильной гемодинамике с развитием непосредственной угрозы для жизни возможно внутривенное введение адреналина. При этом 1 мл 0,1%-ного раствора адреналина разводится в 100 мл изотонического раствора хлорида натрия и вводится с начальной скоростью 1 мкг/мин (1 мл в минуту). При необходимости скорость может быть увеличена до 2-10 мкг/мин. Внутривенное введение адреналина проводится под контролем частоты сердечных сокращений, дыхания, уровня артериального давления (систолическое артериальное давление необходимо поддерживать на уровне более 100 мм рт. ст. у взрослых и более 50 мм рт. ст. у детей).
Побочные эффекты адреналина — головокружение, тремор, слабость; сильное сердцебиение, тахикардия, различные аритмии (в том числе желудочковые), появление болей в области сердца; затруднение дыхания; увеличение потливости; чрезмерное повышение артериального давления; задержка мочи у мужчин, страдающих аденомой предстательной железы; повышение уровня сахара в крови у больных сахарным диабетом. Описаны также случаи развития некрозов тканей при повторном подкожном введении адреналина в одно и то же место вследствие местного сужения сосудов. Противопоказания — артериальная гипертензия; выраженный церебральный атеросклероз либо органическое поражение головного мозга; ишемическая болезнь сердца; гипертиреоз; закрытоугольная глаукома; сахарный диабет; гипертрофия предстательной железы; неанафилактический шок; беременность. Однако даже при этих заболеваниях возможно назначение адреналина при анафилактическом шоке по жизненным показаниям и под строгим врачебным контролем.
Типичные ошибки, допускаемые на догоспитальном этапе
Изолированное назначение Н1-гистаминовых блокаторов при тяжелых аллергических реакциях, равно как и при бронхообструктивном синдроме, не имеет самостоятельного значения, и на догоспитальном этапе это лишь приводит к неоправданной потере времени; использование дипразина (пипольфена) опасно усугублением гипотонии. Использование таких препаратов, как глюконат кальция, хлористый кальций, вообще не показано при острых аллергических заболеваниях. Ошибочным следует считать также позднее назначение ГКС, необоснованное применение малых доз ГКС, отказ от использования топических ГКС и b2-агонистов при аллергическом стенозе гортани и бронхоспазме.
Показания к госпитализации
Пациенты с тяжелыми аллергическими заболеваниями должны быть обязательно госпитализированы.
А. Л. Верткин, доктор медицинских наук, профессор
А. В. Тополянский, кандидат медицинских наук
Хлоропирамин: клинические аспекты применения
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
С конца XX в. наблюдается неуклонный рост и широкое распространение аллергических заболеваний среди населения во всем мире. Кроме того, повсеместно отмечается нарастание тяжести аллергозов, несмотря на явные успехи в изучении их этиологии, иммунопатогенеза и совершенствование фармакотерапии. Если в 1980-е гг. прошлого столетия аллергией страдало 20% населения в промышленно развитых странах, то в настоящее время этот показатель уже приблизился к 40% [1–4].
При этом следует отметить, что в последние десятилетия появляется все больше больных, которые становятся аллергиками в зрелом и пожилом возрасте. Аллергические заболевания – это болезни современной цивилизации, обратная сторона развития прогресса, плата человека за комфортную жизнь. Аллергодерматозы в структуре аллергических заболеваний, согласно ряду отечественных и зарубежных исследований, занимают от 7 до 73%. Заболеваемость атопическим дерматитом (АД), экземой, крапивницей, контактным дерматитом неуклонно растет, в ряде стран данными болезнями страдает около 25% населения [1, 5, 6].
Аллергодерматозы, являясь по большей части хроническими заболеваниями, сопровождающимися не только высыпаниями на коже, но и сильным зудом, представляют собой серьезную медико-социальную проблему. Тяжелое течение дерматоза нередко лишает пациента возможности активно заниматься профессиональной деятельностью, приводит к длительной нетрудоспособности, а порой и к инвалидизации, что отрицательным образом сказывается на качестве жизни больного и вызывает нарушения в психоэмоциональной сфере. Так, эпидемиологические исследования, проведенные зарубежными дерматологами, показали, что у 25–40% пациентов с хроническими дерматозами выявляются те или иные психопатологические расстройства. По данным G. Schneider и соавт., у 70% больных с зудящими дерматозами отмечаются депрессивные расстройства. А на основании анкетирования, проведенного Британской ассоциацией дерматологов, было установлено, что определенный вид дерматоза увеличивает риск суицидальных попыток. Элементы самоповреждающего поведения, в ряде случаев приведшие к завершенному суициду, чаще наблюдались при экземе, крапивнице, акне и псориазе [7, 8].
Неблагоприятная динамика роста этой группы заболеваний обусловлена рядом эндогенных и экзогенных факторов [1, 3, 5, 9].
К внешним факторам относят:
• отсутствие грудного вскармливания;
• загрязнение окружающей среды, особенно в промышленно развитых странах;
• постоянный контакт в быту и/или на производстве с разнообразными химическими веществами (продукты бытовой химии, строительные материалы, косметические средства, синтетическая одежда и обувь и др.), в частности возрастание заболеваемости аллергодерматозами связано с увеличением числа лиц, имеющих аллергогенные профессии (химики, медики, особенно стоматологи, хирурги, пищевики, парикмахеры, строители);
• употребление большого количества лекарственных средств, прежде всего антибиотиков, сульфаниламидов, вакцин, барбитуратов, а также витаминов, пищевых добавок, генно-модифицированных продуктов, фаст-фуда;
• бытовые аллергены, прежде всего домашняя пыль;
• курение.
К внутренним факторам относятся:
• генетическая предрасположенность (АД);
• болезни желудочно-кишечного тракта (ЖКТ);
• эндокринопатии;
• очаги локальной хронической инфекции;
• повышенная нагрузка на психоэмоциональную сферу;
• нервно-психические заболевания.
Во многих исследованиях отечественных и зарубежных авторов выявлено, что городское население болеет аллергодерматозами чаще, чем сельские жители. Подмечено, что в высокоразвитых странах процент страдающих аллергическими заболеваниями среди молодежи значительно выше, чем в развивающихся и слаборазвитых государствах. Так, в странах Западной Европы от 10 до 30% городского населения имеют тот или иной аллергоз. Среди причин, способствующих высокой заболеваемости в городе, выделяют несколько. Во-первых, более сильное загрязнение окружающей среды различными промышленными выбросами, выхлопными газами, парами бензина. Во-вторых, горожане чаще испытывают разнообразные стрессовые ситуации из-за напряженного ритма жизни, в-третьих, в их квартирах скапливается множество бытовых аллергенов (ковры, мягкая мебель, шторы, пуховые одеяла и подушки, строительные лаки и краски и др.). В-четвертых, городские жители часто злоупотребляют высокоаллергенной пищей и, наконец, содержание домашних животных и птиц в условиях города также часто приводит к развитию аллергозов [1, 3, 5].
Теория влияния образа жизни также рассматривается аллергологами как причина увеличения частоты аллергических заболеваний в популяции. Она основана на том, что в результате улучшения санитарных условий жизни человека и пересмотра его гигиенических привычек современные дети меньше контактируют с микробами и гельминтами, а это в свою очередь приводит к недостаточной стимуляции развивающейся иммунной системы. В частности, теория влияния гигиены используется для объяснения более широкой распространенности аллергических болезней в высокоразвитых индустриальных странах по сравнению с развивающимися. Аллергологи также предполагают, что рост числа аллергиков может определять эпигенетика, т. е. способность окружающей среды оказывать влияние на ДНК, активируя одни гены и «приглушая» другие [3, 10].
В современной клинической практике наиболее распространенными аллергодерматозами являются АД, экзема, крапивница и аллергический контактный дерматит (АКД). Они имеют возрастные, половые и клинико-патогенетические особенности.
Так, АД относится к аллергопатологии детского возраста и выявляется в основном на первом году жизни, в структуре детских аллергозов он занимает 50–66,4%. Дерматоз характеризуется полигенным типом наследования. Предполагают, что если один из родителей болен АД, риск развития заболевания составляет 60%, а если оба – 81%. Считается, что у 35% грудных детей, страдающих АД, впоследствии развивается бронхиальная астма. В основе патогенеза заболевания лежит генетически детерминированный патологический иммунный ответ, характеризующийся гиперчувствительностью как к аллергенам, так и к неспецифическим раздражителям [9, 11].
Выделяют IgЕ-зависимый (экзогенный) и IgЕ-независимый (эндогенный) типы АД. IgЕ-зависимый тип характеризуется взаимодействием аллергена с высокоаффинными IgЕ-рецепторами клеток Лангерганса, которое запускает иммунопатологическую воспалительную реакцию. Активация Т-лимфоцитов в острой стадии приводит к инфильтрации кожи Т-хелперами 2-го типа, секретирующими ИЛ-4, ИЛ-13, вследствие чего повышается уровень IgЕ-антител. Взаимодействие аллергена с IgЕ-антителами, фиксированными на поверхности базофилов и тучных клеток, приводит к активации этих клеток и выбросу вазоактивных веществ. При хронической стадии заболевания кожа инфильтрируется Т-хелперами 1-го типа, которые увеличивают уровни ИЛ-5, ИЛ-12, гранулоцитарно-макрофагального колониестимулирующего фактора, гамма-интерферона. При IgЕ-независимом, неаллергическом типе АД уровень IgЕ остается нормальным, отсутствуют специфические IgЕ-антитела, отмечается низкая экспрессия ИЛ-4, ИЛ-13, ИЛ-5 и высокая экспрессия гамма-интерферона. Это более редкая форма АД, встречающаяся у 15–30% лиц, в основном у женщин, и характеризующаяся поздним дебютом болезни [9, 12].
К провоцирующим заболевание факторам относят воздействие различных аллергенов (воздушных, микробных, пищевых), нарушение барьерной функции кожи, способствующее увеличению потери воды и активному проникновению аллергенов через кожу во внутренние среды организма. Синтетическая и шерстяная одежда, пыль, шерсть домашних животных, стрессы и психоэмоциональные перегрузки, сухость кожи, особенно в зимний период, также способствуют обострению патологического процесса. В многочисленных исследованиях, проведенных за рубежом, среди микробных агентов доказана патологическая роль Staphylococcus aureus, который обнаруживается практически всегда при тяжелых формах АД [9, 13].
Главным и неизменным симптомом аллергодерматозов, и прежде всего АД, является зуд кожи. В зависимости от стадии патологического процесса на коже пациента с АД можно наблюдать различные элементы сыпи: отечные розово-красные пятна, папулы, бляшки, пустулы при присоединении вторичной инфекции, экскориации, корочки, явления лихенификации и ксероза. Кожа приобретает бледно-серый оттенок, патогномоничным признаком является белый дермографизм (рис. 1). Излюбленная локализация высыпаний – сгибательные поверхности суставов, тыльная сторона кистей и стоп предплечья, запястья, боковые поверхности шеи и лицо [9].
Экзема редко наблюдается до 20 лет, пик заболеваемости приходится на возраст 20–40 лет, и в структуре аллергодерматозов она составляет 30%. Экзема относится к нервно-аллергическим заболеваниям с поливалентной сенсибилизацией, возникающей в ответ на внутренние и внешние раздражители, порой без видимой причины, и характеризуется капризным, упорным течением с частыми рецидивами. Заболевание часто провоцируется профессиональными факторами. Экзема чаще всего возникает у химиков, стоматологов, хирургов, парикмахеров. По мере увеличения профессионального стажа, с годами число пациентов с экземой растет, нередко наличие экземы связано с потерей дохода или вынужденной сменой профессии. Экзема кистей, например, считается одним из основных заболеваний, сопряженных с потерей доходов [5, 6].
Патогенез экземы связан с нарушением деятельности трех интегративных систем организма: нервной, иммунной и эндокринной. Таким образом, ведущая роль в патогенезе заболевания отводится психовегетативным факторам, эндокринно-гуморальным расстройствам, а также неадекватному ответу иммунной системы (формирование замедленной реакции гиперчувствительности Т-лимфоцитов) на эндогенные и экзогенные раздражители. Рецидивы заболевания возникают на прием лекарственных препаратов, пищевые продукты, косметические средства, продукты бытовой химии, при стрессах, гормональных сбоях, а также при изменениях климата (температуры и влажности). Среди клинических форм экземы наиболее распространенной является истинная экзема, характеризующаяся симметричностью, нечеткостью очагов, полиморфизмом кожной сыпи, хроническим упорным клиническим течением, резистентностью к проводимой терапии (рис. 2). Микробная экзема также широко распространена в популяции и составляет от 12 до 27% всех случаев заболеваемости экземой. Экзематозный процесс развивается на фоне грибкового или микробного поражения кожи как реакция на сенсибилизацию к продуктам жизнедеятельности бактериальных или микотических возбудителей. Высыпания возникают вокруг длительно незаживающих ран, язв, пролежней, свищей от остеомиелита, на фоне длительно текущего, часто нелеченного микотического процесса. Очаги при микробной экземе в большинстве случаев ассиметричные, с четкими границами овальных или округлых очертаний. При профессиональной экземе четко прослеживается «профессиональная отягощенность», высыпания локализуются на открытых участках кожи, патологический процесс характеризуется моновалентной сенсибилизацией, ограниченными высыпаниями, благоприятным исходом при перемене профессии. Себорейная экзема развивается как у взрослых, так и у детей, мужчины болеют чаще, локализуется на себорейных участках кожи, протекает без мокнутия, часто развивается на фоне себорейного дерматита, у ВИЧ-инфицированных может быть одним из проявлений СПИДа [5, 6, 9].
Клинически одним из основных симптомов экземы является зуд кожи. Клинические проявления экземы характеризуется разнообразием форм и вариантов, что зависит от стадии и локализации патологического процесса, характера причинных факторов и особенностей макроорганизма. Большинство разновидностей экземы протекают по единому сценарию, который отражает стадии экзематозного процесса: эритроматозную, везикулезную, мокнущую, крустозную и сквамозную. Некоторые формы экземы могут протекать без мокнутия [9].
Крапивница встречается в основном у взрослых людей. Считается, что каждый четвертый человек хотя бы раз в жизни перенес данное заболевание. В настоящие время под термином «крапивница» понимают целую группу заболеваний с различными этиопатогенетическими механизмами, протекающих остро и хронически и имеющих различный прогноз и исход. Патогенетические аспекты крапивницы включают в себя прежде всего иммунные механизмы, наследственные и физические факторы. Этиологические механизмы включают как экзогенные, так и эндогенные факторы. Экзогенные факторы разделяют на физические (холодовая, аквагенная, холинергическая крапивница), химические (крапивница, связанная с приемом лекарственных средств, пищевых продуктов) и механические (уртикарный дермографизм, отек Квинке от давления). Эндогенные факторы связаны с патологией в органах и системах (очаги хронической инфекции, нарушения функции печени и болезни ЖКТ). В настоящие время этиологическая классификация крапивницы не используется, у одного и того же больного могут встретиться несколько ее вариантов, однако выявление причин заболевания необходимо для эффективного лечения болезни [9, 14, 15].
Клинически крапивница характеризуется появлением распространенных волдырей бледно-розового цвета, сопровождающимся сильным зудом или жжением кожи. Крупные волдыри (диаметром более 8 см) имеют белый центр с красным ободком по периферии (рис. 3). Для крапивницы характерен красный разлитой возвышающийся дермографизм. Высыпания недолговечные, один элемент существует не более 24 ч. Часто элементы исчезают в одном месте и появляются в другом, за счет чего образуются кольца, дуги и линии [9, 15].
АКД одинаково широко распространен как среди мужчин, так и среди женщин и встречается в любом возрасте, тем не менее у маленьких детей и пожилых людей риск развития АКД ниже. Контактные аллергены при АКД разнообразны: лаки, краски, косметические средства, металлы, моющие средства, топические лекарственные препараты. Патогенез АКД сходен с экземой (реакция гиперчувствительности Т-лимфоцитов замедленного типа). Однако в отличие от экземы при АКД не задействованы отягощающие психовегетативные и эндокринно-гуморальные факторы, а в ее основе лежит моновалентная сенсибилизация. Высыпания при АКД представлены отечными папулами и бляшками, везикулами, пузырями, эрозиями и корками в острой стадии, инфильтрацией, шелушением, сухостью – в хронической стадии. Кожная сыпь сопровождается зудом разной степени интенсивности, жжением, горением кожи. Сыпь локализуется не только на месте контакта с раздражителем, но и выходит за его пределы [9].
Одним из главных медиаторов аллергических реакций, принимающих участие в патогенезе большинства аллергодерматозов, является гистамин, который высвобождается при дегрануляции тучных клеток. Обязательное участие гистамина в патогенетических механизмах аллергических заболеваний делает блокаторы Н1-гистаминовых рецепторов средствами терапии первой линии, необходимыми для купирования любого аллергического поражения кожи. В настоящие время все антигистаминные средства принято делить на классические Н1-антагонисты, или противогистаминные препараты первого поколения, и Н1-антагонисты второго поколения. Кроме того, из Н1-антагонистов второго поколения выделяют препараты, являющиеся фармакологически активными конечными метаболитами (они получили название антигистаминные препараты третьего поколения), т. е. пролекарствами, которые в организме преобразуются в необходимое лекарственное средство. Несмотря на появление новых препаратов второго и третьего поколения, характеризующихся отсутствием ряда нежелательных явлений, таких как проходимость через гематоэнцефалический барьер и связанный с ней седативный эффект, стимуляция аппетита, прибавка массы тела, хининоподобный и кокаиноподобный эффект, развитие тахифилоксии при длительном использовании, кратковременность действия, обусловливающая многократность приема, антигистаминные препараты первого поколения до сих пор остаются в арсенале средств для широкого применения в дерматологии и аллергологии для лечения аллергодерматозов. Данная группа лекарственных средств хорошо изучена, накоплен большой опыт использования их на практике, время от времени появляются новые клинические данные об эффективности тех или иных антигистаминных препаратов первого поколения. К тому же каждое антигистаминное средство имеет свои преимущества и недостатки, а выбор врачом наиболее подходящего препарата для пациента определяется конкретной клинической ситуацией, его знаниями характеристик препарата и собственным опытом применения [16, 17].
Одним из наиболее эффективных препаратов, нашедших широкое применение в клинической практике, является хлоропирамин (Супрастин). Препарат представлен в двух формах: таблетированная (содержащая 25 мг хлоропирамина) и инъекционная (2% раствор хлоропирамина в ампулах по 1,0 мл). Препарат можно применять с месячного возраста. Хлоропирамин быстро и полностью всасывается из ЖКТ, его терапевтический эффект развивается в течение 15–30 мин после приема. Максимальная концентрация в крови достигается в течение первого часа, терапевтический уровень концентрации сохраняется в течение 3–6 ч. Препарат распределяется в разных органах, включая ЦНС. Метаболизм хлоропирамина происходит в печени; выделяется он преимущественно через почки с мочой в виде продуктов распада. Выделение препарата у детей может происходить быстрее, чем у взрослых [18–20].
При рассмотрении терапевтических возможностей хлоропирамина следует учитывать следующие аспекты [17–21]:
• Наличие инъекционной формы препарата, у антигистаминных средств второго поколения она отсутствует. Это является неоспоримым преимуществом препарата при использовании его в экстренных клинических случаях, когда необходим немедленный лечебный эффект. Заметный клинический эффект при приеме per os антигистаминных препаратов второго и третьего поколения (цетиризин, дезлоратадин, фексофенадин) наступает не ранее чем через 30 мин.
• Наличие седативного эффекта хлоропирамина необходимо в некоторых клинических случаях: при сильном, изнуряющем зуде, нарушениях сна из-за болезни, чувстве тревоги и беспокойства. В данном случае седативный эффект препарата является терапевтическим.
• Экономический аспект. Относительно невысокая стоимость препарата является привлекательной для пациентов.
В последние годы появились новые данные о механизмах действия Супрастина. Так, в 2003 г. американскими аллергологами был опубликован метаанализ сравнительных данных по изучению седативного действия Н1-блокаторов первого и второго поколения. Согласно исследованиям, разница в частоте седативного действия между антигистаминными препаратами первого и второго поколений не является столь существенной, как предполагалось ранее [21].
По мнению Т. Фицпатрика, при сильном зуде, который сопровождает АД, экзему, крапивницу и др., целесообразно отдавать предпочтение антигистаминным препаратам с выраженным седативным действием, т. е. препаратам первого поколения, например хлоропирамину [22].
Доказано, что дополнительный антихолинергический эффект хлоропирамина значительно уменьшает зуд и кожные высыпания при АД у детей, снижает объем назальной секреции и обеспечивает купирование чихания при ОРВИ [23, 24].
Известно, что при холинергической крапивнице отмечается повышенная плотность холинорецепторов в коже. Согласно проведенным исследованиям российских аллергологов, хлоропирамин является препаратом выбора в лечении данного вида крапивницы и проявляет большую эффективность по сравнению с препаратами второго поколения. В другом исследовании, проведенном во Франции, выявлено, что не только антигистаминное, но и антихолинергическое действие является необходимым в терапии аллергических заболеваний, в т. ч. и аллергодерматозов. Это объясняется тем, что в поздней фазе анафилактической реакции происходит высвобождение ацетилхолина и субстанции Р из пресинаптических нервных окончаний, которые могут поддерживать реакцию аллергического воспаления на уровне холинергической реакции. Препараты первого поколения, в частности хлоропирамин, в отличие от селективных антигистаминов (цетиризин, лоратадин, эбастин), оказывают антихолинергическое действие, блокируя позднюю фазу анафилактической реакции [20, 25].
Прием хлоропирамина также показан перед рентгеноконтрастными исследованиями, когда пациенту, в особенности с отягощенным аллергоанамнезом, осуществляют инфузии высокомолекулярных йодсодержащих средств (верографин, урографин и др.), потенциально способных вызвать развитие побочных реакций (зуд, гиперемия, крапивница, в тяжелых случаях – отек Квинке, анафилактический шок), выявляемых у 3–14% больных. В случаях острых аллергических реакций, когда необходимо парентеральное введение антигистаминных лекарственных препаратов, наличие инъекционной формы хлоропирамина определяет его выбор в качестве препарата первого ряда. При анафилактическом шоке после введения адреналина хлоропирамин вводится в/в медленно (по 1–2 мл 2% раствора), обязательным условием является контроль уровня систолического артериального давления, которое не должно быть ниже 90 мм рт. ст. [20].
Таким образом, использование в клинической практике антигистаминных препаратов 1-го поколения не утратило своей актуальности. Всегда стоит взвешивать целесообразность применения того или иного лекарственного средства в терапии аллергических заболеваний исходя не из его новизны, а с учетом этиопатогенетических, клинических особенностей заболевания и индивидуальных данных больного. Хлоропирамин (Супрастин) благодаря накопленному большому опыту применения имеет широкие показания для использования в различных областях практической медицины и остается испытанным средством для лечения аллергодерматозов у взрослых и детей.