Аллогенная трансплантация костного мозга что это
Высокодозная химиотерапия и трансплантация костного мозга у взрослых больных
Трансплантация стволовых гемопоэтических клеток нашла применение в различных областях онкологии.
Эти клетки используются после высокодозной химиотерапии для снижения длительности депрессии (угнетения) костного мозга и сокращения риска инфекционных осложнений и кровотечений.
Стволовые клетки для трансплантации получают как от самого пациента (аутологичная трансплантация), так и от иммунологически совместимого родственного или неродственного донора (аллогенная трансплантация). Непосредственным источником стволовых гемопоэтических стволовых клеток может быть костный мозг, периферическая или пуповинная кровь.
Одним из наиболее частых показаний для применения стволовых клеток в онкологии является уменьшении длительности периода угнетения кроветворения после противоопухолевой терапии.
Применение современных противоопухолевых препаратов позволяет излечить или продлить жизнь значительному количеству больных со злокачественными новообразованиями.
Однако в ряде случаев проведение стандартной химиотерапии не приводит к длительному противоопухолевому эффекту, что связано с исходной или приобретенной резистентностью (устойчивостью) опухоли к цитостатикам.
Одним из путей ее преодоления является увеличение дозы препаратов. Это увеличивает проникновение противоопухолевых препаратов в раковую клетку и позволяет преодолеть устойчивость к химиотерапии.
Резкое увеличение дозы препаратов приводит к значительному повреждению кроветворных клеток костного мозга и выключению функции кроветворения на много месяцев, что требует применения методик защиты кроветворения.
Основным методом, позволяющим преодолеть токсичность химиотерапии на кроветворение, является трансплантация кроветворной ткани. При этом стволовые клетки, полученные от донора или у самого больного, вводят после окончания химиотерапии, когда препараты полностью вывелись из организма или разрушились, что позволяет быстро восстановить кроветворение.
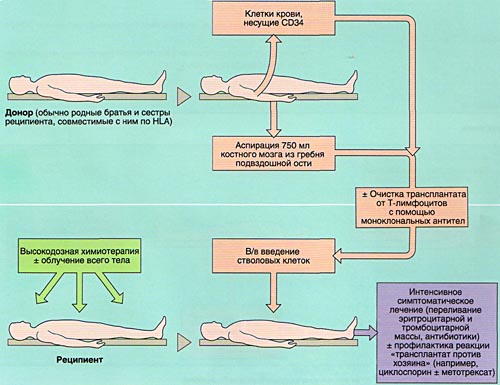
При пересадке аллогенного костного мозга возможно длительное приживление трансплантата только при совпадении донора и реципиента по антигенам главного комплекса гистосовместимости (иммунологической совместимости).
В противном случае развивается выраженная иммунологическая реакция «трансплантат против хозяина» (РТПХ), способная привести к гибели больного.
Наименьшее количество осложнений встречается у совместимых сибсов (родных братьев и сестер).
В то же время сибсы имеют вероятность совпасть иммунологически только в 25% случаев, что указывает на серьезную проблему подбора доноров для пересадки костного мозга. Последние годы отмечены крупные успехи в подборе неродственных доноров.
Следует отметить, что даже полная совместимость не дает абсолютной гарантии отсутствия развития РТПХ, и до 25% больных погибает от осложнений, связанных с трансплантацией.
Важно иметь в виду, что РТПХ способна оказывать и лечебное действие, когда иммунная система донора начинает распознавать опухолевые клетки хозяина и бороться с ними, т.е. проявляется реакция трансплантат против опухоли (РТПО).
При ряде заболеваний (хронический миелолейкоз, острый нелимфобластный лейкоз и др.) наличие этой реакции в значительной степени определяет общий успех лечения.
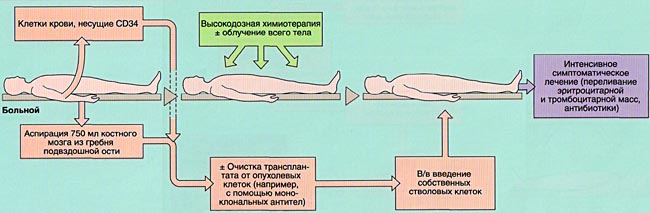
Трансплантация аутологичной (своей собственной) гемопоэтической ткани позволяет избежать возникновения РТПХ и технических сложностей, связанных с подбором донора. С другой стороны, аутологичная трансплантация не сопровождается РТПО и несет чисто вспомогательную функцию поддержки кроветворения после высокодозной химиотерапии.
В настоящее время имеется возможность сохранять собственные кроветворные клетки в жизнеспособном состоянии при низких температурах (замораживании) в течение длительного периода времени.
Долгие годы основным источником стволовых кроветворных клеток был костный мозг. Метод его получения состоит в многократных пункциях плоских костей (в основном тазовых) и получении 1-1,5 литров костно-мозговой взвеси. Такая процедура требует, как правило, общего обезболивания (наркоза).
Нужно отметить, что при опухолевом и лучевом поражении костей таза забор костного мозга может оказаться неудачным.
Костный мозг не является единственным источником кроветворных клеток.
Во взрослом организме небольшая часть стволовых клеток, как и зрелые клетки, выходит в периферическое сосудистое русло. Эти стволовые клетки способны восстанавливать полноценное кроветворение после повреждения его химиотерапией и облучением. Современная аппаратура (сепараторы крови) позволяет эффективно собирать клетки кроветворения из периферической крови даже при их низком содержании. При этом необходимость наркоза отпадает.
В условиях нормального кроветворения для получения достаточного количества стволовых клеток необходимо, как правило, 6 процедур. При каждой такой процедуре обрабатывается 10-12 литров крови.
Проблема низкого количества клеток кроветворения в периферической крови оставалась главным ограничением при использовании данного вида трансплантата. Затем было показано, что после однократного введения некоторых противоопухолевых препаратов (циклофосфамид, этопозид, фторурацил) отмечается значительное увеличение числа стволовых клеток в периферической крови. К недостаткам данного метода относятся: снижение числа лейкоцитов и тромбоцитов, значительные различия в сроках начала роста содержания стволовых клеток в периферической крови у различных больных.
Введение некоторых гемопоэтических факторов роста (нейпоген, лейкомакс и др.) вызывает значительно увеличение поступления клеток кроветворения из костного мозга в периферическую кровь.
Применение аллогенной трансплантации костного мозга
В настоящее время основными показаниями для аллогенной трансплантации стволовых клеток являются
Изучаются возможности применения данного метода у больных
Острые нелимфобластные лейкозы (ОНЛЛ)
Применение стандартной химиотерапии в первой полной ремиссии позволяет добиться длительной выживаемости в 25-35% случаев по сравнению с 45-60% при использовании аллогенной трансплантации стволовых клеток. Применение трансплантации во второй ремиссии сопровождается длительной ремиссией лишь в 20-30% случаев.
Использование аллогенной трансплантации стволовых клеток с первично резистентным (устойчивым к лечению) течением ОНЛЛ позволяет добиться длительной ремиссии в 10-20% случаев.
Острые лимфобластные лейкозы (олл)
Проведение аллогенной трансплантации стволовых клеток в первой полной ремиссии у пациентов с неблагоприятными прогностическими факторами (возраст старше 60 лет, высокий лейкоцитоз и т.д.) позволяет достичь длительной безрецидивной выживаемости в 40-60% случаев.
При отсутствии неблагоприятных факторов аллогенная трансплантация стволовых клеток обычно рекомендуется во второй полной ремиссии.
Хронический миелолейкоз
ХМЛ характеризуется несколькими фазами развития. В ранней (хронической) фазе, длящейся несколько лет, состояние больного может сохраняться относительно удовлетворительным. В фазе акселерации (обострения) в течение нескольких месяцев нарастают гематологические изменения (увеличение числа лейкоцитов, малокровие), и она переходит в фатальную (смертельную) фазу бластного криза.
Стандартные методы лечения могут вызывать длительные ремиссии у части больных, однако единственным излечивающим методом лечения в настоящее время является аллогенная трансплантация стволовых клеток. Эффективность ее зависит от возраста больного, фазы заболевания, периода времени от момента диагноза до трансплантации. Множественные курсы предшествующего лечения значительно улучшают результаты высокодозной химиотерапии и трансплантации.
Наилучшие шансы на достижение длительной ремиссии имеют молодые больные, получившие трансплантацию в хронической фазе в течение 1 года от момента диагноза. Длительная выживаемость у них составляет 75-80% по сравнению с 10-20% у больных, которым трансплантация выполнена в фазе аскселерации.
Миелодиспластический синдром
Аллогенная трансплантация стволовых клеток является единственным методом, излечивающим больных МДС. Применение этого метода позволяет добиться длительной выживаемости в 30-50% случаев. Эти результаты зависят от возраста больных, длительности заболевания и количества опухолевых клеток в костном мозге перед трансплантацией.
Аллогенная минитрансплантация
Аллогенная минитрансплантация, или трансплантация после миелоаблативных (не разрушающих костномозговое кроветворение) режимов получила распространение лишь недавно. Ее применение связано с выявлением лечебной роли РТПО и появлением новых препаратов (флударабин, антитимоцитарный иммуноглобулин), вызывающих глубокую депрессию (угнетение) иммунной системы, но не вызывающих глубокой цитопении (снижение числа клеток крови).
Применение их в комбинации с умеренными дозами бусульфана или мелфалана позволяет эффективно пересаживать донорский костный мозг. При этом РТПО полностью сохраняется. Следует отметить, что эффективность этого метода зависит от массы остаточной опухоли, которая должна быть по возможности минимальной.
Предварительные результаты применения данной методики свидетельствуют о высокой эффективности минитрансплантации при значительно меньшей токсичности в сравнении с классическим методом.
Применение аутологичной трансплантации костного мозга
Основной ролью аутологичной трансплантации костного мозга является восстановление кроветворения после химиотерапии, что позволяет многократно увеличивать разовые дозы некоторых противоопухолевых препаратов. Это дает возможность усиливать противоопухолевый эффект и достигать более высокой безрецидивной выживаемости в сравнении с результатами стандартной химиотерапии.
Наиболее часто данный метод применяется при лечении больных с прогностически неблагоприятными вариантами течения неходжкинских лимфом (лимфосарком), болезни Ходжкина (лимфогранулематоза), множественной миеломы, рака молочной железы, рака яичка и пр.
Неходжкинские лимфомы (нхл)
Применение стандартной химиотерапии у больных с НХЛ высокой и промежуточной степени злокачественности позволяет достичь 40-60% полных ремиссий. Однако у 20-30% больных этой группы отмечаются рецидивы (возврат) болезни. Применение высокодозной химиотерапии в сочетании с аутологичной трансплантацией костного мозга дало возможность значительно улучшить показатели длительной выживаемости у таких больных.
Болезнь ходжкина
У 10-30% больных с распространенными стадиями болезни Ходжкина первичная химиотерапия оказывается неэффективной, а у 40% пациентов возникает рецидив заболевания. Результаты лечения больных, малочувствительных к первичной химиотерапии и с первым ранним рецидивом (в течение первого года), неудовлетворительные.
Применение других схем стандартной химиотерапии позволяет достичь полных ремиссий не более чем у 40-45% больных, однако при этом ремиссии бывают короткими, а выживаемость низкая.
Применение высокодозной химиотерапии в сочетании с аутологичной трансплантацией стволовых клеток позволяет почти в 2 раза увеличить частоту полных ремиссий, а значит, и надежду на увеличение выживаемости.
Множественная миелома
По данным Европейской организации по аутологичным трансплантациям костного мозга, безрецидивная и общая выживаемость 5500 больных множественной миеломой, получавших высокодозную химиотерапию в сочетании с аутологичной трансплантацией стволовых клеток, составила соответственно 28 и 48 месяцев, что превышает результаты стандартной химиотерапии.
Наилучший прогноз (исход) имеют больные моложе 60 лет с I-II стадиями заболевания и уровнем бета-2 микроглобулина менее 4.
Использование высокодозной химиотерапии при других опухолях (рак молочной железы, яичка и др.) находится на этапе изучения. При этом получены обнадеживающие результаты.
Таким образом, высокодозная химиотерапия с трансплантацией аутологичных или аллогенных стволовых кроветворных клеток за последние годы стала эффективным методом лечения многих опухолей. Прогресс в биологии и иммунологии клеток кроветворения позволяет надеяться на еще более эффективное применение этого метода в будущем, в том числе и при распространенных новообразованиях, резистентных (устойчивых) к химиотерапии.
Трансплантация костного мозга и стволовых клеток
Общие принципы
ОБЩАЯ ИНФОРМАЦИЯ О СТВОЛОВЫХ КРОВЕТВОРНЫХ КЛЕТКАХ
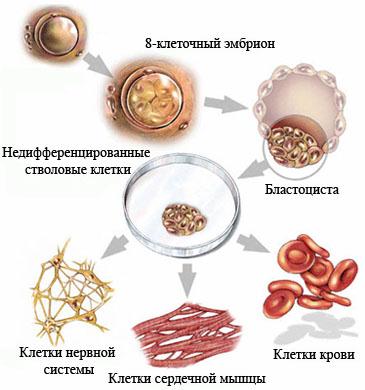
Недифференцированная стволовая клетка, происходящая из бластоцисты, является родоначальницей всех клеток организма, в том числе и стволовой кроветворной клетки (СКК).
Основными свойствами стволовой кроветворной клетки являются возможность дифференцироваться в направлении любого из ростков кроветворения и способность к самоподдержанию.
 Колонии стволовых кроветворных клеток (электронная микроскопия) | 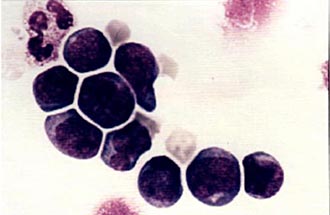 Мононуклеарная фракция, обогащенная клетками CD34, окрашена по Маю-Грюнвальду с докраской по Гимзе. Стволовые клетки, несущие маркер CD34, внешне напоминают малые и средние лимфоциты. |
ИСТОРИЧЕСКАЯ СПРАВКА
Первые работы, посвященные терапевтическому использованию костного мозга, были выполнены в последней декаде XIX века, независимо друг от друга Brown-Sequard, d»Arsonval, Fraser, Billings и Hamilton, которые применяли экстракт костного мозга животных для лечения больных различными видами анемий. Несмотря на положительный эффект, отмеченный всеми авторами, в течение последующих пятидесяти лет использование данной методики носило спорадический характер и не выходило за рамки клинического эксперимента до 1937 года когда Schretzenmayr впервые произвел парентеральное (внутримышечное) введение костного мозга, а в 1939 году Osgood выполнил первое внутривенное введение костного мозга.
Результаты экспериментальных исследований привели клиницистов к идее использования ТКМ при заболеваниях, связанных с поражением костного мозга (лейкозы, апластическая анемия), а также при радиационных воздействиях и проведении химиотерапии, однако основные теоретические и практические проблемы проведения ТКМ удалось преодолеть в 60-е годы. С этого времени ТКМ является одним из методов лечения различных заболеваний крови и иммунной системы.
ВИДЫ ТРАНСПЛАНТАЦИИ КОСТНОГО МОЗГА
Разновидностью АллоТКМ является сингенная ТКМ (трансплантация от однояйцевого близнеца).
ПОКАЗАНИЯ К ТРАНСПЛАНТАЦИИ КОСТНОГО МОЗГА
С развитием появлением колониестимулирующих факторов и развитием технологий клеточной сепарации с 70-х годов для получения гемопоэтических клеток крови вмести костного мозга стали использовать стволовые клетки периферической крови.
Применение клеточных сепараторов значительно упростило проведение процедуры получения стволовых клеток крови, уменьшило число осложнений связанных с дачей наркоза и травматическим повреждения костной ткани.
Еще одним потенциальным источником СКК является пуповинная кровь, основным преимуществом которой является меньшая иммуногенность, однако малое количество стволовых клеток в материале ограничивает ее применение и используется преимущественно в педиатрии или у пациентов с массой тела до 50 кг.
Методика проведения миелотрансплантации различается в зависимости от ее вида (аллогенная или аутологичная), нозологической формы заболевания и ряда других факторов.
ПРАКТИЧЕСКИЕ АСПЕКТЫ МИЕЛОТРАНСПЛАНТАЦИИ
ОПРЕДЕЛЕНИЕ ПОКАЗАНИЙ И ПРОТИВОПОКАЗАНИЙ
Наиболее частыми показаниями к ТКМ/ТСКК являются онкогематологические и гематологические заболевания (лейкозы, злокачественные лимфомы, апластическая анемия, врожденные иммунодефициты и нарушения метаболизма).
Чаше всего ТКМ или ТСКК проводится во время полной ремиссии (ПР), частичной ремиссии (ЧР) или при рецидиве опухоли, чувствительном к химиотерапии. При первичной резистентности к цитостатической терапии результаты ТКМ резко ухудшаются, поэтому в этих случаях операция выполняется относительно редко.
ВЫБОР ДОНОРА
Совместимость костного мозга определяет результаты АллоТКМ. Родственными донорами считаются совместимые по системе HLA братья или сестры реципиента (сибсы). Родители и дети гаплоидентичны (имеют одну общую хромосому из каждой пары, т. е. совпадают между собой на 50%) и не могут быть донорами аллогенного костного мозга. Совместимые сибсы имеются лишь у 20-25% больных, в связи с чем в последние 10 лет активно внедряется АллоТКМ от неродственных HLA-идентичных доноров или частично совместимых родственных доноров.
МОБИЛИЗАЦИЯ, ОБРАБОТКА И ИНФУЗИЯ СТВОЛОВЫХ КРОВЕТВОРНЫХ КЛЕТОК
 А) |  Б) |
А) специальный сосуд (дюар) с жидким азотом для транспортировки контейнеров с костным мозгом
Б) извлеченный из сосуда контейнер с костным мозгом
Инфузия аллогенного, размороженного аутологичного костного мозга или СКК периферической крови проводится внутривенно, капельно после предварительного введения антигистаминных препаратов для предотвращения аллергических реакций.
ИММУНОСУПРЕССИВНАЯ ТЕРАПИЯ (КОНДИЦИОНИРОВАНИЕ)
ПРОФИЛАКТИКА И ЛЕЧЕНИЕ ОСЛОЖНЕНИЙ ПЕРИОДА ЦИТОПЕНИИ
Вскоре после окончания кондиционирования и введения СКК у больного развивается аплазия костного мозга (период отсутствия костного мозгового кроветворения), которая проявляется практически полным отсутствием клеток крови (панцитопенией) и продолжается в среднем 4 недели. Этот период опасен развитием тяжелых осложнений (инфекции, кровоточивость и т.д.).
Основную опасность в периоде цитопении представляют инфекционные осложнения, поэтому их профилактика, своевременное и адекватное лечение являются необходимым условием успешной ТКМ.
Также по показаниям проводится переливание компонентов крови (эритроцитарная масса, тромбомасса, плазма).
Когда нужна пересадка костного мозга?
Пересадка костного мозга — это метод лечения, который используется при различных заболеваниях крови, преимущественно онкологического характера. Его актуальность постоянно растет, поскольку, согласно данным ВОЗ, только лейкемией и лимфомой заболевают до 600 тыс. человек ежегодно. На сегодняшний день количество трансплантаций, выполненных в мире, приближается к 2 млн.
Что такое костный мозг?
Он представляет собой мягкую губчатую ткань внутри костей. В костном мозге из стволовых клеток производится большая часть клеток крови. На самом раннем этапе развития стволовые клетки называются плюрипотентными — они способны превратиться в любую другую клетку нашего организма. Суть пересадки костного мозга как раз и состоит в том, чтобы у человека появились новые, здоровые плюрипотентные стволовые клетки взамен поврежденных.
Что такое пересадка костного мозга?
Первая успешная трансплантация такого рода была проведена еще в 1968 году. С тех пор процедура многократно совершенствовалась. Сегодня в ней выделяют три этапа:
Зачем нужна трансплантация?
Костный мозг пациента может быть поврежден из-за воздействия многих факторов. Наиболее частым из них становится онкологическое заболевание, которое поражает стволовые клетки, в результате чего они теряют способность дифференцироваться и превращаться в зрелые, функционально полноценные клетки крови.
Иногда ткани костного мозга могут необратимо повреждаться под действием длительной химиотерапии или интенсивного лучевого лечения других типов злокачественных опухолей. Соответственно, пересадка может использоваться для:
Важно понимать, что операция по пересадке костного мозга — крайне сложная медицинская манипуляция. Применять ее следует только при наличии строгих показаний. В каждом отдельном случае риски и преимущества такого лечения должны быть тщательно взвешены в ходе обсуждения с лечащим врачом и специалистами по трансплантации.
При каких заболеваниях показана такая пересадка?
Чаще всего процедуру проводят при следующих патологиях:
Типы трансплантации костного мозга
Классифицируют такие процедуры по типу донора и выделяют следующие виды манипуляций:
Центр трансплантации костного мозга клиники «Анадолу»
На базе нашего медицинского центра с 2010 года функционирует специализированный центр пересадки костного мозга. В среднем врачи «Анадолу» проводят 250 пересадок в год у пациентов от 16 лет и старше.
В состав центра входят амбулатория, клиническое отделение трансплантации костного мозга и три лаборатории: генетического типирования, гемофореза, криоконсервации и обработки стволовых клеток. Наши специалисты — высококвалифицированные трансплантологи и гематологи, владеющие всеми современными методиками пересадки костного мозга. В своей работе они неукоснительно следуют международным протоколам лечения онкологических заболеваний крови и соблюдают все меры предосторожности и безопасности.
Отделение трансплантации костного мозга «Анадолу» работает не только с международным, но и турецким банком костного мозга, который позволяет максимально быстро — всего за несколько недель — подобрать подходящего донора. В мировом регистре этот процесс может занимать несколько месяцев.
Материал подготовлен по согласованию с врачом медицинского центра «Анадолу» профессором Зафером Гюльбашем.
Высокодозная химиотерапия и трансплантация костного мозга в детской онкологии
Трансплантация (пересадка) гемопоэтических стволовых клеток (ТГСК) костного мозга и периферических стволовых клеток является одним из ведущих методов лечения детей, страдающих злокачественными опухолями.
Необходимо отметить следующие принципиально важные моменты, от которых зависит успех выполнения ТГСК:
ВИДЫ ТРАНСПЛАНТАЦИИ ГЕМОПОЭТИЧЕСКИХ СТВОЛОВЫХ КЛЕТОК
Трансплантацией гемопоэтических стволовых клеток называется введение реципиенту (больному) взвеси гемопоэтических стволовых клеток (ГСК) после назначение ему миелоаблативных доз облучения и (или) максимально переносимых доз цитостатических (противоопухолевых) препаратов.
В зависимости от источника получения трансплантируемых клеток ТГСК подразделяется на следующие виды:
Показания к выполнению алло-ТГСК у детей со злокачественными опухолями:
Показания для проведения ауто-ТГСК у детей со злокачественными опухолями:
Злокачественные заболевания системы крови.
Абсолютными показаниями для выполнения алло-ТКМ при наличии HLA-совместимого донора костного мозга являются:
Безрецидивная выживаемость в течение 5 лет у больных ХМЛ, перенесших алло-ТКМ в хронической стадии, составляет 50-60%, ОЛЛ (высокий риск, 1-2 ремиссия) – 50-60%, ОнеЛЛ – 45-65%.
После ауто-ТКМ у детей 5-летняя безрецидивная выживаемость при экстрамедуллярном рецидиве ОЛЛ достигает 65%, а при ОнеЛЛ – 50%.
Тем не менее до настоящего времени нет однозначного времени о сроках выполнения алло-ТГСК и ауто-ТГСК у детей при ОЛЛ и ОнеЛЛ, болезни Ходжкина и неходжкинских лимфомах, поскольку результаты стандартной химиотерапии в некоторых случаях не уступают эффективности ТГСК.
РЕЖИМЫ КОНДИЦИОНИРОВАНИЯ
Эффект цитостатической химиотерапии и лучевой терапии при злокачественных опухолях зависит от дозы назначаемых препаратов и дозы облучения. Режимом кондиционирования называется назначение миелоаблативных доз и (или) максимально переносимых доз цитостатических препаратов с целью достижения высокого уровня иммуносупрессии и по возможности полной эрадикации кроветворения (нормального и злокачественного клонов) реципиента перед введением ему ГСК костного мозга или периферической крови.
Степень иммуносупрессии определяет не только приживление аллогенного костного мозга, но вероятность реакции отторжения трансплантата после алло-ТГСК. Выбор комбинации различных цитостатиков и лучевой терапии перед ТГСК зависит от источника трансплантируемых клеток (аллогенный, аутологичный), типа и стадии заболевания )заболевания системы крови, солидные опухоли, рецидив, ремиссия).
Наиболее распространенные режимы кондиционирования
Использование сверхвысоких доз цитостатиков и лучевой терапии часто приводит к развитию осложнений со стороны внутренних органов (сердца, печени, легких, почек и др.) как в ближайшие сроки после назначения высокодозной химиолучевой терапии, так и в отдаленном периоде.
ПОДБОР ДОНОРА КОСТНОГО МОЗГА (ПЕРИФЕРИЧЕСКИХ СТВОЛОВЫХ КЛЕТОК)
Одним из основных факторов, определяющих успешность выполнения алло-ТКМ, является подбор совместимого по HLA- системе донора костного мозга (периферических стволовых клеток) Донором костного мозга может являться полностью совместимый по HLA-системе здоровый человек в возрасте до 50 лет.
В случае отсутствия полностью совместимого донора возможно использование частично совместимого донора. При выборе донора костного мозга не имеют различия по группе крови и половой хромосоме.
Подбор донора периферических стволовых клеток (ПСКК) осуществляется на основании принципов выбора донора костного мозга.
ВЗЯТИЕ КОСТНОГО МОЗГА
Забор костного мозга выполняется под общей анестезией (наркозом), хотя возможно использование перидуральной (спинномозговой) анестезией. Костный мозг получают с помощью игл с большим диаметром отверстия путем множественных пункций гребня крыла подвздошной кости с обеих сторон. Объем костного мозга, получаемы в результате этой процедуры, не должен превышать 10-15 мл/кг массы тела донора.
С целью профилактики развития острой реакции “трансплантат против хозяина” (РТПХ) возможно удаление Т-лимфоцитов с помощью моноклональных антител из аллогенного костного мозга перед его введением. Аутлогичный костный мозг может быть очищен от примеси злокачественных клеток с использованием цитостатиков.
Процедура взятия (эксфузии) костного мозга не вызывает серьезных осложнений у 99% доноров, однако развитие осложнений может быть обусловлено влиянием наркоза или состоянием после быстрой кровопотери.
Инфузия (введение) костного мозга реципиенту при алло-ТКМ или сингенной ТКМ производится внутривенно, капельно, через 24-48 часов после окончания химио- или лучевой терапии. Введение аутологичного костного мозга проводится тем же способом, максимально быстро после его размораживания при температуре +42…+45 гр.С.
ВЗЯТИЕ ПЕРИФЕРИЧЕСКИХ СТВОЛОВЫХ КЛЕТОК
До последнего времени основным источником ГСК при трансплантации был костный мозг (аллогенный, аутологичный).
Вместе с тем ТКМ имеет ряд недостатков:
В вязи с этим была предложена ТПСКК, физиологической основой которой явились данные о выходе стволовых клеток из костного мозга в кровь.
ТПСКК имеет ряд преимуществ по сравнению с ТКМ:
Мобилизация ПСКК может выполняться с помощью цитостатиков (циклофосфан, ифосфамид и др.). Однако у детей основным средством для мобилизации ПСКК являются рекомбинантные ростовые факторы (нейпоген, граноцит, лейкомакс).
Забор ПСКК проводят обычно на 4, 5, 6-й дни с начала введения колониестимулирующего фактора (КСФ). В это время наблюдается значительное повышение количества лейкоцитов периферической крови (в 4-10 раз) и ГСК.
Криоконсервация ПСКК осуществляется методом, аналогичным замораживанию костного мозга.
ОСЛОЖНЕНИЯ, СВЯЗАННЫЕ С ТРАНСПЛАНТАЦИЕЙ ГЕМОПОЭТИЧЕСКИХ СТВОЛОВЫХ КЛЕТОК У ДЕТЕЙ.
Осложнения раннего период после трансплантации (возникают в течение 100 дней после ТГСК).
1. Осложнения, связанные с назначением режима кондиционирования:
2. Осложнения, связанные с инфекциями.
Развитие тяжелых иммунодефицитных состояний после ТГСК приводит к возникновению различных инфекций (бактериальных, вирусных, грибковых), возникающих почти у всех больных на том или ином этапе после ТКМ.
Для профилактики и лечения таких инфекций назначаются соответствующие препараты.
3. Острая реакция “трансплантат против хозяина”.
При алло-ТКМ наиболее грозным осложнением и одной из основных причин смерти остается реакция “трансплантат против хозяина” (о.РТПХ), которая возникает в 30-60% случаев и обычно сопровождается появлением признаков приживления донорского (пересаженного) костного мозга.
При выполнении алло-ТКМ от неродственного совместимого донора костного мозга вероятность развития о.РТПХ возрастает до 80%. Острая РТПХ подразделяется на I, II, III и IV степени в зависимости от интенсивности клинических проявлений.
Существуют данные о взаимосвязи проявлений о.РТПХ с развитием в последующем рецидива злокачественного заболевания, поскольку параллельно о.РТПХ проходит так называемая реакция “трансплантат против лейкоза”.
Таким образом, о.РТПХ I и II степени является желательной, т.к. ее течение либо не требует специального лечения, либо находится под контролем. Это же касается о.РТПХ III и IV степени, но ее появление крайне опасно, так как терапия этого состояния нередко бывает безуспешной (при о.РТПХ III и IV степени смертность достигает 80-100%).
Клиническими проявлениями о.РТПХ являются:
Лечение о.РТПХ проводится большими дозами гормонов, возможно применение моноклональных антител.
4. Реакция отторжения (неприживления) донорских гемопоэтических стволовых клеток
Реакция отторжения (неприживления) донорских гемопоэтических стволовых клеток сопровождается развитием панцитопении и аплазии (снижение количества всех клеток крови и костного мозга) и возникает у 1-3% больных после алло-ТГСК.
Вероятность ее значительно возрастет (до 20%) у больных с анемией, после множественных переливаний крови, а также у получивших донорский костный мозг от частично совместимого донора или после удаления Т-лимфоцитов.
Мерами профилактики развития реакции отторжения являются проведение режима кондиционирования в полных дозах, а также назначение иимунодепрессантов в течение длительного периода времени после алло-ТГСК. При подозрении на отторжение трансплантата необходимо применение ростовых факторов (Г-КСФ, ГМ-КСФ, эритропоэтин).
5.Веноокклюзивная болезнь печени (ВОБ).
Тяжелое осложнение, возникающее у 10-60% больных после ТГСК. Заболевание обусловлено повреждением клеток печени высокими дозами цитостатических препаратов. Клинически ВОБ характеризуется желтухой, быстрым увеличением размеров печени, прибавкой веса, асцитом (скоплением жидкости в животе) и болями в брюшной полости.
При тяжелом течении ВОБ развиваются почечная недостаточность, снижение количества тромбоцитов, энцефалопатия (повреждение головного мозга). Первые признаки ВОБ могут появиться на 10-14 день после ТГСК.
Лечение ВОБ сложное и включает комплекс мероприятий, направленных на подержание вводно-электролитного баланса, мочегонных средств. При развитии почечной недостаточности показан гемодиализ (очищение крови с помощью аппарата искусственной почки).
В качестве мер профилактики развития ВОБ используют гепарин и простагландин Е.
Осложнения позднего периода после трансплантации (возникают позднее 100 дней после ТГСК).
1.Хроническая реакция” трансплантат против хозяина” (хр.РТПХ) наблюдается в 30% и более случаев после алло-ТКМ от HLA-совместимого донора костного мозга и может возникнуть как самостоятельно, так и быть продолжением в течении о.РТПХ.
Клиническими проявлениями хр.РТПХ являются склеротические изменения кожи, депигментация или гиперпигментация кожи, выпадение волос, поражение желудочно-кишечного тракта, легких, печени, суставов, мышц, глаз, атрофия лимфоидных органов.
Хроническая РТПХ подразделяется на ограниченную и распространенную в зависимости от степени вовлечения в процесс кожи и печени. Лечение хр.РТПХ проводится циклоспорином и гормонами. Возможно также сочетание с другими иммунодепрессантами (иммуран).
2.Задержка роста является особенностью течения посттрансплантационного периода у детей. Наиболее часто это осложнение встречается при включении в режим кондиционирования тотального облучения тела (ТОТ) и связано с влиянием больших доз облучения на выработку гормона роста (ГР).
Дефицит (нехватка) ГР наблюдается у 90% детей, подвегшихся облучению головы в момент режима кондиционирования и получавших эту терапию на этапе до ТГСК, а также у 40% детей. получавших облучение только в момент ТГСК.
3.Нарушение функции репродуктивных (воспроизводительных) органов и щитовидной железы. Изменение функции репродуктивных органов связано с непосредственным влиянием высокодозной химиотерапии и лучевой терапии. Менее чем у 10% женщин восстанавливается функция яичников в течение 3-7 лет после ТГСК. Сперматогенез (образование спермы) полностью отсутствует после проведения лучевой терапии, однако в течение длительного периода времени возможно его восстановление.
Нарушение функции щитовидной железы возможно у 40% больных после ТГСК и чаще всего развивается у детей с болезнью Ходжкина (лимфогранулематозом), получавших облучение шеи.
4.Поражение глаз наиболее часто сопутствует развитию хр. РТПХ. Возникновение катаракты является осложнением высокодозной лучевой терапии и выявляется у 20% больных, имевших в режиме кондиционирования ТОТ.
5. Возникновение второй злокачественной опухоли. У больных после ТГСК увеличен риск возникновения второй опухоли (лимфома, лейкоз, опухоль головного мозга, меланома, рак печени, остеогенная саркома, рак щитовидной железы), что связано с применением химиотерапии, облучения и иммунодепрессантов.
Вероятность развития второй опухоли больше у пациентов, возраст которых был менее 30 лет на момент ТГСК и увеличивается параллельно длительности жизни после ТГСК.
Рецидивы (возврат) основного заболевания являются нередкой причиной смерти после ТГСК.
В связи с этим все большее внимание уделяется использованию иммунотерапии (интерлейкин-2, интерфероны и пр.) после трансплантации, особенно после проведения ауто-ТГСК.