Альмагель для кошек для чего
Системный подход к лечению ХПН и ОПН у кошек и собак
Известно расхожее выражение, что все мы состоим из воды. В сфере диализа жидкостная среда организма так и называется – вода. И у людей, и у животных в ней происходят все биохимические процессы, обеспечивающие полноценную жизнь. Здесь же накапливаются токсины, в том числе уремические, сигнализирующие о патологическом состоянии почек, почечной недостаточности.
Активная вода организма составляет 70 % массы тела. Если же рассматривать ее состав в процентных соотношениях, то в самых больших объемах представлены вода плотных тканей и внутриклеточная вода – 40 и 33 процента соответственно. Далее следует интерстициальная жидкость и лимфа – 12 %. Всего 4,5 процента приходится на долю плазмы крови, по столько же – на воду хрящей и необменную воду костей. Наконец, оставшиеся 1,5 % – трансцеллюлярная вода.
Представим живой организм в виде некой емкости. У нас получится сосуд, разделенный множеством мембран, через которые постепенно просачивается вода. Если она загрязнена, то с течением времени станет грязной жидкость во всем сосуде. Из этого наглядного примера обмена веществ понятно, что при почечной недостаточности мочевые токсины накапливаются не только и не столько в крови, но и во всей активной воде организма – и вся она требует очищения. Об этом следует помнить при расчете дозы гемодиализа. Также не стоит забывать о прямой зависимости времени выравнивания уремических токсинов крови и остальной жидкости от степени дегидратации организма: при обычных условиях процесс занимает порядка четырех часов, в обезвоженной же клетке обмен происходит значительно медленнее.
Снова рассмотрим на примере. Возьмем животное массой 20 кг с мочевиной крови 50 ммоль/литр. Из вышесказанного ясно, что такой же уровень уремической интоксикации будет иметь вся вода организма, а это порядка 14 л жидкости – и необходимо очистить весь этот объем. Очевидно, что плазмаферез, удаляющий 30 процентов плазмы, то есть всего 1,5 % от общей воды, окажется неэффективным, и должно быть принято решение о проведении гемодиализа.
Лечение любого заболевания внутренних органов должно начинаться с создания оптимальных условий, при которых они смогут полноценно выполнять свою работу. Такого же подхода требует и почечная недостаточность у кошек или собак, и, соответственно, нефропротекция. Если почки поражены незначительно, интоксикация начнет снижаться сразу после устранения патологии. Необходимо учитывать и основные факторы, без изменения которых положительные результаты окажутся под вопросом. Остановимся на них более подробно.
Послесловие
За годы работы мы выяснили, что большинство врачей в других клиниках неверно оценивают гемодиализ, считая его крайней мерой. Владельцы, «взращенные» на этом заблуждении, приходят к нам с формулировкой «все остальное не помогло» – и почти все обращения за лечением почечной недостаточности у собак и кошек случаются с опозданием, будь то острая или хроническая формы заболевания.
Уважаемые коллеги и владельцы животных! Бесполезно очищать почки, когда они уже мертвы. Гемодиализ – не волшебное средство, спасающее пациента в последнюю секунду. Назначенный своевременно, он дает врачу необходимые часы и дни для осуществления полноценной нефропротекции.
Допустим, у пациента полностью нарушена фильтрационная способность почек, например, с тотальным ОКН при пироплазмозе. Необходимо восстановить канальцевый эпителий – процесс, зачастую длящийся 15-20 дней. Несмотря на все наши капельницы, собака или кошка может элементарно не дожить до выздоровления, умерев от банальной уремии через неделю. Между тем, к нам часто попадают животные с мочевиной 90-100 и креатинином больше 2 500. Как правило, при таком уровне интоксикации в организме нарастают необратимые процессы системной дегенерации обмена веществ – и изменить что-то бывает уже невозможно.
Существует простой способ оценки эффективности терапии при почечной недостаточности у кошек и собак. В начале лечения у животного берется анализ крови на мочевину с креатинином. Повторите исследование не через 5-7 дней, как это обычно бывает, а через сутки, тогда вы точно будете знать, правильно ли выполнены назначения, все ли патологические факторы учтены. Если показатели растут, почка либо мертва, либо вы что-то упустили. Важно проводить исследования в одной лаборатории, чтобы исключить разницу погрешности измерений, которая скроет истинную суточную динамику.
Не залечивайте животное! Когда терапия назначена правильно, улучшение состояния пациента произойдет уже через 12 часов. Если этого не случилось, значит, упущен какой-то фактор, например, неверно определены степени обезвоживания или истощения, Ph плазмы крови, не учтены анемия, наличие сопутствующей инфекции, хронические заболевания и прочее. В этом случае тактику лечения нужно срочно менять.
Хроническая почечная недостаточность у собак и кошек – не диагноз. Это обязан знать каждый врач – и с этим знанием он должен подходить к каждому нефробольному. ХПН – это синдром, обусловленный гибелью нефронов в почке, который наблюдается от нескольких месяцев до нескольких лет. Причинами этого симптомокомплекса могут быть повышенное артериальное давление, хронический пиелонефрит, гидронефроз, нефросклероз, целый ряд аутоиммунных болезней, сахарный диабет и т.д. Иными словами, любые патологические факторы, приводящие к гибели нефронов, – истинная причина, следствием которой уже является ХПН. И ваша главная задача – находить и устранять их.
Алмагель при хпн, пронфера.
Альмагель или ренальцин-принимают с едой чтобы связывался фосфор.. Выставите результаты анализов..
Какой у кошки фосфор? Может вам вообще ничего от фосфора не надо (так тоже бывает).
Вы даете альмагель в чистом виде? Его надо перемешать с небольшой порцией паштета и впихивать в таком виде, а в чистом виде и меня от такой гадости вытошнит. И обязательно привязывать прием альмагеля к еде (т.к. он связывает фосфор именно в еде), можно перед едой, можно в середине, можно после, как приноровитесь.
Какой у кошки фосфор? Может вам вообще ничего от фосфора не надо (так тоже бывает).
Вы даете альмагель в чистом виде? Его надо перемешать с небольшой порцией паштета и впихивать в таком виде, а в чистом виде и меня от такой гадости вытошнит. И обязательно привязывать прием альмагеля к еде (т.к. он связывает фосфор именно в еде), можно перед едой, можно в середине, можно после, как приноровитесь.
За идею с паштетом спасибо )!
Ипактине засыпаю в пустые капсулы, купила капсулы ) лекарство вытрясла ) засыпала ипактине ) таблетки она глотает нормально ) + у нас ещё в лечение фероглобин. Лечим третий день (
а лучше смените на адекватного тк вы все-таки в Москве
а лучше смените на адекватного тк вы все-таки в Москве
а лучше смените на адекватного тк вы все-таки в Москве
Всем огромное спасибо и низкий поклон за участие и поддержек
Альбина Валерьевна Легута:
Добрый день. Все правильно доктор вам назначил. Альмогель обладает обволакивающим эффектом и служит в защите слизистой оболочки желудка. Так как при ХПН мочевина скапливается в организме, она выделяется через все слизистые организма в том числе и через слизистую желудка. Чтобы ее защитить, погасить дискомфорт в желудки, убрать изжогу. Ренальцин при ХПН 3 стадии, к сожалению не панацея Используйте энтеросгель.
энеросгель- сорбент- тоже связывает и выводит мочевину
давая эти препараты надо соблюсти опытным путем баланс,чтобы не было запоров-поносов и был стул
Только зарегистрированные пользователи имеют возможность начинать новые темы. Зарегистрируйтесь и войдите на сайт, введя свои логин и пароль справа в окне, и Вы сможете начать новую тему.
Прежде чем задать вопрос на форуме, ознакомьтесь с темой: «Как правильно задать вопрос вет.врачу», а также со списком ответов на часто задаваемые вопросы, это поможет Вам сэкономить Ваше время и быстрее получить ответ на Ваш вопрос.
Обратите особое внимание на документ: Симптомы заболеваний животных. Возможно, в Вашей ситуации нельзя ожидать ответа на форуме, а нужно срочно вызывать врача или везти животное в ветеринарную клинику!
Прежде чем задать вопрос на форуме, ознакомьтесь со следующими разделами, это поможет сэкономить Ваше время и быстрее получить отсвет на ваш вопрос:
Внимание! Обратите особое внимание на документ «Симптомы заболеваний животных». Возможно, в Вашей ситуации нельзя ожидать ответа на форуме, а нужно срочно вызывать врача или везти животное в ветеринарную клинику!
Альмагель: противопоказания и показания к применению
Альмагель – эффективный и достаточно безопасный препарат, применяемый для лечения заболеваний желудочно-кишечного тракта, однако есть противопоказания. Альмагель относят к группе антацидных средств: он частично нейтрализует действие соляной кислоты и уменьшает выработку желудочного сока, а также обладает анестезирующими свойствами. Его применение позволяет избавиться от боли и дискомфорта, а также устранить причину заболеваний пищеварительной системы.
Фармакологическое действие и показания к применению
Альмагель А: антацидный препарат
Альмагель содержит гидроксид алюминия и магния, вступающие в реакцию нейтрализации с соляной кислотой, ее продукты выводятся почками. Нейтрализация желудочного сока при повышенной кислотности помогает остановить разрушительное действие соляной кислоты на слизистую желудка.
Еще одним компонентом является бензокаин – это местное обезболивающие, снижающее болевые симптомы. В состав также входит сорбит, улучшающий желчевыделение и способствующий нормализации пищеварения. В норме прием Альмагеля дает легкий слабительный эффект, препятствующий возникновению запоров.
Альмагель принимают при острых и хронических заболеваниях пищеварительного тракта. В их числе острый гастрит, а также обострение хронической формы, воспалительные процессы в тонком кишечнике и двенадцатиперстной кишке, язвенная болезнь желудка.
Альмагель также является эффективным средством при расстройствах пищеварения, вызванных нарушением режима питания, длительным приемом лекарств или алкоголя. Он также помогает при обострениях гастрита, спровоцированного курением. Альмагель помогает бороться с пищевыми токсикоинфекциями, рефлюкс-эзофагитом (воспалением пищевода), метеоризмом.
Кроме того, он может применяться в профилактических целях: его назначают, если больному предписано длительное время принимать противовоспалительные препараты. Способность защищать желудок позволяет предотвратить нарушения пищеварения, избежать появления тошноты и других неприятных симптомов.
Преимущества перед другими препаратами
Альмагель отличается несколькими важными качествами, которые сделали его одним из самых востребованных препаратов в борьбе с воспалительными процессами в желудке и кишечнике:
Правильно рассчитанная дозировка и соблюдение врачебных рекомендаций позволяют свести к минимуму проявление гастрита, язвенной болезни и различных нарушений пищеварения, Альмагель имеет очень небольшой список противопоказаний.
Побочные действия и противопоказания
Альмагель: есть противопоказания кприменению
Противопоказания Альмагель имеет, как и другие лекарственные средства. Его нельзя использовать в следующих случаях:
Альмагель в крайне редких случаях дает побочные действия. Со стороны системы пищеварения возможны тошнота, рвота и запоры, препарат также может вызывать чувство сонливости. При долгом употреблении у больных, имеющих нарушения минерального обмена, может наблюдаться размягчение костей – остеомаляция.
Из-за возможных побочных действий и списка противопоказаний нельзя принимать препарат бесконтрольно и заниматься самолечением. Необходимо консультироваться с врачом и строго соблюдать все рекомендации.
Дозировка, основные правила приема
Альмагель часто назначается врачами
Альмагель выпускается в форме, удобной для приема внутрь, относительно приятный вкус позволяет давать его даже маленьким детям без затруднений. Сразу после приема лекарства нельзя пить никакие жидкости: они способны разбавить препарат, уменьшив концентрацию активных веществ, поэтому будет снижена эффективность.
Для взрослых разовая доза составляет 1 чайную ложку геля, ее принимают за полчаса до еды и перед отходом ко сну. Всего в сутки допустимо принимать не больше 16 чайных ложек препарата, курс лечения при максимальной дозировке должен составить не больше 2 недель.
Для детей в возрасте от 2 месяцев до 10 лет необходимо не более трети взрослой дозы, старше 10 лет – половины. Если воспалительный процесс сопровождается рвотой и тошнотой, то сначала будет назначен курс Альмагеля-А, а когда неприятные симптомы исчезнут, будет назначен Альмагель.
Общий курс лечения не должен превышать 3 недель. Если болезнь не вылечена и облегчения состояния не наступает, необходима консультация лечащего врача и подбор других препаратов.
Прием Альмагеля помогает справиться с проявлениями серьезных заболеваний пищеварительного тракта. При разумном подходе и соблюдении врачебных предписаний он приносит улучшение самочувствия и помогает устранить причину негативных симптомов.
Алмагель А суспензия для приема внутрь, 170 мл
В наличии в 597 аптеках
Под заказ в 575 аптеках
| Бренд: | Алмагель |
| Производитель: | ТЕВА |
| Завод производитель: | Балканфарма-Троян АД, Болгария |
| Форма выпуска: | суспензия для приема внутрь |
| Количество в упаковке: | 170 мл |
| Действующие вещества: | алгелдрат+бензокаин+магния гидроксид |
| Возраст от: | 12 лет |
| Назначение: | Изжога |
Описание
Состав и описание
Активное вещество:
5 мл препарата (1 мерная ложка) содержит: алюминия гидроксид гель 2,18 г (в пересчете на AlO3 218 мг), магния гидроксид паста 350 мг (в пересчете на MgO 75 мг), бензокаин 109 мг
Вспомогательные вещества:
Водорода пероксида раствор 30% 0,41 мг, сорбитол 801,15 мг, гиэтеллоза 15,26 мг, метилпарагидроксибензоат 10,90 мг, пропилпарагидроксибензоат 1,363 мг, бутилпарагидроксибензоат 1,363 мг, натрия сахарината дигидрат 0,818 мг, пропиленгликоль 327,00 мг, макрогол 4000 218,00 мг, лимона масло 1,635 мг, этанол 96% 98,10 мг, вода очищенная до 5 мл.
Описание:
Суспензия белого или почти белого цвета с характерным запахом лимона. При хранении на поверхности может выделяться слой прозрачной жидкости. При энергичном взбалтывании гомогенность суспензии восстанавливается.
Форма выпуска:
По 170 мл препарата во флаконе из темного стекла с навинчиваемым пластмассовым колпачком с контролем первого вскрытия. Каждый флакон вместе с инструкцией по применению и мерной ложкой на 5 мл помещают в картонную пачку, на которую дополнительно могут быть нанесены защитные наклейки или по 170 мл препарата во флаконе из полиэтилентерефталата с навинчиваемым пластмассовым колпачком с контролем первого вскрытия. Каждый флакон вместе с инструкцией по применению и мерной ложкой на 5 мл помещают в картонную пачку, на которую дополнительно могут быть нанесены защитные наклейки.
Противопоказания
Показания к применению
Взаимодействие с другими лекарственными средствами
Алмагель А изменяет кислотность содержимого желудка, что оказывает влияние на всасывание, максимальную концентрацию в плазме и биодоступность, а также на выведение большого количества лекарственных средств, применяемых одновременно с ним.
Антациды, содержащие алюминий, уменьшают всасывание блокаторов Нг-гистаминовых рецепторов, атенолола, дигоксина, цефдинира, цефподоксима, хлорохина, тетрациклинов, дифлунисала, бифосфонатов, этамбутола, фторхинолонов, фторида натрия, глюкокортикоидов, индометацина, изониазида, полистиролсульфоната, кетоконазола, линкозамидов, метопролола, нейролептиков, фенотиазинов, пеницилламинов, пропранолола, солей железа, витаминов. Сниженная абсорбция этих препаратов связана с образованием нерастворимых комплексов и/или ощелачиванием содержимого желудка. Чтобы избежать нежелательного лекарственного взаимодействия, следует соблюдать 2- часовой интервал между приемом этих препаратов (4 часа для фторхинолонов) и препарата Алмагель® А.
При одновременном приеме с кишечнорастворимыми таблетками повышенная щелочность желудочного сока может привести к более быстрому растворению их оболочки и вызвать раздражение желудка и двенадцатиперстной кишки.
Одновременное применение с хинидином может привести к повышению концентрации хинидина в плазме и привести к передозировке хинидина.
Следует соблюдать осторожность при одновременном применении препарата Алмагель® А с полистиролсульфонатом, так как возможно снижение эффективности связывания калия со смолой; из-за риска метаболического алкалоза у пациентов с почечной недостаточностью (связанной с применением гидроксида алюминия и гидроксида магния) и риском кишечной непроходимости (связанной с применением гидроксида алюминия). Одновременное применение гидроксида алюминия с цитратами может привести к более высокой концентрации алюминия, особенно у пациентов с нарушением функции почек. Ощелачивание мочи вследствие применения гидроксида магния может изменить выведение некоторых лекарств, в связи с этим наблюдается повышенное выведение салицилатов. Алмагель® А не следует принимать одновременно с сульфониламидами, ввиду наличия бензокаина в его составе. Являясь производным парааминобензойной кислоты, бензокаин действует как антагонист антибактериальной активности сульфаниламидов.
Алмагель® А может повлиять на результаты некоторых лабораторных и функциональных исследований и тестов: он снижает уровень желудочной секреции при определении ее кислотности; нарушает тест визуализации дивертикулов и сцинтиграфии костей при помощи технеция (ТС99); умеренно и на короткое время повышает сывороточный уровень гастрина, повышает сывороточный уровень фосфора, pH сыворотки и мочи.
Передозировка
При однократном превышении дозы не наблюдаются другие признаки передозировки кроме запора, метеоризма, ощущения металлического вкуса.
При продолжительном приеме высоких доз возможны нефрокальциноз, появление тяжелых запоров, легкая сонливость, гипермагниемия. Могут наблюдаться также признаки метаболического алкалоза: изменение настроения или умственной активности, онемение или боль в мышцах, раздражительность и быстрая утомляемость, замедление дыхания, неприятные вкусовые ощущения.
Необходимо сразу предпринять меры по быстрому выведению медикамента из организма посредством промывания желудка (индукция рвоты, прием активированного угля).
Фармакологическое действие
Фармакологическая группа:
Антацидное средство + местноанестезирующее средство
Код ATX: А02АВ10
Оказывает обволакивающее, адсорбирующее действие. Защищает слизистую оболочку желудка за счет стимулирования синтеза простагландинов (цитопротективное действие). Это предохраняет слизистую оболочку от воспалительных и эрозивно-геморрагических поражений в результате применения раздражающих и ульцерогенных агентов, таких как этиловый спирт и нестероидные противовоспалительные препараты (например, индометацин, диклофенак, аспирин, ацетилсалициловая кислота, кортикостероидные препараты).
Терапевтический эффект после приема препарата наступает через 3-5 минут. Продолжительность действия зависит от скорости опорожнения желудка. При приеме натощак действие длится до 60 минут. При приеме через час после приема пищи антацидное действие может продолжаться до 3 часов.
Не вызывает вторичную гиперсекрецию желудочного сока.
Бензокаин оказывает местное обезболивающее действие при наличии выраженного болевого синдрома.
Выведение — выводится через кишечник.
Бензокаин
Бензокаин всасывается в минимальных количествах и практически не оказывает системных эффектов на организм. Его местный обезболивающий эффект наступает через 1-2 минуты после приема суспензии.
Опыт лечения тяжелых нарушений фосфорно-кальциевого обмена при терминальной почечной недостаточности с использованием цинакалцета
Хронические заболевания почек представляют собой серьезную проблему здравоохранения. Это определяется как неуклонным ростом числа больных с хронической почечной недостаточностью, так и высокой стоимостью и относительно неудовлетворительными исходами их ле
Хронические заболевания почек представляют собой серьезную проблему здравоохранения. Это определяется как неуклонным ростом числа больных с хронической почечной недостаточностью, так и высокой стоимостью и относительно неудовлетворительными исходами их лечения [1]. Анализ Базы данных пациентов с заболеваниями почек (USRDS) и результатов исследования NHANES III в США показал, что около 26 млн взрослых, то есть примерно 14,6% от числа населения старше 20 лет, страдают хроническими заболеваниями почек [4]. За последние пять лет число больных, находящихся на заместительной почечной терапии, увеличилось более чем на 25% и на данный момент составляет более 2 млн человек. При этом наибольшее количество больных, получающих заместительную почечную терапию, зарегистрировано в Японии (2230 пациентов на 1 млн жителей) и в США (1650 больных на 1 млн жителей). Наибольший рост числа таких пациентов зафиксирован в развивающихся странах (в том числе в России) — свыше 50% за 5 лет [6].
Исходя из данных о весьма значительной распространенности хронических заболеваний почек и динамике прироста терминальной стадии хронической почечной недостаточности в течение последних 20 лет эксперты прогнозируют и в будущем дальнейший рост численности этой категории больных, тем более что, благодаря значительному техническому прогрессу, заместительная почечная терапия в настоящее время может применяться практически без ограничений [4].
Проблема лечения терминальной стадии хронической почечной недостаточности усугубляется тем, что, несмотря на значительный прогресс в заместительной почечной терапии, ее прогноз все еще остается весьма неблагоприятным. В США сохраняется высокая годичная летальность пациентов, находящихся на заместительной почечной терапии, — более 20%. Ожидаемая продолжительность их жизни значительно короче, чем в сходной возрастной группе. Так, для пациентов в возрасте от 40 до 44 лет она составляет 7,1–11,5 года, а для пациентов от 60 до 64 лет — 2,7–3,9 года. Частота сопутствующих заболеваний у больных с хроническими заболеваниями почек также высока. Их среднее количество у больного, находящегося на заместительной почечной терапии, равно четырем, и основную роль при этом играют заболевания сердечно-сосудистой системы [22].
Пациенты с хроническими заболеваниями почек имеют большую вероятность умереть от осложнений своего заболевания, чем дожить до потребности в диализе. Летальность вследствие заболеваний сердца среди пациентов с терминальной стадией хронической почечной недостаточности в 10 раз выше, чем в общей популяции. Например, по данным американского регистра 2002 года у больных с почечной недостаточностью в 24,8% случаев выявлена ишемическая болезнь сердца, а в 8,7% — инфаркт миокарда [29]. У пожилых пациентов с хронической почечной недостаточностью частота ишемической болезни сердца выше на 22%, латентной ишемии — на 16%, а новых коронарных событий — в 3,4 раза по сравнению с пациентами без нарушения функции почек [6]. По данным исследования HOPE легкая почечная недостаточность (креатинин плазмы 124–200 мкмоль/л), независимо от других факторов риска и лечения, ассоциировалась с увеличением сердечно-сосудистой смертности от инфаркта миокарда и инсульта на 40% [25].
Предметом интереса недавних исследований стал вопрос, в какой мере сопутствующие сердечно-сосудистые заболевания могут быть связаны с нарушениями функции паращитовидных желез, развивающимися параллельно со снижением функции почек. Концепция, в соответствии с которой воздействие на рецепторы, подобные рецепторам паращитовидных желез, обнаруженные во многих органах и тканях, могут играть определенную роль в развитии и прогрессировании сердечно-сосудистых заболеваний у пациентов с хроническими заболеваниями почек, является относительно новой [2].
Вторичный гиперпаратиреоз при хронических заболеваниях почек
У пациентов с хроническими заболеваниями почек нарушенный синтез гормонально-активного витамина D в сочетании с длительной гиперкальциемией и повышенным уровнем фосфатов приводит к вторичному гиперпаратиреозу, одному из наиболее частых и тяжелых осложнений (около 30% пациентов, находящихся на программном гемодиализе) [12]. Это состояние, характеризующееся компенсаторной гиперсекрецией паратиреоидного гормона, приводит как к морфологическим изменениям паращитовидных желез, так и к развитию фиброзного остеита, потере костной массы и к сопутствующим сердечно-сосудистым заболеваниям [20]. Как правило, уровни паратиреоидного гормона в крови начинают повышаться при уменьшении скорости клубочковой фильтрации ниже 60 мл/мин/1,73 м2 [22]. К настоящему времени вопрос о времени появления у пациентов с хроническими заболеваниями почек сопутствующих сердечно-сосудистых заболеваний, их каузальной связи с дисфункцией паращитовидных желез и возможности обратного развития на фоне патогенетического лечения вторичного гиперпаратиреоза до конца не ясен [2, 3].
Давно известно, что паратиреоидный гормон оказывает воздействие на функционирование многих органов и систем [3]. При уремии, выделяясь в супрафизиологических концентрациях, он приобретает черты «универсального уремического токсина», вызывая плейотропную органную дисфункцию. Гиперсекреция паратиреоидного гормона способствует развитию ренальной остеодистрофии, уремической кардиомиопатии, «кальцификации миокарда», клапанов сердца и его проводящей системы, диффузному фиброзу миокарда, внескелетной кальцификации, артериальной гипертензии, ускорению развития атеросклероза, генерализованной васкулопатии, энцефалопатии; влияет практически на все стадии гемопоэза; нарушает секрецию инсулина [3, 15, 17, 20, 25, 31]. Эти события неразрывно связаны (по крайней мере, частично) с избыточной концентрацией паратиреоидного гормона и плохо корригируются заместительной почечной терапией.
Вторичная гиперплазия паращитовидных желез с повышением уровня паратиреоидного гормона в крови развивается практически у всех больных с хроническими заболеваниями почек. Вторичный гиперпаратиреоз у больных с хроническими заболеваниями почек — это компенсаторная гиперфункция паращитовидных желез, исходно направленная на поддержание физиологических параметров минерального и костного обмена, приводящая при прогрессировании почечной недостаточности к необратимым морфологическим изменениям (гипертрофии и гиперплазии главных клеток) паращитовидных желез [3].
Таким образом, своевременная диагностика, профилактика и адекватное лечение вторичного гиперпаратиреоза чрезвычайно важны для повышения качества и продолжительности жизни пациентов с хроническими заболеваниями почек.
Патогенез вторичного гиперпаратиреоза при хронических заболеваниях почек
Патогенез вторичного гиперпаратиреоза при хронических заболеваниях почек до конца не ясен и продолжает уточняться. В развитии вторичного гиперпаратиреоза играют роль разнообразные факторы, что приводит к запуску целого каскада биохимических и патофизиологических изменений, приводящих к необратимым морфологическим изменениям паращитовидных желез [2, 3, 22, 23]: транзиторная и/или персистирующая гиперфосфатемия (ретенция фосфатов); резистентность рецепторов органов-мишеней к паратиреоидному гормону; изменение метаболизма витамина D.
На сегодняшний день в целом остается верной гипотеза Bricker N.?S. (1972), в основу которой были положены представления о том, что при хронической почечной недостаточности главным стимулом к развитию вторичного гиперпаратиреоза является гипокальциемия, которая возникает в ответ на гиперфосфатемию, связанную с ретенцией фосфатов [7, 8]. При хронической почечной недостаточности, особенно в терминальной ее стадии, происходит патологическая фенотипическая модуляция рецепторов (в т. ч. из-за изменения молекулярной структуры и их количества) к ионизированному кальцию на поверхности клеток паращитовидной железы и других органов-мишеней (кость, кишечник, сосуды и прочее), что кардинально изменяет гомеостаз кальция. В результате происходит сдвиг секреторной set-point и клетки паращитовидных желез начинают высвобождать паратиреоидный гормон в ответ не только на низкую, но и на нормальную концентрацию ионизированного кальция в крови больного [5, 9]. Снижение концентрации в крови 1,25-дигидроксихолекальциферола и увеличение концентрации фосфатов также являются прямыми стимуляторами синтеза паратиреоидного гормона [7, 8].
Эти представления легли в основу широкого клинического применения у пациентов, находящихся на заместительной почечной терапии, гипофосфатной диеты, фосфат-связывающих препаратов и кальцитриола. В результате удалось добиться более благоприятного течения ренальных остеодистрофий. Однако это не уменьшило остроту проблемы вторичного гиперпаратиреоза и связанных с ним осложнений со стороны сердечно-сосудистой системы.
Современные стандартные подходы к лечению вторичного гиперпаратиреоза при хронических заболеваниях почек
Современная (стандартная) терапия нарушений минерального обмена и связанных с ним осложнений включает диетические рекомендации по ограничению приема фосфатов, прием аналогов витамина D и фосфат-связывающих препаратов. Это в ряде случаев позволяет контролировать показатели фосфорно-кальциевого обмена и уровень паратиреоидного гормона в пределах целевых значений, установленных K/DOQI [22]. Целью терапии вторичного гиперпаратиреоза является снижение четырех лабораторных показателей: уровня паратиреоидного гормона, кальция и фосфора в сыворотке крови, а также фосфорно-кальциевого произведения (табл. 1).
Cтандартная терапия нарушений минерального и костного обмена по данным литературы более чем в половине случаев не позволяет достичь необходимого клинического эффекта, а в некоторых ситуациях даже противопоказана [20].
Так, лишь 47,5% пациентов, находящихся на программном гемодиализе, соблюдают диету, направленную на ограничение фосфатов, при этом уровень фосфора и кальция сыворотки у этой группы больных не имеет достоверных различий по сравнению с пациентами, не соблюдающими диету. Кроме того, содержание фосфора в различных диетах, назначаемых пациентам, варьирует от 550 до 1000 мг/сутки (18–36 ммоль/сутки), что затрудняет контроль количества поступающих с пищей фосфатов [2].
Адекватный гемодиализ также не всегда позволяет справиться с нарушениями минерального обмена. Известно, что современная гемодиализная терапия позволяет удалять лишь лимитированное количество фосфатов: от 20 до 40 ммоль за сеанс, что за неделю составляет 60–120 ммоль [24]. Более того, риск развития тяжелых форм гиперпаратиреоза (и, как следствие,?— относительный риск смерти) у таких больных прямо пропорционален продолжительности нахождения на гемодиализе (смертность в этой группе больных составляет 44% за 4 года) [1]. Эффективным является увеличение диализного клиренса фосфатов с использованием ежедневного дневного или ночного гемодиализа, гемодиафильтрации [11]. Однако такой подход неприменим в широкой клинической практике.
Эффективность терапии активными формами витамина D, например кальцитриолом, также зачастую не оправдывает ожиданий. Применение этой группы препаратов ограничено, во-первых, из-за исходной или развивающейся на фоне лечения резистентности, что требует назначения их в дозах, превышающих физиологические. Во-вторых, имея относительно узкое «терапевтическое окно» и усиливая всасывание кальция и фосфора в желудочно-кишечном тракте, они приводят к гиперкальциемии, усугубляют гиперфосфатемию и увеличивают фосфорно-кальциевое произведение [28]. Предполагаемые механизмы резистентности к лечению активированными аналогами витамина D при хронической почечной недостаточности включают в себя: опосредованные уремией снижение транспорта кальцитриола в паращитовидные железы; снижение образования комплекса кальцитриол–рецепторы к витамину D; снижение содержания функциональных рецепторов к витамину D в ткани паращитовидных желез [12]. Парикальцитол (Земплар) — синтетический селективный активатор рецепторов витамина D.
Подобные парикальцитолу модифицированные аналоги витамина D имеют меньший кальциемический эффект и, соответственно, более широкое терапевтическое окно [12, 19]. Кроме того, они быстрее, чем кальцитриол, подавляют секрецию паратиреоидного гормона и приводят к менее выраженному увеличению концентрации кальция и фосфора в сыворотке [27]. Парикальцитол сохраняет свою способность снижать паратиреоидный гормон у пациентов с гиперфосфатемией или с устойчивостью к терапии кальцитриолом [18].
Традиционное применение кальциевых фосфат-биндеров позволяет в ряде случаев корригировать гиперфосфатемию и гипокальциемию. Однако эта группа препаратов позволяет абсорбировать не более 50% потребляемого фосфора [16]. Кроме того, как любой другой препарат, фосфат-биндеры не лишены побочных эффектов: гиперкальциемия за счет всасывания кальция; связывание в кишечнике железа наряду с фосфатом; желудочно-кишечные расстройства. Необходимо считаться с тем, что на стандартной диете (1–1,2 г/кг/сутки белка) эффективны только высокие дозы карбоната кальция (9–10 г/сутки). Длительное применение таких доз карбоната кальция в 60% случаев осложняется гиперкальциемией. В настоящее время созданы фосфат-биндеры на полимерной основе, не содержащие ни алюминия, ни кальция и не всасывающиеся в кишечнике: севеламера гидрохлорид (RenaGel), севеламера карбонат (Renvela), Genzyme, Ирландия. Основное различие между ними состоит в том, что последний не вызывает метаболического ацидоза и таким образом не способствует прогрессированию костной болезни. Однако опыта применения этой группы препаратов в России пока нет [2].
В качестве крайней меры пациентам с осложненными формами вторичного гиперпаратиреоза применяется оперативное лечение, которое, к сожалению, подчас также оказывается неэффективным [2].
Указанные трудности в лечении нарушений минерального и костного обмена у больных с хроническими болезнями почек способствовали разработке и внедрению в клиническую практику принципиально новой группы препаратов — кальцимиметиков, изменяющих чувствительность рецепторов паращитовидных желез. Цинакалцет (Код АТХ: Н05ВХ01) производится международной биотехнологической компанией AMGEN (США) и зарегистрирован в Северной Америке под торговым названием Сенсипар, а в Европе — Мимпара.
В России препарат появился относительно недавно, поэтому достаточный опыт его практического применения еще не накоплен. За рубежом цинакалцет активно применяется с 2004 года более чем в 34 странах и хорошо зарекомендовал себя не только с клинической, но и с экономической точки зрения, позволяя заметно снизить затраты на лечение тяжелых осложнений хронических заболеваний почек.
Цинакалцет обладает прямым кальцимиметическим действием, непосредственно снижающим уровень паратиреоидного гормона, повышая чувствительность рецептора к внеклеточному кальцию. Снижение уровня паратиреоидного гормона коррелирует с концентрацией цинакалцета в крови. После перорального приема цинакалцета его максимальная концентрация в плазме крови достигается примерно через 2–6 часов, что сопровождается максимальным снижением уровня паратиреоидного гормона в крови. После этого концентрация цинакалцета начинает снижаться, а уровень паратиреоидного гормона повышается в течение 12 часов после введения дозы, в последующем супрессия паратиреоидного гормона остается примерно на одном и том же уровне до конца суточного интервала при режиме дозирования один раз в день. Примерно 80% вводимой дозы цинакалцета выводится почками, 15% — через желудочно-кишечный тракт. Снижение концентрации цинакалцета происходит в два этапа: первоначальный период полувыведения составляет примерно 6 часов, окончательный — от 30 до 40 часов. Стабильное содержание препарата достигается в течение 7 дней с минимальной кумуляцией. После достижения стабильной фазы концентрация кальция в сыворотке крови остается на постоянном уровне в течение всего интервала между приемами препарата. По данным литературы цинакалцет позволяет существенно снизить уровень паратиреоидного гормона уже к концу второй недели лечения.
В качестве иллюстрации вышесказанному приводится следующий клинический пример:
Больная Х., 64 года, с декабря 2005 года находится на лечении программным гемодиализом (в ГВКГ им. Н.?Н.?Бурденко с апреля 2007 года) по поводу терминальной почечной недостаточности в исходе диабетической нефропатии в сочетании с хроническим пиелонефритом. С 1965 года диагностируется алиментарно-конституциональное ожирение 2–3 степени, с 1996 года — сахарный диабет 2-го типа средней тяжести, а затем — тяжелого течения. С 1998 года — ишемическая болезнь сердца: клиника нагрузочной стенокардии отсутствовала, диагноз верифицирован на основании признаков «безболевой ишемии» миокарда и AV-блокады I степени по данным суточного мониторирования электрокардиограммы. Примерно с того же времени повышение уровня артериального давления (АД) до 220 и 140 мм рт. ст., адаптирована к АД 160/100 мм рт. ст. Постоянная четырехкомпонентная гипотензивная терапия в составе: Альбарел 2 мг/сутки, Амловас 20 мг/сутки, Аккупро 20 мг/сутки, Эгилок 100 мг/сутки — позволяла поддерживать целевой уровень АД (не свыше 140/90 мм рт. ст.) до 2005 года. С целью профилактики атеросклеротических осложнений постоянно принимала статины в суточной дозе 10 мг.
С начала 2005 года присоединяются клинико-лабораторные и инструментальные признаки прогрессирования атеросклероза, «озлокачествления» гипертензивного синдрома: в январе 2005 года появляется микроальбуминурия, которая уже в марте сменяется протеинурией до 1,5 г/сутки; несмотря на регулярный прием рекомендованных гипотензивных препаратов развивается лабильность АД. В связи с этим по рекомендации врачей поликлиники при ситуационном повышении АД свыше 160/100 мм рт. ст. (до двух-трех раз в неделю) принимала дополнительно Кордафлекс 40 мг/сутки. По данным визуализирующих методов исследования (эхокардиографии, рентгенографии органов грудной клетки) определяется достаточно быстрое увеличение массы миокарда (исходно 345 г, в последующем 436 г) с появлением признаков диастолической дисфункции первого типа и клинических симптомов хронической сердечной недостаточности на уровне функциональной классификации (ФК) II, метастатической кальцификации мягких тканей, крупных сосудов и створок аортального клапана (атеросклеротический стеноз устья аорты), что в тот период времени трактовалось как следствие особенно тяжелого течения атеросклероза, и в связи с этим увеличивается суточная доза статинов до 20 мг.
В декабре 2005 года на фоне роста азотемии (креатинин сыворотки крови 780 мкмоль/л) в результате обострения пиелонефрита, присоединения пневмонии у больной диагностируется терминальная стадия хронической почечной недостаточности и начинается лечение программным гемодиализом (3 раза в неделю по 4 часа), проведение которого вначале сопровождалось усугублением тяжести гипертензивного синдрома (АД до 240/140 мм рт. ст.). В марте 2006 и феврале 2007 года на фоне плохо поддающейся коррекции артериальной гипертензии переносит повторные острые нарушения мозгового кровообращения в бассейне левой среднемозговой артерии с исходом в правосторонний гемипарез и сенсорно-моторную афазию. В апреле 2007 года для продолжения лечения переводится в ГВКГ им. Н.?Н.?Бурденко.
В этот период у больной сохраняется выраженная артериальная гипертензия (180–200/80–90 мм рт. ст.), резистентная к стандартной ультрафильтрации и вышеуказанной медикаментозной терапии. Проведение гемодиализа с ультрафильтрацией в ежедневном режиме в течение 6 дней в неделю позволило снизить «сухой вес» на 6 кг, что сопровождалось стабилизацией АД на уровне 160/90 мм рт. ст. Концентрация фосфора в сыворотке крови составляла 2,51 ммоль/л, кальция — 2,62 ммоль/л (фосфорно-кальциевое произведение = 6,58 ммоль2/л2), уровень паратиреоидного гормона — 24,8 пг/мл. Учитывая «высокое» фосфорно-кальциевое произведение и нормальное содержание паратиреоидного гормона, медикаментозная терапия не назначалась, больной рекомендовалась гипофосфатная диета и прием карбоната кальция (до 3 г в сутки), однако соблюдение диетических правил оказалось невозможным из-за двигательных расстройств (правосторонняя гемиплегия) и низкого комплаенса (дисциркуляторная энцефалопатия с выраженными когнитивными расстройствами). Это в течение трех месяцев привело к усугублению гиперфосфатемии и гиперкальциемии (3,0 ммоль/л и 2,7 ммоль/л соответственно).
Несмотря на почти полное обездвиживание больной, предрасполагающее к развитию адинамической болезни кости, появляются лабораторные и клинические признаки гиперпаратиреоза: увеличение уровня паратиреоидного гормона до 488 пг/мл, присоединение нестерпимого кожного зуда. Ультразвуковое исследование паращитовидных желез не выявило аденоматозных изменений. Высокий уровень фосфора сделал невозможным назначение активированных аналогов витамина D. Было принято решение об изменении диализной программы с увеличением времени диализа до 15 часов в неделю и добавлением к стандартному гемодиализу еженедельно проводимой гемодиафильтрации (конвекционный клиренс — 21 литр в неделю), использовались также индивидуальные диализаторы с мембраной повышенной сорбционной активности (полиметилметакрилат) с достижением недельного Kt/V до 3,75. Это позволило приостановить прогрессирование клинических и лабораторных признаков гиперпаратиреоза (уровень паратиреоидного гормона к декабрю 2008 года составлял 504 пг/мл), выраженность кожного зуда уменьшилась, однако уровень фосфора и кальция по-прежнему оставался высоким (фосфорно-кальциевое произведение > 8,2 ммоль2/л2). Когда все методы современной терапии нарушений фосфорно-кальциевого и костного обмена были исчерпаны, нами был назначен цинакалцет (декабрь 2008 года) в стартовой дозе 30 мг/сутки.
В дальнейшем контроль показателей фосфорно-кальциевого обмена и уровня паратиреоидного гормона осуществлялся один раз в месяц. С целью оценки возможного влияния цинакалцета на уровень АД, функцию сердечной мышцы ежемесячно выполнялись трансторакальная эхокардиография, суточное мониторирование АД и ЭКГ. Оценка нарушений диастолической функции левого желудочка сердца выполнялась по общепринятым критериям [10, 13, 14]. Ежедневно контролировались масса тела, уровень АД и частота сердечных сокращений (ЧСС) (утром и вечером).
Динамический контроль за указанными параметрами показал, что через 2 недели лечения у больной Х. стойко снизился уровень как систолического, так и диастолического АД (со 160/90 мм рт. ст. до 140/80 мм рт. ст.), уменьшилась ЧСС (с 90 до 78 ударов в минуту), что подтверждалось данными СМАД и ХМЭКГ в январе 2009 года. Снижение АД и урежение ЧСС позволило откорректировать в сторону уменьшения состав гипотензивной терапии: постепенно были полностью отменены Эгилок и Кордафлекс. Уровни паратиреоидного гормона, кальция и фосфора крови оставались прежними. Поскольку в «Инструкции по применению цинакалцета» заявлено, что транзиторное снижение паратиреоидного гормона начинается через 6 часов после приема первой дозы, а стойкое — через 7 дней лечения, отсутствие эффекта через месяц приема препарата у нашей больной было расценено как следствие недостаточной начальной дозы, в связи с чем она была увеличена до 60 мг/сутки (2 таблетки). Однако появление через два дня стойкой тошноты заставило нас вернуться к исходной дозе цинакалцета 30 мг в сутки. Начальное снижение уровня паратиреоидного гормона до 345 пг/мл отмечено лишь в феврале 2009 года — на третьем месяце лечения цинакалцетом в дозе 30 мг/сутки. Еще через месяц начали снижаться уровни кальция, фосфора в крови и фосфорно-кальциевое произведение. Прием цинакалцета в той же дозе в монотонном режиме в течение четырех месяцев позволил практически нормализовать концентрацию кальция и фосфора сыворотки крови (соответственно 2,06 и 2,24 ммоль/л) к июлю 2009 года, а также снизить активность паратиреоидного гормона до 155 пг/мл.
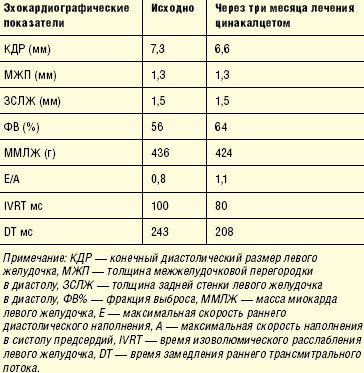
Исходно масса миокарда была повышена до 436 г за счет концентрической гипертрофии и в последующем не изменилась, однако через три месяца лечения цинакалцетом улучшились эхокардиографические показатели функционального состояния сердечной мышцы. Если в начале периода наблюдения имелись все признаки диастолической дисфункции первого типа, характеризующейся нарушением релаксации левого желудочка (аномальная релаксация) и патогенетически связанной с гипертрофией левого желудочка, повышенным уровнем артериального давления и паратиреоидного гормона, то через три месяца лечения цинакалцетом они регрессировали (табл. 2). Незначительно увеличилась фракция изгнания левого желудочка.
Обсуждение
Таким образом, только комплексный подход к лечению нарушений фосфорно-кальциевого обмена и вторичного гиперпаратиреоза с включением в фармакологическую комбинацию кальцимиметиков (цинакалцет) у больной, находящейся на заместительной почечной терапии, позволил поддерживать целевые уровни фосфорно-кальциевого обмена и паратиреоидного гормона, рекомендованные K/DOQI.
В приведенном клиническом случае традиционные подходы к коррекции минерального и костного обмена и связанного с ними вторичного гиперпаратиреоза у больной с терминальной стадией хронической почечной недостаточности, находящейся на гемодиализе, оказались неэффективными, как нам видится, по следующим причинам: невозможность соблюдения гипофосфатемической диеты и приема фосфат-биндеров (карбоната кальция) пациенткой с интеллектуально-мнестическими и двигательными расстройствами; назначение аналогов активированного витамина D (кальцитриол) было ограничено гиперкальциемией.
Дополнение комплексного лечения нарушений минерального обмена цинакалцетом позволило в течение трех месяцев достичь целевых значений минерального обмена и уровня паратиреоидного гормона. Преимуществом цинакалцета в данном случае мы считаем, помимо его очевидной эффективности в отношении гиперфункции паращитовидных желез и минерального обмена, возможность точного дозирования и однократного приема в течение суток.
Более спокойное течение артериальной гипертензии на наш взгляд явилось следствием комплекса причин: сыграли свою роль устранение гипергидратации (исходная масса тела составляла 90 кг, в последующем — 84 кг), успешная коррекции фосфорно-кальциевого обмена и снижение уровня паратиреоидного гормона. Учитывая относительно быстрое достижение нормотензии без увеличения количества и суточной дозировки антигипертензивных препаратов, нельзя исключать непосредственный гипотензивный эффект цинакалцета. Экспериментально были установлены как прямой, так и опосредованный повышенной продукцией NO вазодилятирующий эффект цинакалцета [26], а также его ингибирующее влияние на выработку ренина юкстагломерулярным аппаратом почек [23].
Диспептический синдром в виде тошноты и тяжести в эпигастрии, развившийся на следующий день после увеличения вдвое (до 60 мг) суточной дозы цинакалцета, регрессировал после возвращения к исходной дозе 30 мг так же быстро, как и развился, что не потребовало отмены препарата. Лабораторно-инструментальное обследование (фиброгастродуоденоскопия, ультразвуковое исследование органов брюшной полости, биохимическое тестирование общей и панкератической амилазы в крови и диастазы в моче) не выявило какой-либо патологии со стороны дуоденохоледохопанкреатической зоны, что позволило нам рассматривать развитие данного симптомокомплекса в рамках побочного действия цинакалцета и сделать предварительный вывод о хорошей переносимости препарата. По результатам контролируемых клинических исследований (данные о 656 больных, принимавших цинакалцет, и о 470 больных, принимавших плацебо) наиболее часто встречающимися побочными эффектами были тошнота и рвота, которые отмечались у 31% больных в группе терапии цинакалцетом и у 19% больных в группе плацебо, а также у 27% больных в группе терапии цинакалцетом и у 15% в группе плацебо. Тошнота и рвота были легкой и умеренной степени выраженности и в большинстве случаев носили кратковременный характер. Прекращение терапии в результате развития нежелательных эффектов было вызвано главным образом тошнотой (5%) и рвотой (4%).
Причиной нарушения диастолической функции левого желудочка у больной Х. на наш взгляд являлась концентрическая гипертрофия миокарда, как один из наиболее часто встречающихся вариантов ремоделирования левого желудочка у больных, длительно страдающих артериальной гипертензией и сахарным диабетом. Через три месяца приема цинакалцета стали регрессировать клинические симптомы хронической сердечной недостаточности и эхокардиографические признаки диастолической дисфункции, что более вероятно обусловлено как снижением АД до целевого уровня, так и устранением кардиотоксического действия супрафизиологических коцентраций паратиреоидного гормона. Сыграла свою роль и отмена бета-блокаторов, что стало возможным после назначения цинакалцета, поскольку эта группа препаратов негативно влияет на податливость миокарда. К сожалению, четких рекомендаций и схем терапии больных с диастолической хронической сердечной недостаточностью в настоящее время не существует. Европейское общество кардиологов (ESC) в 1997 г. опубликовало лишь общие направления терапии хронической сердечной недостаточности у больных с диастолической дисфункцией [29]. Поэтому любой положительный опыт лечения нарушений диастолической функции левого желудочка должен тщательно анализироваться.
Кроме того, минимальная эффективная поддерживающая доза цинакалцета 30 мг/сутки, что соответствует 1 упаковке (28 таблеток) на месяц, позволяет говорить о приемлемом фармакоэкономическом профиле препарата.
Таким образом, первый опыт применения цинакалцета при вторичном гиперпаратиреозе у пациентки с терминальной стадией хронической почечной недостаточности, находящейся на программном гемодиализе, оказался более чем положительным. Конечно, для выявления корреляции между снижением уровня паратиреоидного гормона и улучшением течения сердечно-сосудистой патологии необходимо накопить достаточный клинический опыт. Последующие исследования могут подтвердить или опровергнуть данное утверждение.