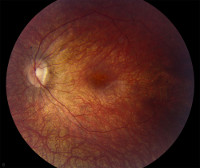
Амавроз лебера это что такое
Амавроз Лебера
Амавроз Лебера – это наследственное заболевание, характеризующееся врожденным поражением светочувствительных клеток сетчатки глаза и в некоторых случаях другими общими нарушениями (аномалии почек, ЦНС). При этой патологии в первые месяцы жизни ребенка или сразу после рождения появляется нистагм, ослабление или отсутствие реакции зрачка на свет. В дальнейшем ребенок может тереть глаза (симптом Франческетти), возникает дальнозоркость и светобоязнь, возможна полная потеря зрения. Диагностика основывается на данных осмотра пациента врачом-офтальмологом, электроретинографии, исследования наследственного анамнеза и генетических анализов. Специфическое лечение амавроза Лебера на сегодняшний день не разработано.
МКБ-10
Общие сведения
Врожденный амавроз Лебера представляет собой гетерогенную группу заболеваний, причиной которых выступают мутации в 18 генах, кодирующих различные белки сетчатки, в том числе опсин. Впервые амавроз был описан еще в XIX веке (в 1867 году) Т. Лебером, указавшим основные проявления этого заболевания – маятниковый нистагм, слепота, появление пигментных пятен и включений на глазном дне. Средняя распространенность заболевания составляет 3:100000 населения.
Амавроз Лебера в равной мере поражает как мужчин, так и женщин. Заболевание составляет примерно 5% от всех наследственных ретинопатий. Современная генетика разрабатывает методики лечения данной патологии, имеются обнадеживающие результаты генной терапии одной из форм амавроза Лебера, обусловленной мутацией в гене RPE65. Отдельно выделяют атрофию зрительных нервов Лебера, которая также характеризуется постепенной потерей остроты зрения и впоследствии полной слепотой. Однако это заболевание совершенно другой генетической природы и обусловлено повреждением митохондриальной ДНК, которая имеет свой уникальный тип наследования (по материнской линии).
Причины
Основной механизм расстройства зрения при амаврозе Лебера – нарушение метаболизма в палочках и колбочках, которое ведет к летальным повреждениям фоторецепторов и их разрушению. Однако непосредственная причина таких изменений различается в зависимости от того, мутация какого именно гена вызвала заболевание.
Один из наиболее распространенных типов амавроза Лебера (тип 2, LCA2) обусловлен наличием мутантного гена RPE65 на первой хромосоме. Известно более 80-ти мутаций этого гена, некоторые из которых, помимо амавроза Лебера, вызывают и определенные формы пигментной абиотрофии сетчатки. Белок, кодируемый PRE65, отвечает за метаболизм ретинола в пигментном эпителии сетчатой оболочки глаза, поэтому при наличии генетического дефекта этот процесс нарушается с развитием побочных метаболических путей. В результате этого синтез родопсина в фоторецепторах прекращается, что и приводит к характерной клинической картине заболевания. Мутантные формы гена наследуются по аутосомно-рецессивному механизму.
Менее распространенная форма амавроза Лебера (тип 14) вызвана мутацией гена LRAT на 4-й хромосоме. Он кодирует белок лецитин-ретинол-ацилтрансферазу, который располагается в микросомах гепатоцитов и обнаружен в сетчатке глаза. Этот фермент участвует в метаболизме ретиноидов и витамина А, из-за наличия мутаций в гене полученный протеин не может полноценно выполнять свои функции, из-за чего развивается дегенерация фоторецепторов, которая клинически проявляется амаврозом Лебера или ювенильной пигментной абиотрофией сетчатки. Имеет аутосомно-рецессивный характер наследования.
Амавроз Лебера тип 8 наиболее часто приводит к врожденной слепоте, ответственный за развитие этой формы заболевания ген CRB1 располагается на 1-й хромосоме и имеет аутосомно-рецессивный характер наследования. При этом выяснено, что кодируемый данным геном белок принимает непосредственное участие в эмбриональном развитии фоторецепторов и пигментного эпителия сетчатки. Более точных данных по патогенезу данной формы амавроза Лебера на сегодняшний день не накоплено. Аналогичная ситуация с мутацией гена LCA5, расположенного в 6-й хромосоме и ассоциированного с 5-м типом амавроза. В настоящее время выявлен только белок, кодируемым данным геном – леберцилин, но его функции в сетчатке непонятны.
Также выявлено две формы амавроза Лебера, которые наследуются по аутосомно-доминантному механизму – тип 7, обусловленный мутацией гена CRX, и тип 11, ассоциированный с нарушением гена IMPDH1. Ген CRX кодирует белок, который обладает множеством функций – контроль развития фоторецепторов в эмбриональный период, поддержание их адекватного уровня во взрослом возрасте, участие в синтезе других протеинов сетчатки (является фактором транскрипции). Поэтому в зависимости от характера мутации гена CRX клиника амавроза Лебера 7-го типа может быть разнообразной – от врожденной слепоты до относительно позднего и вялотекущего ухудшения зрения.
Инозин-5′-монофосфатдегидрогеназа 1, кодируемый геном IMPDH1, представляет собой фермент, регулирующий рост клеток и образование нуклеиновых кислот, однако это пока не позволяет прояснить патогенез того, как нарушения этого белка приводят к 11-му типу амавроза Лебера.
Классификация амавроза Лебера
В настоящее время полностью доказана взаимосвязь между клиническими проявлениями и мутациями определенных генов для 16-ти типов амавроза Лебера. Также имеются указания об открытии еще двух генов, повреждения в которых приводят к такому заболеванию, но пока в этом отношении проводятся дополнительные исследования.
Кроме того, иногда в клинической классификации выделяют не только название поврежденного гена, но и характер мутации, поскольку это имеет значительное влияние на течение амавроза Лебера. Более того, различные типы мутаций в одном и том же гене могут приводить к совершенно разным заболеваниям – например, некоторые разновидности делеций в гене CRX могут приводить не к амаврозу, а к палочко-колбочковой дистрофии. Некоторые мутации генов RPE65, LRAT и CRB1 являются причиной различных форм пигментной абиотрофии сетчатки.
Симптомы амавроза Лебера
Симптоматика амавроза Лебера достаточно вариабельна и зависит от типа заболевания и характера мутации гена. В большинстве случаев при рождении ребенка патология не определяется – даже при осмотре глазного дна изменения наблюдаются лишь в нескольких процентах случаев. По мере его роста родители могут замечать, что ребенок не задерживает взгляд на предметах и окружающих, а в более старшем возрасте может болезненно реагировать на свет (появляется фотофобия), часто тереть глаза и указывать на них пальцем (симптом Франческетти, окулопальцевый синдром). Обнаруживается нистагм, который возникает еще в первые 2-3 месяца жизни и часто является одним из первых проявлений амавроза Лебера, замедленная реакция зрачка на свет или ее полное отсутствие.
В ряде случаев наблюдается врожденная слепота. Если же ребенок родился с относительно сохранной функцией зрения, то в первые годы жизни, помимо указанных симптомов, у его также развивается дальнозоркость, косоглазие, сильно страдает острота зрения. Обычно к 10-ти годам большинство больных с амаврозом Лебера полностью слепнут. В дальнейшем у них могут возникать и другие нарушения зрительного аппарата – кератоконус, катаракта, глаукома. При некоторых типах заболевания могут наблюдаться и сопутствующие нарушения – поражения ЦНС, глухота.
Диагностика
В современной офтальмологии диагностика амавроза Лебера производится на основании осмотра глазного дна, мониторинга динамики изменений в нем, данных электроретинографии. Немаловажную роль играет также изучение наследственного анамнеза, а для некоторых типов заболевания – генетическое секвенирование последовательности ключевых генов.
Дифференциальную диагностику производят с различными формами пигментной абиотрофии сетчатки (при ней сохраняется нормальная или немного сниженная амплитуда волн на электроретинограмме) и некоторыми типами атрофии зрительных нервов.
Лечение амавроза Лебера
На сегодняшний день специфического лечения любого типа амавроза Лебера не существует. На этапе клинических испытаний находится генно-инженерное введение гена RPE65 в сетчатую оболочку глаза больных амаврозом 2-го типа, имеются первые данные о значительном улучшении зрения подопытных больных. В случае же остальных форм заболевания такого прогресса пока нет. Поддерживающее лечение сводится к витаминной терапии, внутриглазным инъекциям сосудорасширяющих средств. При дальнозоркости назначается ношение очков.
Прогноз
В плане сохранения зрения прогноз крайне неблагоприятный, практически 95% больных полностью теряют способность видеть к 10-му году жизни. Кроме того, это наследственное заболевание может осложняться проблемами с ЦНС, почками, эндокринной системой, что требует более тщательного медицинского мониторинга для своевременного выявления подобных нарушений.
Амавроз лебера это что такое
Палочко-колбочковые дистрофии (пигментный ретинит, retinitis pigmentosa, RP) представляют собою клинически и генетически гетерогенную группу расстройств, сопровождающихся прогрессирующей утратой функции фоторецепторов — сначала палочек, а затем и колбочек, приводящей к тяжелым нарушениям зрения. Пигментный ретинит обычно развивается как изолированная аномалия сетчатки, но он также может сопровождаться системными аномалиями.
а) Клиника и симптомы. Врожденный амавроз Лебера (Leber’s congenital amaurosis, LCA) — тяжелая врожденная или дебютирующая в младенческом возрасте несиндромальная ретинальная слепота, описанная Теодором Лебером в 1869 г.
Он охарактеризовал заболевание следующими признаками: блуждающий нистагм, аномальная реакция зрачков, слепота или минимальные зрительные функции по прошествии младенческого возраста, и изначально нормальная картина глазного дна с развивающимися впоследствии пигментными изменениями. Позже Лебер описал более легкую форму того же заболевания, называвшуюся по-разному: ранняя тяжелая дистрофия сетчатки (early onset severe retinal dystrophy — EOSRD), тяжелая дебютирующая в раннем детстве дистрофия сетчатки (severe early childhood onset retinal dystrophy — SECORD), ранний пигментный ретинит.
LCA/EOSRD — наиболее частая наследственная причина тяжелого нарушения зрения у детей, эта патология встречается у 10-18% детей, обучаемых в заведениях для слепых.
С рождения или в течение первых месяцев жизни отмечается тяжелое нарушение зрения, сопровождающееся блуждающими движениями глаз или нистагмом и вялой реакцией зрачков на свет. Часто наблюдаются блиндизмы — «окулодигитальный феномен». При осмотре глазного дна аномалии могут не обнаруживаться, но могут отмечаться различные изменения глазного дна, например бледность диска зрительного нерва, сужение сосудов или пигментная ретинопатия на средней периферии.
Также могут наблюдаться друзы, отек или псевдоотек диска зрительного нерва, пятнистость сетчатки, макулопатия или нумулярная пигментация. У больных младенцев часто выявляется дальнозоркость или, реже, высокая миопия,что указывает на наличие общих факторов, влияющих на развитие заболевания и эмметропизацию.
Хотя у большинства пациентов в младенческом возрасте изменения глазного дна отсутствуют, в старшем детском возрасте развиваются признаки пигментной ретинопатии, бледность диска зрительного нерва и сужение артериол сетчатки. Другие поздно возникающие симптомы, возможно, связанные с блиндизмами, включают в себя энофтальм, кератоконус и катаракту. В исходе острота зрения составляет от 3/60 до световосприятия, заболевание прогрессирует не во всех случаях.
б) Электрофизиология. У младенцев с врожденным амаврозом Лебера электроретинограмма не регистрируется или отмечаются ее тяжелые аномалии. Важное значение имеет дифференциальный диагноз врожденного амавроза Лебера, врожденной стационарной ночной слепоты и ахроматопсии, которые также могут манифестировать в младенческом возрасте нистагмом и низкими зрительными функциями. Зрительные вызванные потенциалы часто не регистрируются, но они могут быть сохранены, несмотря на нерегистрируемую ЭРГ: это может быть связано с более благоприятным прогнозом для зрения.
в) Экстраокулярные проявления амавроза Лебера. Большинство случаев врожденного амавроза Лебера развиваются у в остальном здоровых младенцев, и любые экстраокулярные жалобы и объективные симптомы должны быть изучены на предмет синдромальных дистрофий сетчатки или нейрометаболического заболевания, обычно совместно с педиатром.
г) Молекулярная генетика и патогенез. Врожденный амавроз Лебера и тяжелая дистрофия сетчатки (EOSRD) характеризуются крайней гетерогенностью, причиной заболевания могут быть дефекты более 16 генов (в том числе AIPL1, СЕР290, CRX, CRB1, GYCY2D, IMPDH1, LCA5, LRAT, MERTK, RD3, RDH12, RPGRIP1, RPE65, SPATA7, KCNJ3 и TULP1). Все они наследуются по аутосомно-рецессивному механизму, за исключением CRX, определенные de novo мутации которого наследуются по аутосомно-доминантному механизму.
Эти гены экспрессируются преимущественно сетчаткой или пигментным эпителием. Предполагается, что они выполняют самые разнообразные функции, в том числе влияют на развитие фоторецепторов сетчатки (CRX), участвуют в формировании их структуры (CRB1), механизмов фототрансдукции (GUCY2D), транспорте белков (AIPL1, RPGRIP1) и метаболизме витамина А (RPE65).
Молекулярные генетические тесты в настоящее время позволяют установить диагноз приблизительно в 50-60% случаев, эти данные способствуют прогнозированию. Например, прогноз у пациентов с мутацией RPE65 лучше, чем у пациентов с мутацией GUCY2D. Идентификация патогенной мутации у пациента с врожденным амаврозом Лебера позволяет проводить более точное генетическое консультирование, ставить пренатальный диагноз и, в будущем, возможно, будет применяться для отбора пациентов для генозамещающей терапии.
д) Методы лечения врожденного амавроза Лебера. Существуют животные модели ретинальной слепоты вследствие недостаточности RPE65; методами генной инженерии проведено целевое разрушение гена мышей, или же имеется естественная мутация у собак породы бриар. У мышей фармакологическая коррекция метаболических нарушений с помощью синтетических ретиноидов привела к быстрому восстановлению зрительного пигмента и улучшению функций.
Замещение мутантного гена нормальной копией с помощью вектора на основе аденоассоциированного вируса (adeno-associated virus — AAV), введенного субретинально, приводит к восстановлению электроретинограмм и функций сетчатки как на мышиной модели, так и на модели собак; наблюдалось выраженное стойкое улучшение зрения, подтверждаемое электроретинографией, зрачковыми реакциями и поведенческими реакциями. После успеха этих опытов в США и Великобритании проводились клинические испытания на людях, включавшие субретинальное введение AAV-вектора, содержащего нормальную («дикую») копию RPE65. Сообщается о безопасности метода, при оценке ранних результатов отмечалась вариабельная эффективность.
Вероятно, в будущем будет разработана ген-замещающая терапия и других форм врожденного амавроза Лебера/EOSRD.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в содержание раздела «офтальмология» на сайте
Амавроз лебера это что такое
Государственное бюджетное учреждение здравоохранения города Москвы
«Научно-практический центр специализированной медицинской помощи детям имени В.Ф. Войно-Ясенецкого
Департамента здравоохранения города Москвы»
По рабочим дням с 8.30 до 16.30
Платные услуги: консультации, госпитализация, иные вопросы
По рабочим дням с 8.30 до 16.30
Приёмное отделение стационара
По рабочим дням с 8.30 до 16.30
Запись на прием/исследования по единому справочному тел.: 122, а также через ЕМИАС, инфоматы в холле, лично в регистратуре, www.pgu.ru и mos.ru
+7 (495) 735-09-57
(Канцелярия, ул. Авиаторов, д. 38);
+7 (499) 638-35-00 (Регистратура КДЦ)
+7 (499) 730-98-74
Справочный телефон по вопросам плановой госпитализации
 | +7 (495) 934-17-53, +7 (495) 439-27-10, +7 (495) 539-30-00 |
 | info@npcmed.ru |
 | Москва, ул. Авиаторов, д. 38 |
О центре
Генетическая диагностика врожденного амавроза Лебера тип 2
С 2021 года в генетической лаборатории нашего Центра проводится генетическое исследование гена RPE65 c целью поиска мутаций методом прямого секвенирования по Сэнгеру.
Контакты
КДЦ (приемная), ул. Авиаторов, д. 22:
+7 (495) 934-17-51
Регистратура КДЦ:
+7 (495) 934-17-51
Канцелярия, ул. Авиаторов, д. 38:
+7 (495) 735-09-57
Любое копирование и размещение материалов сайта на сторонних ресурсах допускается только с прямой ссылкой на материал или на главную страницу сайта.
Мы используем сookie
Мы используем cookie
Уведомляем вас, что мы обрабатываем ваши персональные данные с использованием метрических программ. Продолжая навигацию по сайту, вы выражаете свое согласие с Политикой обработки персональных данных, а также на обработку Ваших персональных данных. Подробнее
Мы используем cookie
Уведомляем вас, что мы обрабатываем ваши персональные данные с использованием метрических программ. Продолжая навигацию по сайту, вы выражаете свое согласие с Политикой обработки персональных данных, а также на обработку Ваших персональных данных.
Амавроз Лебера
Внимание! Информация носит ознакомительный характер и не предназначена для постановки диагноза и назначения лечения. Всегда консультируйтесь с профильным врачом!
Что такое амавроз Лебера?
Врожденный амавроз Лебера (сокр. ВАЛ) — редкое генетическое заболевание глаз. Пострадавшие дети часто слепы при рождении. Другие симптомы могут включать косоглазие; быстрые непроизвольные движения глаз (нистагм); необычная чувствительность к свету (светобоязнь); помутнение хрусталика глаз (катаракта); и/или в форме конуса передней части глаза (кератоконус).
Врожденный амавроз Лебера начинается раньше всего и может иметь наиболее тяжкие последствия. Уровень потери зрения при ВАЛ различается от случая к случаю, но остается стабильным в 75% случаев. У примерно 15% детей отмечается прогрессирующая потеря зрения, а у 10% может отмечаться некоторое незначительное, часто временное, улучшение.
Амавроз Лебера характеризуется отсутствием всяческих патологических изменений глаза, которые можно было бы разглядеть визуально, а возникает эта болезнь вследствие нарушения функционирования зрительного нерва вместе с остальными отделами, отвечающими за зрение. Вот почем при ВАЛ глаза обычно кажутся нормальными до первичного осмотра.
Амавроз Лебера обычно наследуется как аутосомно-рецессивное генетическое заболевание.
Признаки и симптомы
Снижение зрительной реакции при рождении является первым признаком заболевания. Часто ребенок тыкает, нажимает и протирает глаза, чтобы стимулировать сетчатку глаза для получения света. Эта деятельность может привести к тому, что глаза станут запавшими или глубоко посаженными (энофтальм).
Другие симптомы могут включать:
Кроме того, у некоторых детей может быть потеря слуха, умственная отсталость и/или задержка развития.
Причины
Врожденный амавроз Лебера является моногенным заболеванием, и по меньшей мере в болезнь вовлечены 27 генов. Изменения (мутации) в этих генах могут составлять около 80-90% диагностированных случаев ВАЛ. Гены, ответственные за оставшиеся 10-20% диагнозов, неизвестны. ВАЛ обычно наследуется как аутосомно-рецессивное генетическое заболевание. Двадцать четыре из генов, связанных с ВАЛ, вызывают только рецессивное заболевание. Известно, что два гена (IMPDH1 и OTX2) вызывают доминантное заболевание. Известно, что один ген (CRX) вызывает доминантное или рецессивное заболевание в зависимости от конкретной мутации.
Рецессивные генетические нарушения возникают, когда человек наследует две копии ненормального гена по одному признаку, по одной от каждого родителя. Если человек получает один нормальный ген и один ген заболевания, человек будет носителем заболевания, но обычно бессимптомным. Риск для двух родителей-носителей, которые оба передадут дефектный ген и заразят ребенка, составляет 25% с каждой беременностью. Риск родить ребенка, который будет носителем, как родители, составляет 50% с каждой беременностью. Шанс для ребенка получить нормальные гены от обоих родителей и быть генетически нормальным для этой конкретной черты составляет 25%. Риск одинаков для мужчин и женщин.
В человеке содержится около 20 000 различных генов, и все люди имеют одну копию нескольких аномальных генов. Родители, которые являются близкими родственниками (брат и сестра), имеют больше шансов, чем несвязанные родители, иметь один и тот же ненормальный ген, что повышает риск рождения детей с рецессивным генетическим расстройством.
В редких случаях амавроз Лебера наследуется как аутосомно-доминантное генетическое заболевание. В настоящее время известно, что мутации в трех генах, CRX, IMPDH1 и OTX2, связаны с этим типом ВАЛ.
Доминантные генетические расстройства возникают, когда только одна копия ненормального гена необходима для того, чтобы вызвать конкретное заболевание. Аномальный ген может быть унаследован от любого из родителей или может быть результатом новой мутации у пострадавшего человека. Риск передачи ненормального гена от пострадавшего родителя к потомству составляет 50% при каждой беременности. Риск одинаков для мужчин и женщин.
Затронутые группы населения
По оценкам, распространенность ВАЛ составляет 1-2 на 100 000 рождений. Это расстройство поражает мужчин и женщин в равных количествах.
Близкие по симптомам расстройства
Симптомы следующих расстройств могут быть схожими с таковыми при врожденном амаврозе Лебера. Сравнения могут быть полезны для дифференциальной диагностики:
Диагностика
Можно пройти генетическое тестирование, которое поможет определить наличие поврежденного гена, вызывающего ВАЛ. Это помогает оценить риск передачи этого заболевания от родителей детям. Тестирование также может помочь получить более точный диагноз, что позволит в дальнейшем следить за новыми открытиями в интересующей сфере, исследовательскими разработками и новыми методами лечения
Стандартные методы лечения
Лечение ВАЛ симптоматическое и поддерживающее. Для семей пострадавших детей рекомендуется генетическое консультирование.
В 2017 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило генную терапию Luxturna (Лукстурна) для лечения детей и взрослых с двумя мутациями в гене RPE65. Лукстурна производится Spark Therapeutics, Inc.
Прогноз
С возрастом обычно снижается зрение, а к третьему или четвертому десятилетию жизни наблюдается полная слепота.
Высшее образование (Кардиология). Врач-кардиолог, терапевт, врач функциональной диагностики. Хорошо разбираюсь в диагностике и терапии заболеваний дыхательной системы, желудочно-кишечного тракта и сердечно-сосудистой системы. Закончила академию (очно), за плечами большой опыт работ.
Специальность: Кардиолог, Терапевт, Врач функциональной диагностики.
Публикации в СМИ
Заболевания сетчатки и зрительного нерва наследственные
Наследственные заболевания сетчатки и зрительного нерва — обширная гетерогенная группа заболеваний, приводящих к снижению или полному отсутствию зрения. В зависимости от преимущественного поражения сетчатки или зрительного нерва выделяют следующие подгруппы.
• Амавроз врождённый — наследуемая абиотрофия палочек и колбочек сетчатки и атрофия зрительных нервов, проявляющиеся быстрым развитием двусторонней центральной скотомы. Наблюдают преимущественно у мужчин, может развиться в любом возрасте (многие формы врождённые — амавроз врождённый Лебера: • тип 1: 204000, GUC2D, GUCSD, LCA1, 600179 [гуанилат циклаза 2D], 17p13; • тип 2: 204100, RPE65 [белок пигментного эпителия сетчатки], 180069, 1p31). Характеризуется прогрессирующим ухудшением зрения. В основе лежат наследуемые заболевания (мутации митохондриального и ядерного геномов). Известно, как минимум, 18 мутаций митохондриальной ДНК и не менее 6 локусов ядерной ДНК. Большую частоту заболевания у мужчин объясняют влиянием андрогенов (например, описан случай резкой потери зрения больным с мутацией MTND4*LHON11778А после терапии андрогенами).
• Атрофия зрительного нерва — конечный результат дистрофических изменений ганглиозных нейронов сетчатки. Первичная атрофия зрительного нерва — генетически обусловленная патология; компонент или единственное проявление при ряде наследственных заболеваний, отличающихся по срокам появления атрофии, степени тяжести, сопутствующим симптомам и типу наследования. Отмечают все основные типы наследования, включая мутации митохондриального генома (атрофия зрительного нерва Лебера, #535000, гены MTND [NADH-убихинон оксидоредуктаза митохондриального генома, КФ 1.6.5.3]).
• Атрофия зрительного нерва — часто компонент наследственных синдромов •• Атаксия Фридрайха с атрофией зрительного нерва и нейросенсорной тугоухостью (136600, Â ) •• Болезнь ван Бухема: иногда первое проявление этой патологии — атрофия зрительного нерва за счёт его сдавления гиперостозными разрастаниями костей черепа •• Атрофия зрительного нерва, глухота и дистальная нейрогенная амиотрофия (258650, r ) •• Метафизарная дисплазия, анетодермия (фокальная атрофия кожи) и атрофия зрительного нерва (250450, r ) •• Атрофия зрительного и слухового нервов с деменцией (311150, À ).
• Дегенерация сетчатки пигментная — прогрессирующая атрофия нейроэпителия с атрофией и пигментной инфильтрацией внутренних слоёв сетчатки. Часто применяемый термин «пигментный ретинит» не совсем точно отражает суть процесса, поскольку воспалительной реакции как таковой не возникает. Основные проявления обусловлены утратой палочек сетчатки. В основе лежит множество мутаций в ряде локусов (например, гены периферина [179605], родопсина [180380], цГМФ управляемого канала фоторецепторов [123825] и др.). Пигментная дегенерация сетчатки, не ассоциированная с другими нарушениями, наиболее часто наследуется как r (268000) и реже как À рецессивная (312600) признак. Доминантное наследование отмечают в 3–4% случаев. Кроме того, атипичный пигментный ретинит наблюдают при множестве других состояний, включая такие рецессивные нарушения, как абеталипопротеинемия (200100), синдромы Альстрема (203800), Рефсума (266500), Барде–Бидла (209900), Лоуренса–Муна (245800), Ашера (276900), Коккейна (216400), паллидарная дегенерация (260200).
• Дегенерация сетчатки коллоидная (сотовидный хориоидит Дойна, *126600, 2p16, ген DHRD, Â ). Множественные очаги округлой формы беловатого цвета, расположенные у диска зрительного нерва и в зоне между верхней и нижней височными артериолами.
• Дистрофия глазного дна Сорсби (#136900, псевдовоспалительная дистрофия глазного дна, 22q12.1–q13.2, ген тканевого ингибитора металлопротеиназы-3 TIMP3 [*188826], Â ). Клинически: дистрофия жёлтого пятна, глазного дна, атрофия сетчатки.
• Дистрофия жёлтого пятна кистозная (*153880, 7p21–p15, ген MDDC, Â ). Клинически: кистозный отёк жёлтого пятна, беловатые точечные отложения в стекловидном теле, дальнозоркость, косоглазие, снижение остроты зрения, перицентральный пигментный ретинит.
• Дистрофия палочек и колбочек, типы и гены: • тип 1, 600624, CORD1, CRD1, 18q21.1 q21.3; • тип 2, 120970, CRX, CORD2, CRD, 602225, 19q13.3
• Дистрофия пигментного эпителия сетчатки, 179605 (мутации гена периферина RDS, RP7), 6p21.1 cen
• Дистрофия сетчатки ранняя (аутосомно рецессивная): 180069, ген RPE65, 1p31
• Дистрофия хориоидеи центральная (215500, ген CACD, 17p)
Дифференциальная диагностика • Инфекционные ретинопатии — вирусные (краснуха) или бактериальные (сифилис) • Остаточные явления экссудативной отслойки сетчатки • Вторичные токсические ретинопатии (хлорохин или фенотиазины) • Другие патологические состояния (окклюзия глазной артерии, травмы).
Течение и прогноз • Прогноз наиболее неблагоприятный при врождённых формах • Течение в большинстве случаев хроническое, медленно прогрессирующее.
МКБ-10 • H31.2 Наследственная дистрофия сосудистой оболочки глаза • H35.5 Наследственные ретинальные дистрофии • Q14 Врождённые аномалии [пороки развития] заднего сегмента глаза
ПРИЛОЖЕНИЯ
Слепота цветовая (ахроматопсия) — отсутствие цветового зрения. Возможность различать любые цвета (трихромазия, основы теории цветного зрения предложил в 1802 г. Томас Янг) определяется присутствием в сетчатке всех трёх зрительных пигментов (для красного, зелёного и синего — первичные цвета). Дихромазии — дефекты цветового восприятия (преимущественно у мужчин; например, разные дефекты у мужчин составляют 8% общей популяции) по одному из первичных цветов — подразделяют на протанопии, дейтанопии и тританопии (от греч. первый, второй и третий [имеются в виду порядковые номера первичных цветов: соответственно красный, зелёный, синий]) • Протанопия (страдает восприятие красного, примерно 25% случаев цветовой слепоты) • Дейтанопия (цветовая слепота по восприятию зелёного, около 75% всех случаев) • Тританопия (страдает преимущественно восприятие фиолетового цвета, дефектное зрение по синему и жёлтому) • Дальтонизм — нарушение цветового зрения — неспособность различать красный и зеленый цвета. МКБ-10. H53.5 Аномалии цветового зрения.
Слепота преходящая (amaurosis fugax) — острый эпизод полной или частичной потери зрения, длящийся обычно не более 10 мин. Причины: кратковременная ишемия в бассейне сонной артерии (как правило, эмболия артерий сетчатки). Лечение • Лекарственная терапия •• Антигипертензивные средства •• Фибринолитические средства •• Антиагреганты (ацетилсалициловая кислота, дипиридамол) • Хирургическое: эндартерэктомия сонной артерии. МКБ-10. G45.3 Преходящая слепота.
Хориоидеремия Х-сцепленная (*303100, ген CHM, Xq21.2; форма с глухотой и ожирением, 303110) — наследственная болезнь глаз, прогрессирующие понижение остроты зрения, сужение полей зрения, гемералопия и близорукость; характерные изменения глазного дна (почти полное отсутствие сосудистого рисунка, резкие контуры и красновато-коричневый цвет жёлтого пятна, нечёткость границ диска зрительного нерва). Синоним: атрофия сосудистой оболочки прогрессирующая. МКБ-10. H31.2 Наследственные дистрофии сосудистой оболочки глаза.
Код вставки на сайт
Заболевания сетчатки и зрительного нерва наследственные
Наследственные заболевания сетчатки и зрительного нерва — обширная гетерогенная группа заболеваний, приводящих к снижению или полному отсутствию зрения. В зависимости от преимущественного поражения сетчатки или зрительного нерва выделяют следующие подгруппы.
• Амавроз врождённый — наследуемая абиотрофия палочек и колбочек сетчатки и атрофия зрительных нервов, проявляющиеся быстрым развитием двусторонней центральной скотомы. Наблюдают преимущественно у мужчин, может развиться в любом возрасте (многие формы врождённые — амавроз врождённый Лебера: • тип 1: 204000, GUC2D, GUCSD, LCA1, 600179 [гуанилат циклаза 2D], 17p13; • тип 2: 204100, RPE65 [белок пигментного эпителия сетчатки], 180069, 1p31). Характеризуется прогрессирующим ухудшением зрения. В основе лежат наследуемые заболевания (мутации митохондриального и ядерного геномов). Известно, как минимум, 18 мутаций митохондриальной ДНК и не менее 6 локусов ядерной ДНК. Большую частоту заболевания у мужчин объясняют влиянием андрогенов (например, описан случай резкой потери зрения больным с мутацией MTND4*LHON11778А после терапии андрогенами).
• Атрофия зрительного нерва — конечный результат дистрофических изменений ганглиозных нейронов сетчатки. Первичная атрофия зрительного нерва — генетически обусловленная патология; компонент или единственное проявление при ряде наследственных заболеваний, отличающихся по срокам появления атрофии, степени тяжести, сопутствующим симптомам и типу наследования. Отмечают все основные типы наследования, включая мутации митохондриального генома (атрофия зрительного нерва Лебера, #535000, гены MTND [NADH-убихинон оксидоредуктаза митохондриального генома, КФ 1.6.5.3]).
• Атрофия зрительного нерва — часто компонент наследственных синдромов •• Атаксия Фридрайха с атрофией зрительного нерва и нейросенсорной тугоухостью (136600, Â ) •• Болезнь ван Бухема: иногда первое проявление этой патологии — атрофия зрительного нерва за счёт его сдавления гиперостозными разрастаниями костей черепа •• Атрофия зрительного нерва, глухота и дистальная нейрогенная амиотрофия (258650, r ) •• Метафизарная дисплазия, анетодермия (фокальная атрофия кожи) и атрофия зрительного нерва (250450, r ) •• Атрофия зрительного и слухового нервов с деменцией (311150, À ).
• Дегенерация сетчатки пигментная — прогрессирующая атрофия нейроэпителия с атрофией и пигментной инфильтрацией внутренних слоёв сетчатки. Часто применяемый термин «пигментный ретинит» не совсем точно отражает суть процесса, поскольку воспалительной реакции как таковой не возникает. Основные проявления обусловлены утратой палочек сетчатки. В основе лежит множество мутаций в ряде локусов (например, гены периферина [179605], родопсина [180380], цГМФ управляемого канала фоторецепторов [123825] и др.). Пигментная дегенерация сетчатки, не ассоциированная с другими нарушениями, наиболее часто наследуется как r (268000) и реже как À рецессивная (312600) признак. Доминантное наследование отмечают в 3–4% случаев. Кроме того, атипичный пигментный ретинит наблюдают при множестве других состояний, включая такие рецессивные нарушения, как абеталипопротеинемия (200100), синдромы Альстрема (203800), Рефсума (266500), Барде–Бидла (209900), Лоуренса–Муна (245800), Ашера (276900), Коккейна (216400), паллидарная дегенерация (260200).
• Дегенерация сетчатки коллоидная (сотовидный хориоидит Дойна, *126600, 2p16, ген DHRD, Â ). Множественные очаги округлой формы беловатого цвета, расположенные у диска зрительного нерва и в зоне между верхней и нижней височными артериолами.
• Дистрофия глазного дна Сорсби (#136900, псевдовоспалительная дистрофия глазного дна, 22q12.1–q13.2, ген тканевого ингибитора металлопротеиназы-3 TIMP3 [*188826], Â ). Клинически: дистрофия жёлтого пятна, глазного дна, атрофия сетчатки.
• Дистрофия жёлтого пятна кистозная (*153880, 7p21–p15, ген MDDC, Â ). Клинически: кистозный отёк жёлтого пятна, беловатые точечные отложения в стекловидном теле, дальнозоркость, косоглазие, снижение остроты зрения, перицентральный пигментный ретинит.
• Дистрофия палочек и колбочек, типы и гены: • тип 1, 600624, CORD1, CRD1, 18q21.1 q21.3; • тип 2, 120970, CRX, CORD2, CRD, 602225, 19q13.3
• Дистрофия пигментного эпителия сетчатки, 179605 (мутации гена периферина RDS, RP7), 6p21.1 cen
• Дистрофия сетчатки ранняя (аутосомно рецессивная): 180069, ген RPE65, 1p31
• Дистрофия хориоидеи центральная (215500, ген CACD, 17p)
Дифференциальная диагностика • Инфекционные ретинопатии — вирусные (краснуха) или бактериальные (сифилис) • Остаточные явления экссудативной отслойки сетчатки • Вторичные токсические ретинопатии (хлорохин или фенотиазины) • Другие патологические состояния (окклюзия глазной артерии, травмы).
Течение и прогноз • Прогноз наиболее неблагоприятный при врождённых формах • Течение в большинстве случаев хроническое, медленно прогрессирующее.
МКБ-10 • H31.2 Наследственная дистрофия сосудистой оболочки глаза • H35.5 Наследственные ретинальные дистрофии • Q14 Врождённые аномалии [пороки развития] заднего сегмента глаза
ПРИЛОЖЕНИЯ
Слепота цветовая (ахроматопсия) — отсутствие цветового зрения. Возможность различать любые цвета (трихромазия, основы теории цветного зрения предложил в 1802 г. Томас Янг) определяется присутствием в сетчатке всех трёх зрительных пигментов (для красного, зелёного и синего — первичные цвета). Дихромазии — дефекты цветового восприятия (преимущественно у мужчин; например, разные дефекты у мужчин составляют 8% общей популяции) по одному из первичных цветов — подразделяют на протанопии, дейтанопии и тританопии (от греч. первый, второй и третий [имеются в виду порядковые номера первичных цветов: соответственно красный, зелёный, синий]) • Протанопия (страдает восприятие красного, примерно 25% случаев цветовой слепоты) • Дейтанопия (цветовая слепота по восприятию зелёного, около 75% всех случаев) • Тританопия (страдает преимущественно восприятие фиолетового цвета, дефектное зрение по синему и жёлтому) • Дальтонизм — нарушение цветового зрения — неспособность различать красный и зеленый цвета. МКБ-10. H53.5 Аномалии цветового зрения.
Слепота преходящая (amaurosis fugax) — острый эпизод полной или частичной потери зрения, длящийся обычно не более 10 мин. Причины: кратковременная ишемия в бассейне сонной артерии (как правило, эмболия артерий сетчатки). Лечение • Лекарственная терапия •• Антигипертензивные средства •• Фибринолитические средства •• Антиагреганты (ацетилсалициловая кислота, дипиридамол) • Хирургическое: эндартерэктомия сонной артерии. МКБ-10. G45.3 Преходящая слепота.
Хориоидеремия Х-сцепленная (*303100, ген CHM, Xq21.2; форма с глухотой и ожирением, 303110) — наследственная болезнь глаз, прогрессирующие понижение остроты зрения, сужение полей зрения, гемералопия и близорукость; характерные изменения глазного дна (почти полное отсутствие сосудистого рисунка, резкие контуры и красновато-коричневый цвет жёлтого пятна, нечёткость границ диска зрительного нерва). Синоним: атрофия сосудистой оболочки прогрессирующая. МКБ-10. H31.2 Наследственные дистрофии сосудистой оболочки глаза.