Амоксициллин или супракс для детей что лучше
Антимикробная терапия острого среднего отита в педиатрической практике
Острый средний отит (ОСО) является одним из частых воспалительных заболеваний у детей младшего и среднего возраста [2, 5, 7]. По числу осложнений ОСО занимает второе место среди ЛОР-патологии [4, 10, 11], у 30% детей приобретает затяжное течение и склонно
Острый средний отит (ОСО) является одним из частых воспалительных заболеваний у детей младшего и среднего возраста [2, 5, 7]. По числу осложнений ОСО занимает второе место среди ЛОР-патологии [4, 10, 11], у 30% детей приобретает затяжное течение и склонность к рецидивированию [1]. Острый средний отит — это остро развившееся воспаление полостей среднего уха (барабанной полости, сосцевидного отростка, слуховой трубы), проявляющееся одним или несколькими симптомами (боль в ухе, повышение температуры тела, выделения из уха, у маленьких детей понос, тошнота).
Довольно часто ОСО являются так называемым бактериальным осложнением острых респираторных вирусных инфекций (ОРВИ). При этом может отсутствовать болевой синдром и снижение слуха, а симптомы наблюдающейся общей интоксикации нередко расцениваются врачом как клиническое проявление основного заболевания. Острое воспаление среднего уха выявляется у 19,7% детей, больных ОРВИ (обследовано 3567 пациентов) [8].
При типичном остром среднем отите воспалительный процесс в полостях среднего уха не выходит за рамки выстилающей их слизистой оболочки. Отражающая этот процесс патолого-анатомическая картина достаточно типична и характеризуется отеком, капиллярной гиперемией и лейкоцитарной инфильтрацией слизистой оболочки, особенно ее субэпителиального слоя. А в эпителиальном, покровном слое отмечается некоторое увеличение числа продуцирующих слизь бокаловидных клеток, поэтому в экссудате, образующемся при остром воспалении среднего уха, всегда есть та или иная примесь слизи. В совокупности указанные изменения приводят к выраженной гиперплазии слизистой оболочки среднего уха, особенно в барабанной полости, где ее толщина способна увеличиваться в 30 раз и более. Происходит накопление экссудата, который поначалу может быть серозным, затем серомукозным и далее — мукозно-гнойным и гнойным. Слуховые косточки, которые оказываются погруженными в утолщенную слизистую оболочку барабанной полости и скопившийся в ней экссудат, в значительной степени теряют свою подвижность, что вместе с тугоподвижностью воспалительно-измененной барабанной перепонки обусловливает существенное ухудшение слуховой функции. При увеличении количества экссудата в среднем ухе, давление, оказываемое им на барабанную перепонку, повышается, и это приводит к нарушению микроциркуляции, трофическим и некротическим изменениям барабанной перепонки, следствием которых является образование ее перфорации и появление трансмеатальной отореи.
В детском возрасте острый средний отит имеет ряд особенностей и возникает чаще, чем у взрослых, прежде всего из-за анатомо-физиологических особенностей: более широкая, короткая и горизонтально расположенная слуховая труба, наличие аденоидных вегетаций, более быстрое нарушение функции мерцательного эпителия при воспалении. Несформированный иммунитет может приводить к реактивному и часто осложненному течению детских инфекционных заболеваний. В младенческом возрасте увеличивается риск развития внутричерепных осложнений из-за незаращения каменисто-чешуйчатой щели височной кости, через которую инфекция может проникать в полость черепа, поражая мозговые структуры. Следует отметить, что диагностика отита у детей раннего возраста осложнена из-за ограниченного вербального контакта и затруднений при отоскопии [3].
Основными профилактическими мероприятиями острого среднего отита являются предупреждение и своевременное лечение простудных заболеваний, обучение правильному туалету носа (поочередно правой и левой половин).
Лечение острого среднего отита должно быть комплексным и включать адекватные терапевтические мероприятия, которые можно разделить на местные и общие. Для уменьшения отека в области носоглоточного устья слуховой трубы и восстановления ее вентиляционной и дренирующей функций используют назальные сосудосуживающие капли (Нафтизин, Тизин и т. п.), которые необходимо закапывать в нос при запрокинутой назад голове. Обязательным является лечение сопутствующего ринита или риносинусита. Препараты, вводимые в слуховой проход, должны быть комбинированными и обладать противовоспалительным действием, противобактериальным и противогрибковым, антиаллергическим и обезболивающим эффектами. В ряде случаев, в частности при тяжелом течении отита, необходимо прибегать к антибиотикам системного действия.
При выборе лекарственного средства следует учитывать эпидемиологическую ситуацию, особенности клинической картины, возраст пациента, наличие сопутствующих заболеваний, сведения о ранее проводимой антибактериальной терапии и переносимости лекарственных препаратов.
Антибиотик, применяемый для терапии отитов, должен обладать не только высокой эффективностью, широким спектром антибактериального действия и хорошим проникновением в очаг воспаления, но и низкой токсичностью, удобством приема.
Микробиологическая диагностика средних отитов основана на бактериологическом исследовании содержимого среднего уха, полученного при парацентезе или тимпанопункции. Исследования, проведенные в США, Европе и Японии, показали, что самым распространенным возбудителем острого среднего отита является Streptococcus pneumoniae, на втором месте — нетипируемые штаммы Haemophilus influenzae, на третьем месте — Moraxella catarrhalis. Менее чем 10% ОСО вызываются другими микроорганизмами, например стрептококками группы А и Staphylococcus aureus. Этиология ОСО не может быть установлена по клинической картине, однако следует отметить, что пневмококковый ОСО обычно протекает тяжелее, чаще приводит к развитию осложнений и не склонен к саморазрешению. Из 90 серотипов S. pneumoniae только несколько вызывают ОСО. Наиболее распространены из них серотипы 19, 23, 6, 14, 3 и 18. Использование вакцины, содержащей капсульные полисахариды 7–8 наиболее часто встречаемых серотипов S. pneumoniae, способно предотвратить более чем 80% ОСО пневмококковой этиологии. Большинство штаммов H. influenzae, вызывающих ОСО, являются нетипируемыми. По современным данным, около 20–50% H. influenzae, выделяемых при ОСО, продуцируют бета-лактамазы [9].
Результаты многочисленных многолетних исследований сходны с результатами зарубежных авторов и показывают, что наиболее вероятными возбудителями острого среднего отита в России являются St. aureus, St. epidermidis, S. pneumoniae и H. influenzae, несколько реже Streptococcus pyogenes, S. viridans, M. catarrhalis анаэробы.
В лечении ОСО многочисленными исследованиями достоверно доказана эффективность цефалоспоринов как антибактериальных препаратов широкого спектра действия, в частности Cупракса (цефиксима) — представителя 3-го поколения цефалоспоринов. Супракс обладает высоким уровнем антибактериальной активности, улучшенными фармакокинетическими свойствами, расширенным, по сравнению с цефалоспоринами предыдущих поколений, спектром действия. Бактерицидное действие препарата обусловлено ингибированием пептидогликана — основного структурного компонента клеточной стенки бактерий. Биодоступность препарата (около 50%) позволяет исключить парентеральный путь введения. Максимальная концентрация в крови достигается уже через 4 ч. Супракс хорошо проникает в место инфицирования. Период полувыведения зависит от дозы и составляет 3–4 ч, а в тканях препарат задерживается на более длительный срок, что позволяет принимать его 1 раз в сутки. Препарат хорошо переносится больными. Эти свойства Супракса позволяют считать целесообразным его применение в детской оториноларингологической практике.
Было проведено обследование и лечение 30 детей с ОСО 7–12 лет (девочек — 14, мальчиков — 16). Всем пациентам проводили лечение Супраксом из расчета 5 мг/кг 2 раза в сутки в течение 6 дней.
В качестве контрольных использовали результаты, полученные при наблюдении за аналогичной в количественном и возрастном отношении группой детей, получавших амоксициллина клавуланат (2 дозировочные ложечки по 5 мл (312 мг) 3 раза в сутки парентерально в течение 6 дней).
Обследование включало: ЛОР-осмотр, аудиометрию, тимпанометрию, компьютерную томографию околоносовых пазух, рентгенографию височных костей по Шюллеру и Майеру, клинический анализ крови, бактериологическое исследование отделяемого из слухового прохода при наличии перфорации барабанной перепонки.
По данным микробиологического исследования отделяемого, полученного из слухового прохода у 18 детей обеих групп, среди возбудителей преобладал S. pneumoniae — у 11 детей, реже встречались St. aureus — у 4, H. influenzae — у 2 пациентов, в одном случае роста микрофлоры получено не было.
В результате лечения зафиксировано уменьшение клинических проявлений и положительная динамика объективных критериев заболевания у детей из основной и контрольной групп (тимпанометрия, аудиометрия, клинический анализ крови). Эффективность Супракса была сравнимой с амоксициллина клавуланатом, считающимся препаратом выбора при ОСО [6].
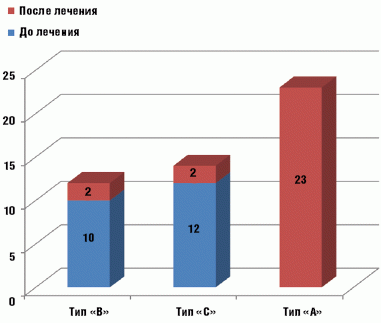
В основной группе до начала лечения у всех детей зарегистрирована кондуктивная тугоухость, тимпанограмма типа «В» выявлена у 10, «С» у 12 детей, 8 детям тимпанометрия не проводилась из-за наличия перфорации. По окончании курса лечения Супраксом кондуктивная тугоухость сохранялась у 7 пациентов, тимпанограмма «А» зафиксирована у 23, «В» у 2 и «С» у 2 пациентов, 3 детям тимпанометрия не проводилась из-за наличия перфорации (рис. 1).
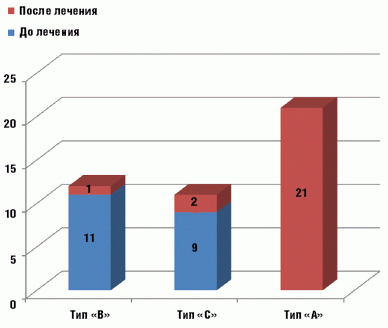
В контрольной группе до начала лечения у всех детей зарегистрирована кондуктивная тугоухость, тимпанограмма типа «В» выявлена у 11, «С» — у 9 больных, 10 детям тимпанометрия не проводилась из-за наличия перфорации. По завершении 6-дневного курса терапии амоксициллина клавуланатом кондуктивная тугоухость сохранялась у 9 пациентов, тимпанограмма типа «А» зафиксирована у 21, «В» — у 1, «С» — у 2 детей, 6 пациентам тимпанометрия не проводилась из-за наличия перфорации (рис. 2).
Нежелательных эффектов, требующих отмены препаратов, ни в одной из групп зафиксировано не было.
Таким образом, подтверждена высокая эффективность и безопасность препарата Супракс при остром среднем отите у детей. Супракс может быть рекомендован для широкого применения в детской оториноларингологической практике.
Литература
О. В. Зайцева, кандидат медицинских наук
ФГУ НКЦ оториноларингологии ФМБА России, Москва
Антибиотики в арсенале участкового педиатра для лечения болезней органов дыхания
Хотя диагностика и лечение респираторной патологии у детей занимают ведущее место в работе педиатра, антибактериальная терапия требуется практически всего 6–8% больным этой категории — в основном с отитом, синуситом, стрептококковой ангиной, л
Хотя диагностика и лечение респираторной патологии у детей занимают ведущее место в работе педиатра, антибактериальная терапия требуется практически всего 6–8% больным этой категории — в основном с отитом, синуситом, стрептококковой ангиной, лимфаденитом, пневмонией, а также при бронхитах, вызванных только микоплазмой и хламидиями. К сожалению, и у нас, и за рубежом далеко не изжито избыточное применение этих препаратов — их применяют подчас у 30–80% детей с острыми респираторными вирусными инфекциями (ОРВИ). Не принося пользы, такая практика повышает риск развития устойчивости флоры и побочных явлений, дезориентируя к тому же врача: не получив эффекта от антибиотика при вирусной инфекции, врач переходит на резервные препараты, которые также не дают эффекта. Поэтому основной вопрос — показаны ли антибиотики данному больному? — решать положительно следует при только доказанной (или вероятной тяжелой) бактериальной инфекции. И хотя доказать бактериальную природу острых респираторных заболеваний (ОРЗ) удается редко, накопленные данные позволяют врачу с высокой вероятностью не только выявить таких детей, но и очертить круг вероятных возбудителей и их чувствительность к антибиотикам. В табл. 1 представлены формы респираторной патологии, при которых показано и не показано назначение антибиотика, а также симптомокомплекс, позволяющий заподозрить пневмонию в отсутствие четких физикальных данных, и значения маркеров воспаления, при которых введение антибиотика оправдано.
В табл. 2 представлены основные возбудители бактериальных ОРЗ; очевидно, что спектр возбудителей ОРЗ у детей невелик, что облегчает выбор препарата, который действует на вероятных возбудителей конкретного заболевания. Эти данные для антибиотиков, которые следует применять в амбулаторных условиях, приведены в табл. 3.
К счастью, резистентность к пенициллину циркулирующих среди населения России пневмококков (менее 10% штаммов) во много раз ниже, чем, например, в странах Юго-Запада Европы (40–50%). Но следует учитывать, что среди детей в детских дошкольных учреждениях (ДДУ) и особенно в интернатах 50–60% выделенных штаммов пневмококков устойчивы к пенициллину. Пневмококки сохраняют 100-процентную чувствительность к амоксициллину (а также к цефтриаксону), но устойчивы к ко-тримоксазолу, тетрациклину, гентамицину и другим аминогликозидам. Устойчивость пневмококков к пенициллинам не связана с выработкой лактамазы (она обусловлена потерей пенициллин-связывающих белков), поэтому применение ингибитор-защищенных пенициллинов не повышает эффективности лечения. Устойчивость пневмококков к макролидам растет быстрее (до 15–20% штаммов в некоторых регионах), в меньшей степени она растет к 16-членным макролидам: джозамицину, мидекамицину, спирамицину.
Haеmophilus influenzae (как бескапсульные, так и типа b) в России чувствительны к амоксициллину, доксициклину, цефалоспоринам 2 и 3 поколений, всем аминогликозидам. Но эти возбудители не чувствительны к пенициллину, цефалексину, цефазолину, большинству макролидов — кроме азитромицина (его применение при отитах и синуситах ограничено низкой его концентрацией в соответствующих полостях).
Под влиянием лечения H. influenzae вырабатывает лактамазы, инактивирующие лактамные препараты (в т. ч. пенициллин и амоксициллин), поэтому у детей, леченных ранее (а также у детей из ДДУ), применяются с начала лечения амоксициллин/клавуланат или цефуроксим аксетил.
Бета-гемолитический стрептококк группы А (БГСА) чувствителен ко всем антибиотикам, кроме аминогликозидов, однако в ряде регионов частота устойчивых к макролидам штаммов может достигать 15%. Moraxella catarrhalis, способная продуцировать лактамазу, выделяемая обычно у леченых ранее детей, чувствительна к макролидам, цефалоспоринам, аминогликозидам, но резистентна к амоксициллину.
Золотистый стафилококк редко вызывает «амбулаторные» формы поражения дыхательных путей (гнойный синусит, шейный лимфаденит); он, как правило, не чувствителен к пенициллинам, есть и штаммы, резистентные к цефалексину и амоксициллину/клавуланату, а его чувствительность к макролидам быстро снижается, если лечение длится более 5–7 дней. Препаратами выбора является цефалексин внутрь, а при более тяжелых формах — оксациллин (парентерально), а в случае устойчивости к нему — ванкомицин.
В амбулаторной практике назначают препараты первого выбора, если нет оснований предполагать наличие лекарственной устойчивости (табл. 4). При подавляющем большинстве форм эффективны оральные формы пенициллинов, цефалоспоринов первого-второго поколений и макролидов, их надежнее всего вводить в детской лекарственной форме — гранулах, диспергируемых таблетках Солютаб или сиропе, позволяющей точное дозирование.
Наиболее используемый препарат первого выбора — амоксициллин (Флемоксин Солютаб и др.), на него приходится (по весу) 1/3 всех выпускаемых в мире антибиотиков. Его биодоступность выше, чем у ампициллина внутрь, что вытеснило последний из арсенала педиатра. Другие препараты первого выбора: феноксиметилпенициллин (сироп Оспен) и цефалексин используют только для лечения стрептококкового тонзиллита, а макролиды — «атипичных» инфекций (микоплазмоз и хламидиоз), а также для лечения кокковых инфекций у больных с аллергией на пенициллины.
С препаратов второго выбора начинают лечение только в случае предшествующей (за последние 2–3 месяца) терапии антибиотиками, а также при внутрибольничной инфекции (у ребенка, заболевшего через 1–3 суток после выписки из стационара). Наиболее используемый препарат — амоксициллин/клавуланат — Амоксиклав, Аугментин, Флемоклав Солютаб), эффективный как против пневмо- и стрептококков, так и гемофильной палочки и моракселл. Цефалоспорины второго поколения (цефуроксим аксетил — Зиннат, который намного активнее цефаклора в отношении пневмо- и стрептококков) также эффективны как препараты второго выбора. Используются возрастные дозировки, однако для амоксициллина/клавуланата и Зинната в ряде инструкций указаны заниженные (20–30 мг/кг/сут) дозы, которые могут оказаться недостаточными (см. наблюдение) — они не должны быть ниже 45–50 мг/кг/сут.
Средства третьего выбора (резервные, обычно парентеральные) применяют только в случаях полирезистентности, обычно в условиях стационара.
Не используют при респираторной патологии ко-тримоксазол и тетрациклин ввиду роста устойчивости к ним пневмотропной флоры, а также оральные цефалоспорины третьего поколения — цефтибутен (Цедекс) и цефиксим (Супракс), которые могут быть недостаточно активными в отношении кокковой флоры, в частности, пневмококков.
Оральные антибиотики не используют при тяжелых острых процессах. К ним относится гнойный синусит (протекает с отеком щеки или окологлазной клетчатки), он часто требует оперативного вмешательства, лимфаденит с признаками гнойного воспаления (спаянность с гиперемированной кожей, флюктуация). У детей с крупом важно исключить эпиглоттит — бактериальное воспаление надгортанника, также вызывающее инспираторный стридор как при вирусном крупе, но с фебрильной температурой, интоксикацией, болями при глотании при отсутствии лающего кашля, дисфонии. Для эпиглоттита характерно усиление диспноэ в положении на спине, нейтрофильный лейкоцитоз, он требует ранней интубации для профилактики асфиксии. Эти заболевания, как и осложненная плевритом и деструкцией пневмония, требуют госпитализации, перед которой следует ввести парентерально препарат широкого спектра — цефтриаксон (80 мг/кг), который должен быть в укладке скорой и неотложной помощи и у каждого участкового врача.
В остальных случаях используются оральные препараты (табл. 4). При подозрении на острый средний отит (или его диагностике при отоскопии) адекватно назначение амоксициллина в дозе 50 мг/кг/сут, или амоксициллина/клавуланата в той же дозе (преодоление устойчивости некапсульного гемофилюса и моракселл), или, у леченного недавно ребенка, в дозе 80–100 мг/кг/сут амоксициллина для преодоления возможной сниженной чувствительности пневмококков в полости среднего уха. В последнем случае желательно использовать Аугментина или Флемоклава Солютаб с соотношением амоксициллина и клавулановой кислоты 7:1. Срок лечения — 10 дней у детей до двух лет и 7 дней — у старших.
Та же лечебная тактика эффективна при негнойном бактериальном синусите, который диагностируют на второй-третьей неделе ОРЗ при сохранении заложенности носа, часто также лихорадки, болей в проекциях пазух.
Большие сложности возникают при лечении острого тонзиллита, который лишь в 30% случаев вызывается БГСА, а в остальных — аденовирусом или вирусом Эпштейна–Барр (инфекционный мононуклеоз). Для них одинаково характерны острое начало, лихорадка с ознобом или без, боль в горле при глотании, гиперемия, отечность миндалин, часто также язычка и мягкого неба, гнойный детрит в лакунах, налеты, увеличение лимфоузлов (без нагноения). Стрептококковый тонзиллит отличается от вирусного отсутствием кашля и катара, конъюнктивита, болезненностью лимфоузлов и падением температуры через 24–48 ч после назначения антибиотика. Аденовирусный тонзиллит отличают конъюнктивит и назофарингит, мононуклеоз — назофарингит, увеличение печени и селезенки, появление в крови широкоплазменных лимфоцитов. Положительный высев делает диагноз БГСА-инфекции бесспорным, как и повышение антистрептолизина-О (АСЛ-О), поэтому во всех случаях острого тонзиллита показаны такие исследования.
При доказанном стрептококковом тонзиллите, как и при неясности этиологического диагноза (особенно у детей старше 6 лет и в весеннее время), назначают один из пенициллинов, цефалексин или макролид, которые приводят к падению температуры через 14–36 часов, подтверждая диагноз стрептококкового тонзиллита; в этих случаях лечение следует продолжить до 10 дней (для азитромицина — в дозе 12 мг/кг/сут — 5 дней). При отсутствии эффекта антибиотик можно отменить, оставив лишь симптоматическое лечение.
При поражении нижних дыхательных путей (его признаки — тахипноэ или диспноэ, наличие хрипов, укорочение перкуторного звука) важно дифференцировать вирусный бронхит от пневмонии, в подавляющем большинстве случаев — бактериальной.
Вирусный бронхит — самую частую форму поражения нижних дыхательных путей (75–300 на 1000 детей) — важно дифференцировать с бактериальной пневмонией, частота которой существенно ниже (4–15 на 1000 детей). Это тем более важно, что осложнение вирусного бронхита, в т. ч. бронхиолита у грудных детей, бактериальной пневмонией наблюдается крайне редко. Против пневмонии говорит субфебрильная температура (исключение — хламидийные формы в первые месяцы жизни, при которых ведущий симптом — тахипное) или если фебрильная поначалу температура в течение 1–3 дней снижается до субфебрильной. Типичное для бронхита обилие хрипов или признаки обструкции наблюдаются лишь при «атипичной» микоплазменной пневмонии — при этом они асимметричны и нередко сопровождаются укорочением перкуторного звука. Асимметрия хрипов наблюдается и при вызванном микоплазмой бронхите, что является показанием для рентгенографии. Для типичной (пневмококковой, гемофилюсной) пневмонии хрипы если и есть, то локальные, часто на фоне жесткого или ослабленного дыхания над участком легкого, нередко с укорочением перкуторного звука (наблюдение). К сожалению, эти локальные признаки определяются далеко не у всех больных пневмонией.
Таким образом, на основании физикальных данных обычно нетрудно исключить типичную пневмонию и назначить симптоматическую терапию вирусного бронхита. При подозрении на пневмонию (при отсутствии угрожающих симптомов) стартовый препарат — амоксициллин 50 мг/кг/сут, а у недавно леченых детей амоксициллин/клавуланат 50 мг/кг/сут или цефуроксим аксетил — 40–60 мг/кг/сут, которые, как правило, дают быстрый эффект. Отсутствие эффекта обычно указывает на «атипичную» этиологию пневмонии и требует смены препарата на макролид.
Инфекцию микоплазмой, обусловливающей у детей старше 5 лет около половины всех пневмоний (между пневмонией и бронхитом при неплотном легочном инфильтрате трудно провести грань), следует заподозрить при стойкой (5–10 дней) высокой температуре, обычно с нерезким токсикозом (не вызывающим сильной тревоги родителей), с необильными катаральными симптомами и конъюнктивитом, с обильными, мелкопузырчатыми (как у грудных детей с бронхиолитом) хрипами, но выслушиваемыми асимметрично. Характерный признак — отсутствие эффекта от назначения амоксициллина и других лактамных препаратов; назначение любого макролида в возрастной дозе приводит в течение 1–3 дней к апирексии и уменьшению явлений бронхита.
Участковые педиатры часто неверно интерпретируют симптомы этих двух видов пневмоний, назначая при более «шумных» (сопровождающихся обилием хрипов) атипичных пневмониях «более сильные» цефалоспорины, не дающие эффекта, а при типичных пневмониях с минимумом хрипов — «более слабые» макролиды. В ряде случаев типичной пневмонии макролиды дают быстрый эффект, однако вследствие роста устойчивости пневмококка они могут не давать эффекта. Поэтому следует стремиться делать стартовые назначения соответственно более вероятной форме пневмонии. Полагаться при этом на выявление, например, антител к микоплазме не надежно, т. к. на первой неделе IgM-антител может еще не быть, а ПЦР может выявлять антиген у носителей.
Для подтверждения или исключения бактериальной инфекции обычно используются так называемые маркеры бактериального воспаления — уровни лейкоцитоза, С-реактивного белка, в последнее время — также прокальцитонина. Нередко приходится видеть ребенка с ОРВИ без видимых бактериальных очагов, который получает антибиотики только потому, что у него выявлен лейкоцитоз порядка 10–15×10 9 /л. У большинства таких больных ОРВИ течет гладко без применения антибиотиков. Доказано, что только лейкоцитоз > 15×10 9 /л, абсолютное число нейтрофилов > 10×10 9 /л и/или палочкоядерных > 1,5×10 9 /л (а также С-реактивный белок (СРБ) > 30 мг/л и прокальцитонин > 2 нг/мл) более или менее надежно указывают на возможность бактериальной инфекции, тогда как более низкие цифры встречаются при вирусных инфекциях достаточно часто. Так, у детей с ОРВИ, бронхитом, крупом лейкоцитоз 10–15×10 9 /л встречается у 1/3, СРБ 15–30 мг/л — у 1/4 больных. При тонзиллитах, вызванных аденовирусами и вирусом Эпштейна–Барр, у 1/3 детей лейкоцитоз лежит в пределах 10–15×10 9 /л, а 1/3 — выше 15×10 9 /л, уровни СРБ 30–60 мг/л выявляются у 1/4 детей, а у 1/3 — выше 60 мг/л.
Следует учитывать и то, что при бактериальных инфекциях лейкоцитоз наблюдается далеко не всегда: так, при гнойном отите и типичной пневмонии у 40% больных лейкоцитоз не превышает 15´109/л, а при катаральном отите и атипичной пневмонии — у 90%.
Литература
В. К. Таточенко, доктор медицинских наук, профессор
НЦЗД РАМН, Москва
Наблюдение
Настя К. 4,5 лет поступила на 4-й день болезни, сопровождавшейся температурой 39 °C, кашлем. Две дозы Флемоклава Солютаба по 15 мг/кг эффекта не дали.
При поступлении: навязчивый кашель, покраснение правой щеки, укорочение над правым легким сверху, хрипов нет. Кровь: Л — 31,6 ´ 109/л, п/я — 29%, с/я 57%, СОЭ 36 мм/час, СРБ 60 мг/л, ПКТ 10 нг/мл.
Доза Флемоклава Солютаба 45 мг/кг привела к падению Т° к концу дня, быстрому улучшению состояния и нормализации картины в легких через 2 недели. Курс лечения — 5 дней.
Диагноз: крупозная пневмония