Анаприлин или сотагексал при аритмии что лучше
Современные подходы в терапии фибрилляции предсердий
Стенограмма лекции
Общая продолжительность: 22:08
Оксана Михайловна Драпкина, исполнительный директор Интернет Сессии, секретарь межведомственного совета по терапии РАМН:
— Следующая лекция вводит нас в интересный мир аритмии. Профессор Дощицын Владимир Леонидович. «Современные подходы к терапии больных с фибрилляцией предсердий».
Дощицын Владимир Леонидович, профессор:
В проблеме решения больных с фибрилляцией предсердий очень много аспектов и спорных вопросов. Позвольте мне сегодня остановиться именно на спорных вопросах, которые во многих своих аспектах не имеют общепринятой трактовки.
Прежде всего, напомню, что фибрилляция предсердий – одна из наиболее значимых аритмий. Распространенность ее по современным данным в общей популяции достигает 2%. У людей преклонного и старческого возраста составляет до 10%. Эта аритмия относится к таким, которые всегда требуют какого-то вмешательства.
Эта аритмия вызывает значимое повышение риска эмболических осложнений. Эмболия, связанная именно с фибрилляцией предсердий, составляет более половины всех кардиальных эмболий. В основном это инсульты. Но могут быть фибрилляции предсердий, связанные и с эмболией артерий: почечных, нижних конечностей, мезентериальных, в том числе из малого круга кровообращения – эмболией легочных артерий.
Наличие мерцательной аритмии увеличивает риск тромбоэмболии в 5 раз. У больных с ревматическими пороками, особенно митральными – в 20 раз.
Новые аспекты классификации, которая в прошлом году была предложена Европейским кардиологическим обществом. Хорошо известная, впервые выявленная аритмия еще неизвестно куда выльется. Она может стать постоянной. Может быть пароксизмальной, персистирующей.
Наиболее спорный вопрос – это отличие пароксизмальной от персистирующей. Было предложено два критерия отличия. Первый – временной – 7 суток (меньше пароксизмальная, больше персистирующая). Второй – способность к самостоятельному купированию (якобы свойственен пароксизмальной и не свойственен персистирующей).
Тут получилась довольно большая путаница. Короткие менее семи дней эпизоды, проходящие от приема лекарств, инъекции и так далее, некоторые относили к персистирующей. Более длительные и самостоятельно прекращающиеся – к пароксизмальной.
Сейчас Европейское кардиологическое общество предлагает в основном ориентироваться на временной критерий. Меньше семи дней – пароксизм, больше – персистирующая. Предложено выделять еще одну форму – длительно персистирующую. Она может длиться много месяцев и даже более года. Но допускает тактику восстановления ритма (контроля ритма), если удается, например, воздействовать на причину мерцательной аритмии заболевания, лежащего в основе.
Постоянная форма – когда мы уже не говорим о такой возможности, а говорим только о тактике контроля частоты ритма.
Хорошо известно, что мы можем придерживаться двух тактик ведения больного с рецидивирующей, то есть пароксизмальной или персистирующей фибрилляцией. Первая тактика наиболее импонирует больному и врачу. Это восстановление и удержание синусового ритма. Но правомочна и другая стратегия – поддержание числа сердечных сокращений (антикоагулянтная, антиагрегантная терапия) при сохранении фибрилляции предсердий при условии приемлемого качества жизни.
Было очень много исследований по сравнению этих двух стратегий. В конечном итоге на сегодняшний день эти исследования не показали принципиальной разницы (в смысле основного жизненного прогноза) в этих двух тактиках ведения. Правомочно и то и другое. Врачу приходится самому выбирать тактику.
На основании чего конкретный врач, конкретный больной определяет, будет он восстанавливать у больного ритм с мерцательным предсердием или не будет.
Я хотел бы здесь начать с последней строчки. Субъективная переносимость аритмии пациентом. Хочет ли пациент восстанавливать ритм. В одном случае он этого просто жаждет, категорически настаивает. В другом случае он аритмии не чувствует и критически настроен к настоятельному желанию врача восстановить ему синусовый ритм. Это один из важнейших критериев. Если больной не хочет, не ощущает аритмии, его качество жизни для него приемлемо, то это один из важнейших моментов выбора тактики контроля частоты ритма, а не контроля самой аритмии.
Вторая снизу строчка. Возможность воздействия на этиологию. Если такая возможность есть (а очень часто она есть), то мы этой возможностью пользуемся. Это является важнейшим условием эффективного воздействия на качество жизни и на возможность удержания синусового ритма. Если такой возможности нет (врожденный какой-то порок, где невозможно хирургическое вмешательство), нет и реальных шансов на удержание синусового ритма. Более приемлема тактика контроля частоты и качества жизни.
Третий пункт снизу. Риск «нормализационных» тромбоэмболий (допустим, инсульта при восстановлении синусового ритма). Когда такой инсульт наиболее высок. Если есть тромбы в левом предсердии. Если уже были эпизоды тромбоэмболических осложнений (в частности, инсульт, транзиторные ишемические атаки и так далее). Высокий риск «нормализационных» тромбоэмболий заставляет предпочитать тактику не восстановления ритма, а тактику контроля частоты при сохраняющейся аритмии. Не всегда есть возможность уменьшить риск «нормализационных» тромбоэмболий с помощью активной антикоагулянтной терапии.
Насколько легко удается с помощью антиаритмических препаратов удержать и восстановить синусовый ритм. Если удается легко, то это в пользу того, что мы можем применять тактику контроля ритма. Если приходится делать с большим трудом, очень часто, использовать большие дозы, то это, скорее, данные в пользу того, что придется избрать тактику контроля частоты ритма.
Далее. Частота и продолжительность эпизодов аритмии. Вообще насколько длительный анамнез. Со временем устанавливается стойкая аритмия. Обычно аритмия течет так, что приступы, эпизоды учащаются, удлиняются, хуже купируются. Этому способствует наличие выраженных органических изменений сердца. Вот те факторы, которые приходится учитывать врачу в вопросе, будет или не будет он восстанавливать ритм. Но все-таки естественно желание и врача и пациента восстановить и удержать ритм.
Какие возможности у нас для этого есть. Европейское кардиологическое общество издало рекомендации в прошлом году. Препараты с доказанной эффективностью. Здесь показаны те, которые зарегистрированы в России. На самом-то деле их перечислено больше. Но среди них много таких, которых у нас не применяют.
Препараты первого ряда с доказанной эффективностью. «Пропафенон» («Propafenone») («Пропанорм» («Propanorm») и «Амиодарон» («Amiodarone») («Кордарон» («Cordarone»). В принципе, и тот и другой можно применять и перорально и внутривенно. Но внутривенного пока еще «Пропафенона» у нас нет. Пероральный «Кордарон» («Cordarone») не очень удобен для купирования, так как он действует медленно и приходится давать достаточно большие дозы. Реально это «Таблетка в кармане» «Пропафенона» и внутривенное введение «Кордарона».
Кроме того, менее эффективные и более токсичные препараты. Насчет недостаточно изученных – это, пожалуй, не совсем точно. Особенно для нашей страны, потому что уже много десятилетий применяется «Новокаин-амид» («Novokain-amid») и «Хинидин» («Chinidinum»). Они используются реже. Класс рекомендаций и уровень доказательств ниже.
Что мы имеем реально. Помимо того, что названо («Кордарон» и «Пропафенон» внутривенный), есть еще «Нибентан» («Nibentan»), который сейчас используется достаточно редко. Пероральный «Пропафенон», «Кордарон» и «Хинидин».
Есть ли что-нибудь помимо этого. Врачи используют для купирования еще и «Таблетку в кармане». Допустим, есть «Ритмилен», раньше довольно часто использовался. Есть бета-блокаторы «Обзидан», «Анаприлин» («Anaprilin»), которые тоже используются (во всяком случае, практическими врачами нередко рекомендуются).
Но доказано, что эти препараты все-таки менее эффективны. В основном сегодня реально рекомендуются два препарата. Это «Пропанорм» и «Кордарон».
Существует несколько схем. Я хочу обратить особое внимание на стратегию «Таблетка в кармане», потому что это позволяет в амбулаторных условиях купировать пароксизмы без госпитализации.
И другая, более осторожная схема, когда врач по какой-то причине опасается сразу давать такую большую разовую дозу. Первый прием – две таблетки внутрь. Через час, если нет эффекта, еще одна таблетка (150 мг). Еще через 4-6 часов при отсутствии эффекта еще одна таблетка. Общая эффективность ниже 56%.
Я хочу подчеркнуть, что если больному не знаком этот препарат, то в самый первый его прием следует давать не 300 мг, а одну таблетку – 150 мг. Возможны на любой антиаритмический препарат непредсказуемые эффекты.
Сохранение синусового ритма. В последних рекомендациях Европейского кардиологического общества названы пять препаратов. Среди них «Кордарон», «Дронедарон» («Dronedarone») или «Мультаб» или «Кавенит», который у нас не зарегистрирован. «Пропанорм», «Соталол» («Sotalol») и «Соталекс» («Sotalex»).
По сути четыре препарата, которые мы можем применять, они у нас есть в аптеках. «Кордарон», «Пропанорм», «Соталекс», и появился сейчас «Мультаб» («Дронедарон»). С «Мультабом» мы еще пока большого опыта не имеем. Только имеем достаточно солидный опыт международных исследований. У нас в стране он еще недостаточно изучен.
«Кордарон», «Пропафенон» и «Соталол» изучены достаточно хорошо. Они имеют примерно сопоставимую эффективность. Доказано, что эти три препарата имеют значимый профилактический эффект.
На практике врачи иногда применяют и другие препараты. В нашей стране существует опыт использования «Этацизина» («Ethacyzin»), «Аллапинина» («Allapinin»). Раньше довольно широко применяли Ритмилен (Дизопирамид», «Disopyramide»).
«Дизопирамид» сейчас применяется очень редко в Европейских странах, что связано, в основном, с его частыми побочными действиями. «Аллапинин» и «Этацизин» имеют существенно меньшую международную доказательную базу. Может быть, со временем эта база появится, и они займут какое-то место. Но на сегодняшний день это не входит в международные рекомендации и лишь упоминается в отечественных рекомендациях.
Большой спорный вопрос. Можем ли мы применять препараты первого класса (в частности, «Пропафенон») для купирования и профилактики эпизодов мерцания предсердий у больных артериальной гипертонией и хроническими формами ишемической болезни сердца.
Были исследования «CAST-1», «CAST-2» и другие, которые показали, что у больных острым инфарктом миокарда, перенесших инфаркт миокарда, у больных с сердечной недостаточностью было отмечено ухудшение жизненного прогноза при длительном применении этих препаратов.
Фактически было доказано, что острый инфаркт миокарда, низкая фракция выброса и выраженная сердечная недостаточность по Нью-Йоркской классификации 3-4-ой стадии – это противопоказания для назначения препаратов 1-го С-класса.
Мета-анализы этих же исследований «CAST» показали, что если эти препараты эффективны в малых дозах и в виде коротких курсов (так называемое «легкое подавление»), причем это касается и желудочковых аритмий, то это «легкое подавление» сопровождается улучшением прогноза. Не ухудшением, а, наоборот, улучшением. Если эти препараты (1С-класс) даются в комбинации с бета-блокаторами, то риск смерти уменьшается, то есть нивелируется негативный эффект.
На сегодняшний день такое положение еще остается действительным. Антиаритмики 1-го класса рекомендуются в основном больным без выраженных органических изменений сердца.
Однако остается вопрос: что такое выраженные органические изменения сердца. Разъяснение, данное в ряде авторитетных литературных источников. Под этим понимают острые формы ишемической болезни сердца, выраженные признаки сердечной недостаточности со снижением фракции выброса и выраженная гипертрофия левого желудочка (ГЛЖ) с увеличением толщины стенок более 14 мм.
Если ничего этого нет, а есть просто артериальная гипертония и стабильное течение хронической формы ИБС, то это не является категорическим противопоказанием к назначению препаратов 1-го класса для купирования и в небольших дозах для профилактики.
В связи с этим в прошлом году в России было проведено очень крупное исследование «Простор». Оно ставило целью изучение эффективности и безопасности «Пропонорма» у больных с проходящей мерцательной аритмией при наличии умеренно выраженных признаков сердечной недостаточности с сохраненной систолической функцией левого желудочка.
Центры Москва, Московская область, Новосибирск, Иркутск, Рязань, Челябинск, Нижний Новгород. Показаны имена руководителей, было очень много исполнителей. В исследование было включено более ста человек. Рандомизация 4-6 недель базовой терапии, артериальной гипертонии и ишемической болезни сердца, которая включала тиазидные диуретики, ингибиторы АПФ, бета-адреноблокаторы, статины, дезагреганты, если нужно, непрямые антикоагулянты. Потом рандомизация либо «Пропанорм» либо «Кордарон» в течение 12-ти месяцев.
Группы рандомизаций либо «Пропанорм» либо «Кордарон» были сопоставимы. Примерно одинаковый процент и степени артериальной гипертонии, и степени сердечной недостаточности, и характеристик фибрилляции предсердий.
Результаты. Профилактическая эффективность «Пропанорма» и «Кордарона» через 6 и 12 месяцев. Высота столбиков сопоставима, статистически незначимо отличается. И тот и другой препарат были эффективны.
Частота отмены из-за побочных действий, досрочное выбывание. В целом 26 больных на «Кордароне», 25,2% на «Пропафеноне». Основное побочное действие – удлинение интервала QT и отмена из-за угрозы проаритмического эффекта.
Антиаритмическая эффективность «Пропафенона» не уступает антиаритмической эффективности «Кордарона». Статистически незначимо отличает.
Таким образом, при отсутствии постинфарктной кардиопатии со сниженной фракцией выброса «Пропафенон» может быть использован в качестве аритмического препарата. Желательно его использование в сочетании с бета-блокаторами. При этом повышается безопасность и увеличивается эффективность. Наконец, «Пропафенон» лучше переносим по сравнению с «Кордароном».
Это исследование показывает принципиальную возможность применения препаратов 1-го класса у больных с умеренно выраженной органикой, в том числе и с ишемической болезнью сердца. Я хочу подчеркнуть, что речь идет о применении умеренных доз. Это не подразумевает непременно длительный, непрерывный прием препаратов. Хотя в исследовании эти препараты давались непрерывно.
Помимо того, что изучено, для профилактики рецидивов используются бета-адреноблокаторы, блокаторы кальциевых каналов, в частности «Верапамил» («Verapamil»). Это доказано. Блокаторы кальциевых каналов (то есть «Верапамил»), ингибиторы АПФ – это препараты, которые имеют серьезную доказательную базу как реально действующие, уряжающие частоту рецидивов аритмии.
Менее изученные группы препаратов, которые тоже имеют определенную доказательную базу в плане эффективности для профилактики рецидивов. Антагонисты рецепторов ангиотензина, статины и Омега-3 полиненасыщенные жирные кислоты в виде препарата «Омакор» («Omakor»).
Это новое направление, которое на сегодняшний день имеет свои спорные аспекты, но и достаточную доказательную базу. Именно препарат. Не пищевые добавки, не рыбий жир, а «Омакор» (так в Европе называется) и «Ловаза» («Lovaza») (в США).
Этиловые эфиры: эйкозапентаеновой и докозагексаеновой кислоты, собранные в одну капсулу. При длительном курсовом приеме имеются доказательства того, что этот препарат усиливает антиаритмический эффект «Амиодарона», «Пропафеона» и других антиаритмиков разных классов в смысле профилактики рецидивов фибрилляции желудочков. Этот препарат еще и подкупает тем, что он практически не имеет побочных действий, то есть на уровне плацебо. Достаточно хорошо переносится.
Эти аспекты на сегодняшний день не общеприняты (многие из них спорные), но я хотел их коснуться и осветить.
Как жить с мерцательной аритмией
Мерцательная аритмия (МА) – самое распространённое нарушение ритма. Регистрируется повсеместно и встречается практически во всех возрастных группах, но частота ее возникновения увеличивается с каждым десятилетием жизни.
При своевременном обращении к врачу, правильно подобранном лечении и выполнении пациентом всех назначений доктора прогноз при данном заболевании достаточно благоприятный и качество жизни больного значительно не страдает.
Это касается пациентов всех возрастных групп, в том числе и пожилых.
В норме в сердце человека есть проводящая система. Она подобна электрической проводке и ее функция – из синусового узла, расположенного в левом предсердии, проводить импульсы на мышцу сердца, благодаря чему оно сокращается. При мерцательной аритмии функцию одного «источника питания» (синусового узла) берут на себя множественные аритмические очаги в предсердии и сердце сокращается хаотично. Именно поэтому эту аритмию еще называют delirium cordis (бред сердца).
Как и любое заболевание, МА имеет свои особенности течения. Начинается она, как правило, с внезапно развившегося эпизода (пароксизма), который может завершиться так же внезапно, как и начался.
Дальнейшее течение этого заболевания абсолютно непредсказуемо. После первого пароксизма нередко эта аритмия «затихает» на долгие годы, а потом может появиться в самый неожиданный момент. Или, наоборот, после первого эпизода срывы ритма становятся все чаще. И, как правило, при учащении, удлинении пароксизмов МА она постепенно переходит в постоянную форму, то есть поселяется в сердце пациента уже навсегда.
В ряде случаев, когда пароксизмы повторяются достаточно часто и изнуряют больного, переход аритмии в постоянную форму приносит ему облегчение, потому что каждый эпизод срыва и восстановления ритма сердца «раскачивает» его и приводит к осложнениям.
Мерцательную аритмию принято подразделять на следующие формы:
1.По механизмам развития;
A. фибриляция предсердий
Б. трепетание предсердий:
Основными причинами развития МА являются:
5.инфекции (ОРВИ, грипп, сепсис)
7.нарушение режима труда и отдыха (работа без выходных и отпусков, частые командировки)
8.обострение любой сопутствующей патологии
9.онкологические заболевания, особенно после курсов лучевой и химиотерапии
МА может быть выявлена при регистрации электрокардиограммы, при измерении артериального давления (мигает значок «аритмия» на экране тонометра), либо сам пациент ощущает непривычное для него сердцебиение.
В случае обнаружения МА пациент должен незамедлительно обратиться к аритмологу, либо кардиологу. Ему будет предложено амбулаторное обследование или, при необходимости, госпитализация.
Оптимальным считается срок обращения за медицинской помощью в течение 48 часов с момента развития МА, так как в этом случае можно максимально быстро, эффективно и безопасно восстановить ритм.
В последнем случае искусственное восстановление синусового ритма с помощью лекарств называют медикаментозной кардиоверсией. В случае, когда ритм сердца восстанавливают с помощью электрического тока (дефибриллятором), говорят об электрической кардиоверсии
Так или иначе, любая форма этого заболевания нуждается в лечении. Мировым кардиологическим сообществом давно разработана стратегия ведения таких пациентов и обозначены основные цели лечения больных с мерцательной аритмией.
К ним относятся:
1. Контроль ритма /контроль частоты пульса
Если же нарушение ритма беспокоит более чем один-два раза в год, необходим постоянный прием антиаритмичеких средств.
Тактика по активному восстановлению и удержанию нормального (синусового) ритма с помощью ААП называется тактикой контроля ритма. Она предпочтительна у тех пациентов с пароксизмальной, перманентной и персистирующей формами заболевания, кто ведет активный образ жизни и не имеет солидной сопутствующей патологии.
При достаточно частых, затяжных эпизодах МА постоянная плановая антиаритмическая терапия также обязательна. Нередко учащение пароксизмов – это естественное течение заболевания. Но в ряде случаев эта форма МА обусловлена неправильным лечением, когда пациент принимает лекарства в недостаточной дозе, либо не лечится вовсе. Именно врач –аритмолг призван подобрать ту схему лечения, которая поможет пациенту справиться с болезнью. При ее неуспешности пациенту может быть рекомендована консультация кардиохирурга – аритмолога на предмет хирургического лечения МА.
В случае перехода этой аритмии в постоянную форму, активное восстановление ритма не показано в силу неэффективности. Под воздействием длительно существующей аритмии меняются структура и функция сердца и оно «привыкает» жить с аритмией. И «отучить» его от нее уже невозможно. У таких пациентов применяется тактика контроля пульса, то есть с помощью лекарственных средств достигается частота сердечных сокращений, комфортная для пациента. Но активных попыток восстановления ритма уже не делается.
В качестве антиаритмических средств на сегодняшний день используются:
профилактика инсульта и тромбоэмболий
При МА нет единого, скоординированного выброса крови сердцем, часть крови застаивается в его камерах и, в виде тромбов, может поступать в сосуды. Чаще всего страдают сосуды головного мозга и развивается инсульт.
Во время приема этих препаратов пациент должен следить за наличием кровотечений и раз в квартал контролировать общий анализ крови и креатинин. (при приеме ривароксабана, дабигатрана и апиксабана)., либо не реже раза в месяц исследовать МНО (международное нормализованное отношение) при приеме варфарина. Это необходимо для того, чтобы правильно рассчитать дозу препарата и следить за его безопасностью.
Ацетилсалициловая кислота (аспирин, кардиомагнил, тромбоасс) для профилактики тромбоэмболий рутинно не используется, так как степень защиты от венозного тромбоза при ее применении составляет всего 25%.
профилактика развития сердечной недостаточности
Сердечная недостаточность (СН) – осложнение многих заболеваний сердца, в том числе и МА. Это состояние обусловлено отсутствием полноценной насосной функции сердца, вследствие чего жидкая часть крови застаивается в тканях и органах, что проявляется одышкой и отёками.
С целью профилактики и лечения СН применяются ингибиторы АПФ (эналаприл, лизиноприл, периндоприл и др.), верошпирон(эплеренон), мочегонные (торасемид, фуросемид, гипотиазид).
3.Хирургическое лечение применяется в случае отсутствия эффекта от медикаментозных средств и проводится в специализированных кардиохирургических клиниках.
Виды хирургического лечения МА:
Хирургия аритмий вообще и МА в частности – это «последний патрон», применяемый при неуспешности медикаментозной терапии.
После хирургического лечения с целью профилактики рецидивов аритмии пациентам назначается плановая антиаритмическая терапия.
Таким образом, лечение мерцательной аритмии – это образ жизни, подразумевающий «работу над собой» пациента. И в этом ему помогает врач-аритмолог.
Важно понимать, что подбор антиаритмической терапии занимает определенное время, требует повторных осмотров врача и ряда исследований в динамике ( общеклинические анализы, исследование уровня гормонов щитовидной железы, УЗИ сердца и холтеровское мониторирование ЭКГ, регистрацию электрокардиограммы) и к этом следует отнестись с пониманием. В ряде случаев требуется замена одного лекарственного препарата на другой.
Жизнь с мерцательной аритмией – процесс непростой и очень важно, чтобы пациент чувствовал поддержку и помощь доктора. Мы рады помочь Вам в этом и готовы предложить программы диспансерного наблюдения кардиолога, аритмолога и кардиохирурга в нашей клинике.
Бета-адреноблокаторы III поколения в лечении сердечно-сосудистых заболеваний
Современную кардиологию невозможно представить без препаратов группы бета-адреноблокаторов, которых в настоящее время известно более 30 наименований.
Современную кардиологию невозможно представить без препаратов группы бета-адреноблокаторов, которых в настоящее время известно более 30 наименований. Необходимость включения бета-адреноблокаторов в программу лечения сердечно-сосудистых заболеваний (ССЗ) очевидна: за последние 50 лет кардиологической клинической практики бета-адреноблокаторы заняли прочные позиции в профилактике осложнений и в фармакотерапии артериальной гипертонии (АГ), ишемической болезни сердца (ИБС), хронической сердечной недостаточности (ХСН), метаболическом синдроме (МС), а также при некоторых формах тахиаритмий. Традиционно в неосложненных случаях медикаментозное лечение АГ начинают с бета-адреноблокаторов и диуретиков, снижающих риск развития инфаркта миокарда (ИМ), нарушения мозгового кровообращения и внезапной кардиогенной смерти.
Концепция опосредованного действия лекарственных средств через рецепторы тканей различных органов была предложена N.?Langly в 1905 г., а в 1906 г. H.?Dale подтвердил ее в практике.
В 90-е годы было установлено, что бета-адренорецепторы подразделяются на три подтипа:
Способность блокировать влияние медиаторов на бета1-адренорецепторы миокарда и ослабление влияния катехоламинов на мембранную аденилатциклазу кардиомиоцитов с уменьшением образования циклического аденозинмонофосфата (цАМФ) определяют основные кардиотерапевтические эффекты бета-адреноблокаторов.
Антиишемический эффект бета-адреноблокаторов объясняется снижением потребности миокарда в кислороде, вследствие уменьшения частоты сердечных сокращений (ЧСС) и силы сердечных сокращений, возникающих при блокировании бета-адренорецепторов миокарда.
Бета-блокаторы одновременно обеспечивают улучшение перфузии миокарда за счет уменьшения конечного диастолического давления в левом желудочке (ЛЖ) и увеличения градиента давления, определяющего коронарную перфузию во время диастолы, длительность которой увеличивается в результате урежения ритма сердечной деятельности.
Антиаритмическое действие бета-адреноблокаторов, основанное на их способности уменьшать адренергическое влияние на сердце, приводит к:
Бета-адреноблокаторы повышают порог возникновения фибрилляции желудочков у больных острым ИМ и могут рассматриваться как средства профилактики фатальных аритмий в остром периоде ИМ.
Гипотензивное действие бета-адреноблокаторов обусловлено:
Препараты из группы бета-адреноблокаторов отличаются по наличию или отсутствию кардиоселективности, внутренней симпатической активности, мембраностабилизирующим, вазодилятирующим свойствам, растворимости в липидах и воде, влиянию на агрегацию тромбоцитов, а также по продолжительности действия.
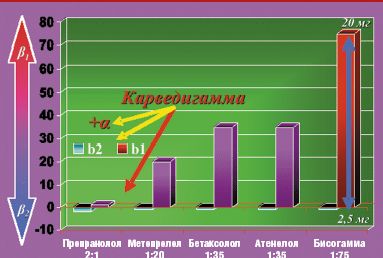
Влияние на бета2-адренорецепторы определяет значительную часть побочных эффектов и противопоказаний к их применению (бронхоспазм, сужение периферических сосудов). Особенностью кардиоселективных бета-адреноблокаторов по сравнению с неселективными является большое сродство к бета1-рецепторам сердца, чем к бета2-адренорецепторам. Поэтому при использовании в небольших и средних дозах эти препараты оказывают менее выраженное влияние на гладкую мускулатуру бронхов и периферических артерий. Следует учитывать, что степень кардиоселективности неодинакова у различных препаратов. Индекс ci/бета1 к ci/бета2, характеризующий степень кардиоселективности, составляет 1,8:1 для неселективного пропранолола, 1:35 — для атенолола и бетаксолола, 1:20 — для метопролола, 1:75 — для бисопролола (Бисогамма). Однако следует помнить, что селективность дозозависима, она снижается с повышением дозы препарата (рис. 1).
В настоящее время клиницисты выделяют три поколения препаратов с бета-блокирующим эффектом.
I поколение — неселективные бета1- и бета2-адреноблокаторы (пропранолол, надолол), которые наряду с отрицательными ино-, хроно- и дромотропными эффектами обладают способностью повышать тонус гладкой мускулатуры бронхов, сосудистой стенки, миометрия, что существенно ограничивает их использование в клинической практике.
II поколение — кардиоселективные бета1-адреноблокаторы (метопролол, бисопролол), благодаря высокой селективности в отношении бета1-адренорецепторов миокарда обладают более благоприятной переносимостью при длительном применении и убедительной доказательной базой долгосрочного прогноза жизни при лечении АГ, ИБС и ХСН.
В середине 1980-х годов на мировом фармацевтическом рынке появились бета-адреноблокаторы III поколения с низкой селективностью к бета1, 2-адренорецепторам, но с сочетанной блокадой альфа-адренорецепторов.
Препараты III поколения — целипролол, буциндолол, карведилол (его дженерический аналог с брендовым названием Карведигамма®) обладают дополнительными вазодилятирующими свойствами за счет блокады альфа-адренорецепторов, без внутренней симпатомиметической активности.
В 1982–1983 годах в научной медицинской литературе появились первые сообщения о клиническом опыте применения карведилола при лечении ССЗ.
Ряд авторов выявили протективное действие бета-адреноблокаторов III поколения на клеточные мембраны. Это объясняется, во-первых, ингибированием процессов перекисного окисления липидов (ПОЛ) мембран и антиоксидантным действием бета-блокаторов и, во-вторых, снижением влияния катехоламинов на бета-рецепторы. Некоторые авторы связывают мембранстабилизирующее действие бета-блокаторов с изменением проводимости натрия через них и ингибированием ПОЛ.
Указанные дополнительные свойства расширяют перспективы применения данных лекарственных средств, поскольку нивелируют характерное для первых двух поколений отрицательное влияние на сократительную функцию миокарда, углеводный и липидный обмен и в то же время обеспечивают улучшение перфузии тканей, позитивное влияние на показатели гемостаза и уровень оксидативных процессов в организме.
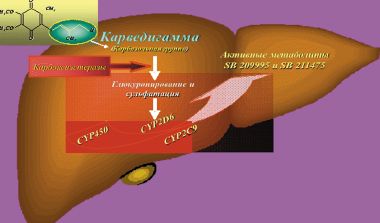
Карведилол метаболизируется в печени (глюкуронирование и сульфатация) с помощью ферментной системы цитохрома Р450, с использованием семейства ферментов — CYP2D6 и CYP2C9. Антиоксидантное действие карведилола и его метаболитов обусловлено наличием в молекулах карбазольной группы (рис. 2).
Метаболиты карведилола — SB 211475, SB 209995 угнетают ПОЛ в 40–100 раз активнее, чем сам препарат, а витамин Е — примерно в 1000 раз.
Применение карведилола (Карведигаммы®) при лечении ИБС
Согласно результатам целого ряда завершенных многоцентровых исследований, бета-адреноблокаторы оказывают выраженный антиишемический эффект. Необходимо отметить, что антиишемическая активность бета-адреноблокаторов соизмерима с активностью антагонистов кальция и нитратов, но, в отличие от этих групп, бета-адреноблокаторы не только улучшают качество, но и увеличивают продолжительность жизни пациентов с ИБС. Согласно результатам метаанализа 27 многоцентровых исследований, в которых приняло участие более 27 тыс. человек, селективные бета-адреноблокаторы без внутренней симпатомиметической активности у больных с острым коронарным синдромом в анамнезе снижают риск развития повторного ИМ и смертность от инфаркта на 20% [1].
Однако не только селективные бета-адреноблокаторы положительно влияют на характер течения и прогноз у пациентов с ИБС. Неселективный бета-адреноблокатор карведилол также продемонстрировал очень хорошую эффективность у больных со стабильной стенокардией. Высокая антиишемическая эффективность данного препарата объясняется наличием дополнительной альфа1-блокирующей активности, способствующей дилятации коронарных сосудов и коллатералей постстенотической области, а значит — улучшению перфузии миокарда. Кроме того, карведилол обладает доказанным антиоксидантным эффектом, связанным с захватом свободных радикалов, высвобождающихся в период ишемии, что обусловливает его дополнительное кардиопротекторное действие. Одновременно карведилол блокирует апоптоз (программируемая смерть) кардиомиоцитов в зоне ишемии, сохраняя объем функционирующего миокарда. Как было показано, метаболит карведилола (ВМ 910228) обладает меньшим бета-блокирующим эффектом, но является активным антиоксидантом, блокируя перекисное окисление липидов, «отлавливая» активные свободные радикалы OH–. Этот дериват сохраняет инотропный ответ кардиомиоцитов на Ca++, внутриклеточная концентрация которого в кардиомиоците регулируется Ca++-насосом саркоплазматического ретикулума. Поэтому карведилол оказывается более эффективным в лечении ишемии миокарда через ингибирование повреждающего действия свободных радикалов на липиды мембран субклеточных структур кардиомиоцитов [2].
Благодаря этим уникальным фармакологическим свойствам, карведилол может превосходить традиционные бета1-селективные адреноблокаторы в плане улучшения перфузии миокарда и способствовать сохранению систолической функции у больных ИБС. Как показано Das Gupta et al., у больных с дисфункцией ЛЖ и сердечной недостаточностью, развившейся вследствие ИБС, монотерапия карведилолом снижала давление наполнения, а также увеличивала фракцию выброса (ФВ) ЛЖ и улучшала показатели гемодинамики, при этом не сопровождаясь развитием брадикардии [3].
Согласно результатам клинических исследований у больных хронической стабильной стенокардией, карведилол снижает ЧСС в покое и при физической нагрузке, а также увеличивает ФВ в покое. Сравнительное исследование карведилола и верапамила, в котором принимало участие 313 пациентов, показало, что, по сравнению с верапамилом, карведилол в большей степени уменьшает ЧСС, систолическое АД и произведение ЧСС ´ АД при максимально переносимой физической нагрузке. Более того, карведилол обладает более благоприятным профилем переносимости [4].
Важно, что карведилол, по-видимому, более эффективен при лечении стенокардии, чем обычные бета1-адреноблокаторы. Так, в ходе 3-месячного рандомизированного многоцентрового двойного слепого исследования карведилол напрямую сравнивали с метопрололом у 364 пациентов со стабильной хронической стенокардией. Они принимали карведилол по 25–50 мг два раза в сутки или метопролол по 50–100 мг два раза в сутки [5]. В то время как оба препарата продемонстрировали хорошее антиангинальное и противоишемическое действие, карведилол более значительно увеличивал время до депрессии сегмента ST на 1 мм при физической нагрузке, чем метопролол. Переносимость карведилола была очень хорошей, и, что важно, при увеличении дозы карведилола не произошло заметных изменений типов нежелательных явлений.
Примечательно, что карведилол, не обладающий, в отличие от других бета-адреноблокаторов, кардиодепрессивным действием, улучшает качество и продолжительность жизни пациентов с острым ИМ (CHAPS) [6] и постинфарктной ишемической дисфункцией ЛЖ (CAPRICORN) [7]. Многообещающие данные были получены в ходе исследования Carvedilol Heart Attack Pilot Study (CHAPS) — пилотного исследования влияния карведилола на развитие ИМ. Это было первое рандомизированное исследование, в котором сравнивали карведилол с плацебо у 151 больного после острого ИМ. Лечение начинали в течение 24 часов с момента появления болей в грудной клетке, а дозу препарата увеличивали до 25 мг два раза в сутки. Главными конечными точками исследования были функция ЛЖ и безопасность препарата. Больных наблюдали в течение 6 месяцев с момента начала заболевания. Согласно полученным данным, частота развития серьезных кардиальных событий уменьшилась на 49%.
Полученные в ходе исследования CHAPS эхографические данные 49 пациентов со сниженной ФВ ЛЖ (
А. М. Шилов*, доктор медицинских наук, профессор
М. В. Мельник*, доктор медицинских наук, профессор
А. Ш. Авшалумов**
*ММА им. И. М. Сеченова, Москва
**Клиника Московского института кибернетической медицины, Москва