Анекдот что лучше альцгеймер или паркинсон лучше
Болезнь Паркинсона и Альцгеймера: сходства и различия
Многие люди, особенно те, которые не являются медиками, считают, что болезни Паркинсона и Альцгеймера – это похожие заболевания, и протекают они одинаково. Но это не совсем так. У них и правда много схожего, но есть и ключевые различия.
Сходства болезней
Различия
Их значительно больше. Начнем с того, что поражаются разные клетки головного мозга, отсюда и различная симптоматика. При болезни Альцгеймера страдают нейроны коры головного мозга, а при болезни Паркинсона — нейроны, синтезирующие дофамин, молекулы которого отвечают за эмоции и движения.
Есть данные, что при вскрытии пациентов, умерших от Паркинсона, обнаруживаются и поражения головного мозга (амилоидные бляшки), характерные для Альцгеймера. Но многие врачи считают, что это была сочетанная патология, т. е. у пациентов было сразу два заболевания.
Сильно различается симптоматика. При болезни Альцгеймера в первую очередь страдает память, а вслед за ней и интеллект. Начинается все с забывчивости, которая со временем прогрессирует — человек теряет документы и вещи, а затем их находят в странных местах, забывает оплатить счета и выполнять повседневные дела. Потом присоединяются более серьезные симптомы:
Затем присоединяются следующие симптомы:
Также есть различия в прогнозе заболевания. Болезнь Паркинсона протекает более благоприятно. Симптомы можно контролировать, а на начальной стадии заболевания можно предотвратить прогрессирование с помощью специальных лекарств и даже хирургических методов лечения. В частности, могут применяться малоинвазивные операции на головном мозге, например, нейростимуляция.
При болезни Альцгеймера эффективных методов лечения или контроля нет. Можно только немного замедлить ухудшение памяти и нарушение умственных способностей.
Болезнь Паркинсона: у больных появилась надежда
Боксер Мохаммед Али, политики Ясер Арафат и Мао Цзэдун, Папа Римский Иоанн Павел II, художник Сальвадор Дали, актер Майкл Джей Фокс (обаятельный Марти из фильма «Назад в будущее») – всех этих людей в разном возрасте объединила общая беда – болезнь Паркинсона. Еще несколько десятилетий назад это заболевание считалось приговором. Но, к счастью, сегодня появились средства, способные если не остановить болезнь, то по крайней мере значительно облегчить жизнь пациентов, страдающих этим хроническим неврологическим заболеванием.
Лекарства – по схеме
Поскольку причиной развития болезни является дефицит в головном мозге дофамина, больным требуется вводить его извне. К сожалению, доставить само это вещество невозможно – оно плохо проникает через гематоэнцефалический барьер и по пути распадается. Но зато можно ввести больному биологический предшественник дофамина – препарат, который, попав в кровь и достигнув мозга, уже на месте превратится в нужный нейромедиатор. Такой препарат применяется в неврологии уже около 40 лет. В конце 60‑х годов он совершил настоящую революцию, потому что эффект от его применения у пациентов был наиболее впечатляющий, особенно в первые годы приема. Это было похоже на чудо: человек, которого била дрожь и мертвой хваткой сковывал высокий мышечный тонус, выпивал таблетку и на глазах становился внешне практически здоровым.
После того как это лекарство стало широко применяться на практике, смертность людей с болезнью Паркинсона сократилась вдвое. Но, к сожалению, действие лекарства весьма непродолжительно – всего 1,5–3 часа, и оно вызывает ряд побочных эффектов. Дело в том, что в норме у человека дофамин выделяется равномерно, а при приеме лекарства – скачкообразно. Во время резкого повышения концентрации дофамина в организме, которое наступает спустя какое-то время после употребления таблетки, у больного начинается сильный приступ двигательной дискинезии, во время которого тело не слушается своего хозяина и совершает непроизвольные размашистые движения; и, наоборот, при резком снижении концентрации возникает обездвиженность. В связи с этим многие пациенты раньше опасались принимать это лекарство. Но врачи уверены, что бояться не нужно. Ведь сегодня можно успешно бороться побочными эффектами с помощью дополнительных препаратов, которые усиливают и продлевают лечебный эффект и сглаживают неприятные моменты. Эти лекарства в составе комплексной терапии очень эффективны, особенно у молодых пациентов.
Сегодня существует 7 групп противопаркинсонических средств, и в каждой из них имеются еще не менее 3–4 препаратов. Их выбор и схема лечения очень сложны, они зависят от возраста больного, формы, стажа заболевания и многих других обстоятельств. Поэтому врач, занимающийся ведением таких больных, должен быть очень знающим и опытным. Помимо своевременности лечения важна его непрерывность – лекарственные «каникулы» для больных очень вредны.
Нужна, как дырка в голове?
В последнее время появились более радикальные способы, которые находятся на стыке консервативного и нейрохирургического лечения.
Первые стереотаксические операции (таламотомия, паллидотомия и др.) на головном мозге были сделаны в 50–60‑х годах. Они проходили под местным наркозом. На голову больному надевался особый шлем, затем в нужном отделе черепа пациента высверливалось крошечное отверстие, через которое по точным расчетам вводилась тонкая канюля с проходившим через нее жидким азотом. Уничтожить «вредный» участочек в головном мозге можно было не только холодом, но и электрокоагуляцией или химическим способом. Это воздействие разрушало определенное ядро и тем самым прерывало поток патологической импульсации, в результате дрожание у пациента уходило буквально в ту же секунду. Но, увы, если делать операцию не на одной, а на двух сторонах головы (что чаще всего требуется при этой болезни), то в большинстве случаев возникают побочные явления: трудности с речью, проблемы с глотанием и пр. Поэтому область применения таких операций была не очень велика.
Но в начале 90‑х годов французский ученый Бенабид придумал метод глубокой электростимуляции мозга. В ходе этой операции под контролем специальной аппаратуры в те же структуры мозга, что и при деструктивных операциях, вводится электрод, стимулирующий нужное ядро. От этого электрода отходит провод, который проводится под кожей и заканчивается под ключицей пациента, где устанавливается источник питания. И с помощью небольшого наружного устройства (размером с мобильный телефон) врач программирует вживленный электрод на работу в определенном ритме. Самому пациенту достаточно нажимать 2–3 кнопки, чтобы включать и выключать устройство или поменять одну программу на другую, в зависимости от своего состояния. Если же случится сбой программы, необходимо обратиться к врачу, который проведет полноценное «перепрограммирование» (это случается, к счастью, не столь часто).
Операция эта очень сложная и долгая (двусторонняя длится около 8 часов), специалистов, владеющих этой методикой, – единицы. Зато эффект от нее столь же впечатляющий, как и при таламотомии, но без негативных последствий. Разве что в будущем нельзя будет проводить МРТ и другие магнитные процедуры. Хотя такая операция стоит порядка 1 миллиона рублей и по этой причине недоступна для большинства пациентов, но с недавних пор ее включили в перечень высокотехнологической медицинской помощи, поэтому при наличии квот в медицинских учреждениях это вмешательство всем нуждающимся проводят бесплатно. К сожалению, пока центров, где применяют этот метод, в нашей стране очень мало и все они расположены в Москве (Научный центр неврологии РАМН, Институт нейрохирургии им. Бурденко РАМН, Лечебно-реабилитационный центр Минздравсоцразвития).
В будущее – с оптимизмом!
Есть и немедикаментозные средства лечения этой болезни. Среди них – транскраниальная магнитная стимуляция (разновидность физиотерапии), а также правильно организованная лечебная физкультура, помогающая больным преодолевать скованность и нарушения равновесия. Для двигательной реабилитации пациентов с болезнью Паркинсона широко используются компьютерные программы и технологии виртуальной реальности, роботизированные устройства, тренажеры (обладающие низким сопротивлением) и другие высокотехнологичные аппараты.
На ранних этапах заболевания пациентам показаны занятия с определенными элементами бойцовских искусств и танцами, игры с мячом, передвижение по пересеченной местности (в том числе на лыжах), «мягкая» аэробика. На поздних этапах – ходьба (обычная и на месте), упражнения для стоп и подъем по ступенькам, имитация гребли на тренажере, плавание.
В связи с огромной значимостью этой медицинской проблемы в нашей стране около года назад было создано Национальное общество по изучению болезни Паркинсона и расстройств движений. Организация занимается обучением специалистов, разработкой сайта для пациентов, страдающих этим заболеванием, и их родственников (www.parkinsonizm.ru), регистром паркинсонизма в стране, а также проведением тематических конгрессов 1 раз в 2–3 года, выпуском специализированных бюллетеней для врачей и т. д. Организаторы общества надеются, что благодаря их работе диагноз «болезнь Паркинсона» вскоре перестанет быть приговором.
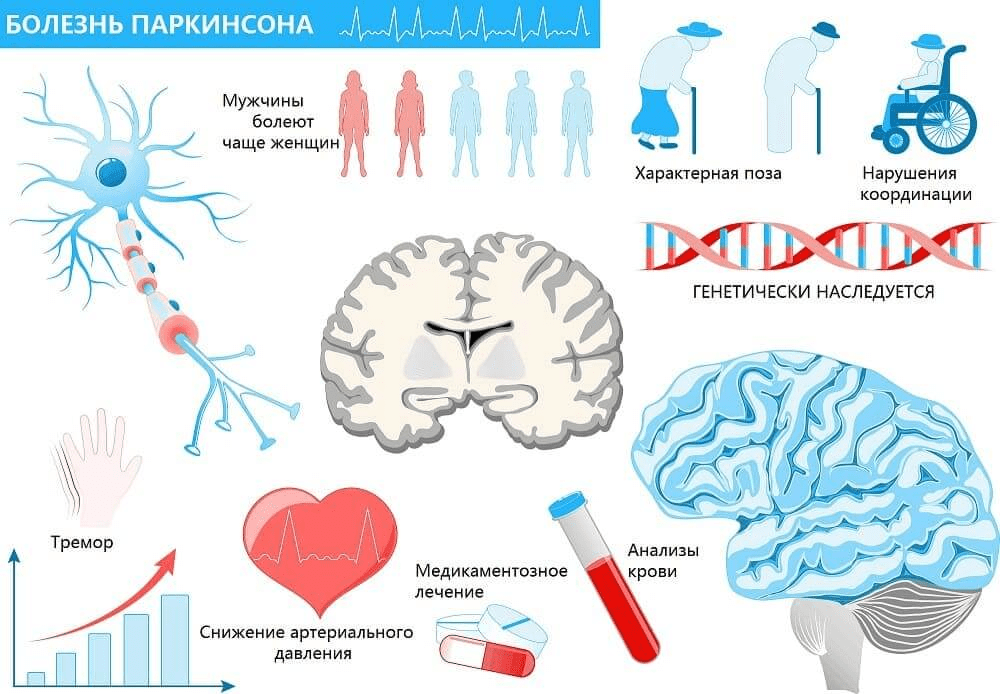
Впервые этот недуг описал английский врач Джеймс Паркинсон в 1817 году в своем «Эссе о дрожательном параличе». Средний возраст начала болезни – 55 лет. В то же время у 10% больных заболевание возникает в самом расцвете сил, до 40 лет – это так называемый ювенильный паркинсонизм.
Известно, что болезнь Паркинсона возникает из-за нарушения выработки дофамина – одного из нейромедиаторов (вещества, служащие для передачи импульсов в головном мозге). Это ведет к нарушению функций клеток в отделах мозга, отвечающих за движения. В результате у больных возникают непроизвольный тремор (дрожь в конечностях), заторможенность, затруднения при ходьбе, а затем и трудности при глотании.
Помимо первичного, ученые выделяют также паркинсонизм вторичный, который вызывают инфекции и другие заболевания головного мозга (например, энцефалит, атеросклероз сосудов мозга), а также повторные травмы головы. Известен токсический паркинсонизм. При нем страдают не одна, а сразу обе стороны тела. Эту разновидность болезни могут спровоцировать чрезмерный прием лекарств (в основном нейролептиков) или работа на вредном производстве (в том числе в сельском хозяйстве, где есть контакт с пестицидами, гербицидами и другими химическими удобрениями). В нашей стране, к сожалению, сильно распространен токсический паркинсонизм у молодых людей, связанный с избытком в их организме марганца. Эта разновидность болезни вызвана не профессиональными вредностями, а употреблением суррогатных наркотиков, в состав которых входит марганцовка.
Сергей Иллариошкин: «По самым скромным подсчетам, около 35 млн людей в мире страдают болезнью Альцгеймера и болезнью Паркинсона»
Насколько опасны эти расстройства, как совершенствуется их диагностика и на чем строится современная терапия? Эти и другие вопросы задал корреспондент remedium.ru Сергею Иллариошкину, заместителю директора по научной работе, руководителю отдела исследований мозга ФГБНУ «Научный центр неврологии», члену-корреспонденту РАН, профессору, д.м.н.
Сергей Николаевич, БА и БП – две наиболее часто встречающиеся нейродегенеративные патологии, угрожающие людям пожилого и старческого возраста. Что объединяет эти заболевания и каковы основные отличия – в патогенезе, механизме возникновения?
– Речь идет о представителях возраст-зависимых заболеваний, в ряду которых БА стоит на первом месте по распространенности, а БП – на втором. Как и многие другие возрастные патологии, они ассоциированы со старением человека, по мере которого в клетках организма происходят определенные изменения.
К примеру, в нейронах начинают накапливаться белковые агрегаты, которые клетка не может растворить и вывести безопасным образом. Накопление таких труднорастворимых белков в нейронах, а затем и в паренхиме мозга объединяет данные заболевания в общую группу церебральных протеинопатий. Это общий механизм развития нейродегенеративных заболеваний, методы лечения которых в значительной степени направлены на борьбу с патологическими скоплениями аномально скрученных белков. При этом данные заболевания различаются как видами накапливаемых белков, так и структурами мозга, которые затрагиваются.
В случае БА происходит накопление белков – бета-амилоидов в участках, связанных с памятью. Основным звеном патогенеза БП является формирование нейротоксических агрегатов белка альфа-синуклеина, которые концентрируются в структурах мозга, отвечающих за двигательные системы. Поэтому различается и клиническая картина данных заболеваний.
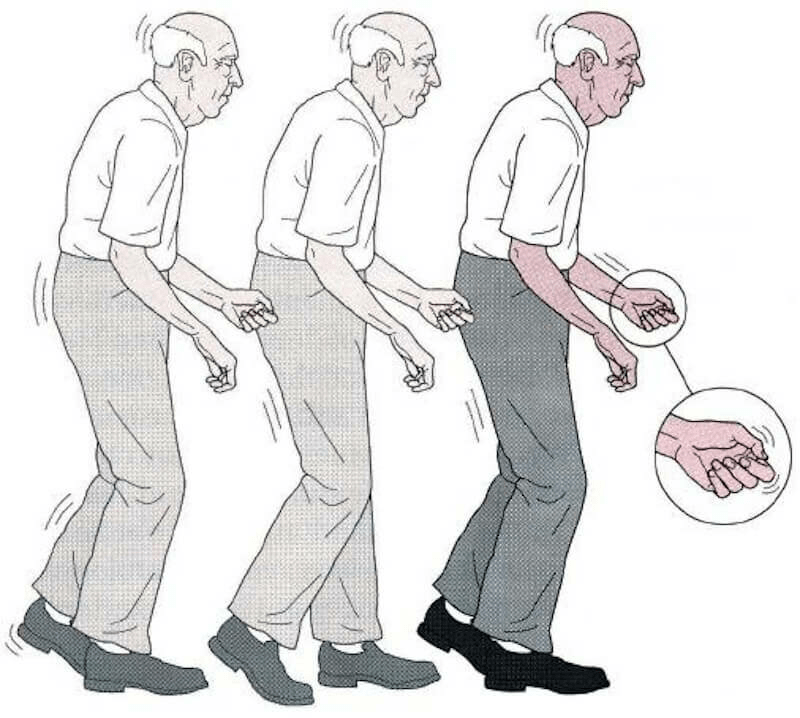
У людей, страдающих БА, нарушается память и происходит нарастание других когнитивных расстройств, вплоть до деменции, тогда как у пациентов с БП наблюдаются характерные двигательные расстройства, связанные с нарушением самообслуживания, ходьбы. Это если совсем кратко.
Лечение Альцгеймера: последние новости
Поделиться:
Эпидемия деменции
Болезнь Альцгеймера и болезнь Паркинсона — пожалуй, самые известные и самые распространенные заболевания центральной нервной системы. И количество больных неуклонно растет: мы стали жить дольше, а главный фактор риска в обоих случаях — возраст.
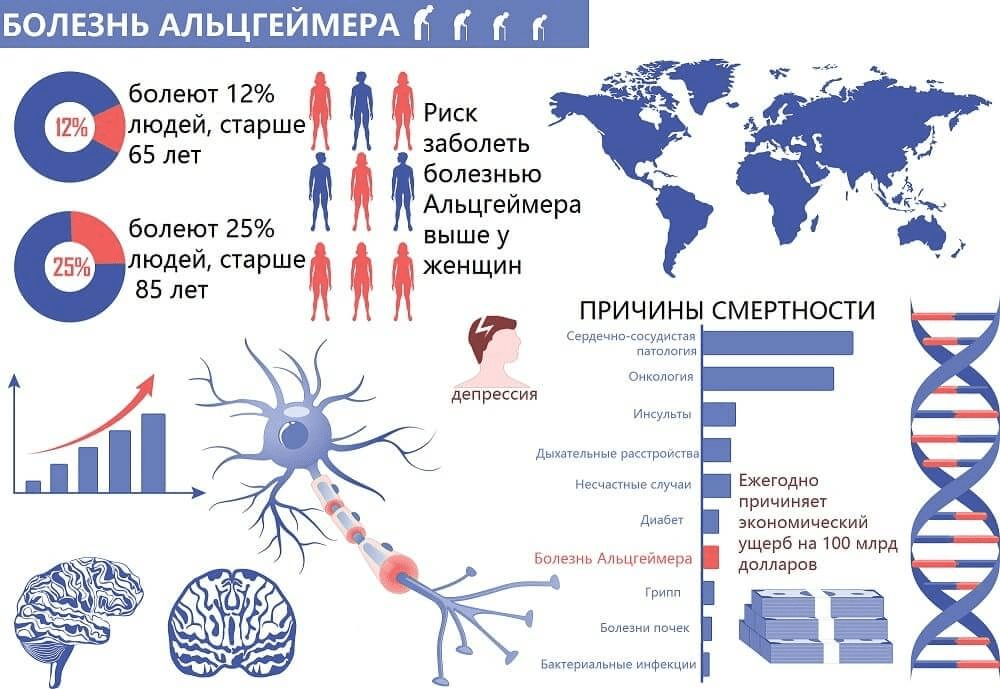
Описанным Алоизом Альцгеймером заболеванием страдает почти половина людей старше 85 лет. В России официально больны порядка 1,8 млн. Всего же в мире в настоящий момент болезнь Альцгеймера диагностирована примерно у 44 млн. человек.
К сожалению, пока все попытки ученых одолеть это заболевание оказываются тщетны. Появился даже научный анекдот: «Если вы — больная Альцгеймером мышь, вам повезло. Если человек, тогда это проблема». Действительно, очень часто можно прочесть в новостях о новом средстве от Альцгеймера, но клинические испытания всегда проваливаются или до них не доходит вовсе. Модельных грызунов с болезнью Альцгеймера лечить научились, а люди обречены страдать. Тем не менее работы ведутся по всему миру. И вот чего удалось достичь только за последнее время.
Понимание
Иногда исследователи предлагают самые невероятные версии возникновения болезни Альцгеймера. Например, в марте 2016 года интернациональная группа ученых и врачей во главе с профессором Рутом Итзаки из Оксфорда опубликовала статью, в которой предполагается, что есть три основные причины болезни Альцгеймера: вирус (вирус герпеса человека первого типа) и два вида бактерий (хламидии и спирохеты). Доказательств — кроме логических рассуждений по поводу известных данных (присутствия вируса герпеса в мозге больных) — в статье не приводится.
Ученые из детского госпиталя Бостона смогли понять, как разрушается память во время болезни Альцгеймера. Оказывается, в этом случае на здоровые синапсы распространяется механизм «поедания» глией неправильных или слабых синапсов.
Некоторого прогресса удалось достичь и в понимании того, почему вообще образуется белок бета-амилоид в головном мозге (напомним, именно скопления этого белка, именуемые амилоидными бляшками, мешают проведению нервного сигнала и вызывают гибель нейронов при болезни Альцгеймера). Ученые из Гарвардского университета предположили, что бета-амилоид действует так же, как и антимикробные белки, формирующие волокна вокруг клеток. Оказалось, что в чашках Петри бета-амилоид прекрасно уничтожает некоторые микробы, например кишечную палочку и стрептококк.
Читайте также:
Болезнь Альцгеймера и герпес
На технологической выставке Re:publica в Германии команда разработчиков и ученых из Университетского колледжа Лондона (UCL), Университета Восточной Англии и коммуникационного гиганта Deutche Telecom представили игру для смартфонов Sea Hero Quest, которая поможет бороться с болезнью Альцгеймера. При ее помощи ученые могут тестировать память сотен тысяч человек, что чрезвычайно важно для накопления данных о болезни. В игре участник должен провести корабль по лабиринту, который ему ранее показали на экране. По словам исследователей, если раньше они могли тестировать 200 человек в год, то сейчас такой объем данных они получают за минуту.
Одну из важнейших работ 2016 года выполнила команда ученых из Массачусетского технологического института и японского института RIKEN под руководством нобелевского лауреата Сусуму Тонегавы. Ученые обнаружили, куда исчезают воспоминания при болезни Альцгеймера, и, что более важно, определили, что они поддаются восстановлению. Оказалось, все дело в дендритных шипиках, которые отращивают клетки памяти (энграммные клетки), когда формируется воспоминание. Профессор Тонегава объясняет, что если человек хочет что-то вспомнить, его «клетки-формуляры» должны активироваться с помощью энториальной коры. Но если плотность дендритных шипиков во время «образовательного» процесса не росла, то позже, когда из энториальной коры подается сигнал «вызова», он не достигает ядра энграммных клеток. При помощи методов оптогенетики Тонегаве удалось вернуть мышам память.
Диагностика
Ученые из Университета Отаго обнаружили новый маркер, по которому можно диагностировать болезнь Альцгеймера, взяв на анализ небольшое количество крови пациента. В ходе исследования биохимики обнаружили, что небольшие молекулы из обширного класса микроРНК, локализованные в человеческом мозге и крови, — очень хорошие кандидаты для диагностики болезни Альцгеймера. Определяя специфический набор микроРНК, исследователи Отаго смогли диагностировать болезнь Альцгеймера в 86 % случаев.
Еще один важный способ ранней диагностики болезни предложил союз офтальмологов, неврологов и спектроскопистов из Центра по разработке лекарств Университета Миннесоты. Авторы разработали метод эндоскопической спектроскопии сетчатки в ближнем инфракрасном диапазоне. Используя так называемое рэлеевское рассеяние света на амилоидных агрегатах, они сумели уверенно диагностировать заболевание задолго до возникновения неврологических симптомов у мышей.
А ученые из Каролинского института в Швеции показали, что патологические процессы — воспаление — начинаются в мозге за 20 лет до начала симптомов. И их можно увидеть по вспышке активности астроцитов, глиальных клеток мозга. Единственная беда: эту вспышку можно «засечь» только позитронно-эмиссионной томографией, а это очень дорого и совсем не годится для скрининга.
Лечение
Несмотря на скепсис, некоторые лекарства от Альцгеймера таки добрались до клинических испытаний. Американские и швейцарские ученые сообщили об успехе ранних клинических испытаний биопрепарата, способного замедлить прогрессирование болезни, а результаты уже опубликованы в Nature.
Созданный компаниями Biogen и Neurimmune препарат Адуканумаб направлен на удаление бета-амилоидных бляшек. Он представляет собой моноклональные человеческие антитела, которые связываются с растворимой и нерастворимой формами бета-амилоида и участвуют в их выведении из нервной ткани. Примечательно, что эти антитела обнаружили у пожилых людей с естественной устойчивостью к болезни.
Очень интересное и нестандартное решение борьбы с болезнью Альцгеймера предложили японские химики-органики (один из которых работает еще и в Казани) — они выяснили, что очень простое и очень токсичное вещество акролеин в небольших дозировках мешает формироваться амилоидным бляшкам. Конечно, «кормить» людей акролеином никто пока не собирается, но, тем не менее, возможно, это тоже может стать новым импульсом для разработчиков лекарств.
Новую технологию борьбы с Альцгеймером предложили ученые из Университета Лозанны. Они испытывают капсулу, которая имплантируется под кожу черепа и производит антитела к амилоидным белкам, которые метят амилоидные бляшки и заставляет иммунную систему «чистить» мозг от этого «мусора». На мышах система работает.
Альцгеймер и ВИЧ
И еще одна новость из области болезни Альцгеймера. Сложно сказать — хорошая она или плохая. В апреле 2016 года был зафиксирован первый в истории ВИЧ-положительный пациент с достоверно диагностированной болезнью Альцгеймера. То есть, с одной стороны, инфицированные вирусом иммунодефицита человека пациенты стали доживать до «возраста Альцгеймера» (пациенту — 71), а с другой — было опровергнуто господствующее в неврологии мнение, что воспаление, вызванное вирусом, предохраняет от образования амилоидных бляшек. Теперь диагноз «ВИЧ-ассоциированные когнитивные расстройства» (HAND), вероятнее всего, придется пересматривать.
В развитии болезни Паркинсона и болезни Альцгеймера участвует один и тот же фермент
Повышенная активность аспарагиновой эндопептидазы приводит к накоплению патологически разрезанных фрагментов белка. Они формируют скопления, повреждающие нейроны.
.jpg) |
| Изображение: New York Post |
На первый взгляд, между механизмами развития болезни Паркинсона и болезни Альцгеймера мало общего. Заболевания поражают разные участки мозга, и на вероятность их развития влияют разные факторы риска. К развитию болезни Альцгеймера приводит формирование нейрофибрилл, сформированных тау-белком, а болезнь Паркинсона вызывается образованием сгустков альфа-синуклеина. Симптоматика и методы лечения заболеваний также различаются.
Впрочем, как показали исследователи Университета Эмори в Атланте, на биохимическом уровне два заболевания могут быть связаны общим ферментом. Ранее было установлено, что за образование патологических включений при болезни Альцгеймера отвечает фермент аспарагиновая эндопептидаза (AEP). В ходе своей работы AEP разрезает тау-белок таким образом, что он начинает слипаться, оказывая токсическое воздействие. Оказалось, что аналогичным образом этот фермент работает и в отношении альфа-синуклеина у пациентов с болезнью Паркинсона.
Активность AEP в головном мозге пациентов с болезнью Паркинсона была повышена, что приводило к образованию значительного количества неправильно разрезанного альфа-синуклеина. Вероятность того, что этот белок образует патологические комплексы, значительно выше, чем у альфа-синуклеина полной длины. Образующиеся комплексы оказывали токсический эффект, разрушая нейроны, отвечающие за дофаминэргическую передачу. У экспериментальных животных при увеличении концентрации патологического альфа-синуклеина уменьшалось число дофаминергических нейронов и нарастала двигательная симптоматика. Принудительное отключение гена, ответственного за выработку AEP, приводило к противоположному эффекту.
AEP – не единственный фермент, который способен разрезать альфа-синуклеин на патологические фрагменты, отметил Кэцян Е (Kequiang Ye), руководитель исследования. Кроме того, и неразрезанная форма белка тоже способна образовывать комплексы, повреждающие нейроны. Тем не менее, работа, которую авторы опубликовали в журнале Nature Structural & Molecular Biology, позволяет глубже понять биохимию заболеваний и может способствовать разработке новых лекарственных методов.


 Читайте также:
Читайте также: 