Аневризма в печени что это такое
Аневризма печеночной артерии
Этиология аневризма печеночной артерии
Распространенные причины заболевания травмы (35% всех случаев), инфекции желчевыводящих путей, узелковый полиартериит, атеросклероз, желчекаменная болезнь, эрозия артериальной стенки; дегенерация стенки сосуда или врожденные дефекты также могут быть причиной заболевания.
Раннее выявление и ранняя диагностика являются ключом к профилактике и лечению этого заболевания.
Осложнения
Аневризма печеночной артерии приводит к кровотечению из верхних отделов, желудочно-кишечным осложнениям и геморрагическому шоку.
Симптомы
Общие симптомы аневризмы печеночной артерии черный стул, боли в животе, желтуха, систолический шум. 80% пациентов имеют тупую боль в правой верхней части живота или правом подреберье. Более половины пациентов могут иметь рвоту с кровью или черный стул, желтуху до кровотечения. Желтуха обычно вызвана сдавлением общего желчного протока, камнем в печеночном протоке или при наличии этих причин одновременно. Около трети пациентов могут иметь лихорадку, инфекцию желчевыводящих путей или воспаление самой печеночной артерии.
Осмотр
Анализ крови и биохимические тесты, как правило, не имеют особого значения, хотя если заболевание сопровождается инфекцией желчевыводящих путей, может быть лейкоцитоз. Рентген верхних отделов желудочно-кишечного тракта, желудка или двенадцатиперстной кишки может выявить признаки заболевания. Чаще всего при диагностировании опираться на селективную абдоминальную ангиографию.
Следует также исключить заболевания с похожими симптомами: травму печеночной артерии, язвы двенадцатиперстной кишки, рак желчных путей и портальную гипертензию.
Лечение
Лечение заболевания состоит из хирургии и поддерживающей терапии (она длится10-30 дней). При аневризме печеночной артерии летальность может достигать от 40% до 100%. Если наблюдается нарушение кровообращения проводится процедура шунтирования. При аневризме внутрипеченочных ветвей печеночной артерии, сегменты печени могут подвергаться частичной гепатэктомии.
В последние годы, с совершенствованием техники и технологии вмешательства применяют операции, трансплантацию микро-кольца, или введение специального клея, успех таких процедур составляет около 76%.
Послеоперационная интенсивная терапия включает уход за пациентом, если ему было осуществлено шунтирование, применяется антикоагулянтная терапия от 1 до 2 недель.
Из препаратов в послеоперационном лечении используют те, что улучшают циркуляцию крови. Из травяных используют: куркуму, шалфей, сафлору, ревень.
Прогноз
Прогноз этого заболевания во многом зависит от ранней диагностики и соответствующего хирургического лечения. Как только начинается кровотечение, смертность высокая.
1. С детства прививайте хорошие привычки в еде. Придерживайтесь сбалансированной диеты, кушайте разнообразные овощи и фрукты. Разумная диета: потребление продуктов с высоким содержанием клетчатки, витаминов и микроэлементов.
2. Для укрепления нашей собственной нервной системы, старайтесь в любой ситуации оставаться спокойными, выполняйте физические упражнения, следите за кровяным давлением. Долгосрочные психическое напряжение, тревога, раздражительность, пессимизм и другие эмоции, приводят кору головного мозга к возбудимости. Будте оптимистами, позитивное отношение к жизни является важной мерой в профилактике заболевания. Не доводите себя до состояния хронической усталости, развивайте хорошие привычки.
Инфаркт печени (K76.3)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Примечания
Данное состояние известно также под названиями «ишемический (гипоксический) гепатит», «шоковая печень» и другие. Однако, по мнению большинства авторов, их применение неправомочно по следующим причинам:
— признаков воспаления, отвечающих значению термина гепатит, не наблюдается;
— шок (нарушение перфузии вследствие снижения артериального давления) не является единственной причиной возникновения инфаркта печени.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Этиология и патогенез
Двойное кровоснабжение (a. hepatica, v. porta) обуславливает редкость инфарктов в печени.
К инфаркту печени может привести нарушение кровотока во внутрипеченочных ветвях одного или обоих сосудов. Объективно об инфаркте печени говорят чаще всего в связи с уменьшением кровотока по a. hepatica, которая обеспечивает 50-70% необходимого тканям кислорода. Воротная вена отвечает за 65-75% притока крови к печени и за 30-50% оксигенации тканей. Артериальный приток крови тесно связан с венозным, так что общий поток крови через печень остается постоянным.
Принято говорить о равном участии артерии и вены в кровоснабжении (оксигенации) печени, хотя в экстремальных условиях возможно «перераспределение нагрузки». Механизм регулирования общего кровотока опосредован только печеночной артерией, воротная вена не может регулировать поток крови. Артериальный кровоток регулируется конкретным участками, осуществляющими выброс аденозина (мощного вазодилататора). Когда кровоток высок, аденозин быстро удаляется, что приводит к артериальной вазоконстрикции. И наоборот, когда портальный кровоток является низким, аденозин-опосредованный вазодилатационный эффект в артериальных сосудах необходим для увеличения общего кровотока.
Причины ишемии печени могут быть самыми разнообразными:
1. Системное понижение артериального давления:
— шок (в 50% случаев);
— синдром компрессии чревного ствола.
2. Печеночная артерия. Локальное снижение кровотока:
— тромбоз (любой этиологии);
— эмболия (любой этиологии);
— перекрут добавочной доли печени;
— сдавление опухолью (крайне редко);
— манипуляции (хирургические и диагностические) как эндоартериальные (например, ангиография), так и собственно на тканях печени (например, радиоабляция опухоли); вторая после шока причина ишемии печени;
— травма артерии (включая разрыв).
3. Печеночная воротная вена:
— тромбоз и эмболия (любой этиологии);
— компрессия извне.
К ятрогенным повреждениям относятся:
— артериальная гипотензия, вызывающая недостаточную перфузию внутренних органов и уменьшение портального кровотока;
— действие анестетиков;
— правожелудочковая или левожелудочковая недостаточность;
— тяжелая гипоксемия;
— реперфузионное повреждение печени.
— больные циррозом печени особенно чувствительны к повреждающему действию интраоперационной ишемии, так как ткань печени при этой патологии в большей степени зависит от кровотока по печеночной артерии.
Острая непроходимость печеночной артерии может быть возникать в результате тромбоза у больных с системными васкулитами (узелковый периартериит и другие), миелопролиферативными заболеваниями (полицитемия, хронический миелолейкоз). Она возникает при опухоли (сдавленне, прорастание, эмболия) атеросклерозе, воспалительных процессах в соседних органах, после травмы и т.п.
Причиной закупорки артерий может стать эмболия при инфекционном эндокардите и других заболеваниях сердца (особенно сопровождающихся мерцанием предсердий), при атероматозе аорты. Возможна случайная перевязка или травма печеночной артерии при операции.
Патогенез
Артериальное кровоснабжение печени изменчиво: варьируют сами ветви печеночной артерии и многочисленные анастомозы. Поэтому последствия окклюзии печеночной артерии зависят от ее места, коллатеральной циркуляции и состояния портального кровотока. Очень опасны окклюзии основного ствола, а также ситуации при одновременном нарушении кровообращения в системе воротной вены.
Инфаркты при окклюзии концевых ветвей и недостаточном коллатеральном кровотоке имеют сегментарный характер, они редко достигают в диаметре 8 см, хотя описаны случаи, когда некротизируется целая доля и даже желчный пузырь.
Морфологический картина. Инфаркт печени всегда ишемический с окружающей застойной геморрагической полоской. Субкапсулярпые поля не затронуты в связи с добавочным кровоснабжением. По периферии инфаркта портальные поля сохранены.
Этиология:
— прием контрацептивов;
— сдавление воротной вены извне опухолями, кистами;
— воспалительные изменения стенки воротной вены (при язвенной болезни, аппендиците, травмах брюшной стенки, живота);
— при циррозе печени;
— при интраабдоминальном сепсисе;
— при компрессии вены опухолью;
— при панкреатите и других воспалительных процессах в брюшной полости;
— как послеоперационное осложнение;
— при травмах;
— при дегидратации;
— при нарушении коагуляции.
Эпидемиология
Признак распространенности: Крайне редко
Распространенность неизвестна. Предполагается преобладание пациентов старшего возраста.
Аневризма в печени что это такое
Аневризмы висцеральных артерий (АВА) встречаются довольно редко и в большинстве наблюдений являются диагностической находкой при обследовании больного. По данным мировой литературы, частота АВА при аутопсиях составляет от 0,01 до 0,2% [8]. АВА классифицируются по происхождению: врожденные и приобретенные; по морфологии: истинные и ложные; по форме: мешотчатые и веретенообразные [1, 2]. Наиболее часто из АВА встречаются аневризмы селезеночной артерии (60-80%), затем следуют аневризмы печеночной артерии (20%), аневризмы гастродуоденальной, панкреатодуоденальной артерий, артерии поджелудочной железы (6%); реже наблюдаются аневризмы верхней брыжеечной артерии (5,5%), чревного ствола (4%); аневризмы артерий других локализаций встречаются менее чем в 4% наблюдений [2, 9]. Особняком стоит проблема диагностики и лечения аневризм почечных артерий, встречающихся гораздо чаще и занимающих второе место после аневризм селезеночной артерии [6].
Этиология АВА довольно широка. Причинами появления истинных АВА являются атеросклероз, фибромышечная дисплазия, нарушение в строении коллагеновых волокон и часто встречающееся разрушение медии сосудистой стенки, выражающееся в потере или фрагментации эластиновых нитей и уменьшении мышечных волокон. Однако, по данным литературы, атеросклеротические изменения сосудистой стенки рассматриваются как вторичные проявления. Псевдоаневризмы появляются вследствие травматического повреждения сосудистой стенки, вызванного в том числе ятрогенией, инфицированием, воспалением или васкулитами. Изменение структуры окружающих тканей также способствует развитию АВА. Наглядным примером является неблагоприятное воздействие ферментативной системы поджелудочной железы на окружающие ткани при развитии панкреатита [10].
Аневризмы селезеночной артерии (АСА)
АСА встречаются чаще всего. Для АСА характерна четкая связь с половой принадлежностью пациента, у женщин они встречаются в 4 раза чаще, чем у мужчин [11]. Данное соотношение объясняется агрессивным воздействием на сосудистую стенку селезеночной артерии повышенного уровня эстрогенов [9]. Среди женщин с АСА 40% являются повторнородящими [11] и у 10% выявляются деструктивные изменения печени с исходом в цирроз и развитием портальной гипертензии, приводящей к повышению давления в бассейне селезеночной артерии [11]. Фибродисплазия как основной фактор появления АСА отмечается в 2% наблюдений [11] в сочетании с изменениями в структуре почечных артерий. Псевдоаневризмы селезеночной артерии, как правило, возникают в результате развития панкреатита и панкреатических псевдокист. Как правило, АСА достигают 4 см в диаметре, мешковидные, протекают асимптомно и располагаются в средней или дистальной трети селезеночной артерии [10]. Гораздо реже встречаются веретенообразные АСА. Частота разрывов АСА зависит от размера аневризм и достигает 12% с летальностью 36% [5]. Разрывы АСА во время беременности, часто происходящие в III триместре, являются катастрофой и приводят к смерти плода и матери в 70-90% наблюдений [10].
Развернутая клиническая картина при АСА проявляется, как правило, при разрыве. Пациенты в момент разрыва АСА ощущают острую боль в области левого подреберья с иррадиацией в подлопаточную область, что сопровождается выраженной гипотонией. Начинающийся разрыв АСА происходит изнутри в толщу аневризматического мешка с последующим разрывом внешней оболочки и кровоизлиянием в брюшную полость; описанный процесс известен под названием «феномен двойного разрыва» [10].
В большинстве наблюдений АСА можно визуализировать при плановой рентгенографии органов грудной клетки как сосудистый кальцинат, имеющий вид круга [11]. Диагностика АСА дополняется применением мультиспиральной компьютерной томографии, а также селективной ангиографии.
Хирургическое лечение АСА сводится к резекции аневризматического мешка, перевязке селезеночной артерии и спленэктомии при больших размерах аневризматического мешка и расположении в воротах селезенки. После спленэктомии образовавшееся пространство заполняют большим сальником [11]. Дистальная панкреатотомия может быть выполнена при расположении аневризмы в паренхиме поджелудочной железы. Сохранение селезенки без реконструкции артериального сегмента может привести к инфаркту этого органа с развитием абсцесса. В случае возможности реконструкции производят резекцию аневризматического мешка с восстановлением структуры селезеночной артерии с помощью наложения анастомоза конец в конец или протезированием артерии аутовенозным трансплантатом.
Известны наблюдения эндоваскулярных вмешательств при АСА. Однако несмотря на малую травматичность применяемых методик, существуют ограничения в использовании эндоваскулярной хирургии. Для оптимального результата необходимо наличие широкой шейки АСА и расположения последней в проксимальной трети селезеночной артерии, что приведет к «выключению» аневризмы из кровотока и улучшению перфузии селезенки и снижению риска разрыва. Кроме того, применение стент-графта позволяет облегчить доступ к селезеночной артерии во время эмболизации селезенки при гиперспленизме. Однако естественный извитой ход селезеночной артерии, дистальное расположение аневризм существенно ограничивают проведение стента, поэтому открытое хирургическое вмешательство выходит на первый план [11].
Аневризмы печеночной артерии (АПА)
АПА занимают второе место по частоте среди аневризм непарных висцеральных ветвей брюшного отдела аорты, составляя 20%, половина из которых представлена ложными аневризмами. Расположение аневризм помогает в выявлении причины и определении дальнейшей тактики ведения больного. Внутрипеченочные аневризмы ветвей печеночной артерии часто образуются в результате травмы, ятрогенных повреждений после биопсии или оперативных вмешательств на печени, воздействия инфекционных агентов или вследствие васкулита. Внепеченочные аневризмы, как правило, наблюдаются после трансплантации печени, общехирургических манипуляций, чрескожных вмешательств на желчевыводящих путях, закрытой травмы живота, а также сопровождают гепатоцеллюлярный рак [10].
Как правило, АПА одиночные, веретенообразные или мешотчатые и в 80% наблюдений располагаются внепеченочно. Очень малая доля АПА протекает с определенной симптоматикой (дискомфорт в эпигастральной области вследствие расширения аневризматического мешка, болевой синдром, характерный для панкреатита) [11]. Иногда АПА могут вызывать желтуху или гемобилию. Описанные симптомы составляют триаду Квинке и отмечаются у 1 / 3 больных [10]. Чаще всего АПА диагностируют с помощью применения селективной ангиографии, компьютерной томографии, ультразвуковой диагностики или МРТ. Рентгенография малоинформативна ввиду низкой частоты атеросклеротического поражения артериальной стенки.
От 20 до 40% АПА осложняются разрывом, что приводит к летальному исходу в 35-40% наблюдений [10]. Велик риск разрыва неатеросклеротических АПА. Разрыв АПА чаще происходит в гепатобилиарное пространство, приводя к гемобилии, в желудочно-кишечный тракт, полость желчного пузыря, воротную вену, а также в брюшную полость [5].
Аневризмы гастродуоденальной, панкреатодуоденальной артерий и артерии поджелудочной железы
В большинстве наблюдений развитию аневризм указанных артерий способствуют панкреатит, язвенная болезнь желудка и двенадцатиперстной кишки, повышение артериального давления в соответствующих бассейнах при окклюзии чревного ствола, перенесенные оперативные вмешательства на поджелудочной железе. Большинство больных предъявляют жалобы на боль в эпигастральной области с иррадиацией в спину. Разрывы аневризм сопровождаются кровотечением в полость желудка, двенадцатиперстной кишки, реже через желчевыводящие пути и панкреатические протоки. F. Boudghene и соавт. сообщали об успешном лечении 32 аневризм панкреатодуоденальных артерий с применением транскатетерной эмболизации. Следует подчеркнуть, при использовании эндоваскулярного лечения очень важно произвести поиск «питающей» артерии, так как в перигастральной области имеется очень развитая сосудистая сеть. С целью контроля за эффективностью проведенного лечения необходим ангиографический контроль в динамике [4, 5, 10].
Аневризмы чревного ствола (АЧС)
АЧС встречаются в 4% всех аневризм висцеральных ветвей аорты и часто являются асимптомными. В 13% наблюдений отмечаются разрывы с летальностью более 50%. Клиническая картина при разрыве АЧС представлена кровотечением в брюшную полость или в желудочно-кишечный тракт. Часто АЧС бывает дегенеративными, сочетаются в 20% наблюдений с аневризмами аорты и в 40% наблюдений с аневризмами других висцеральных артерий. В большинстве наблюдений АЧС являются диагностическими находками. При лечении АЧС применяют традиционное хирургическое вмешательство в объеме резекции аневризмы с восстановлением проходимости чревного ствола путем анастомозирования конец в конец. Если это невозможно, то производят целиакоаортальное протезирование синтетическими протезами или аутовеной. Частое расположение аневризм в проксимальном отделе чревного ствола и отсутствие шейки ограничивают применение эндоваскулярного вмешательства [5, 10].
Аневризмы верхней брыжеечной артерии (АВБА)
АВБА составляют 5,5% всех аневризм висцеральных артерий, часто сопровождаются дискомфортом и болью в животе, варьирующей от тупой до нестерпимой и ассоциирующейся с «кишечной жабой». Они бывают мешотчатыми и веретенообразными, обычно располагаются в проксимальной части ВБА рядом с устьем панкреатодуоденальной артерии и средней толстокишечной артерии. Причинами развития АВБА являются грибковые поражения с вторичным присоединением бактериальной микрофлоры, связанные с бактериальным эндокардитом, наркоманией. Также имеются сведения о влиянии дегенерации медии, травмы и болезни Бекета. От 38 до 50% аневризм осложняются разрывами.
Выбор метода лечения зависит от состояния гемодинамики больного и операционного риска. Наиболее часто применяется традиционное хирургическое лечение. Варианты оперативных вмешательств включают резекцию, ушивание или перевязку аневризмы с выполнением артериальной реконструкции или без нее. Допускается перевязка ВБА и ЧС в связи с выраженным развитием коллатерального кровообращения. Однако реконструктивная хирургия с применением аутовенозного или синтетического трансплантата незаменима при высокой угрозе разрыва аневризмы или наличии признаков ишемии кишечника. Ввиду наиболее частого захвата аневризмой проксимального отдела ВБА, отсутствия зоны имплантации стента ограничивают применение эндоваскулярного лечения [3, 5, 10].
Аневризмы почечных артерий (АпА)
АпА часто рассматривают отдельно от остальных аневризм висцеральных ветвей ввиду отличной этиологии и значительно меньшего риска разрыва и низкой летальности. АпА тесно связаны с артериальной гипертензией. Частота истинных АпА составляет примерно 0,015-1%. Появлению АпА способствует дегенерация медии и фибродисплазия, а также фрагментация внутренней эластической пластинки, обнаруженная при гистологических исследованиях. В определенной степени развитию АпА способствуют артериальная гипертензия и атеросклероз. Редкими причинами являются нейрофиброматоз и неспецифический артериит. Большинство АпА мешотчатые и в 75% наблюдений они расположены в ветвях первого или второго порядка, менее чем в 10% наблюдений отмечается интрапаренхимальное расположение аневризм. Большинство АпА протекает асимптомно и лишь в 30% наблюдений имеют место злокачественная гипертензия, болевой синдром, гематурия, инфаркт почки и разрыв. Наиболее серьезным осложнением, встречающимся в 30% наблюдений, является разрыв АпА. Летальность достигает 10%. Однако имеются сведения о сочетании АпА с АСА у беременных, при разрыве во время беременности летальность достигает 80-90% [11].
АпА выявляются с помощью ультразвуковой диагностики, брюшной аортографии и мультиспиральной компьютерной томографии.
Лечение АпА заключается в применении как консервативных методов, так и хирургического лечения. Консервативный метод лечения используют при асимптомных АпА. Аневризмы диаметром до 2 см требуют динамического наблюдения. В случае злокачественной гипертензии, проявления урологических симптомов рекомендуют проведение диссекции, эмболизации, локальной компрессии путем эндоваскулярного вмешательства у женщин репродуктивного возраста или в периоде беременности. При хирургическом лечении производят резекцию аневризмы с последующей реконструкцией почечной артерии. При эндоваскулярном лечении в основном применяют стент-графты с учетом адекватного почечного кровотока. Однако при больших размерах аневризмы, распространении ее на паренхиму почки и при подозрении на разрыв производят резекцию почки или нефрэктомию с резекцией аневризмы и перевязкой пораженной почечной артерии. Оптимальным вариантом при хирургическом вмешательстве является забрюшинный доступ, обеспечивающий хорошую экспозицию почечной артерии и почки [6, 11]. В эпоху развития эндоваскулярной хирургии последнюю рассматривают как оптимальный вариант ввиду малой травматичности и хорошего отдаленного результата [7].
Таким образом, аневризмы висцеральных артерий являются редким сосудистым заболеванием и часто осложняются разрывом. Наиболее распространены аневризмы селезеночной, печеночной и почечных артерий. Клиническая картина крайне скудна и в основном проявляется в момент разрыва. Диагностический спектр включает ультразвуковое исследование, мультиспиральную компьютерную томографию с применением контрастных веществ; для оценки возможности применения эндоваскулярных методик используют селективную ангиографию. Выбор метода лечения зависит от тяжести состояния больного, клинических проявлений, а также локализации аневризмы и ее морфологии. Предпочтение отдают эндоваскулярным методикам, являющимся малотравматичными и обеспечивающими хороший долгосрочный результат. Однако в каждом конкретном наблюдении тактика ведения больного индивидуальна, выбор оптимального способа лечения аневризм висцеральных артерий основывается на данных всего спектра возможных диагностических манипуляций.
Аневризма аорты
Причины развития аневризмы аорты
Точные причины патологического расширения аорты до сих пор не установлены. Общепринятой является точка зрения, считающая врожденную слабость соединительной ткани основным фактором развития заболевания. В пользу этой теории говорит множественность аневризм в различных отделах артериальной системы. К другим факторам риска относятся:
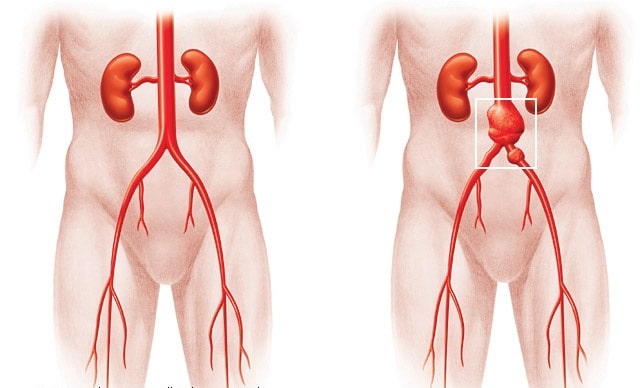
Строение аорты и особенности локализации аневризмы
Аорту принято делить на несколько отделов, в каждом из которых может развиться аневризма:
Течение аневризмы аорты
Неосложненная аневризма аорты медленно, но неуклонно растет в размерах и начинает сдавливать окружающие ткани, вызывая болевые ощущения. При развитии тромбоза аневризматического мешка и переносе фрагментов тромбов по кровотоку могут появиться признаки недостаточности кровообращения конечностей (трофические язвы, некрозы пальцев) или внутренних органов (почечная недостаточность, нарушение спинального кровообращения). Чем больше диаметр аневризмы, тем выше риск ее разрыва. При наличии симптомов аневризмы брюшного отдела аорты и размера свыше 5 см в диаметре риск разрыва повышается до 20% в год, то есть через 5 лет погибают все пациенты. Аневризма аорты через выпячивание стенки может давить на окружающие ткани подобно опухоли, вызывая разрушение поясничных позвонков и даже грудины.
Осложнения аневризмы аорты
Диаметр аорты в области аневризмы значительно увеличен, поэтому кровоток в зоне этого мешка замедлен. В патологической емкости могут образоваться тромбы, которые уменьшают функционирующий просвет аорты и тем самым нормализируют скорость кровотока. Однако тромботические массы являются рыхлой и нестабильной структурой. При некоторых условиях отдельные кусочки этих тромбов могут отрываться и переноситься с током крови в ниже- или вышележащие отделы сосудистого русла, приводя к закупорке артерии и развитию острой недостаточности кровообращения (гангрене, инсульту).
В ряде случаев просвет аневризмы может тромбироваться полностью, в этом случае развивается картина острой недостаточности кровообращения в частях тела, расположенных ниже по течению аорты. Если этот процесс происходит в брюшной аорте, то это может быть инфаркт кишечника (гибель кишки) или гибель обеих ног.
Прогноз заболевания
Без хирургического вмешательства расширение постоянно прогрессирует, чем и опасно течение аневризмы аорты. При аневризмах диаметром меньше 4 сантиметров риск разрыва невысокий. Если она выявляется у больных пожилого возраста (старше 70 лет), то вмешательство сосудистого хирурга не требуется, достаточно динамического наблюдения. При диаметре более 5 см риск разрыва очень серьезный, поэтому показания к хирургическому лечению должны быть более активными. Тромбоэмболии в большинстве случаев не зависят от размера аневризматического мешка, поэтому при их появлении необходимо всегда ставить вопрос о хирургическом лечении.
Современное лечение аневризмы
Осложнения аневризмы требуют неотложной операции. Своевременное хирургическое вмешательство может сохранить жизнь. Такое вмешательство должно проводиться в стационаре, имеющем все необходимое как для эндоваскулярного, так и открытого хирургического лечения аневризмы. Хотя разрыв аневризмы может быть прооперирован, в этих случаях удается спасти только около 50% пациентов. Даже если пациент переживет операцию, у него нередко начнут развиваться осложнения со стороны почек, некроз кишечника или ишемия ног. Любые другие осложнения, связанные с аневризмами, такие как эмболия, боль в животе, кишечная непроходимость требуют срочной операции по ее устранению.Плановое лечение имеет определенные показания, которые зависят от локализации аневризмы, возраста пациента, сопутствующих заболеваний сердца и легких. Если диаметр аневризмы превышает 50 мм риск разрыва становится неприемлемым. Боль в животе, эмболия в конечности, нарушения функции кишечника при аневризме являются показанием к хирургической операции. Если аневризма увеличивается в размерах более, чем на 10% в год, это тоже является фактором риска разрыва и заставляет принять решение о хирургическом лечении. Риск разрыва аневризмы брюшной аорты диаметром 7 см и более составляет почти 20% в год. Для устранения аневризмы аорты не существует легкого метода. Эта патология представляет серьезные сложности для хирургов.

