Ангидрид уксусной кислоты что это такое
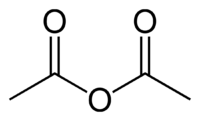
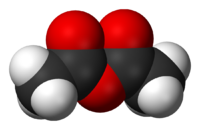
Уксусный ангидрид
| Уксусный ангидрид | |
 | |
 | |
| Общие | |
|---|---|
| Химическая формула | C4H6O3 |
| Физические свойства | |
| Состояние (ст. усл.) | жидкость |
| Молярная масса | 102,09 г/моль |
| Плотность | 1,082 г/см³ |
| Термические свойства | |
| Температура плавления | −73,1 °C |
| Температура кипения | 139,8 °C |
| Оптические свойства | |
| Показатель преломления | 1,3902 |
| Классификация | |
| Рег. номер CAS | 108-24-7 |
| SMILES | CC(=O)OC(C)=O |
У́ксусный ангидри́д (ангидри́д у́ксусной кислоты́), (CH3CO)2O, бесцветная с резким запахом жидкость, растворимая в бензоле, эфире и др. органических растворителях; tкип 139,5°С, плотность 1,082 г/см 3 (20°С). В 100 граммах холодной воды растворяется примерно 14 граммов уксусного ангидрида, который медленно реагирует с водой, образуя уксусную кислоту; при нагревании реакция ускоряется.
Синтез
Уксусный ангидрид получается общими для всех ангидридов карбоновых кислот методами. Например:
POCl3 + 4CHЗCOONa = 2(CHЗCO)2O + NaPO3 + 3NaCl
POCl3 + 4CHЗCOONa = 2(CHЗCO)2O + NaPO3 + 3NaCl
образующийся в ходе реакции ацетат алюминия, под действием температуры разлагается на уксусный ангидрид и оксид алюминия:
Использование
См. также
Полезное
Смотреть что такое «Уксусный ангидрид» в других словарях:
УКСУСНЫЙ АНГИДРИД — (СН3С0)20 бесцветная жидкость с резким запахом, tK 1ш= 139,9°С; получают нагреванием паров уксусной (см.) при 700°С в присутствии катализатора; применяют главным образом в производстве ацетилцеллюлозы, при синтезе аспирина, душистых и… … Большая политехническая энциклопедия
уксусный ангидрид — (СН3СО)2О, бесцветная с резким запахом жидкость, tкип 139,6°C. Применяют для ацилирования, например в производстве ацетилцеллюлозы, душистых и лекарственных веществ. * * * УКСУСНЫЙ АНГИДРИД УКСУСНЫЙ АНГИДРИД, (СН3СО)2О, бесцветная с резким… … Энциклопедический словарь
уксусный ангидрид — acetanhidridas statusas T sritis chemija formulė (CH₃CO)₂O atitikmenys: angl. acetic anhydride rus. ацетангидрид; уксусный ангидрид ryšiai: sinonimas – acto rūgšties anhidridas sinonimas – etano rūgšties anhidridas … Chemijos terminų aiškinamasis žodynas
Уксусный ангидрид — ангидрид уксусной кислоты, (CH3CO)2O, бесцветная с резким запахом жидкость, растворимая в бензоле, эфире и др. органических растворителях; tkип 139,5 °С, плотность 1,082 г/см3 (20 °С). У. а. один из реагентов, широко применяемых в… … Большая советская энциклопедия
УКСУСНЫЙ АНГИДРИД — ангидрид уксусной кислоты, (CH3CO)2O бесцветная жидкость с резким запахом; tnл 139,9 °С. Применяется для введения группы СН3СО (ацетилирования) при получении ацетата целлюлозы, душистых и лекарств. в в, красителей и др … Большой энциклопедический политехнический словарь
Уксусный ангидрид — C4H6O3 = (СН3CO)2О является представителем ангидридов органических жирных кислот формулы СnН2nО2. Он может быть получен в небольших количествах при действии фосфорного ангидрида на уксусную кислоту (Этар, Гал). Обыкновенно его получают так: при… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
УКСУСНЫЙ АНГИДРИД — (СН3СО)2О, бесцв. с резким запахом жидкость, tкип 139,6 °С. Применяют для ацилирования, напр. в произ ве ацетилцеллюлозы, душистых и лекарств. в в … Естествознание. Энциклопедический словарь
Ангидрид — Ангидриды в неорганической химии солеобразующие оксиды, проявляющие кислотные свойства (см. Кислотные оксиды). Ангидриды в органической химии соединения, состоящие из двух кислотных остатков (например, карбоновых или фосфиновых… … Википедия
УКСУСНЫЙ АЛЬДЕГИД — то же, что ацеталъдегид. УКСУСНЫЙ АНГИДРИД (CH3CO)2O, мол. м. 102,09; бесцв. прозрачная подвижная жидкость с резким запахом; т. пл. 73,1 X т. кип. 139,60C: 1,0820; 1,3906; t крит 295,8 0C, р криг 4,6 МПа; 0,901 мПа … Химическая энциклопедия
Ангидрид уксусной кислоты
Смотреть что такое «Ангидрид уксусной кислоты» в других словарях:
Этиловый эфир уксусной кислоты — Этилацетат Этилацетат (этиловый эфир уксусной кислоты) СН3 СОО СH2 СH3 бесцветная летучая жидкость с приятным фруктовым запахом. Содержание 1 Получение … Википедия
Ангидрид — Ангидриды в неорганической химии солеобразующие оксиды, проявляющие кислотные свойства (см. Кислотные оксиды). Ангидриды в органической химии соединения, состоящие из двух кислотных остатков (например, карбоновых или фосфиновых… … Википедия
Кислоты и ангидриды — КИСЛОТЫ И АНГИДРИДЫ. Кислоты класс химических соединений характеризующихся диссоциацией в водном растворе с образованием гидратированных ионов H+. Ангидриды химические соединения, производные органических и неорганических кислот, образующиеся при … Российская энциклопедия по охране труда
Уксусный ангидрид — ангидрид уксусной кислоты, (CH3CO)2O, бесцветная с резким запахом жидкость, растворимая в бензоле, эфире и др. органических растворителях; tkип 139,5 °С, плотность 1,082 г/см3 (20 °С). У. а. один из реагентов, широко применяемых в… … Большая советская энциклопедия
УКСУСНЫЙ АНГИДРИД — ангидрид уксусной кислоты, (CH3CO)2O бесцветная жидкость с резким запахом; tnл 139,9 °С. Применяется для введения группы СН3СО (ацетилирования) при получении ацетата целлюлозы, душистых и лекарств. в в, красителей и др … Большой энциклопедический политехнический словарь
Уксусный ангидрид — Уксусный ангидрид … Википедия
Предельные органические кислоты — (хим.) П. органические кислоты можно рассматривать как продукты замещения водородных атомов предельных углеводородов (см. Парафины) карбоксильными группами (см. Кислоты). Смотря по числу последних различают кислоты П. одноосновные, общей формулы… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Предельные органические кислоты* — (хим.) П. органические кислоты можно рассматривать как продукты замещения водородных атомов предельных углеводородов (см. Парафины) карбоксильными группами (см. Кислоты). Смотря по числу последних различают кислоты П. одноосновные, общей формулы… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Сульфоновые кислоты — или сульфокислоты (жирного ряда) С. кислотами называются производные серной кисл. OH SO2 OH, получающиеся через замену одного из гидроксилов ее углеводородными остатками, напр. CH8 SO2 OH. Так происходят одноосновные С. кислоты. При замещении… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Химическое исследование ангидрида уксусной кислоты
Храмченко В.Е., к. ф.-м. н., эксперт ЭКО УФСКН РФ по Кемеровской области.
В кругах наркозависимых ангидрид уксусной кислоты в основном применяется в качестве реагента для получения ацетилированного опия и, как правило, реализуется в шприцах однократного применения или в защитных колпачках от инъекционных игл в небольших количествах. Встречаются также случаи, когда «недобросовестные» наркоторговцы разбавляют сбываемый ангидрид концентрированной уксусной кислотой, а также другими органическими растворителями. Данные обстоятельства во многом и определяют выбор метода химического идентификационного исследования.
Общедоступным и широко используемым методом предварительной идентификации уксусного ангидрида, наряду с определением рН жидкости, является наблюдение за его растворением в холодной воде. При добавлении небольшого количества уксусного ангидрида к нескольким миллилитрам воды происходит расслоение смеси, при этом ангидрид уксусной кислоты, имеющий большую плотность, чем вода, будет находиться в нижнем слое. При смешивании безводной уксусной кислоты с водой выделяется тепло и наблюдается уменьшение объема (контракция), объясняющаяся образованием гидрата, при этом концентрацию водных растворов уксусной кислоты определить на основании плотности не удается.
В случае чистого химического вещества уксусный ангидрид может быть легко и быстро идентифицирован рефрактометрическим методом. Значение показателя преломления для уксусного ангидрида при 20 град. C составляет nD = 1,3904, для уксусной кислоты nD = 1,3718.
В случае смесей и небольших количеств представленного на исследование вещества наиболее эффективным оказывается применение метода капельных реакций. В 1920 г. Н.А. Тананаев предложил для проведения анализа использовать одну или несколько капель исследуемого вещества. Реакции проводят на фильтровальной бумаге, часовом стекле, специальных пластинках с углублениями или в маленьких фарфоровых тиглях. При выполнении анализа на часовые стекла наносят исследуемый раствор и реактивы и наблюдают появление или растворение осадков определенного цвета. Уксусный ангидрид можно отличить от уксусной кислоты проведением следующих качественных реакций (2).
Реакция Меншуткина и Васильева. При добавлении к уксусному ангидриду нескольких капель анилина наблюдается выпадение белого осадка ацетанилида. Однако следует помнить, что анилин способен давать ацетанилид не только с уксусным ангидридом, но и с выделяющейся при их взаимодействии уксусной кислотой. Более специфической реакцией является ацетилирование 2,4-дихлоранилина, осуществляемое только уксусным ангидридом. В этом случае выделение 2,4-дихлорацетанилида наблюдается при добавлении к уксусному ангидриду нескольких капель 50% раствора 2,4-дихлоранилина в эфире.
Реакция с селенитом натрия. Уксусный ангидрид удается обнаружить в присутствии уксусной кислоты по красному аморфному осадку селена, выпадающему при кипячении анализируемой жидкости с кристалликом селенита натрия. Растворы уксусной кислоты при этом остаются совершенно прозрачными.
Реакция с нитратом лантана и йодом. Очень чувствительной и весьма характерной реакцией для уксусной кислоты является взаимодействие ее нейтрализованного раствора с 5% раствором нитрата лантана в присутствии 0,02 Н раствора йода и незначительным количеством аммиака. Если на холоде не наблюдается появления ярко-синей окраски, то полученную смесь веществ медленно доводят до кипения.
Реакция образования индиго. Данная реакция является наиболее специфичной и чувствительной для уксусной кислоты. Анализируемую жидкость помещают в пробирку и смешивают с прокаленной известью. Отверстие пробирки закрывают отрезком фильтровальной бумаги, смоченной раствором о-нитробензальдегида. При нагревании пробирки под действием выделяющихся паров ацетона бумажка приобретает синий цвет индиго. Гомологи уксусной кислоты подобного окрашивания не дают.
Реакция с хлоридом железа (III). Хлорид железа способен вступать в реакцию с нейтральными растворами ацетатов с образованием ацетата железа (III) темно-красного цвета. При нагревании до кипения раствора, содержащего большое количество ацетат-ионов, выпадает объемистый красно-коричневый осадок основного ацетата железа.
Образование пахнущих веществ. Подобные реакции способны давать соединения, содержащие свободную ацетильную группу, вступающую во взаимодействие со спиртами с образованием сложных эфиров. Так, при нагревании уксусной кислоты или ее растворимых солей с несколькими крупинками п-толуолсульфокислотой и каплей амилового спирта наблюдается появление характерного запаха амилацетата (грушевой эссенции), который особенно выражен после выливания пробы в воду. Если вместо амилового спирта использовать этанол, появится приятный яблочный запах этилацетата.
Таким образом, на основе описанных капельных реакций даже при малом объеме представленной жидкости можно установить, является ли данное вещество уксусным ангидридом, уксусной кислотой или их смесью.
При проведении химического исследования следует обратить особое внимание на соблюдение техники безопасности. Ангидрид уксусной кислоты легко всасываться в организм через кожу и слизистые оболочки, а также при вдыхании паров. Опасное загрязнение воздуха достигает довольно быстро при испарении этого вещества при 20 град. C. Уксусный ангидрид оказывает разъедающее действие на глаза, кожу и дыхательные пути. Вдыхание его паров вызывает затруднение дыхания, одышку, боли в горле и отек легких, причем данные симптомы могут быть отсроченными. Кроме того, при температуре свыше 49 град. C могут образоваться взрывоопасные смеси: пар/воздух (3).
СОДЕРЖАНИЕ
Структура и свойства
Уксусный ангидрид, как и большинство ангидридов кислот, представляет собой гибкую молекулу с неплоской структурой. Систему пи связь через центральные предложения кислорода очень слабая стабилизация резонанса по сравнению с диполь-дипольного отталкивания между двумя карбонильными атомами кислорода. Энергетические барьеры для вращения связи между каждой из оптимальных апланарных конформаций довольно низки.
Производство
Уксусный ангидрид получают путем карбонилирования из метилацетата :
В меньшей степени уксусный ангидрид получают также реакцией кетена ( этенона ) с уксусной кислотой при 45–55 ° C и низком давлении (0,05–0,2 бар).
H 2 C = C = O + CH 3 COOH → (CH 3 CO) 2 O (Δ H = −63 кДж / моль)
Из-за низкой стоимости уксусный ангидрид обычно покупается, а не готовится для использования в исследовательских лабораториях.
Реакции
Ацетилирование спиртов и аминов
Спирты и амины легко ацетилируются. Например, реакция уксусного ангидрида с этанолом дает этилацетат :
Ацетилирование ароматических колец
Ароматические кольца ацетилируются уксусным ангидридом. Обычно для ускорения реакции используются кислотные катализаторы. Показательны превращения бензола в ацетофенон и ферроцена в ацетилферроцен:
Получение других ангидридов кислот
Предшественник геминальных диацетатов
Гидролиз
Уксусный ангидрид растворяется в воде примерно до 2,6% по весу. Водные растворы имеют ограниченную стабильность, потому что, как и большинство ангидридов кислот, уксусный ангидрид гидролизуется с образованием карбоновых кислот. В этом случае образуется уксусная кислота, продукт реакции полностью смешивается с водой:
Приложения
В крахмальной промышленности уксусный ангидрид является обычным ацетилирующим соединением, используемым для производства модифицированных крахмалов (E1414, E1420, E1422).
Безопасность
Уксусный ангидрид
Содержание
Структура и свойства [ править ]
Уксусный ангидрид, как и большинство ангидридов кислот, представляет собой гибкую молекулу с неплоской структурой. [3] пи система связи через центральные предложения кислорода очень слабая стабилизация резонанса по сравнению с диполь-дипольного отталкивания между двумя карбонильными атомами кислорода. Энергетические барьеры для вращения связи между каждой из оптимальных апланарных конформаций довольно низки. [4]
Производство [ править ]
Уксусный ангидрид получают путем карбонилирования из метилацетата : [6]
В меньшей степени уксусный ангидрид получают также реакцией кетена ( этенона ) с уксусной кислотой при 45–55 ° C и низком давлении (0,05–0,2 бар). [7]
H 2 C = C = O + CH 3 COOH → (CH 3 CO) 2 O (Δ H = −63 кДж / моль)
Из-за низкой стоимости уксусный ангидрид обычно покупается, а не готовится для использования в исследовательских лабораториях.
Реакции [ править ]
Ацетилирование спиртов и аминов [ править ]
Спирты и амины легко ацетилируются. [10] Например, реакция уксусного ангидрида с этанолом дает этилацетат :
Ацетилирование ароматических колец [ править ]
Ароматические кольца ацетилированы уксусным ангидридом. Обычно для ускорения реакции используют кислотные катализаторы. Показательными являются превращения бензола в ацетофенон [12] и ферроцена в ацетилферроцен: [13]
Получение других ангидридов кислот [ править ]
Предшественник геминальных диацетатов [ править ]
Гидролиз [ править ]
Уксусный ангидрид растворяется в воде примерно до 2,6% по весу. [17] Водные растворы обладают ограниченной стабильностью, поскольку, как и большинство ангидридов кислот, уксусный ангидрид гидролизуется с образованием карбоновых кислот. В этом случае образуется уксусная кислота, продукт реакции полностью смешивается с водой: [18]
Приложения [ править ]
В крахмальной промышленности уксусный ангидрид является распространенным соединением ацетилирования, используемым для производства модифицированных крахмалов (E1414, E1420, E1422).

