Антихолинергический эффект что это такое
Антихолинергический эффект что это такое
Распространенные лекарственные средства и растения, которые могут индуцировать антихолинергический синдром, перечислены в таблице ниже. Необходимо помнить, что потенциально все ТЦА способны вызывать припадки и аритмии при передозировках.
— Центральная нервная система. У пациентов с пониженным клиренсом лекарственных средств, включая пожилых людей и алкоголиков, могут наблюдаться признаки спутанности сознания, возбуждения и нервозности без выраженных антихолинергических симптомов.
Длительность комы обычно невелика: в одной серии наблюдений средняя продолжительность комы составила 6,4 ч. Случаи комы, длящейся более 24 ч. редки, являются свидетельством осложнений и бывают обусловлены одновременным приемом депрессантов центральной нервной системы.
У пожилых пациентов, принимающих антидепрессанты, может ухудшиться память. Пациенты с комой, достаточно глубокой, чтобы привести к утрате функции ствола мозга, редко выздоравливают, однако пациенты после передозировок лекарства могут полностью выздороветь, независимо от неврологических проявлений.
Это говорит о том, что необходимо продолжать интенсивное лечение любого пациента, принявшего сверхвысокие дозы трициклических антидепрессантов (ТЦА), если даже по проявлениям или по данным первоначальных оценок у пациента необратимый инсульт.
Терапевтическое применение амитриптилина вызывает острую дистонию и экстрапирамидные симптомы. Внутривенное введение 10 г проциклидина может прекратить приступ.
— Припадки. В сообщении, направленном Комиссии по безопасному применению медикаментов в Великобритании в ноябре 1979 г., указано, что зарегистрировано небольшое число припадков после применения амитриптилина и имипрамина (внедрены до 1970 г.) в сопоставлении с мапротилином и миансерином (внедрены после 1970 г.).
При припадках, индуцированных трициклическими антидепрессантами (ТЦА), отмечается повышение общей концентрации трициклических антидепрессантов (ТЦА) в плазме. Факторы риска, предрасполагающие к возникновению припадков, перечислены в таблице ниже.
Сообщения о припадках, вызванных антидепрессантами, позволяют отметить следующее:
1. Значительная доля припадков, обусловленных применением антидепрессантов, развивается у лиц с идентифицируемыми предрасполагающими факторами, такими как припадки в семейном анамнезе, неврологические и медицинские условия, одновременный прием других лекарственных средств и токсикомания.
2. Риск припадков возрастает после передозировок, т. е. существует зависимость между дозой и припадками.
3. Риск возникновения припадков после передозировок выше при применении амоксапина и мапротилина, чем при применении других антидепрессивных средств, но нет подобных сравнительных данных для бупропиона, флуоксетина и кломипрамина.
4. Взаимосвязь между дозой и риском возникновения припадков наблюдается при применении некоторых антидепрессантов в терапевтических дозах.
5. Быстрое увеличение дозы может повысить риск возникновения припадков.
6. Кумулятивный риск, при котором принимается во внимание длительность лечения, изучался редко, и изменения дозы могли внести путаницу.
Сообщалось, что после применения терапевтических доз трициклических антидепрессантов (ТЦА) наблюдались тремор, акатизия, миоклонус, дискинезия, делирий, седативный эффект, нарушения памяти, нейролептический синдром и мания.
— Рабдомиолиз. Припадки и кома являются факторами риска, предрасполагающими к развитию рабдомиолиза. Наличие только припадков или только комы не позволяет с уверенностью прогнозировать риск.
— Отек легких. Отек легких, индуцируемый трициклическими антидепрессантами, может развиться через 5—48 ч после приема лекарства. Существует сходство между респираторным дистресс-синдромом взрослых, вызванным передозировкой трициклических антидепрессантов (ТЦА), «синдромом героиновых легких» и поражением легких, обусловленным проглатыванием метадона.
В число сходных признаков входят диффузные двусторонние легочные инфильтраты на рентгенограммах грудной клетки, гипоксемия, некардиогенный отек легких и данные посмертного исследования, включающие утолщение межальвеолярных перегородок, лимфоцитарные инфильтраты и отек.
Рентгенографические свидетельства отека легких наблюдаются примерно у 10 % пациентов, получивших сверхвысокие дозы трициклических антидепрессантов (ТЦА). По данным одного из исследований, у пациентов, в плазме которых средний уровень трициклических антидепрессантов при поступлении в стационар превышал 2000 нг/мл, отмечается повышенная тенденция образования двусторонних альвеолярных инфильтратов, сопутствующих острому поражению легких.
Если у пациентов высокая пиковая концентрация трициклических антидепрессантов (ТЦА) в плазме, может быть рекомендована повторная рентгенограмма грудной клетки, даже если при поступлении пациента в стационар она была нормальной. Рентгенографические аномалии могут выявляться у некоторых пациентов с относительно низким уровнем трициклических антидепрессантов (ТЦА) в плазме при поступлении в стационар.
Смертные случаи, отмечаемые при некардиогенном отеке легких, подчеркивают возможность развития респираторного дистресс-синдрома у взрослых после сильных передозировок трициклических антидепрессантов (ТЦА). Такой отек легких может не коррелировать с гипо-тензией при поступлении в стационар. Shannon и Lovejoy считают, что у каждого третьего пациента с тяжелыми передозировками трициклических антидепрессантов (ТЦА) развиваются легочные осложнения; у каждого шестого — аспирационная пневмония и у каждого седьмого — отек легких.
В одной серии наблюдений у 9 % пациентов с передозировками трициклических антидепрессантов (ТЦА) отмечены клинические и рентгенографические показатели, соответствующие респираторному дистресс-синдрому взрослых.
— Состояние сердечно-сосудистой системы. Большинство случаев смерти после передозировок трициклических антидепрессантов (ТЦА) происходит до или вскоре после поступления пациента в больницу. Опасные для жизни аритмии и/или остановка сердца обычно наблюдаются на фоне выраженных электрокардиографических изменений, гипотензии, угнетения дыхания, комы или судорог и редко в виде единичных явлений.
Гипотензия типична после сильных передозировок трициклических антидепрессантов (ТЦА). 22-Летняя женщина проглотила 300 мг амитриптилина, что привело к инфаркту миокарда. Женщина выздоровела. Гипотензия, по-видимому, является прогностическим фактором. Гипотензия часто развивается независимо от концентрации трициклических антидепрессантов (ТЦА) в крови и ширины комплекса QRS. Гипотензия может быть тесно связана с развитием аритмий и отека легких. Гипотензия при поступлении в стационар может отмечаться после применения терапевтических доз трициклических антидепрессантов (ТЦА).
Сама по себе она не имеет большой прогностической ценности. Потенциальные электрокардиографические показатели передозировок циклических антидепрессантов представлены в таблице ниже.
Распространенными причинами летального исхода являются сердечно-сосудистая интоксикация с устойчивым угнетением функции миокарда, желудочковая тахикардия и фибрилляция желудочков. При передозировках, приведших к летальному исходу, перед смертью наблюдаются главным образом брадикардии; однако чаще всего в качестве причин смерти называют тахиаритмии и фибрилляцию желудочков. Тяжелые аритмии могут внезапно развиться у пациентов, у которых по прибытии в стационар было нормальное кровяное давление и отмечались лишь незначительные электрокардиографические изменения.
— Функция печени. Холестатические и гепатические реакции, обусловленные применением ТЦА, представляют собой идиосинкразические реакции гиперчувствительности и обычно являются слабовыраженными и обратимыми. Сообщалось о тяжелом поражении печени с молниеносным развитием печеночной недостаточности и летальным исходом.
— Состояние желудочно-кишечного тракта. Передозировка трициклических антидепрессантов (ТЦА) может вызвать ишемию кишечника, требующую резекции. У пожилых людей и у пациентов с неврологическими заболеваниями передозировка трициклических антидепрессантов (ТЦА) способна привести к псевдообструкции, спонтанной перфорации слепой кишки и фекальному перитониту. Многократное применение активированного угля в качестве лечебного средства после передозировки амитриптилина привело к образованию угольного безоара и незначительной закупорке кишечника.
— Синдромы отмены. Отмена трициклических антидепрессантов (ТЦА) может привести к развитию следующих синдромов, связанных с холинергиче-ским «рикошетом»:
1) анорексии, тошноты, рвоты, диареи, профузного потоотделения, миалгии, недомогания, головной боли, озноба, утомляемости и беспокойства;
2) бессонницы, сопровождающейся «сновидениями наяву»;
3) акатизии или паркинсонизма и
4) гипомании или мании.
По данным частных сообщений, резкое прекращение терапевтического приема ТЦА вызывало преходящие поведенческие аберрации, в частности делирий после применения доксепина, манию и гипоманию, паническую тревожность и симптомы, предполагающие холинергическую гиперактивность, после амитриптилина, а также чрезмерную двигательную активность, клинически неотличимую от акатизии, после применения имипрамина.
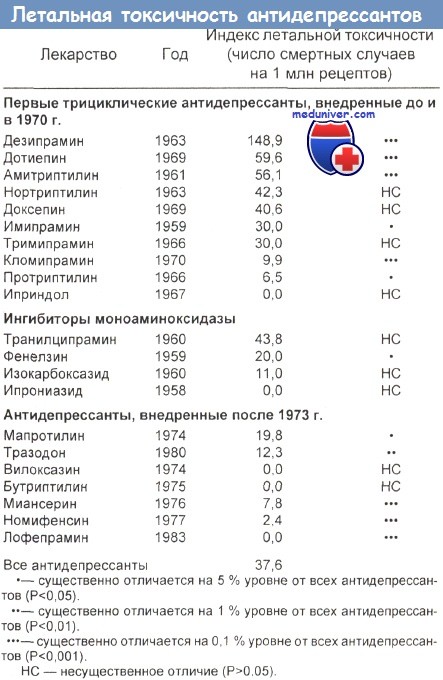
— Смертные случаи. В Великобритании проводилось исследование, в ходе которого сравнивалось число смертных случаев после отравления разными антидепрессантами. Сделанный при этом анализ выписанных рецептов позволил сделать вывод, что вероятность летального исхода при передозировках амитриптилина, дотиепина, доксепина, тримипрамина и мапротилина во всех возрастных группах выше, чем после передозировки миансерина и карпипрамина.
У такого рода исследований есть определенные методологические слабости (различные популяционные группы, данные наблюдений в больницах сопоставляются с данными наблюдений обще практикующих врачей, использование более одного вещества и т. д.). Сопоставление индексов летальной токсичности некоторых трициклических антидепрессантов и антидепрессантов второго поколения показало, что старые трициклические антидепрессанты (ТЦА) токсичнее, чем лекарства второго поколения того же терапевтического класса.
Ценность подобных данных об индексах летальной токсичности будет выше, если они будут дополнены данными исследований, проводимых в других странах.
Клиника отравления новыми циклическими антидепрессантами
— Амоксапин и локсапин. Передозировки амоксапина могут нарушить рефлексы ствола головного мозга, после чего наступает выздоровление. Роговичные рефлексы восстанавливаются через 24 ч после проглатывания лекарства; окулоцефалическая и окуловестибулярная реакции иногда не восстанавливаются в течение 36—48 ч.
Скрининг пациентов, у которых отсутствовали окулоцефалические и роговичные рефлексы, показал, что больные страдали персистентными неврологическими расстройствами, у 37-летней женщины, проглотившей около 875 мг амоксапина, развился нейролептический синдром. Хотя утверждается, что амоксапин оказывает меньшее воздействие на сердечную функцию, чем другие ТЦА, передозировки амоксапина могут вызвать обострение и сердечной недостаточности, и аритмии.
— Мапротилин. Сочетание высоких доз мапротилина с синусовой тахикардией и патологическими электрокардиограммами предопределяет высокий риск возникновения единичных и множественных припадков. Минимальная токсическая доза мапротилина — 425—750 мг. Считают, что самая низкая летальная доза мапротилина равна 3 г, но известны случаи выживания даже после проглатывания 5 г препарата. У 50-летней женщины, найденной мертвой, содержание мапротилина в крови составляло 1 мкг/мл.
— Миансерин. Хотя применение миансерина редко вызывает сердечные аритмии, передозировка миансерина (количество препарата неизвестно) в одном случае привела к опасным для жизни желудочковым аритмиям, в том числе к полиморфной желудочковой тахикардии, при этом концентрация миансерина в сыворотке в 20—50 раз превышала терапевтический уровень.
Терапевтическая концентрация миансерина (плюс деметилмиансерин) — 100 нг/мл, а тяжелая интоксикация отмечается при концентрациях выше 500 нг/мл. Резкое сужение зрачков наблюдалось при передозировке миансерина, составившей 1200 мг. Применение налоксона не привело к нормализации зрачков. В течение 6 ч больной был в сознании, диаметр его зрачков при этом был равен 2 мм. Спустя 24 ч величина зрачков нормализовалась.
Через 2 ч после передозировки концентрация миансерина в крови составляла 390 нг/мл, а уровень деметилмиансерина — 7 нг/мл. После симптоматического лечения пациент выздоровел.
— Тразодон. Передозировка тразодона в одном случае вызвала припадки и развитие гипонатриемии. Пациент выжил. Сильная передозировка тразодона (4,5 мг) вызвала тяжелую сердечную интоксикацию (синусовую брадикардию, удлинение интервала Q—Tc, «пируэтное» нарушение ритма, остановку сердца), кому и почечную недостаточность, что привело к смерти пациента.
В присутствии других депрессантов центральной нервной системы часто отмечается угнетение дыхания, но, по имеющимся сообщениям, остановка дыхания происходила после проглатывания 2,2 и 3,0 г тразодона.
— Вилоксазин. У пациентов, проглотивших вилоксазин в дозах от 1 до 6,5 г в сочетании с бензодиазепином, развились гипотензия и кома. Пациенты выздоровели в течение 24 ч. Электрокардиографические аномалии после передозировки вилоксазина наблюдались у немногих пациентов, хотя имеются частные сообщения о случаях кардиогенного шока с нарушением проведения и нижней коронарной ишемии.
Сообщалось о случае возникновения припадков после применения терапевтической дозы — 300 мг/сут. Не сообщалось о случаях летального исхода после передозировок вилоксазина. Седативный эффект, гипотензия, нежелательные антихолинергические эффекты и увеличение массы тела обычно не представляли собой проблемы, если вилоксазин применяли в терапевтических дозах. Тошнота отмечается у 20—50 % пациентов и является главной причиной, по которой пациенты прекращают прием этого лекарства.
— Каприпрамин. Острое отравление каприпрамином изучалось парижской группой исследователей. Клинические проявления были такими же, как при передозировках ТЦА: много антихолинергических симптомов и замедление внутрижелудочкового проведения. Такие нарушения проведения отмечаются после проглатывания 1 г или большего количества каприпрамина. Описан случай летального исхода после проглатывания каприпрамина и этилового спирта, концентрация каприпрамина в крови при этом составляла 2,0 мг/л (2 мкг/мл).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Неврологические расстройства
Экстрапирамидная симптоматика
Основным побочным эффектом типичных, значительно реже атипичных антипсихотиков считается экстрапирамидная симптоматика, отчасти напоминающая остаточные проявления эпидемического энцефалита: дистонии, скованность, гиперкинезы, акатизия и поздняя дискинезия.
Типичные антипсихотики часто вызывают экстрапирамидную симптоматику: острую дистонию (окулогирные кризы и тортиколлис), паркинсонизм (брадикинезия, тремор, ригидность мышц), акатизию (двигательное, субъективно тягостное бесспокойство) (таблица 33).
Таблица 33. Экстрапирамидная симптоматика, регистрируемая на фоне приема типичных антипсихотиков
Частота встречаемости
Патогенетические механизмы
Время появления
Факторы риска
Лечение
Ранние (острые) дискинезии: окулогирные кризы и тортиколлис
Дефицит дофаминергической активности в базальных ганглиях
Молодой возраст, высокая дозировка
Неотложное назначение антихолинергических препаратов и в дальнейшем снижение дозы антипсихотика
Паркинсонизм (брадикинезии, тремор, мышечная ригидность)
Блокада D2-рецепторов в базальных ганглиях
1-10 неделя терапии
Высокая дозировка препарата
Снижение дозы антипсихотика и назначение пероральных антихолинергических препаратов
Акатизия (моторное и субъективное бесспокойство), тасикинезия
Блокада D2-рецепторов и снижение концентрации железа в базальных ганглиях
1-10 неделя терапии
Низкий уровень железа в сыворотке крови
Уменьшение дозы препарата, назначение бензодиазепинов и бета-блокаторов.
Механизм развития неизвестен, в большинстве источников связывается пролонгированной блокадой рецепторов дофамина (D2).
Начиная с 12 недели терапии
Пожилой возраст, женский пол, органическое заболевание мозга, доминирование негативной симптоматики, выраженные аффективные расстройства, высокие дозы антипсихотиков
Снижение дозировки антипсихотика с последующим переходом на прием атипичных антипсихотиков (клозапин), витамин Е в сравнительно высоких дозах
Выраженность экстрапирамидной симптоматики на фоне приема эквивалентных доз различных антипсихотиков представлена в таблице 34.
Таблица 34. Выраженность экстрапирамидной симптоматики на фоне приема различных антипсихотиков
Препарат
Эквивалентная доза (мг) хлопромазин =100
Риск появления экстрапирамидной симптоматики
Острая дистония проявляется максимальным сокращением определенных групп мышц, обычно мышц языка и грудинно-ключично-сосцевидной. Однако возможно распространение спазма и на другие группы мышц (опистоклонус, тортиколлис, окулогирные кризы и др.). Проявления острой дистонии сопровождаются выраженным психическим возбуждением и в ряде случаев напоминает поведение при истерии. Обычно острая дистония наблюдается в начале лечения нейролептиками (бутирофеноны, фенотиазины) и чаще возникает у лиц молодого возраста.
Острая дистония требует неотложной терапии, особенно если речь идет о спазме мышц гортани, опасном в связи с задержкой дыхания. Лечение дистонии обычно проводится с помощью препаратов, обладающих антимускариновым (проциклидин, акинетон) или антихолинергическим эффектом, при этом предпочтительно внутримышечное введение препаратов.
Проявления острой дистонии
Паркинсонизм характеризуется тремором, ригидностью мышц, чувством скованности, замедленностью движений. Выраженная акинезия может напоминать проявления кататонии.
Обычно он развивается спустя несколько недель после назначения нейролептиков (псевдопаркинсонизм). Большему риску развития паркинсонизма подвержены пожилые люди.
Паркинсонизм считается одной из значимых причин прекращения приема антипсихотиков (Perkins D., 2002).
Симптомы паркинсонизма, индуцированного приемом антипсихотиков
При экстрапирамидной ригидности мышцы напряжены, эластичность их утрачена. Наблюдается равномерное повышение тонуса мышц, как сгибателей, так и разгибателей. Экстрапирамидная ригидность может свидетельствовать о вовлечении в процесс таких глубоких структур мозга, как черная субстанция.
При пассивных движениях отмечается сопротивление, иногда с прерывистыми задержками («симптом зубчатого колеса»), маскообразное лицо, сгорбленная поза, семенящая походка, слюнотечение.
При появлении паркинсонизма следует последовательно уменьшить дозу антипсихотика, перейти с традиционного нейролептика на атипичный антипсихотик. Паркинсонизм лечится оральным приемом антимускариновых и антихоленергических препаратов (циклодол, проциклидин и др.). В ряде случаев показано применение L — Допы.
Препараты, используемые для терапии паркинсонизма, представлены в таблице 38.
Таблица 38. Препараты для лечения паркинсонизма
Препараты
Диапазон доз
Тригексифенидил (Паркопан, Циклодол)
25 мг раза в сутки, 50 мг 2 раза в сутки
100 мг раза в сутки
Акатизия
Акатизия — это нарушение моторики, субъективно переживаемое как интенсивное и крайне неприятное ощущение неусидчивости, желания постоянно двигаться, особенно выраженное в нижних конечностях. Стремление к движению, сопровождается однообразными действиями, мучительным чувством неловкости.
Акатизия не может контролироваться больным и поэтому вызывает сильное беспокойство, тревогу, возбуждение. Слабовыраженная акатизия может не проявляться моторной активностью, а ограничиваться тревогой, чувством внутреннего бесспокойства.
Обычно акатизия развивается в первые две недели после начала лечения антипсихотиками, увеличении их дозы, смене медикаментов, реже она фиксируется после нескольких месяцев терапии.
Она появляется при назначении как типичных, так и атипичных антипсихотиков. Ввиду тягостности акатизии для пациента, появления у него ощущения безнадежности при этом состоянии, считается одной из значимых причин возникновения суицидальных мыслей.
Акатизия считается основной причиной отказа пациентов от приема антипсихотических препаратов (Арана Д., Розенбаум Д., 2004), причем она может возникнуть при приеме любого антипсихотика, включая клозапин. Вследствие вышесказанного предполагают, что риск возникновения актизии не связан с блокадой D2-рецепторов. Однако при приеме липофильных, центрально-активных антагонистов альфа-адренорецепторов (пропранолол), выраженность акатизии слабеет, что может указывать на роль адренергических механизмов в генезе этого осложнения терапии (Lima A. et al., 2004).
При переходе от акатизии и таксикинезии к паркинсонизму возникает крайне неприятное для больного состояние, когда насильственная потребность в движениях не может реализоваться из-за обездвиженности, возникающей вследствие развития мышечной ригидности. Замечено, что такое состояние чаще всего возникает у молодых женщин.
Поздняя акатизия (acathisia tarda) иногда появляется после отмены нейролептиков, Она проявляется чрезмерной двигательной активностью вследствие выраженного общего беспокойства, сопровождается чувством дискомфорта, возникающим во время медленной ходьбы, неприятными ощущениями в коже и мышцах, внутренней тревогой и мышечной напряженностью.
Акатизию бывает сложно отличить от ажиатации и тревоги. Здесь следует иметь в виду, что при увеличении дозы антипсихотика тревожное возбуждение, обусловленное психозом, ослабевает в своей выраженности, напротив при снижении дозы антипсихотика — исчезают проявления акатизии.
К препаратам первого ряда, купирующими симптомы акатизии, относятся: пропранолол, применяемый в дозе 3 раза в сутки, антихолинергические средства и бензодиазепины (таблица 39). Однако следует иметь в виду возможную устойчивость симптомов этого осложнения к проводимой терапии. В последних исследованиях обнаружено преимущество амантадина — сульфата (ПК — Мерц) (100 — 300 мг/сут.) перед циклодолом, особенно у пожилых больных шизофренией, в отношении купирования проявлений акатизии и брадикинезии.
Таблица 39. Препараты для лечения акатизии
Класс препаратов
Препараты
Средние дозы
Элиминация (часы)
Поздняя дискинезия (тардивная дискинезия)-расстройство координированных актов движения, включающее в себя аномальные непроизвольные движения. С одной стороны, она выражается в замедленности движений, небольшой акатизии, с другой-периодически возникающими сокращениями разных групп мышц, обычно оральной зоны лица: сокращение жевательных мышц, гримасы лица. Реже поздняя дискинезия проявляется в виде других гиперкинезов, напоминающих проявления хореи: хореоатетоза, миоклонии, тиков, спастической кривошеи, блефороспазма. Сравнительно редко тардивная дискинезия касается мышц респираторной системы.
Интересно отметить, что еще до появления нейролептиков у больных шизофренией в ряде случаев обнаруживались проявления симптомов дискинезии. Эти симптомы также были отмечены у гастроэнтерологических больных, в течение длительного времени принимавших метоклопрамид.
Механизм развития поздней дискинезии в настоящее время неивестен, однако в большинстве источников он связывается с пролонгированной блокадой рецепторов дофамина.
К факторам риска возникновения этого осложнения сегодня относят: пожилой возраст, женский пол, органическое заболевание мозга, доминирование негативной симптоматики, выраженные аффективные расстройства, высокие дозы длительное время используемых типичных антипсихотиков.
Поздняя дискинезия наблюдается у больных, длительно — на протяжении нескольких месяцев и лет — лечившихся нейролептиками. В течение первых лет лечения вероятность ее появления обычно невелика и достигает всего лишь 5% (Kane J. с соавт., 1988).
Важно отметить, что симптомы поздней дискинезии могут усилиться при приеме препаратов, используемых для лечения паркинсонизма. Вследствие вышесказанного рекомендуется отмена холинолитиков при возникновении поздних дискинезий.
Поздняя дискинезия может временно исчезать после увеличения доз нейролептиков и, напротив, усиливаться после снижения дозы или резкой отмены препарата (50% случаев появления поздней дискинезии зарегистрировано после резкой отмены нейролептиков).
Отмечены случаи ее появления через несколько месяцев после отмены нейролептиков, даже у больных, годами их принимавших.
Значимым предиктором поздней дискинезии считается возникновение острой экстрапирамидной симптоматики.
У больного может быть усиление симптомов этого неврологического расстройства, если он не знает, что за ним наблюдают. Также проявления дискинезии усиливаются при попытке пациента выполнять задания, требующие быстрого чередования движений.
Для предотвращения дискинезии следует тщательно исследовать неврологический статус пациента каждые 6 месяце в терапии, а также оценить его при предполагаемом изменении дозы препарата.
Принято считать, что поздняя дискинезия является резистентным состоянием, плохо поддающимся лечению. Это достаточно опасное осложнение терапии, которое в небольшом проценте случаев может привести к инвалидности больного, обезображиванию его внешности.
При обнаружении признаков поздней дискинезии в первую очередь необходимо аккуратно снизить дозу антипсихотика и затем перейти на прием атипичных антипсихотиков.
Отмечена высокая эффективность купирования тардивных дискинезий при переходе с традиционных нейролептиков на клозапин.
Эффективного лечения поздней дискинезии не найдено, однако некоторые психиатры считают, что витамин Е в сравнительно высоких дозах (400 МЕ раза в сутки) способен временно редуцировать ее проявления. Более стойкий эффект подобной терапии возможен у лиц молодого возраста или при относительно недавнем возникновении этого осложнения.
Препараты, используемые для лечения паркинсонизма, обладают центральным антихолинергическим эффектом. Они могут редуцировать экстрапирамидную симптоматику, тормозя действие ацетилхолина на центральном и периферическом уровне. Механизм их действия заключается в снижении холинергического влияния в базальных ганглиях ЦНС и достижении баланса с уменьшенным воздействием на системы дофамина после приема нейролептиков.
В последние годы для терапии как ранних, так и поздних экстрапирамидных расстройств некоторые специалисты рекомендуют использовать амантадины (ПК — Мерц). Амантадины являются антагонистами NMDA рецепторов глутамата и одновременно обладают холинолитической активностью. Они обладают нейропротекторным эффектом, усиливают синтез дофамина в пресинаптических терминалях и увеличивают высвобождение этого медиатора в синаптическую щель, тормозят процесс обратного захвата дофамина, тем самым стимулируя рецепторы дофамина. В случае необходимости активной инфузионной терапии ПК — Мерц применяют внутривенно капельно по 500,0 мл (250,0 мл 2 раза в день) в течение дней в зависимости от тяжести состояния больного. После курса инфузий рекомендуется прием таблетированной формы препарата по 0,1 г 3 раза в день в течение 1 месяца. Для профилактики экстрапирамидных расстройств препарат назначается по 0,5 таб. 3 раза в сутки (150 мг) с последующим увеличением дозы через 1 неделю до 3 таб. 3 раза в день (300 мг) в течение всего курса терапии антипсихотиками. При терапии ранних дистоний и дискинезий ПК — Мерц вводится внутривенно капельно 400 мл (200 мг) 1 раз в сутки (со скоростью 50 кап. в мин.), с последующим переходом на прием таблеток 3 раза в сутки (300 МГ) в течение 1 месяца. При возврате ранней экстрапирамидной симптоматики рекомендуется длительный прием перпарата в дозе 300 мг в сутки. В случае развития паркинсонизма, поздних дискинезий и дистоний ПК — Мерц назначается по 0,5 та. 3 раза в сутки (150 мг) с последующим увеличением дозы через 1 неделю до 1 та. 3 раза в сутки При сохраняющихся, несмотря на терапию амантадином, экстрапирамидных расстройствах возможно увеличение суточной дозы ПК — Мерц до 6 таб. в сутки (600 мг).
Большинство побочных эффектов, особенно тех, которые существовали сравнительно недолго, после прекращения приема психотропных средств, чаще всего исчезают. Как отмечалось выше, хорошо поддаются коррекции лекарственный паркинсонизм, дистония и акинезия, в меньшей степени тремор и плохо — акатизия.
Плановое, профилактическое совместное назначение препаратов, применяемых для лечения паркинсонизма, обычно не рекомендуется из-за возможного отсутствия экстрапирамидной симптоматики при лечении некоторыми антипсихотиками. Развитие неблагоприятных побочных эффектов, возникающих в процессе лечения корректорами, в основном обусловлено холинолитическим действием и проявляется сухостью во рту, расширением зрачков, ухудшением течения глаукомы, нарушением когнитивных процессов, расстройством мочеиспускания, запорами, тошнотой, головокружением, галлюцинациями, эйфорией, гипертермией. Кроме того, возникает потенциальная опасность злоупотребления препаратами центрального антихолинергического действия. При необходимости приема корректоров желательна их отмена не позже чем через три месяца терапии, в связи с возможностью развития устойчивости к действию антипсихотиков. Побочные эффекты, возникающие в процессе терапии корректорами, представлены в таблице 40.
Таблица 40. Побочные эффекты корректоров