Автобус болезнь что за болезнь
Боковой амиотрофический склероз
Боковой амиотрофический склероз
Симптомы
Ранние симптомы БАС включают в себя:
Заболевание часто начинается с рук, ног или конечностей, а затем распространяется на другие части тела. С дебютом заболевания симптоматика начинает прогрессировать, мышцы становятся слабее и затем возникает парализация. В конечном итоге происходит нарушение актов жевания глотания и дыхания.
Причины
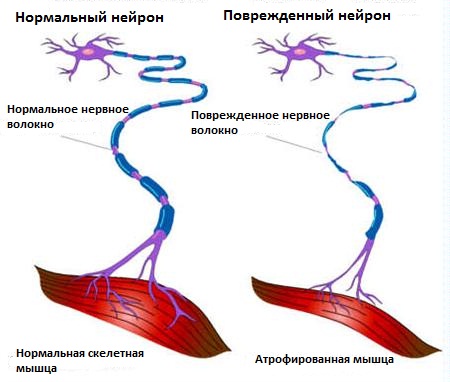
При боковом амиотрофическом склерозе нервные клетки, контролирующие движения (моторные нейроны) начинают постепенно отмирать, что приводит к постепенному ослаблению мышц и их атрофии. БАС передается по наследству в 5-10 процентах случаев. В остальных случаях БАС возникает, судя по всему спонтанно.
В настоящее изучается несколько возможных причин БАС, в том числе:
Факторы риска
Основные факторы риска БАС включают в себя:
Факторы внешней среды, увеличивающие риск этого заболевания включают в себя:
Осложнения

Диагностика
При появлении некоторых из ранних симптомов нервно-мышечных заболеваний необходимо обратиться к лечащему врачу, который при необходимости направит на консультацию к неврологу. Но даже своевременное обращение к неврологу не гарантирует того что диагноз будет выставлен сразу так как требуется некоторое время для верификации диагноза. Невролога будет интересовать история болезни и неврологический статус.
Боковой амиотрофический склероз достаточно сложно диагностировать на ранних стадиях, так как симптоматика схожа с другими неврологическим заболеваниями. Из диагностических методов используются следующие:
Лечение
В связи с тем, что процессы при боковом амиотрофическом склерозе не дается повернуть вспять, то лечение направлено на замедление прогрессирования симптоматики.
Медикаментозное лечение. Препарат рилузол (RILUTEK) является первым и единственным препаратом, одобренным для замедления БАС. Препарат оказывает тормозящее влияние на прогрессирование заболевания у некоторых пациентов возможно за счет снижения уровня глутамата – вещества являющегося медиатором в нервной системе и уровень, которого у пациентов с БАС часто повышен. Кроме того возможно назначение других медикаментов для уменьшения таких симптомов как запор мышечные судороги усталость гиперсаливация боль депрессия.
ЛФК. Физические упражнения под наблюдением врача ЛФК позволяют поддержать мышечную силу и диапазон движений на более длительный период деятельность сердечно-сосудистой системы и улучшить общее самочувствие.
Использование ходунков или инвалидной коляски тоже позволяет сохранять определенный объем движений.
Психологическая помощь. Нередко требуется помощь психолога в связи осознанием пациентом неизлечимости заболевания. Хотя в некоторых случаях продолжительность жизни может превышать 3-5 лет и достигать 10 лет.
Кинетозы или синдромы укачивания: лечение и профилактика
Опубликовано в журнале:
Медицинский cовет №11-12 2011
Холин А.А., д.м.н., профессор,
РНИМУ им. Н.И. Пирогова, Холина Е.И., поликлиника №4 УД Президента РФ, Москва
Наиболее известными разновидностями кинетозов вляются морская, автомобильная, вагонная, воздушная болезни, менее известными – верховой езды, космическая, а также болезнь лифта, качелей, аттракционов. Примерно 30% взрослой популяции и 60% детей подвержены синдромам укачивания. Комплексный подход к проблеме кинетозов, сочетание нелекарственных методов профилактики и дифференцированного медикаментозного лечения способствует нормализации самочувствия.
Ключевые слова: кинетоз, синдром укачивания, вестибулярный аппарат, головная боль, головокружение, тошнота.
Синдромы укачивания или кинетозы — это патологическая реакция организма на непривычное движение. Наиболее известными разновидностями данных состоянийя вляются морская, автомобильная, вагонная, воздушная болезни, менее известными — верховой езды, космическая, а также болезнь лифта, качелей, аттракционов и т.п.
Кодировка заболевания по МКБ-10 — T75.3, по МКБ-9 — 994.6.
Во время качки и при изменении положения тела у человека происходит раздражение вестибулярного органа, зрительного анализатора и рецепторов внутренних органов, а дисбаланс, возникающий между информацией, получаемой от вестибулярного аппарата и органов зрения, приводит к возникновению патологических неприятных ощущений.
Рецепторы вестибулярного аппарата, реагирующие на ускорения, и зрительные рецепторы, передающие в мозг информацию о быстром смещении в пространстве окружающих предметов, играют основную роль в развитии укачивания. Возбуждение симпатического отдела вегетативной нервной системы и двигательных ядер блуждающего нерва (парасимпатическое влияние), обусловленное гиперактивацией периферических рецепторов (вестибулярных и зрительных) приводит к возникновению симптомов укачивания. Центральные аксоны сенсорных нейронов вестибулярного ганглия оканчиваются на нейронах вестибулярных ядер: верхнего (Бехтерева), нижнего (Роллера), латерального (Дейтерса) и медиального (Швальбе), составляющих единый функциональный комплекс, объединяющий афферентную информацию от вестибулярных ганглиев и проприоцепторов. Вестибулярные ядра являются подкорковыми центрами познотонических и статокинетических рефлексов, обусловливающих регуляцию равновесия, глазодвигательных рефлексов и опосредованных через гипоталамус вестибуло-висцеральных реакций, с механизмом которых связаны проявления клинические проявления кинетозов.
Предрасположенность отдельных людей к различных формам кинетозов зависит от индивидуальных особенностей органа равновесия. Функциональная незрелость и легкая возбудимость вестибулярного аппарата, который окончательно созревает лишь к 12—16-ти годам, способствует особой предрасположенности детей к синдромам укачивания. (считается, что от укачивания страдает более 60% детей в возрасте до 12 лет). Точная популяционная частота кинетозов не изучена. Примерно 30% взрослой популяции подвержены синдромам укачивания [1, 8, 10].
Симптомы кинетозов известны с глубокой древности, однако первое подробное научное описание морской болезни, опубликованное в 1881 г журнале «Ланцет», принадлежит J.A.Irwin [6].
В настоящее время в зависимости от доминирующей симптоматики кинетозы условно разделяют на четыре основные формы [1, 8, 10]:
При всех разновидностях кинетозов обычно наблюдаются такие вегетативные симптомы как бледность и повышенное потоотделение.
Диагноз и дифференциальный диагноз [1, 2, 4, 5, 8].
Различные формы кинетозов обычно несложно диагностировать на основании жалоб, анамнеза и клинической картины. Однако симптомы укачивания могут быть проявлением различных неврологического заболеваний и соматической патологии, что требует дополнительных методов обследования. Для дифференциальной диагностики патологии в центральных или периферических вестибулярных отделах используют методики нистагмографии, калорической пробы, вестибулярных вызванных миогенных потенциалов, компьютерной динамической постурографии. С целью исключения объемных образований, пороков развития, а также демиелинизирующих процессов проводят магнитно-резонансную томографию. Ультразвуковая допплерография позволяет оценить церебральный кровоток. Специфические иммунологические реакции используют для исключения инфекционного поражения ЦНС.
Кинетозы следует дифференцировать с:
Медикаментозные средства для лечения синдрома укачивания [1, 7, 8, 9. 10, 11].
Метоклопрамид – специфический блокатор дофаминовых (D2) и серотониновых рецепторов. Назначают внутрь взрослым — по 5—10 мг 3—4 раза в сутки за 30 мин до еды, таблетку проглатывают целиком и запивают небольшим количеством воды. Максимальная разовая доза составляет 20 мг, суточная — 60 мг. Детям старше 6 лет назначают по 5 мг 1—3 раза в сутки.
Антигистаминные средства:
Дименгидринат — блокатор H-1 или H-3 гистаминовых рецепторов внутреннего уха и вестибулярных ядер (драмина, сиель, тагиста, дедалон и др). Драмина (дименгидринат 50 мг) назначают внутрь перед едой взрослым — по 1—2 табл. 2—3 раза в сутки, детям от 1 года до 6 лет — 1/4 – 1/2 табл. 2—3 раза в сутки; от 7 до 12 лет — 1/2-1 табл. 2—3 раза в сутки. Для профилактики кинетозов — по 1—2 табл. за 30 мин до поездки. Максимальная суточная доза для взрослых не должна превышать 7 таблеток.
Блокаторы Н-1 гистаминовых рецепторов (прометазин, дифенгидрамин, меклозин, циклизин). Прометазин (в таблетках и драже по 0,025 и 0,05 г) назначают детям в возрасте от 1 до 2 лет внутрь — по 5—10 мг 1—2 раза/сут; от 2 до 5 лет — по 5—10 мг 1—3 раза/сут; от 5 до 10 лет — по 5—15 мг 1—3 раза/сут; старше 10 лет и подросткам по 5—20 мг 1—3 раза/ сут. Для взрослых суточная доза составляет 75—100 мг.
Бонин (меклозин гидрохлорид 25 мг) — блокатор Н-1 гистаминовых рецепторов, оказывающий М-холиноблокирующее и седативное действие. Назначают внутрь взрослым и детям старше 12 лет по 25—100 мг/сут в 3—4 приема. Для профилактики — однократно, по 25—50 мг за 1 ч до путешествия.
При кинетозах также применяют м-холиноблокаторы (Аэрон, пластыри со скополамином), комбинированные препараты (сочетание гидрохлорида хлорфеноксамина, 8-хлортеофиллина и кофеина — Родаван).
Ноотропные препараты (анвифен, пирацетам, билобин и др.) применяют при кинетозах для улучшения мозгового метаболизма и мозгового кровотока, а также повышения уровня адаптации ЦНС.
Анвифен (аминофенилмасляной кислоты гидрохлорид) выпускается в капсулах по 50 и 250 мг.
Главным преимуществом Анвифена являются его капсулированная форма, более щадящая по отношению к ЖКТ и специальная детская дозировка 50 мг – уникальная на рынке.
Препарат является ноотропным средством, облегчающим ГАМК-опосредованную передачу нервных импульсов в ЦНС (прямое воздействие на ГАМКергические рецепторы), а также обладает транквилизирующим действием в сочетании с активирующим, антиагрегационным, антиоксидантным и умеренным противосудорожным эффектами. Анвифен улучшает мозговой кровоток (увеличивает объемную и линейную скорость, уменьшает сопротивление сосудов, улучшает микроциркуляцию, оказывает антиагрегационное действие) и уменьшает вазовегетативные симптомы кинетозов. При курсовом приеме препарат повышает физическую и умственную работоспособность (внимание, память, скорость и точность сенсорно-моторных реакций). Анвифен также уменьшает проявления астении, улучшает самочувствие, повышает интерес и инициативу без седации или возбуждения, способствует снижению чувства тревоги, напряженности и беспокойства, нормализует сон. Препарат принимают внутрь, после еды, 2—3-х недельными курсами. Дозировки: взрослым и детям с 14 лет по 250—500 мг 3 раза в день (максимальная суточная доза 2500 мг). Однократная максимальная доза у взрослых и детей с 14 лет составляет 750 мг; у лиц старше 60 лет — 500 мг. Детям с 3-х до 8 лет — по 50—100 мг 3 раза в день (1—2 50 мг капсулы х 3 раза в день); от 8 до 14 лет — по 250 мг 3 раза в день. Однократная максимальная доза у детей до 8 лет составляет 150 мг; от 8 до 14 лет — 250 мг. Для профилактики укачивания принимают 250—500 мг препарата однократно за 1 ч до предполагаемого начала качки или при появлении первых симптомов.
Гомеопатические средства сочетают высокую эффективность и отсутствие побочных эффектов, практически не имеют противопоказаний, могут приниматься детьми, беременными женщинами и пожилыми людьми. В зависимости от специфики симптомов и особенностей конституционального типа их применяют как в виде комплексных препаратов, так и в виде монопрепаратов. Гомеопатические препараты следует применять за 15—20 минут до еды или через час после приема пищи.
Коккулин (Cocculus indicus С4, Nux vomica С4, Tabacum С4, Petroleum С4) — впрофилактических целях рассасывают по 2 таблетки 3 раза в день накануне и в день поездки, в лечебных целях — по 2 таблетки каждый час до улучшения состояния.
Вертигохель (Anamirta cocculus D4, Conium maculatum D3, Ambra grisea D6, Petroleum rectificatum D8). Разовая доза препарата составляет: взрослым и детям от 6 лет — по 10 капель, детям до 1 года — по 1—2 капли, 1—3 года – по 3 капли, 3—6 лет — по 5 капель 3—4 раза в сутки. Капли растворяют в 10 мл воды и выпивают, задерживая на несколько секунд во рту, либо не растворяя капают под язык. При приступе головокружения и тошноты принимают разовую возрастную дозу каждые 15 минут до улучшения состояния, но в течение не более 2 часов. Далее препарат принимают 3 раза в сутки. Курс лечения при хроническом состоянии составляет 2—4 недели.
Авиаморе (Veratrum album С200, Cocculus С200, Borax С200) применяют по 1 таблетке или 1 карамели на один приём независимо от возраста и массы тела и держат во рту до полного растворения. Приём начинают за 1 час до посадки в транспортное средство; повторно применяют при необходимости 1 раз в 30 минут, но не более 5 раз в день. Препарат особо эффективен при устранении боязни резкого движения вниз (воздушных ям).
Для лечения кинетозов применяют следующие гомеопатические монопрепараты [3]:
Для купирования тяжелой формы синдрома укачивания в качестве средств неотложной помощи применяют:
Профилактические мероприятия при кинетозах:
Тренировка вестибулярного аппарата.
Лицам, предрасположенным к кинетозам, следует тренировать свой вестибулярный аппарат. Во время летнего отдыха полезно качаться в гамаке и на качелях, постепенно увеличивая амплитуду. Также полезны занятия физкультурой, упражнения с наклонами, поворотами головы, вращениями туловища, кувырки, вращения и стояние в позе «березки». Адаптации к езде с ускорениями способствуют спортивные игры, сочетающие бег и прыжки с меняющимся ускорением (волейбол, баскетбол, большой теннис, футбол), а также велосипедные прогулки и занятия на горных лыжах. При регулярных тренировках вестибулярный аппарат перестает отвечать патологическим возбуждением. Профилактике кинетозов также способствуют занятия бальными танцами и аэробикой.
Синдромы укачивания являются часто встречаются в практике невролога и педиатра. Комплексный подход к проблеме кинетозов, сочетание нелекарственных методов профилактики и дифференцированного медикаментозного лечения способствует нормализации самочувствия, преодолению ограничений при различных видах активности и существенно повышают качество жизни пациентов.
Профессиональные болезни водителей. Особенности профзаболеваний. Особенности профзаболеваний
Профессиональные болезни водителей. Особенности профзаболеваний. Особенности профзаболеваний
Особенности профзаболеваний
Существует такое понятие как профзаболевания — профессиональные заболевания. Это патологии, которые развиваются вследствие многолетнего занятия какой-то деятельностью, включающей в себя негативные для здоровья факторы. При этом:
Водители тоже имеют ряд своих профессиональных «болячек », связанных со спецификой многолетнего времяпрепровождения «за баранкой». Общие деструктивные факторы здесь можно выделить следующие:
Профзаболевания водителей
Эти три фактора влекут за собой целый букет водительских профзаболеваний:
Геморрой. Не самая тяжёлая и опасная «водительская » патология, но зато самая известная. Венозный отток крови в принципе проблематичен. Вены имеют очень тонкую мышечную стенку, поэтому их сократительная способность гораздо ниже по сравнению с артериями. Вены не могут толкнуть кровь обратно к сердцу в достаточной степени. Ситуация осложняется еще и вертикальным положением тела человека (геморрой можно рассматривать как одну из многочисленных плат за прямохождение). Оттоку венозной крови к сердцу мешает гравитация. В венозной стенке много эластина. В результате с возрастом вены неизбежно начинают медленно, но верно растягиваться. Растянутая вена вмещает больший объём крови, который, соответственно, ещё сложнее отправить обратно к сердцу для обогащения кислородом. Развитие мышц нижних конечностей и двигательная активность способствуют улучшению венозного оттока, тогда как гиподинамия ускоряет вышеописанный процесс. Геморрой — это не что иное, как растянутые вены прямой кишки. Длительное сидение приводит к застою крови в тазовой области. Если это многократно повторяется в течение солидного временного интервала, вены прямой кишки растягиваются и в исходное состояние уже вернуться не могут. Последствия: выпадение геморроидальных узлов, тромбоз геморроидального узла, нарушения стула, постоянный дискомфорт, боль, зуд и жжение.
Остеохондроз. Дегенеративное заболевание позвоночника, точнее межпозвоночных хрящевых дисков. Этиология данного заболевания сложная, мультифакторная. Разумеется, немалую роль играет генетический фактор, однако суть всех основных теорий сводится примерно к следующему: хондроциты начинают в меньшей степени синтезировать протеины межклеточного матрикса, а их собственная пролиферация замедляется, при этом усиливаются процессы апоптоза (естественная гибель хондроцитов). Это многолетний процесс, но постепенно хрящевая ткань истончается, теряет свои амортизирующие свойства. Позвонки начинают пережимать истончающиеся межпозвоночные диски. Это приводит к ущемлению нервов, межпозвоночным грыжам, а также к тому, что позвонки начинает сильнее давить друг на друга. А это приводит к постепенному разрушению уже костной ткани. Конечно, данный процесс длится многие годы и десятилетия, а скорость и интенсивность его протекания строго индивидуальны. Но помимо генетического фактора значительную роль играют и экзогенные факторы, условия и образ жизни. Межпозвоночные диски сами по себе имеют очень бедную васкуляризацию, приток крови к ним слабый. Соответственно, и трофика слабая. Большое влияние у фактора двигательной активности. В движениях позвонки периодически расходятся, ослабляя давление на диски. Движение способствует усилению притока крови, образованию новых капилляров. Это тормозит дегенеративные процессы. Такой же мощный, только негативный обратный эффект оказывает хроническая гиподинамия. Водитель длительное время находится в сидячем положении. В таком положении позвонки всё сильнее и сильнее сдавливают хрящевые диски. Это заметно ускоряет их разрушение. К тому же здесь присутствует комплекс негативных факторов, действующих опосредованно — остеохондрозу способствует плохая экология и постоянный стресс.
Шейный миозит. Может возникать как следствие остеохондроза, а может быть самостоятельным заболеванием. Шейный миозит связан с воспалением нервных окончаний, иннервирующих мышцы шеи и грудного отдела спины. Воспаляться нервные окончания могут по причине ущемления, что свойственно остеохондрозу. А также по причине простуживания. Причём, как ни странно, подобное происходит в летний период. В летнюю жару водители ездят с открытым окном. Многочасовое воздействие ветра из окна может привести к воспалению нерва. Причём подобное «остывание » происходит совершенно незаметно для человека. Схожим способом можно застудить горло в летнюю жару, выпив ледяной воды или съев мороженое. Наконец, шейный миозит обусловлен тем, что водитель долгое время находится в одной позе, имеет место длительный тензор шейных мышц. Ответной физиологической реакцией на подобное является последующая миалгия.
Респираторные и кожные заболевания. Выхлопные газы содержат множество канцерогенов, но в первую очередь они вызывают раздражение кожных покровов и воспаление слизистой оболочки дыхательных путей. У водителей часто развивается аллергический дерматит профессионального характера. В некоторых случаях формируется атопическая триада: ринит, бронхиальная астма, дерматит. Фрагменты сажи и другие жесткие частицы выхлопных газов оседают в бронхах и альвеолах. Постепенно они обрастают фиброзными капсулами. И если таких капсул становится слишком много, функциональная легочная активность снижается. У водителей со стажем флюорограмма часто показывает наличие подобных включений в легких.
Артериальная гипертензия. Как и остеохондроз является сложным мультифакторным заболеванием. Повышенное давление напрямую связано с малой двигательной активностью. Ключевую роль здесь отводят тому, что малоподвижный образ жизни приводит к уменьшению силы сердечных сокращений и их учащению (тахикардия ).
Ожирение. Вероятно, здесь даже не нужны какие-то комментарии. По статистике в России каждый второй человек со стажем регулярного вождения больше 5 лет страдает той или иной степенью ожирения.
Важно упомянуть, что практически все профессиональные заболевания хотя бы частично, но связаны между собой. Яркий пример: остеохондроз, артериальная гипертензия и ожирение.
Поэтому водителям рекомендуется не пренебрегать периодическим медицинским осмотрам и следить за своим здоровьем!
Боковой (латеральный) амиотрофический склероз (и синдром БАС)
Боковой (латеральный) амиотрофический склероз (БАС) (также известен как болезнь моторных нейронов, Мотонейронная болезнь, болезнь Шарко, в англоязычных странах — болезнь Лу Герига) — прогрессирующее, неизлечимое дегенеративное заболевание центральной нервной системы, при котором происходит поражение как верхних (моторная кора головного мозга), так и нижних (передние рога спинного мозга и ядра черепно-мозговых нервов) двигательных нейронов, что приводит к параличам и последующей атрофии мышц.
Болезнь известна не так давно. Впервые описана Жан-Мартеном Шарко в 1869г. По статистике выявляется у 2-5 человек на 100 000 населения в год, что говорит о том, что данная патология относительно редко встречается. Всего в мире насчитывается около 70 тысяч больных боковым амиотрофическим склерозом. Обычно заболевание заявляет о себе у людей старше 50 лет.
Совсем недавно было высказано мнение, что случаи бокового амиотрофического склероза чаще регистрируются у высокоинтеллектуальных людей, профессионалов в своем деле, а также у спортсменов-атлетов, которые на протяжении всей жизни отличались крепким здоровьем.
Точная этиология БАС неизвестна.
Сущность болезни заключается в дегенерации двигательных нейронов, т.е. под воздействием ряда причин запускается процесс разрушения нервных клеток, ответственных за сокращения мышц. Этот процесс затрагивает нейроны коры больших полушарий, ядер головного мозга и нейроны передних рогов спинного мозга. Двигательные нейроны погибают, а их функции никто больше не выполняет. Нервные импульсы к мышечным клеткам больше не поступают. И мышцы слабеют, развиваются парезы и параличи, атрофия мышечной ткани.
Если в основе бокового амиотрофического склероза лежит мутация в гене супероксиддисмутазы-1, то процесс выглядит примерно следующим образом. Мутантная супероксиддисмутаза-1 накапливается в митохондриях двигательных нейронов (в энергетических станциях клетки). Это «мешает» нормальному внутриклеточному транспорту белковых образований. Белки соединятся друг с другом, как бы слипаются, и это запускает процесс дегенерации клетки.
Если причиной становится избыток глутамата, то механизм запуска разрушения двигательных нейронов выглядит так: глутамат открывает каналы в мембране нейронов для кальция. Кальций устремляется внутрь клеток. Избыток кальция, в свою очередь, активирует внутриклеточные ферменты. Ферменты как бы «переваривают» структуры нервных клеток, при этом образуется большое количество свободных радикалов. И эти свободные радикалы повреждают нейроны, постепенно приводя к их полному разрушению.
Предполагается, что роль других факторов в развитии БАС также заключается в запуске свободнорадикального окисления.
Классификация БАС, формы:
Общими симптомами, характерными для любой из форм бокового амиотрофического склероза, являются:
Начальные проявления заболевания:
•слабость в дистальных отделах рук, неловкость при выполнении тонких движений пальцами, похудание в кистях и фасцикуляции (мышечные подергивания)
•реже заболевание дебютирует слабостью в проксимальных отделах рук и плечевом поясе, атрофиями в мышцах ног в сочетании с нижним спастическим парапарезом
•возможно также начало заболевания с бульбарных расстройств – дизартрии и дисфагии (25% случаев)
•крампи (болезненные сокращения, спазмы мышц), нередко генерализованные, встречаются практически у всех больных БАС, и нередко являются первым признаком заболевания
Для БАС в большинстве случаев характерна асимметричность симптоматики.
При этой форме заболевания возможно два варианта:
Также может дебютировать двумя способами:
В руках по мере прогрессирования болезни формируется парез с атрофическими изменениями, повышением рефлексов, повышением тонуса и патологическими стопными признаками. Аналогичные изменения возникают и в ногах, но несколько позже.
Это разновидность бокового амиотрофического склероза, когда заболевание протекает с преимущественным поражением центрального мотонейрона. При этом во всех мышцах туловища и конечностей формируются парезы с повышением мышечного тонуса, патологическими симптомами.
Бульбарная и высокая формы БАС являются прогностически неблагоприятными. Больные с таким началом заболевания имеют меньшую продолжительность жизни по сравнению с шейно-грудной и пояснично-крестцовой формами. Какими бы ни были первые проявления заболевания, оно неуклонно прогрессируют.
Парезы в различных конечностях приводят к нарушению способности самостоятельно передвигаться, обслуживать себя. Вовлечение в процесс дыхательной мускулатуры приводит вначале к появлению одышки при физической нагрузке, затем одышка беспокоит уже в покое, появляются эпизоды острой нехватки воздуха. В терминальных стадиях самостоятельное дыхание просто невозможно, больным требуется постоянная искусственная вентиляция легких.
Продолжительность жизни больного БАС составляет по разным данным от 2 до 12 лет, однако более 90% больных умирают в течение 5 лет от момента постановки диагноза. В терминальную стадию болезни больные полностью прикованы к постели, дыхание поддерживается с помощью аппарата искусственной вентиляции легких. Причиной гибели таких больных может стать остановка дыхания, присоединение осложнений в виде пневмонии, тромбоэмболии, инфицирования пролежней с генерализацией инфекции.
Среди параклинических исследований наиболее существенное диагностическое значение имеет электромиография. Выявляется распространенное поражение клеток передних рогов (даже в клинически сохранных мышцах) с фибрилляциями, фасцикуляциями, позитивными волнами, изменениями потенциалов двигательных единиц (увеличивается их амплитуда и длительность) при нормальной скорости проведения возбуждения по волокнам чувствительных нервов. Содержание КФК в плазме может быть незначительно повышено
Боковой амиотрофический склероз нужно заподозрить:
•при развитии слабости и атрофий, а возможно и фасцикуляций (мышечных подергиваний) в мышцах кисти
•при похудания мышц тенара одной из кистей с развитием слабости аддукции (приведения) и оппозиции большого пальца (обычно асимметрично)
•при этом наблюдается затруднение при схватывании большим и указательным пальцами, затруднения при подбирании мелких предметов, при застегивании пуговиц, при письме
•при развитии слабости в проксимальных отделах рук и плечевом поясе, атрофий в мышцах ног в сочетании с нижним спастическим парапарезом
•при развитии у пациента дизартрии (нарушений речи) и дисфагии (нарушений глотания)
•при появлении у пациента крампи (болезненных мышечных сокращений)
Диагностические критерии БАС:
Критерии подтверждения БАС:
Диагноз БАС подьверждается:
Дифференциальный диагноз БАС (синдромы похожие на БАС):
•Спондилогенная шейная миелопатия.
•Опухоли краниовертебральной области и спинного мозга.
•Краниовертебральные аномалии.
•Сирингомиелия.
•Подострая комбинированная дегенерация спинного мозга при недостаточности витамина В12.
•Семейный спастический парапарез Штрюмпеля.
•Прогрессирующие спинальные амиотрофии.
•Постполиомиелитический синдром.
•Интоксикации свинцом, ртутью, марганцем.
•Недостаточность гексозаминидазы типа А у взрослых при ганглиозидозе GM2.
•Диабетическая амиотрофия.
•Мультифокальная моторная невропатия с блоками проведения.
•Болезнь Крейцтфельдта-Якоба.
•Паранеопластический синдром, в частности при лимфогранулематозе и злокачественной лимфоме.
•Синдром БАС при парапротеинемии.
•Аксональная нейропатия при болезни Лайма (Лайм-боррелиозе).
•Синдром Гийена-Барре.
•Миастения.
•Рассеянный склероз
•Эндокринопатии (тиреотоксикоз, гиперпаратиреоз, диабетическая амиотрофия).
•Доброкачественные фасцикуляции, т.е. фасцикуляции, продолжающиеся годами без признаков поражения двигательной системы.
•Нейроинфекции (полиомиелит, бруцеллез, эпидемический энцефалит, клещевой энцефалит, нейросифилис, болезнь Лайма).
•Первичный боковой склероз.
Диагностические исследования при синдроме БАС.
Для уточнения диагноза и проведения дифференциального диагноза при синдроме БАС рекомендутся следующее обследование больного:
Анализ крови (СОЭ, гематологические и биохимические исследования)
Рентгенография органов грудной клетки
Исследование функций щитовидной железы
Определение содержания витамина В12 и фолиевой кислоты в крови
Креатинкиназа в сыворотке
МРТ головного мозга и при необходимости, спинного мозга
Эффективного лечения заболевания не существует. Единственный препарат, ингибитор высвобождения глутамата рилузол (Рилутек), отодвигает летальный исход на 2 – 4 месяца. Его назначают по 50 мг два раза в день.
Основу лечения составляет симптоматическая терапия:
•Физическая активность. Пациент должен по мере своих возможностей поддерживать физическую активность По мере прогрессирования заболевания возникает необходимость в кресле-каталке и других специальных приспособлениях.
•Диета. Дисфагия создаёт опасность попадания пищи в дыхательные пути • Иногда возникает необходимость в питании через зонд или в гастростомии.
•Применение ортопедических приспособлений: шейного воротника, различных шин, устройств для захвата предметов.
•При крампи (болезненным мышечных спазмах): карбамазепин (Финлепсин, Тегретол) и/или витамин Е, а также препараты магния, верапамил (Изоптин).
•При спастичности: баклофен (Баклосан), Сирдалуд, а также клоназепам.
•При слюнотечении атропин, или гиосцин (Бускопан).
•При невозможности приема пищи вследствие нарушения глотания накладывают гастростому или вводят назогастральный зонд. Раннее проведение чрезкожной эндоскопической гастростомии продлевает жизнь пациентов в среднем на 6 месяцев.
•Церебролизин в высоких дозах (10-30 мл в/в капельно 10 дней повторными курсами). Существует ряд небольших исследований, показывающих нейропротективную эффективность церебролизина при БАС.
•Антидепрессанты: Серталин или Паксил или Амитриптилин (часть больных БАС предпочитает именно его как раз из-за побочных действий – он вызывает сухость во рту, соответственно уменьшает гиперсаливацию (слюнотечение), часто мучающую больных БАС).
•При появлении дыхательных нарушений: искусственная вентиляция легких в условиях стационаров, как правило, не проводится, но некоторые больные приобретают портативные приборы ИВЛ и проводят ИВЛ в домашних условиях.
•Ведутся разработки к применению гормона роста, нейротрофических факторов при БАС.
•Последнее время активно ведутся разработки лечения стволовыми клетками. Этот метод обещает быть перспективным, но все же пока находится на стадии научных экспериментов.
•Боковой амиотрофический склероз является фатальным заболеванием. Средняя продолжительность жизни больных БАС 3 – 5 лет, тем не менее, 30% больных живут 5 лет, а около 10 – 20% живут более 10 лет от начала заболевания.
•Неблагоприятные прогностические признаки – пожилой возраст и бульбарные нарушения (после появления последних больные живут не более 1 – 3 лет).