Азелик или скинорен что
Скинорен: при каких кожных болезнях помогает, как применять, где купить
Скинорен – это препарат, положительно зарекомендовавший себя в дерматологии. Его используют как в лечении подростковых угрей, так и для устранения повышенной пигментации кожи, розацеа или себорейного дерматита.
Разновидности препарата Скинорен
Скинорен выпускается только с целью нанесения на проблемную кожу. В аптеке продается гель и крем одноименного названия.
Главный компонент в обоих лекарствах – азелаиновая кислота. Один грамм геля содержит 150 мг кислоты, в одном грамме крема ее чуть больше – 200 мг.
В составе геля 15% также присутствуют: триглецириды, гидроксид натрия, лецитин, пропиленгликоль, эдедат динатрия, полиакриловая и бензойная кислоты, полисорбат и очищенная вода.
Гель представляет собой массу сероватого или слегка желтоватого цвета со слабым лекарственным запахом, непрозрачный. Купить его можно в тюбиках объемом 15, 30 или 50 г, помещенных в коробочку в комплекте с инструкцией.
Крем 20% дополнительно содержит: бензойную кислоту, глицерол, глицерилстеарат макрогола, пропиленгликоль, смесь из цетостеарилового спирта и глицеридов жирных кислот масла кокоса, цетостеарил этилкапронат и очищенную воду.
Крем Скинорен имеет однородную структуру и белый цвет. Продается в тюбиках из алюминия объемом 30 г, помещенных в картонную упаковку вместе с инструкцией.
Как действует Скинорен
Терапевтический эффект от применения Скинорена обусловлен лечебными свойствами азелаиновой кислоты, способной достигать глубоких слоев эпидермиса, но при этом практически не попадать в общую систему кровообращения.
Согласно инструкции по применению Скинорен оказывает воздействие по четырем направлениям:
очищает кожу от угревой сыпи за счет подавления роста бактерий, находящихся на коже и провоцирующих закупорку сальных желез;
снимает воспаление, тем самым препятствует появлению новых угрей;
способствует отшелушиванию омертвевших частичек кожи с ее поверхности;
борется с пигментацией кожи за счет способности блокировать выработку меланина в избыточном количестве.
При регулярном использовании геля или крема проходит угревая сыпь, проявления розацеа или себорейного дерматита, повышенная пигментация кожного покрова.
Заметный эффект можно заметить через 14-28 дней надлежащего применения.
Благодаря более жидкой консистенции и отсутствии маслянистой основы гель быстрее проникает в дерму и дает более быстрый результат в сравнении с кремом. К тому же гель более подходит для лиц с жирной кожей, так как имеет водянистую основу.
В каких случаях поможет Скинорен
Оба вида препарата применяются для устранения угревой сыпи, протекающей в легкой или средней форме тяжести. Мазь или гель эффективны как при обычных прыщах, так и при угрях с гнойным содержимым.
Крем дополнительно назначают при чрезмерной пигментации кожи по типу мелазмы (к примеру, при хлоазме).
Гель дополнительно показан при диагнозе розацеа, даже осложненной узелками и пузырьками на поверхности кожи.
Предостережения в применении средства
Крем и гель противопоказаны при гиперчувствительности к азелаиновой кислоте или вспомогательным веществам из состава лекарственных средств.
не применяют для борьбы с угревой сыпью обе формы препарата до достижения 12 лет;
не назначают для лечения розацеа и гиперпигментации у подростков до 18 лет.
При диагнозе бронхиальная астма препараты назначают с осторожностью.
Производитель средств предупреждает о возможном наступлении побочных эффектов:
чаще всего возможны: неприятное ощущение жжения и зуда, местное покраснение кожи, шелушение верхнего слоя кожи, стянутость и сухость;
реакции гиперчувствительности – отеки глаз и лица, отек Квинке, бронхоспазм;
ухудшение состояния – проявления себореи, обесцвечивание участков кожи, усиление появления угревых высыпаний.
При ухудшении состояния или дискомфорте во время курса лечения необходимо отменить препарат и посетить врача.
Можно ли Скинорен женщинам в положении или кормящим грудью
Применять средство разрешается только по рекомендации врача, так как серьезных исследований о влиянии азелаиновой кислоты на данную категории пациентов не проводилось.
О проникновении кислоты в женское молоко также неизвестно, поэтому перед использованием препаратов врач должен оценить все вероятные негативные последствия для ребенка и возможную пользу для матери.
Запрещается допускать контакт ребенка с кожей, на которую нанесен Скинорен.
Как применять Скинорен
Крем или гель необходимо наносить только на чистую сухую кожу. После использования препарата необходимо вымыть руки с мылом, а область нанесения нельзя закрывать повязкой.
Гель или крем наносят дважды в день – с утра и вечером. Для нанесения на лицо достаточно полоски длиной 2,5 см, состав можно слегка втереть в кожу. Данная схема подходит и для лечения угревой сыпи у подростков 12-18 лет.
Минимальная продолжительность терапии угревых высыпаний – один месяц, допускается более длительное применение.
Использование препарата в лечение мелазмы должно происходить не менее трех месяцев, розацеа – не менее двух месяцев.
При появлении раздражения в процессе лечения необходимо уменьшить количество наносимого препарата или сократить количество применений до одного раза в день.
Если Скинорен назначен для терапии повышенной пигментации, то для предотвращения обострения или рецидива необходимо пользоваться солнцезащитными средствами.
Дополнительная информация
При использовании крема или геля следует остерегаться попадания состава на слизистые оболочки рта, в глаза, на открытые раны. Если это произошло, то место случайного попадания необходимо обильно промыть водой.
Крем Скинорен эффективен только в лечении мелазмы, расположенной в эпидермисе и дерме. На расположенную только в дерме препарат влияния не оказывает.
При лечении розацеа следует воздерживаться от косметики, содержащей спирт, абразивные или отшелушивающие средства.
Как хранить
Лекарственное средство необходимо хранить при температуре до 30°C в течение трех лет с даты выпуска. После вскрытия тюбик с лекарством хранят не более полугода.
Условия продажи, цена
Купить крем Скинорен в Москве можно без рецепта в любой аптеке или через интернет. Цена за тюбик геля объемом 15 г начинается от 750 руб., 50 г – от 1 500 руб. Крем Скинорен стоит от 1 170 руб. за 30 г.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Наружная терапия угревой болезни: работа над ошибками
Е. Н. Волкова, Л. А. Ильин, А. Б. Воробьев, Е. О. Рюмина
Кафедра дерматовенерологии (зав. — проф. Е. Н. Волкова) московского факультета ГОУ ВПО Российский государственный медицинский университет Росздрава; Кожновенерологический диспансер № 9, Москва
Анализируются типичные ошибки в назначении и применении дифферина, описаны его структура и уникальная кинетика, результаты исследования терапевтической эффективности различных лекарственных форм. Приведены факты, свидетельствующие о высокой эффективности и безопасности дифферина в терапии угревой болезни.
Ключевые слова: вульгарные угри, постакне, адапален, дифферин, ошибки применения, эффективность
Typical mistakes in prescription and usage of differin are analyzed. Structure and unique kinetics of this preparation are described and results of effectiveness studies of different drug formulations are presented. Authors present facts illustratinf high effectiveness and safety of differin in acne therapy.
Key words: acne, post-acne, adaplen, differin, therapeutic mistakes, effectiveness
Заболевание, в основе которого лежит патология пилосебоцейного комплекса, правильнее называть угревой болезнью — УБ (точка зрения авторов), так как оно представлено комплексом симптомов, патогенетически объединенных в единый патологический процесс, и психоэмоциональными нарушениями. Термин «вульгарные угри» и «акне» характеризуют лишь один конкретный симптом заболевания [2, 7].
Сегодня накоплен огромный опыт терапии УБ, разработаны алгоритмы лечения в зависимости от степени тяжести с учетом терапевтического индекса акне как основы дифференцированного подхода к ведению больных. Современные схемы включают назначение системных препаратов и средств наружной терапии на фоне правильно подобранного базового ухода [1, 2, 8].
На сегодняшний день наиболее эффективным противоугревыми средствами для местного применения являются ретиноиды, которые способны вызывать специфический биологический ответ в результате связывания и активации рецепторов ретиноевой кислоты. К ретиноидам 3-го поколения для местной терапии акне относят адапален, представляющий собой производное нафтойной кислоты с ретиноидподобным действием.
В России адапален зарегистрирован под названием Дифферин® («Galderma», Швейцария), который выпускается в виде 0,1% геля на водной основе и 0,1% крема [3, 4, 5, 9, 11].
Несмотря на продолжительное использование дифферина для местного лечения УБ, обширного опыта его клинического применения отмечаются отдельные ошибки при его использовании. Часть из них связана с недостаточной информированностью врача и неправильной трактовкой имеющейся информации. Существует и «страх врача» при назначении местных ретиноидов.
Проведем работу над ошибками.
Ошибка 1: неправильный выбор лекарственной формы.
Адапален имеет 2 лекарственные формы для наружного применения — гель и крем. При выборе лекарственной формы следует помнить, что эффективность действия препарата определяется взаимосвязями в системе «препарат—основа—кожа». Именно правильное увлажнение рогового слоя значительно усиливает проникновение веществ.
Обычно лечение начинают с геля. Если у пациента чувствительная и сухая кожа, то рекомендован дифферин-крем. Он содержит увлажняющие некомедогенные компоненты.
Необходимо соблюдать режим дозирования. Гель и крем бережно, без особого усилия, наносят на пораженные участки кожи 1 раз в день на ночь на чистую сухую кожу.
Ошибка 2: необоснованные «завышенные» ожидания быстрого результата.
Дифферин — препарат патогенетического действия, поэтому назначение препарата сегодня не приведет к проявлению результата завтра! Это необходимо учитывать врачу и объяснять пациенту (проводить его «обучение»). Отсутствие быстрого визуального эффекта может приводить к отказу пациентов от лечения! А между тем препарат является высокоэффективным средством в лечении УБ. Его терапевтическая эффективность связана с тем, что молекула адапалена селективно связывается с ретиноидчувствительными рецепторами (RAR) у-типа сально-волосяных фолликулов (СВФ), что приводит к уменьшению сцепленности кератиноцитов и ускоряет их десквамацию (т. е. реализуется комедонолитическое действие препарата) [9, 11]. Отсутствие взаимодействия с рецепторами RAR-a СВФ, стимуляция которых ведет к появлению шелушения и резкой сухости кожи, позволяет свести к минимуму побочные реакции, которые наблюдались ранее при использовании ретиноидов 1-го поколения. Антипролиферативная активность дифферина по отношению к себоцитам связана со стимуляцией RXR-a. В результате уменьшаются размеры сальной железы и сокращается продукция кожного сала. Третьим звеном патогенеза, на которое воздействует препарат, является воспаление. Адапален ингибирует API — участок в промоторной зоне гена, что приводит к подавлению образования цитокинов — интерлейкинов (ИЛ)-1а, ИЛ-1р, и ИЛ-8; фактора некроза опухоли (ФНО-a), системы комплемента. Инактивация фермента циклооксигеназы ведет к уменьшению образования ЛТВ4 — главного посредника во взаимодействии нейтрофилов, лимфоцитов, моноцитов и эозинофилов в воспалительной реакции. Кроме того, адапален блокирует Toll-рецептор 2-го типа (TLR-2), рецепторы моноцитов, предотвращая связывание с ними микроорганизмов и последующий выброс противовоспалительных цитокинов. Таким образом, дифферин оказывает действие на все звенья патогенеза УБ [3, 8, 9, 11].
Ошибка 3: неправильное формирование группы больных.
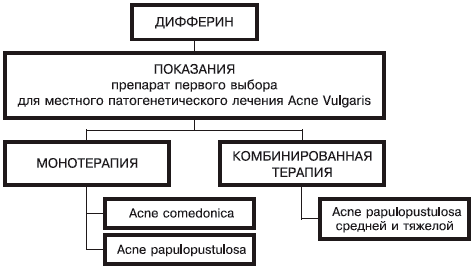
Дифферин — не панацея для лечения всех видов акне — это тоже ошибка: для его назначения существуют определенные показания (рис. 1).
Рис. 1. Показания для применения дифферина.
Ошибка 4: неправильное определение продолжительности лечения дифферином.
В среднем курс лечения составляет до 12 нед, для этого требуется не менее 30 г препарата в форме геля или крема (при нанесении препарата только на область лица). Терапевтический эффект развивается после 4—8 нед лечения, стойкое улучшение — после 3-месячного курса. Такая длительная терапия не только наиболее рациональна и эффективна, но и предотвращает формирование постакне.
Ошибка 5: неинформированность об особенностях дифферина.
Следует знать о двух нюансах.
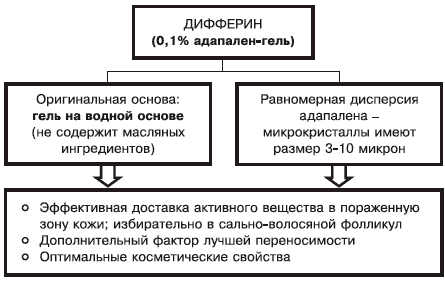
Нюанс 1: состав основы, ее физикохимические характеристики определяют как свойства препарата, так и его способность к проникновению в кожу (рис. 2).
Рис. 2. Фармакодинамическая характеристика дифферина (0,1% адапелена-геля).
Нюанс 2: размер микрокристаллов действующего вещества.
Микрокристаллы адапалена в препарате имеют диаметр от 3 до 10 мк. Оказывается, если диаметр микрокристаллов действующего вещества составляет менее 3 мк — препарат беспорядочно распределяется между сально-волосяным фолликулом и роговым слоем кожи; при диаметре более 10 мк — препарат остается на поверхности кожи.
Правильный размер частиц активного вещества в дифферине — залог эффективного лечения [9, 11]. Вопрос — так ли это в джинерике? (результатов таких исследований не предоставлено).
Ошибка 6: не учитывается возможность комбинирования препаратов.
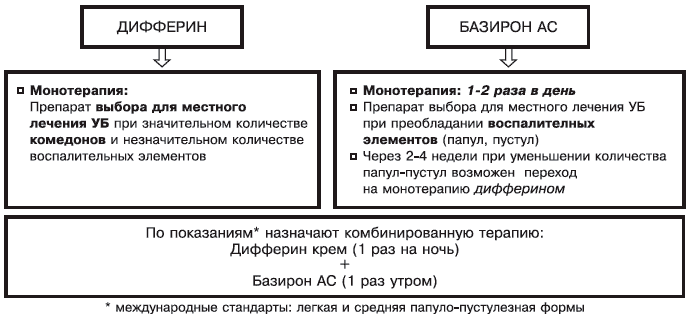
Дифферин сохраняет лечебное действие в комбинации с местными антибактериальными противоугревыми средствами (эритромицин, клиндамицин, бензоила пероксид) [3, 6, 10, 12]. Это расширяет возможности его применения даже при обилии пустулезных элементов. Наиболее целесообразно назначать дифферин в комбинации с базироном АС (рис. 3).
Рис. 3. Применение Дифферина в комбинации с Базироном АС.
Ошибка 7: недооценка показаний к применению дифферина.
Дифферин — местное средство не только для базового патогенетического лечения больных акне. Он показан как препарат поддерживающей терапии, а также при переводе пациента с системной терапии, например акнекутаном, на местную. Такая тактика — не только залог эффективного лечения, но и стойкой длительной ремиссии и профилактики постакне.
Таким образом, правильное применение дифферина позволяет избежать ошибок, преодолеть страх перед назначением ретиноидов. Повысить эффективность лечения больных УБ. Вся история применения дифферина свидетельствует о том, что он является высокоэффективным базовым препаратом для лечения акне легкой и средне-тяжелой степени — показания к его применению строго определены.
Для достижения выраженного и стойкого эффекта необходимо длительное назначение дифферина, что предотвращает появление и развитие новых элементов. При наличии папуло-пустулезных элементов целесообразно применение дифферина в комбинации с препаратом антибактериального действия — базироном АС.
Эффективность и переносимость терапии дифферином были оценены нами при наблюдении 62 пациенток в возрасте от 16 до 22 лет с длительностью заболевания от 1 года до 6 лет. У 26 (42%) пациенток высыпания локализовались только на лице, у 23 (37,1%) — на лице и груди, у 13 (20,9%) — на спине.
В зависимости от степени тяжести УБ пациентки были распределены на 2 группы. 1-ю группу (n = 29) составили больные легкой степенью акне, у которых доминировали комедоны и единичные папулы; 2-ю (n = 33) — больные папуло-пустулезной формой заболевания.
Больным 1-й группы проводили только наружное лечение дифферином в виде геля или крема (в зависимости от состояния кожи) в сочетании с правильным уходом. Препарат наносили тонким слоем 1 раз в день вечером на предварительно очищенную кожу лосьоном сетафил.
Больным 2-й группы дифферин назначали в комбинации с базироном АС в виде геля, который наносили на предварительно очищенную кожу однократно утром. Контроль количества открытых и закрытых комедонов, папул и пустул производили до начала терапии, а также каждый месяц.
Наиболее быстро регрессировали воспалительные элементы: через 3—5 нед число пустул и папул уменьшилось на 25—30%. Наблюдали значительное уменьшение жирности кожи: она становилась более матовой и ровной, исчезал сероватый оттенок. Через 6—8 нед у больных отсутствовали явления себореи и раздражения кожи; новые элементы не появлялись. В 1-й группе регресс высыпаний происходил медленнее. Количество комедонов уменьшилось, начиная с 8-й недели терапии, причем регресс элементов на спине был менее значительным. К 10—12-й неделе их число уменьшилось вдвое, новые элементы не появлялись. Заметно уменьшалась сальность кожи, улучшалась ее текстура за счет сглаживания неровностей, уменьшения толщины. Кожа приобретала естественный цвет, становилась гладкой. Улучшение кожного процесса сопровождалось значительным улучшением настроения пациенток, уменьшением тревожности.
Окончательный эффект от терапии наблюдали к концу 4—5-го месяца, когда комедоны и папулопустулезные высыпания регрессировали более чем на 70—75%. Выявлено, что нанесение базирона АС на поствоспалительные гиперпигментированные пятна и рубцы приводило к их побледнению. В результате лечения клиническая ремиссия наступила у 22 (35,5%) больных, значительное улучшение (регресс высыпаний на 70—80%) — у 26 (42%), улучшение (регресс высыпаний на 50—60%) — у 13 (21%) и неэффективным лечение оказалось у 1 больной.
Таким образом, дифферин является высокоэффективным базовым препаратом первого выбора для патогенетической терапии акне.
Для достижения выраженного и стойкого терапевтического эффекта необходимо длительное назначение дифферина. Препарат сохраняет лечебное действие в комбинации с местными антибактериальными средствами (базирон АС), что определяет целесообразность применения дифферина при наличии папуло-пустулезных элементов. Оригинальная основа (гель на водной основе), равномерная дисперсия микрокристаллов адапалена определяют эффективную доставку активного вещества в пораженную кожу (избирательно в сальноволосяной фолликул), лучшую переносимость препарата и оптимальные косметические свойства.
Рациональная терапия дифферином — залог успешной терапии угревой болезни и профилактики постакне.
1. Волкова Е. Н. // Лечащий врач. — 2007. — № 4. — С. 21— 28.
2. Волкова Е. Н., Осипова Н. К. // Рос. журн. кож. и вен. бол. — 2009. — № 5. — С. 53—58.
3. Волкова Е. Н, Осипова Н. К // Клин. дерматол. и венерол. — 2010. — № 2. — С. 72—77.
4. Гущина Н. С., Корчевая Т. А. // Рус. мед. журн. — 2005. — Т. 13, № 7. — С. 482—485.
5. Орлова Н. А // Клин. дерматол. и венерол. — 2003. — № 4. — С. 53—56.
6. Самгин М. А., Монахов С. А. // Вест. дерматол. и венерол. — 2003. — № 4. — С. 37—39.
7. Самгин М. А., Монахов С. А. // Рос. журн. кож. и вен. болезней. — 2005. — № 3. — С. 55—64.
8. Самгин М. А., Монахов С. А. // Рос. журн. кож. и вен. болезней. — 2006. — № 6. — С. 85—87.
9. Data on file. Galderma Laboratories, Ins. Medical Departament. — 1994.
10. Eady E. A., Farmery M. R, Ross J. I. et al. // Br. J. Dermatol. — 1994. — Vol. 131. — P. 331—336.
11. Michel S., Jomard A., Demarschez. // Br. J. Dermatol. — 1998. — Vol. 139 (suppl. 52). — P. 3—7.
12. Swinyer L. J., Baker M. D, Swinyer T. A., Mills O. H. Jr. // Br. J. Dermatol. — 1988. — Vol. 119, N 5. — P. 615—622.
Азелик или скинорен что
Акне и розацеа — наиболее распространенные заболевания в практике дерматолога и косметолога. Диагностика и выбор алгоритма терапии представляют определенные трудности. Высокая распространенность, хроническое рецидивирующее течение, выраженные психоэмоциональные расстройства, снижение качества жизни пациентов с акне и розацеа объясняют важность задачи дальнейшего совершенствования терапии.
Розацеа
Механизмы, вызывающие патологический процесс при розацеа и акне, изучены не конца. Розацеа является хроническим заболеванием кожи с участками покраснения (преимущественно в лицевой области), образованием гнойничковых и других высыпаний. При исследовании RISE, проведенном в России и Германии и включившем соответственно 3013 и 3052 лиц в возрасте 18—65 лет, выявлено 5% больных с розацеа в России и 12% — в Германии [1]. Среди больных розацеа в обеих странах женщины составляли 75% (средний возраст 40 лет), для больных была характерна светлая кожа (фототипы II и III по шкале Фитцпатрика) [2]. Распространенность розацеа коррелирует с фототипом кожи и общей солнечной активностью в регионе проживания, что демонстрирует ключевую роль инсоляции в провоцировании заболевания [3].
Розацеа классифицируют четырьмя подтипами и одним вариантом заболевания:
— эритемато-телеангиэктатическая (подтип 1);
— папуло-пустулезная (подип 2);
— фиматозная (подтип 3);
— офтальмическая розацеа (подтип 4).
Выделяют вариант гранулематозной розацеа, которую чаще регистрируют у людей с IV и V фототипом кожи. В исследовании RISE основным подтипом был эритемато-телеангиэктатический (подтип 1), что подтверждается результатами и других исследований [4, 5].
Розацеа характеризуется формированием эритемы, эдемы, ощущения жгучей боли. Гистологически обнаруживают расширенные кровеносные сосуды без признаков неоангиогенеза. При всех формах заболевания наблюдается накопление тучных клеток и фибробластов в зоне поражения, что свидетельствует о синтезе хемокинов и ростовых факторов, вызывающих миграцию этих клеток в дерму. При эритематозной форме (наиболее распространенной) повышено число сенсорных нейронов, непосредственно вовлеченных в патогенез заболевания. Поскольку при розацеа наблюдается расширение сосудов, приводящее к локальному обогащению питательными веществами тканей, это может быть причиной присоединения вторичной инфекции. У части больных в очагах воспаления выявляют клещей рода демодекс. Роль клещей в патогенезе розацеа остается дискуссионной. Показано, что розацеа ассоциирована с патологией пищеварительного тракта, дисфункцией эндокринной системы, изменениями в сально-волосяном аппарате и соединительной ткани дермы, иммунными нарушениями, психовегетативными расстройствами, повышением количества микроорганизмов на кожном покрове [6—9]. Причиной соматических заболеваний может быть повышенная реактивность сосудов не только кожи, но и других органов.
Акне является заболеванием кожи, характеризующимся гиперплазией сальных желез, гиперкератозом и образованием комедонов — сально-роговых пробок в протоках сальных желез с частичной или полной их закупоркой. Заболевание чаще всего начинается в пубертатном периоде при адренархе и характеризуется повышенной продукцией сала, что приводит к снижению локального иммунитета в сальных железах и присоединению вторичной инфекции, наиболее часто вызванной Propionibacterium acnes — анаэробной грамположительной бактерией. Бактерия P. acnes использует жирные кислоты кожного сала, в том числе пропионовую, стимулирующую размножение микроорганизма. При избыточной продукции меняется состав кожного сала, снижается уровень линолевых кислот, увеличивается уровень сквалена и перекисных липидов, повышается уровень насыщенных жиров [3, 10, 11]. Комедоны развиваются в местах, богатых сальными железами: на лице (99%), спине (60%) и груди (15%) [12].
В отличие от розацеа акне является распространенным кожным заболеванием, составляя 20—30% всех случаев дерматологических заболеваний [12]. Прогрессирующее течение акне, толерантность к проводимой терапии, косметические недостатки снижают качество жизни пациентов, вызывают значительный дискомфорт и психоэмоциональные расстройства преимущественно депрессивного характера [13, 14].
Патогенез акне связан с увеличенной продукцией кожного сала и дисбалансом липидов секрета сальных желез. Колонизация P. acnes является следствием снижения местного иммунитета и дополнительным стимулом его активации. В норме P. acnes составляют до 50% микроорганизмов, колонизирующих кожу с большим количеством сальных желез и только 5—10% в остальных участках тела [15]. Воспалительный процесс в области сально-волосяного фолликула приводит к развитию фолликулярного гиперкератоза и обтурации протоков сальных желез (микрокомедон, комедон).
Общие характеристики розацеа и акне
Анализ полиморфизма генов показывает наличие генетической предрасположенности к обоим заболеваниям, по крайней мере, у половины больных [16—25]. Однако распространенность акне свидетельствует о том, что патогенез заболевания ассоциирован с полиморфностью многих генов [3].
Общим для обоих заболеваний является преимущественная локализация процесса на коже лица. В эффекторной фазе розацеа и акне принимает активное участие врожденный иммунитет. Роговой слой кожи представляет основную преграду для патогенов. Большое значение имеет поддержание определенной кислотности кожи, так называемой «кислотной мантии Маркионини», состоящей из компонентов потового и сального секретов, в состав которой входят молочная кислота, свободные жирные кислоты, уроканиновая кислота и другие компоненты, обеспечивающие коже кислый рН (5,3—5,6). Показано, что при акне рН кожи повышается, что поддерживает пролиферацию в кожном сале основных комменсалов — бактерии P. acnes и, как результат, способствует активации механизмов врожденного иммунитета, в частности синтеза клетками, выстилающими потовые и сальные железы, антимикробных пептидов (АМП) [26].
АМП — это низкомолекулярные соединения, состоящие из аминокислот (пептиды) и обладающие антимикробной активностью против широкого спектра микроорганизмов: грамотрицательных и грамположительных бактерий, вирусов, простейших и грибов [27]. АМП относятся к первой линии защиты и присутствуют конституционально; их уровень увеличивается при воспалении или травме. К АМП относят α-, β-и θ-дефензины, кателицидины, S100-белки, РНКазы.
В патогенезе розацеа показана роль антимикробных пептидов, синтез которых осуществляется нейтрофилами, тучными клетками, макрофагами, находящимися в периваскулярном пространстве [28—32]. Активация тучных клеток является результатом расширения сосудов и связана с противомикробной и репаративной функциями этих клеток. Особую роль в патогенезе розацеа играет кателицидин, из которого в результате протеолитического гидролиза в клетках образуется пептид LL-37, играющего одну из главных ролей в патогенезе розацеа [32].
Врожденная иммунная система также принимает участие в развитии акне. Изменение количества и состава кожного сала активирует иммунную систему задолго до появления комедонов [33]. Основными АМП, вовлеченными в патогенез акне, являются β-дефензины 1 и 2 [34—36]. Также, как и при розацеа, в патогенез акне вовлечены нервные окончания сосудов кожи; доказана роль повышенной продукции нейропептида кортикотропин-рилизинг-гормона и повышения экспрессии рецептора меланокортина 1 [37—39]. При акне показана также активация toll-подобных рецепторов на клетках врожденной системы [40].
Таким образом, при акне и розацеа по разным причинам нарушается нормальный гомеостаз кожного покрова лица, что обусловливает активацию врожденного иммунитета, нарушение кислотности кожи, присоединение специфической инфекции, дополнительно стимулирующей врожденный иммунитет.
Азелаиновая кислота в терапии акне и розацеа
Одним из широко применяемых топических средств в дерматологии и косметологии является азелаиновая кислота (АК). АК — конечный продукт окисления линолевой кислоты, который образуется естественным путем в нормальной коже. После нанесения на кожу препараты АК легко проникают в эпидермис и дерму. В системный кровоток попадает до 4% от общей дозы. АК восстанавливает кислотность кожи, что само по себе оказывает лечебное действие. Так, терапевтическим эффектом обладают и другие кислоты, например ретиноевая, ацетилсалициловая, фруктовые [41, 42]. Кроме влияния на рН кожи, АК, в частности, подавляет синтез реактивных форм кислорода нейтрофилами, усиливает экспрессию гена p53 в себоцитах, что ведет к их гибели; оказывает местное антиандрогенное действие за счет снижения активности 5a-редуктазы I типа и, соответственно, уменьшает концентрацию дигидротестостерона в себоцитах, тем самым нормализуя процессы кератинизации и салоотделения [43, 44]. Показано, что АК оказывает антиоксидантное действие, снижает продукцию супероксидных и гидроксильных радикалов и уменьшает воспаление [45]. При длительном использовании АК наблюдается нормализация процесса дифференцировки клеток эпидермиса, снижается поствоспалительная гиперпигментация [46].
По данным клинических исследований [47] АК эффективна как в виде монотерапии, так и в сочетании с антибиотиками. АК в виде монотерапии может быть рекомендована для лечения комедонального акне, папулопустулезного акне легкой и средней степеней тяжести, для поддерживающей терапии [48, 49]. При тяжелом папулопустулезном и конглобатном акне рекомендована комбинация АК с системными антибиотиками. Монотерапия А.К., бензоил пероксидом (БПО) и местными ретиноидами оказывает сопоставимый эффект [48]. Так, в работе H. Gollnick и соавт. [48] приведены данные двух клинических исследований, включивших 351 и 229 больных акне, по сравнительной эффективности 15% геля АК с 5% гелем БПО и 1% гелем клиндамицина. Авторы показали, что применение препаратов в течение 4 нед обеспечивало равную во всех группах 70% эффективность по снижению числа воспалительных элементов. Побочные эффекты в виде локального жжения и раздражения больше были выражены в группе пациентов, применявших БПО, чем в группе лиц, использовавших АК [48]. Минимальные побочные эффекты наблюдались в группе больных, пролеченных гелем клиндамицина. В исследовании G. Stinco и соавт. [49] изучали себостатическое действие АК, адапалена и БПО при лечении 65 больных акне средней тяжести. С помощью себуметрии оценивали уровень секреции кожного сала в области лица. Все используемые препараты оказывали сравнимый терапевтический эффект, однако только АК и БПО обеспечивали снижение продукции кожного сала. По отзывам больных, АК переносится лучше, чем местные ретиноиды или БПО. В косметологии АК активно используют в виде пилинга для проблемной, пористой кожи и для лечения поствоспалительной гиперпигментации. В российских рекомендациях по ведению больных акне АК (25% крем или 15% гель) указан как препарат первой линии для монотерапии комедональных и воспалительных акне. Для лечения акне у женщин в качестве базисной терапии рекомендованы ретиноиды в комбинации с АК.
Для наружного лечения розацеа 2-го типа (папуло-пустулезной) Российское общество дерматовенерологов и косметологов, а также Американское общество по акне и розацеа рекомендуют метронидазол, АК, клиндамицин и другие препараты [50, 51]. Данные ряда клинических исследований показали эффективность монотерапии розацеа 15% гелем АК [52—55]. В ходе метаанализа 2016 г., включившего 57 рандомизированных клинических исследований с общим числом участников 13 630 (больные розацеа 1-го и 2-го подтипов), сравнили эффективность топических препаратов метронидазола, АК, ивермектина, бримонидина и других, а также системных антибиотиков или их сочетаний с топическими ретиноидами. Лучшие результаты были показаны при использовании топического метронидазола и АК [56, 57]. При длительной терапии для поддержания контроля папулопустулезной розацеа в качестве поддерживающей терапии рекомендовано применение АК до 6 мес [58].
Микронизация
АК слаборастворима в водных растворах, соответственно эффективная концентрация пропорциональна растворенной доле А.К. Для увеличения эффективности плохо растворимых веществ используют микронизацию и нанонизацию препаратов. Нанонизированные и микронизированные формы лекарственных средств позволяют повысить биодоступность, растворимость и стабильность препаратов, лучшее проникновение коллоидов через барьеры тканей и клеточные мембраны. С точки зрения биофармацевтики наноразмер является идеальным, однако с точки зрения производства лекарств получение наночастиц проблематично, что связано с имеющимися методами их получения. По этим причинам микронизация труднорастворимых препаратов является наиболее подходящим решением. Микронизация может включать измельчение активного вещества различными методами с последующим введением в различные носители (гидрогели, кремы, пенки).
Российские врачи в арсенале сегодня имеют несколько препаратов, содержащих АК, один из них микронизированный препарат — 15% гель Азелик (АО «Акрихин»). Для повышения эффективности действия высоких концентраций АК требуется повышение растворимости кислоты в основе в виде геля. Гель Азелик 15% (АО «Акрихин», Россия) является единственным отечественным микронизированным препаратом, размер частиц АК составляет менее 100 мкм [59]. Микронизированная форма обеспечивает легкое проникновение препарата через роговой слой кожи, что способствует реализации антибактериального, кератолитического и депигментирующего эффектов АК [59]. Это позволяет считать гель Азелик препаратом выбора для лечения акне, а также препаратом первой линии в терапии папулопустулезной розацеа.
Авторы заявляют об отсутствии конфликта интересов.