Азотная кислота чем опасна
Меры предосторожности при работе с азотной кислотой
Сфера применения азотной кислоты весьма разнообразна. В промышленных масштабах это вещество применяется:
Кроме того, азотная кислота входит в состав ракетного топлива и используется в качестве реагента в химической промышленности. Не стоит забывать, что азотная кислота – остаточно опасное для здоровья (а в некоторых случаях, и для жизни) человека. Данная кислота имеет 3 класс опасности, а ее пары весьма токсичны для организма человека.
Вредное воздействие азотной кислоты на организм человека
Азотная кислота может попасть в организм человека несколькими путями:
Именно от того, при каких условиях и каким образом кислота «проникла» в организм человека, зачастую зависит степень поражения внутренних органов и их систем. Если пары азотной кислоты проникли в дыхательные пути при ингаляционном методе поражения, то степень токсического воздействия во многом будет определяться концентрацией азотной кислоты и временем воздействия на организм.
Кроме прочего, токсический эффект во многом зависит от общего состояния человека, который подвергся вредному воздействия азотной кислоты, его возраста и пола. Также немаловажное значение имеют индивидуальная чувствительность человека к азотной кислоте и некоторые особенности взаимодействия организма с этим веществом.
Интересным фактом является то, что ученые доказали, что если человек постоянно имеет контакт с азотной кислотой, то она оказывает значительно менее разрушительное воздействие на его организм, чем в тех случаях, когда такое воздействие происходит редко. Проведя исследования на лабораторных животных, ученые установили, что при некотором незначительном, но постоянном воздействии на организм подопытных азотной кислоты, в их организме образуется своеобразный барьер, который при следующих контактах не позволяет парам проникать в альвеолы и легочные капилляры.
Симптомы отравления азотной кислотой
Среди наиболее распространенных симптомов отравления азотной кислотой можно выделить следующие:
Впоследствии развивается болевой шок и другие необратимые изменения. У отравившегося отказывают все органы и системы. Такое состояние часто приводит к смерти пациента. Чтобы избежать подобных ситуаций, необходимо неукоснительно соблюдать меры безопасности при работе с азотной кислотой: использовать защитные перчатки, фартуки, респираторы, защитные очки и другие средства защиты.
При правильном применении и соблюдении мер предосторожности азотная кислота может использоваться во всех сферах жизни человека, купить азотную кислоту вы можете в нашей компании.
чем опасна азотная кислота для человека
Сфера применения азотной кислоты весьма разнообразна. В промышленных масштабах это вещество применяется:
Кроме того, азотная кислота входит в состав ракетного топлива и используется в качестве реагента в химической промышленности. Не стоит забывать, что азотная кислота – остаточно опасное для здоровья (а в некоторых случаях, и для жизни) человека. Данная кислота имеет 3 класс опасности, а ее пары весьма токсичны для организма человека.
Азотная кислота может попасть в организм человека несколькими путями:
Именно от того, при каких условиях и каким образом кислота «проникла» в организм человека, зачастую зависит степень поражения внутренних органов и их систем. Если пары азотной кислоты проникли в дыхательные пути при ингаляционном методе поражения, то степень токсического воздействия во многом будет определяться концентрацией азотной кислоты и временем воздействия на организм.
Кроме прочего, токсический эффект во многом зависит от общего состояния человека, который подвергся вредному воздействия азотной кислоты, его возраста и пола. Также немаловажное значение имеют индивидуальная чувствительность человека к азотной кислоте и некоторые особенности взаимодействия организма с этим веществом.
Интересным фактом является то, что ученые доказали, что если человек постоянно имеет контакт с азотной кислотой, то она оказывает значительно менее разрушительное воздействие на его организм, чем в тех случаях, когда такое воздействие происходит редко. Проведя исследования на лабораторных животных, ученые установили, что при некотором незначительном, но постоянном воздействии на организм подопытных азотной кислоты, в их организме образуется своеобразный барьер, который при следующих контактах не позволяет парам проникать в альвеолы и легочные капилляры.
Среди наиболее распространенных симптомов отравления азотной кислотой можно выделить следующие:
Чтобы предотвратить ожог, следует работать с концентрированной азотной кислотой в резиновых перчатках. В то же время обращение с азотной кислотой менее опасно, чем, например, с серной, она быстро испаряется и не остаётся в неожиданных местах. Брызги азотной кислоты следует смывать большим количеством воды, а ещё лучше смачивать раствором соды.
Дымящая азотная кислота при хранении под действием теплоты и на свету частично разлагается, чем выше температура и чем концентрированнее кислота, тем быстрее идёт разложение. В связи с этим хранят её в прохладном и тёмном месте. Выделяющийся диоксид азота растворяется в кислоте и придаёт ей бурую окраску. Разбавленную кислоту легко приготовить, выливая концентрированную кислоту в воду.
Разбавленную азотную кислоту хранят и перевозят в таре из хромистой стали, концентрированную – в алюминиевой таре, т.к. концентрированная кислота пассивирует алюминий, железо и хром из-за образования нерастворимых плёнок оксидов: небольшие количества хранят в стеклянных бутылках. Азотная кислота сильно разъедает резину. Поэтому бутылки должны быть с притёртыми или полиэтиленовыми пробками.
Налив производится в железнодорожные цистерны и автоцистерны из нержавеющей стали, стеклянные бутыли в деревянной или полиэтиленовой обрешетке, специальные бочки из нержавеющей стали, канистры из полимерного материала.
Осуществляется железнодорожным транспортом в цистернах, крытых вагонах, а также автомобильным транспортом в соответствии с правилами перевозки грузов, действующими на транспорте данного вида.
Азотная кислота
Азотная кислота – важный, но опасный химический реактив
Современная химия насчитывает огромное количество химических реактивов: щелочи, кислоты, реагенты, соли и другие. Среди них кислоты – самая распространенная группа. Кислоты – это сложные водородосодержащие соединения, атомы которых могут замещаться атомами металла. Сфера их применения обширна. Она охватывает многие отрасли производства: химическую, машиностроительную, нефтеперерабатывающую, пищевую, а также медицину, фармакологию, косметологию; широко используется в быту.
Азотная кислота и ее определение

Форма выпуска азотной кислоты зависит от ее концентрации:
— обычная – 65 %, 68 %;
— дымная – 86 % и более. Цвет «дыма» может быть белым, если концентрация составляет от 86 % до 95 %, или красным – свыше 95 %.
В настоящее время производство сильно- или слабоконцентрированной азотной кислоты проходит следующие этапы:
1. процесс каталитического окисления синтетического аммиака;
2. как результат – получение смеси нитрозных газов;
3. впитывания воды;
4. процесс концентрирования азотной кислоты.
Хранение и транспортировка
— каждая тара помечается надписью «Опасно».
Где применяется химический реактив?
Сфера применения азотной кислоты в настоящее время огромна. Она охватывает многие отрасли промышленности, такие как:
— химическую (изготовление взрывчатых веществ, органических красителей, пластмасс, натрия, калия, пластмасс, некоторых видов кислот, искусственного волокна);
— сельскохозяйственную (производство азотных минеральных удобрений или селитры);
— металлургическую (растворение и травление металлов);
— фармакологическую (входит в состав препаратов по удалению кожных образований);
— ювелирное производство (определение чистоты драгоценных металлов и сплавов);
— военную (входит в состав взрывчатых веществ как нитрующий реагент);
— ракетно-космическую (одна из составляющих ракетного топлива);
— медицину (для прижигания бородавок и других кожных образований).
Азотная кислота чем опасна
Массовая доля прокаленного остатка, %, не более
По желанию заказчика предоставляем азотную кислоту с концентрацией азотной кислоты от 10% до 57% с предоставлением сертификатов подтверждающих качество данной продукции.
Применение Азотной кислоты:
Применяют азотную кислоту в виде водных растворов, является одной из составных частей царской водки, содержится в пробирных кислотах. В промышленности применяют для получения комбинированных азотных удобрений, для растворения руд и концентратов, в производстве серной кислоты, различных органических нитропродуктов, в ракетной технике как окислитель горючего. В качестве сырья в производстве аммиачной селитры, в процессах травления металлов, для разделения золота и серебра. Также азотная кислота нашла применение в производстве взрывчатых веществ, производстве полупродуктов для получения синтетических красителей и других химикатов пищевой и не пищевой промышленности для мытья технологического оборудования (баки, трубопроводы, конвейерные линии и т.д.), а так же устранения остатков сырья (молочные камни, и др.). В электронной и радиоэлектронной промышленности и др.
Класс опасности Азотной кислоты:
1. При попадании на кожу концентрированная азотная кислота вызывает тяжелые ожоги.
2. Пары азотной кислоты и оксидов азота раздражают верхние дыхательные пути, вызывают конъюнктивиты и поражают роговицы глаз.
4. Помещения, в которых проводят работы с концентрированной азотной кислотой, должны быть оборудованы приточно-вытяжной вентиляцией.
5. Средствами индивидуальной защиты являются фильтрующий противогаз с коробкой марок В, М, БКФ с фильтром для защиты от тумана азотной кислоты по ГОСТ 12.4.121, защитные очки с резиновой полумаской или защитный щиток из оргстекла, или шлем от противогаза, резиновые кислотозащитные перчатки, специальная кислотозащитная одежда в соответствии с типовыми отраслевыми нормами, утвержденными в установленном порядке.
Меры предосторожности при работе с Азотной кислотой
Чтобы предотвратить ожог, следует работать с концентрированной азотной кислотой в резиновых перчатках. В то же время обращение с азотной кислотой менее опасно, чем, например, с серной, она быстро испаряется и не остаётся в неожиданных местах. Брызги азотной кислоты следует смывать большим количеством воды, а ещё лучше смачивать раствором соды.
Дымящая азотная кислота при хранении под действием теплоты и на свету частично разлагается, чем выше температура и чем концентрированнее кислота, тем быстрее идёт разложение. В связи с этим хранят её в прохладном и тёмном месте. Выделяющийся диоксид азота растворяется в кислоте и придаёт ей бурую окраску. Разбавленную кислоту легко приготовить, выливая концентрированную кислоту в воду.
Разбавленную азотную кислоту хранят и перевозят в таре из хромистой стали, концентрированную – в алюминиевой таре, т.к. концентрированная кислота пассивирует алюминий, железо и хром из-за образования нерастворимых плёнок оксидов: небольшие количества хранят в стеклянных бутылках. Азотная кислота сильно разъедает резину. Поэтому бутылки должны быть с притёртыми или полиэтиленовыми пробками.
Упаковка:
Налив производится в железнодорожные цистерны и автоцистерны из нержавеющей стали, стеклянные бутыли в деревянной или полиэтиленовой обрешетке, специальные бочки из нержавеющей стали, канистры из полимерного материала.
Транспортировка:
Осуществляется железнодорожным транспортом в цистернах, крытых вагонах, а также автомобильным транспортом в соответствии с правилами перевозки грузов, действующими на транспорте данного вида.
Азотная кислота
Азо́тная кислота́ (HNO3), — сильная одноосновная кислота. Твёрдая азотная кислота образует две кристаллические модификации с моноклинной и ромбической решётками.
Азотная кислота смешивается с водой в любых соотношениях. В водных растворах она практически полностью диссоциирует на ионы. Образует с водой азеотропную смесь с концентрацией 68,4 % и tкип120 °C при атмосферном давлении. Известны два твёрдых гидрата: моногидрат (HNO3·H2O) и тригидрат (HNO3·3H2O).
Физические и физико-химические свойства
При кристаллизации из водных растворов азотная кислота образует кристаллогидраты:
Твёрдая азотная кислота образует две кристаллические модификации:
Плотность водных растворов азотной кислоты как функция её концентрации описывается уравнением
где d — плотность в г/см³, с — массовая доля кислоты. Данная формула плохо описывает поведение плотности при концентрации более 97 %.
Химические свойства
Высококонцентрированная HNO3 имеет обычно бурую окраску вследствие происходящего на свету процесса разложения:
При нагревании азотная кислота распадается по той же реакции. Азотную кислоту можно перегонять (без разложения) только при пониженном давлении (указанная температура кипения при атмосферном давлении найдена экстраполяцией).
Золото, некоторые металлы платиновой группы и тантал инертны к азотной кислоте во всём диапазоне концентраций, остальные металлы реагируют с ней, ход реакции при этом определяется её концентрацией.
HNO3 как сильная одноосновная кислота взаимодействует:

в) вытесняет слабые кислоты из их солей:
При кипении или под действием света азотная кислота частично разлагается:
Азотная кислота в любой концентрации проявляет свойства кислоты-окислителя, при этом азот восстанавливается до степени окисления от +4 до −3. Глубина восстановления зависит в первую очередь от природы восстановителя и от концентрации азотной кислоты. Как кислота-окислитель, HNO3 взаимодействует:
а) с металлами, стоящими в ряду напряжений правее водорода:
б) с металлами, стоящими в ряду напряжений левее водорода:


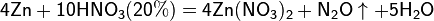

Все приведенные выше уравнения отражают только доминирующий ход реакции. Это означает, что в данных условиях продуктов данной реакции больше, чем продуктов других реакций, например, при взаимодействии цинка с азотной кислотой (массовая доля азотной кислоты в растворе 0,3) в продуктах будет содержаться больше всего NO, но также будут содержаться (только в меньших количествах) и NO2, N2O, N2 и NH4NO3.
Единственная общая закономерность при взаимодействии азотной кислоты с металлами: чем более разбавленная кислота и чем активнее металл, тем глубже восстанавливается азот:
увеличение концентрации кислоты 
С золотом и платиной азотная кислота, даже концентрированная не взаимодействует. Железо, алюминий, хром холодной концентрированной азотной кислотой пассивируются. С разбавленной азотной кислотой железо взаимодействует, причем в зависимости от концентрации кислоты образуются не только различные продукты восстановления азота, но и различные продукты окисления железа:

Азотная кислота окисляет неметаллы, при этом азот обычно восстанавливается до NO или NO2:



и сложные вещества, например:
Некоторые органические соединения (например амины, скипидар) самовоспламеняются при контакте с концентрированной азотной кислотой.
Некоторые металлы (железо, хром, алюминий, кобальт, никель, марганец, бериллий), реагирующие с разбавленной азотной кислотой, пассивируются концентрированной азотной кислотой и устойчивы к её воздействию.
Смесь азотной и серной кислот носит название «меланж».
Азотная кислота широко используется для получения нитросоединений.
Смесь трех объёмов соляной кислоты и одного объёма азотной называется «царской водкой». Царская водка растворяет большинство металлов, в том числе золото и платину. Её сильные окислительные способности обусловлены образующимся атомарным хлором и хлоридом нитрозила:


Нитраты
Азотная кислота является сильной кислотой. Её соли — нитраты — получают действием HNO3 на металлы, оксиды, гидроксиды или карбонаты. Все нитраты хорошо растворимы в воде. Нитрат-ион в воде не гидролизуется.
Соли азотной кислоты при нагревании необратимо разлагаются, причём состав продуктов разложения определяется катионом:
а) нитраты металлов, стоящих в ряду напряжений левее магния:
б) нитраты металлов, расположенных в ряду напряжений между магнием и медью:
в) нитраты металлов, расположенных в ряду напряжений правее ртути:
Нитраты в водных растворах практически не проявляют окислительных свойств, но при высокой температуре в твердом состоянии являются сильными окислителями, например, при сплавлении твердых веществ:
Цинк и алюминий в щелочном растворе восстанавливают нитраты до NH3:
С азотной кислотой не реагируют стекло, фторопласт-4.
Исторические сведения
Методика получения разбавленной азотной кислоты путём сухой перегонки селитры с квасцами и медным купоросом была, по видимому, впервые описана трактатах Джабира (Гебера в латинизированных переводах) в VIII веке. Этот метод с теми или иными модификациями, наиболее существенной из которых была замена медного купороса железным, применялся в европейской и арабской алхимии вплоть до XVII века.
В XVII веке Глаубер предложил метод получения летучих кислот реакцией их солей с концентрированной серной кислотой, в том числе и азотной кислоты из калийной селитры, что позволило ввести в химическую практику концентрированную азотную кислоту и изучить её свойства. Метод Глаубера применялся до начала XX века, причём единственной существенной модификацией его оказалась замена калийной селитры на более дешёвую натриевую (чилийскую) селитру.
Во времена М. В. Ломоносова азотную кислоту называли крепкой водкой.
Промышленное производство, применение и действие на организм
Азотная кислота является одним из самых крупнотоннажных продуктов химической промышленности.
Производство азотной кислоты
Современный способ её производства основан на каталитическом окислении синтетического аммиака на платино-родиевых катализаторах (процесс Оствальда) до смеси оксидов азота (нитрозных газов), с дальнейшим поглощением их водой


Концентрация полученной таким методом азотной кислоты колеблется в зависимости от технологического оформления процесса от 45 до 58 %.
Впервые азотную кислоту получили алхимики, нагревая смесь селитры и железного купороса:
Чистую азотную кислоту получил впервые Иоганн Рудольф Глаубер, действуя на селитру концентрированной серной кислотой:
Дальнейшей дистилляцией может быть получена т. н. «дымящая азотная кислота», практически не содержащая воды.
Применение
Действие на организм
Азотная кислота и её пары очень вредны: пары вызывают раздражение дыхательных путей, а сама кислота оставляет на коже долгозаживающие язвы. При действии на кожу возникает характерное желтое окрашивание кожи, обусловленное ксантопротеиновой реакцией. При нагреве или под действием света кислота разлагается с образованием высокотоксичного диоксида азота NO2 (газа бурого цвета). ПДК для азотной кислоты в воздухе рабочей зоны по NO2 2мг/м






































