Как клостридии влияют на организм
Клостридии вызывают острые кишечные инфекции.
Бактерии рода Клостридий вырабатывают наиболее сильные из известных ядов – ботулотоксин, тетаноспазмин и другие.
Клостридии – бактерии в составе постоянной собсвтенной микрофлоры кишечника. Растут строго без доступа воздуха и их очень трудно идентифицировать.
В организме человека клостридии являются стимуляторами Т-регуляторных клеток, которые снижают аллергическую настроенность организма. Один из клостридиальных метаболитов – бутират –защищает нас через интерлейкин 10. к
Кроме того, клостридии учавствуют в обмене липидов, в обмене желчных кислот и их частичном выведении из организма, подавляют рост и развитие в ЖКТ болезнетворных бактерий, расщепляют до молекулярного состояния белки.
В кишечнике новорожденных детей клостридии появляются к 6-7 дню жизни.
У детей на грудном вскармливании уровень клостридий держится в норме.
У детей при раннем введении смешанного или искусственного вскармливании клостридий превышает норму.
Анализ на дисбактериоз
Количество клостридий у взрослых:
Повышенное содержание клостридий часто наблюдается у людей старшего возраста на фоне физиологического снижения бифидобактерий.
Также повышенное содержание мясных продуктов в диете может спровоцировать рост клостридий с превышением естественной нормы.
При дисбактериозах надо регулировать эубактерии, клостридии, бифидо- и лактобактерии.
Лечшими препаратами для коррекции микрофлоры в сторону нормы являются жидкие синбиотики бифидум баг и трилакт. В них запредельное количество живых бактерий плюс жидкая среда в качестве пребиотика.
Живые культуры бифидо- и лактобактерий вместе с частью культуральной среды работают как биокатализаторы, стимулирующие восстановление кишечного гомеостаза в сторону нормы.
Людям старшего возраста необходимо 2 раза в год проводить профилактические курсы бифидум баг+трилакт для восстановления бифидобактерий, латофлоры, клостридий и др. А также регулярно употреблять в пищу кисломолочные продукты.
Трилакт и Бифидум БАГ – это безопасная микробиологическая профилактика и терапия дисбиотических нарушений ЖКТ.
Клостридии. Всегда рядом, всегда начеку
Ботулизм, столбняк, газовая гангрена… Об этих заболеваниях наслышаны если не все, то очень многие люди. Но если от столбняка существуют вакцины, например АКДС (адсорбированная коклюшно-дифтерийно-столбнячная сыворотка), то от псевдомембранозного колита, некротического энтерита, ботулизма или газовой гангрены таких вакцин нет. А вызываются все эти заболевания бактериями рода Clostridium.
Одним из наиболее распространенных видов клостридий является Clostridium difficile. Ее высевают из почвы, воды (в том числе и морской). Благодаря возможности образовывать эндоспоры (покрываться оболочкой и переживать неблагоприятный период в состоянии своеобразной «спячки») этот вид может длительно, до двух месяцев, сохраняться во внешней среде. Более того, в состоянии эндоспоры клостридия диффициле выдерживает даже кипячение. Чувствительность к антибиотикам у Clostridium difficile от природы очень низкая, поэтому лечение посредством антибиотикотерапии зачастую терпит фиаско.
Clostridium difficile входит в нормофлору (является представителем нормального микробного состава) желудочно-кишечного тракта, обитая преимущественно в толстом кишечнике. Хотя отдельные его представители встречаются и во рту, и в тонком отделе кишечника, и во влагалище у женщин. Чаще всего Clostridium difficile обнаруживается в кишечнике новорожденных (около половины младенцев), а из детей старше 2 лет и взрослых каждый 10 является обладателем этой бактерии.
Clostridium difficile вызывает такие заболевания как псевдомембранозный колит и антибиотикоассоциированные диареи. Патогенные (болезнетворные) свойства этой клостридии обусловлены выделением токсинов А и В, а также белка, угнетающего перистальтику (сократительную функцию) кишечника.
Антибиотикодиссоциированные диареи (сокращенно – ААД) могут вызываться не только клостридией дифициле, а и множеством других микроорганизмов (сальмонеллами, кандидами, клостридией перфрингенс, золотистым стафилококком, клебсиеллой). Этот вид диарей является наиболее частой внутрибольничной инфекцией и связана такая тенденция с тем, что в больницах, во-первых, концентрируется большая масса больных и здоровых людей. А во-вторых, здесь используется множество антибиотиков и дезинфицирующих средств, которые способствуют образованию генераций (поколений) микроорганизмов, устойчивых к антибиотикам. Поэтому в мире ежегодно регистрируется около миллиона случаев ААД. Возникновение антибиотикоассоциированных диарей связано с тем, что антимикробные препараты подавляют как патогенную, так и нормальную микрофлору. Даже однократный прием антибиотиков широкого спектра действия может послужить причиной развития ААД.

Несмотря на это, дети младенческого возраста практически не болеют антибиотикоассоциированными диареями, вызываемыми клостридией диффициле. Связано это с тем, что дети получают с материнским молоком достаточно иммунных факторов, которые могут сдерживать размножение Clostridium difficile. Более того, в младенческом организме нет такого количества сопутствующей условно-патогенной микрофлоры, которая ослабляет иммунитет.
Антибиотикозависимые диареи могут иметь разную симптоматику и течение: от легкой диареи до тяжелейшего псевдомембранозного энтероколита (ПМК). Последний чаще всего вызывается именно клостридией диффициле.
В процессе течения заболевания отмечаются следующие симптомы:
При отсутствии лечения количество смертельных случаев составляет до 30 %.
Характерная особенность болезней, вызванных Clostridium difficile, является то, что около четверти случаев через время повторяются (рецидив заболевания). Причиной этого явления становятся споры клостридий, которые переживают период лечения, либо повторное заражение. Как правило, после лечения больные выздоравливают, или чувствуют себя значительно лучше, но спустя несколько дней (от 3 до 7) развивается рецидив.
Еще одна клостридия, которая может вызывать такие болезни желудочно-кишечного тракта, как пищевые токсикоинфекции и некротический энтерит, — Clostridium perfringens.
Некротический энтерит характеризуется формированием язв и эрозий и деструктивными (разрушающими) изменениями в слизистой оболочке. Первым симптомом заболевания является возникновение участков геморрагического некроза в начальных отделах тощей кишки. Эти участки имеют красный цвет. Наблюдается также сужение просвета кишечника в месте воспаления, за счет отечности стенки. Происходит тромбоз (закупорка) мелких кровеносных сосудов (артериол). У больного отмечаются озноб и лихорадка, рвота и кровавый пенистый понос.
Clostridium perfringens производит ферменты, расщепляющие белки (протеиназа), коллаген (коллагеназа), гиалуроновую кислоту (гиалуронидаза).

Профилактика заболеваний, причиной которых являются клостридии, в первую очередь заключается в соблюдении санитарно-гигиенических норм и правил: мытье и ошпаривание овощей и фруктов; длительная термическая обработка. Но немаловажным является также нормализация микрофлоры и укрепление иммунитета. Причем, как в процессе лечения, так и в процессе предупреждения этих болезней. Ограниченное и строго подконтрольное врачам применение антибиотиков, отказ от самолечения также очень важны для профилактики возникновения АДД и других болезней, связанных с клостридиями.
Клостридия клостридии волк: С. difficile vs С. scindens
Клостридия клостридии волк: С. difficile vs С. scindens
Автор
Редактор
Тело человека населено триллионами микроорганизмов, совокупность которых называют микробиомом. Микробиом выполняет множество важных функций — от синтеза витаминов до расщепления сложных компонентов пищи. «Здоровая» микрофлора постоянно конкурирует за ограниченные питательные ресурсы с патогенными микроорганизмами, тем самым подавляя их рост. Однако из-за приема антибиотиков или других причин нормальный состав микробиома может нарушаться, и тогда патогены получают возможность размножаться неконтролируемо, вызывая болезни. Один из таких патогенов — бактерия Clostridium difficile, возбудитель псевдомембранозного колита. Борьба с С. difficile осложняется ее устойчивостью к большинству известных антибиотиков. Но недавно было показано, что рост С. difficile можно успешно подавлять не лекарствами, а при помощи родственного ему вида — С. scindens. Это открытие послужит основой для создания «умных» лекарств-пробиотиков: эффективных против С. difficile, но безопасных для полезной микрофлоры.
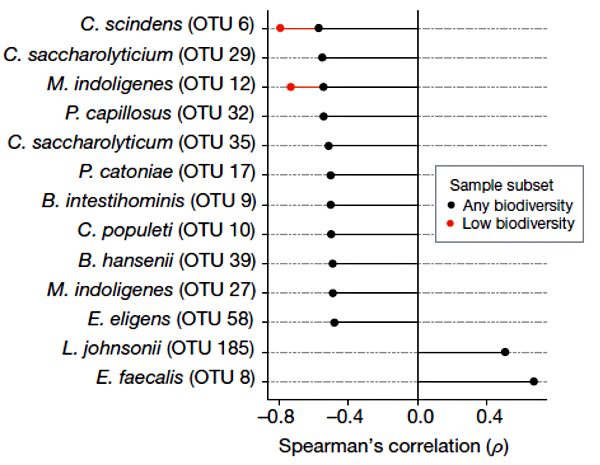
Рисунок 1. Корреляция между присутствием конкретных бактериальных таксонов в микробиоме и устойчивостью к заражению C. difficile [3].
Антибиотики эффективны в борьбе со множеством смертельных заболеваний, но вместе с тем они наносят существенный урон микробиому человека. После курса антибиотиков человек, как правило, более подвержен заражению различными патогенами. Clostridium difficile — грамположительная подвижная бактерия, основной возбудитель острых внутрибольничных кишечных инфекций. За последние 15 лет число смертельных случаев, обусловленных размножением С. difficile, возросло по меньшей мере в 10 раз, особенно среди пожилых и ослабленных людей [1]. Борьба с С. difficile осложняется тем, что при неблагоприятных условиях этот вид образует споры, выдерживающие действие антибиотиков. Такая особенность позволяет бактериям повторно колонизировать кишечник спустя несколько недель и даже месяцев после окончания лечения.
Недавно было показано, что трансплантация микробиомов здоровых доноров вылечивает тяжелые инфекции C. difficile [2]. Однако оставалось неизвестным, какие именно члены микробиома восстанавливают устойчивость организма к инфекции C. difficile и какими механизмами. И вот наконец вышла статья, которая проливает свет на довольно необычный механизм межвидовых взаимодействий в микробиоме [3].
О мышах и людях
C. difficile — не только человеческая беда, но и мышиная. Для начала микробиомы мышей пробовали травить разными антибиотиками и смотрели, как от этого меняется восприимчивость к C. difficile. В целом антибиотики не столько уменьшают суммарное число бактерий в кишечнике, сколько существенно нарушают расстановку сил — соотношение разных таксономических групп. Оказалось, что восприимчивость к C. difficile четко коррелирует с общим снижением видового разнообразия микробима. Удалось выделить горстку из 11 условных видов (операционных таксономических единиц), ассоциированных с устойчивостью к заражению C. difficile (рис. 1). Многие из них оказались тоже клостридиями (кластер Clostridium XIVa). Ученые обратили внимание на один таксон, присутствие которого сильнее всего коррелировало с резистентностью к C. difficile, даже у животных с экстремально низким видовым разнообразием микробиома. Героем оказался Clostridium scindens.
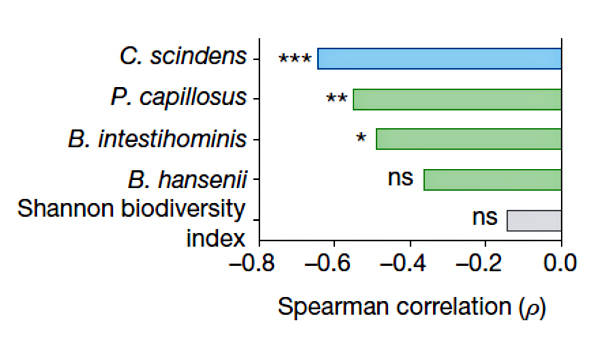
Рисунок 2. Корреляция между приживлением видов-кандидатов в микробиоме и устойчивостью к C. difficile [3].
Но то у мышей. Как же обстоят дела у человека? Для определения видов, связанных с устойчивостью к инфекции C. difficile, исследовали микробиомы пациентов, перенесших аллогеную трансплантацию гемопоэтических стволовых клеток. Большинство из них проходило химиотерапию и/или лучевую терапию одновременно с курсом антибиотиков во время трансплантации. Ослабленный иммунитет и снижение видового разнообразия микробиома делают этих пациентов легкой мишенью для C. difficile. У человека удалось найти два основных вида, с которыми не уживались C. difficile. Наиболее сильным ингибитором оказался C. scindens, как и у мышей. Как будто бы победа?
Для проверки ингибирующего эффекта C. scindens вместе с несколькими другими перспективными бактериями запустили в кишечники животных, недавно принимавших антибиотики (рис. 2). Оказалось, что такая микробная трансплантация существенно облегчила течение инфекции, вызванной C. difficile, а также положительно сказалась на снижении смертности и увеличении массы тела по сравнению с контролем. Наиболее заметную устойчивость к C. difficile обеспечивал, как и ожидалось, C. scindens. Приживление трасплантированных бактерий в микробиоме отслеживали по наличию гена соответствующей 16S рРНК. Устойчивость к C. difficile росла прямо пропорционально обилию C. scindens. То есть улучшение приживаемости C. scindens может повысить защиту против C. difficile. Примечательно, что такая аккуратная замена плохой клостридии на очень похожую, но хорошую, не нарушает существующий в микробиоме баланс (ни качественный, ни количественный). Своеобразная антидотная терапия, только на уровне микробиома. Все это открывает искрящиеся горизонты для разработки безопасных лекарств против C. difficile. Но как именно C. scindens противостоит C. difficile?
Механизм ингибирующего действия
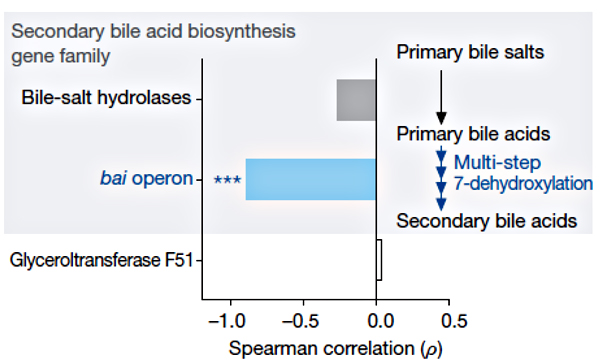
Рисунок 3. Корреляция между устойчивостью к C. difficile и наличием семейств генов, необходимых для синтеза вторичных желчных кислот [3].
Известно, что некоторые вторичные желчные кислоты могут ухудшать рост C. difficile in vitro [4]. У очень большого числа микробиомных бактерий есть ген bsh, кодирующий гидролазу желчных кислот. Однако у редкой бактерии (ужасно малой доли микробиомных организмов) есть все гены, необходимые для осуществления полного пути биосинтеза желчных кислот. Редкой бактерией, конечно же, оказалась C. scindens, обладающая критическим для синтеза вторичных желчных кислот геном 7α-гидроксистероид-дегидрогеназы (рис. 3). Именно на этой уникальной биохимической особенности и зиждется защитный механизм C. scindens против C. difficile. Внедрение C. scindens в микробиом животных, восприимчивых к C. difficile, восстанавливает необходимый уровень и соотношение вторичных желчных кислот: дезоксихолевой (DCA) и литохолевой (LCA). Обе эти кислоты подавляют рост C. difficile пропорционально своей концентрации. Примечательно, что C. scindens повышает количество вторичных желчных кислот до физиологического уровня и препятствует росту C. difficile даже у животных, прошедших курс антибиотикотерапии. Этот механизм консервативен — реализуется как в микробиоме мыши, так и в микробиоме человека.
Терапевтические перспективы
* — О черных делишках кишечных микробов-диверсантов, сокращающих пул желчных кислот и стимулирующих развитие атеросклероза, читайте в статье «Не доверяйте рекламе, или потенциальная связь метаболизма и развития атеросклероза» [6] — Ред.
Инфекция Сlostridium difficile
Широкое применение антибиотиков в России в течение 2020 (не в последнюю очередь обусловленное пандемией вируса SARS-Cov-2) привело к тому, что врачи-гастроэнтерологи стали чаще встречаться с такими осложнениями антибиотикотерапии как антибиотик-ассоциированные диареи и колиты. Одной из наиболее частых причин этих нарушений ―15-25% случаев ― является инфекция Clostridium difficile (по новой классификации Clostridiodes difficile).
Clostridium difficile (C.difficile) представляет собой споропродуцирующую бактерию, впервые описанную в 1935 году. Она вызывает широкий спектр желудочно-кишечных нарушений: от бессимптомного носительства до крайне тяжелого (фульминантного) колита. Споры бактерий, попав в желудочно-кишечный тракт здорового человека, пройдут транзитом, не вызывая никаких изменений. У части здоровых лиц бактерия может выявляться в образцах стула, опять же не проявляясь симптомами. У людей, имеющих факторы риска, споры прорастают, что приводит к образованию вегетативных форм C.difficile. Часть бактерий способны продуцировать токсины, что приводит к развитию заболевания.
Некоторые эпидемиологические данные.
Факторы риска развития заболеваний, вызванных C.difficile.
1) Терапия антибиотиками в течение 8 недель до начала появления кишечных симптомов. Антибиотикотерапия увеличивает риск развития инфекции в 8 раз.
2) Возраст старше 65 лет (для амбулаторных пациентов риск ниже, чем для госпитализированных)
3) Стационарное лечение более 4 недель (и нахождение в учреждениях длительного ухода, хосписах). Каждая неделя пребывания в стационаре увеличивает риск инфицирования на 8%. Нахождение в отделении интенсивной терапии увеличивает риск в 2 раза.
4) Химиотерапия и применение иммуносупрессоров
5) Прием препаратов из группы ингибиторов протонной помпы (риск возрастает в 2,9-3,6 раза)
6) Сопутствующие заболевания (хроническая болезнь почек, в том числе требующая проведения диализа, инсульт, сахарный диабет, хроническая сердечная недостаточность, алкоголизм, хроническая обструктивная болезнь легких, недостаточность питания, ВИЧ-инфекция, онкопатология, воспалительные заболевания кишечника и т.д.) и состояния (беременность).
Как видим, на первом месте среди факторов риска развития клостридиальной инфекции находятся антибиотики. Именно антибиотик-ассоциированные нарушения, вызванные C.difficile, чаще всего встречаются в практике гастроэнтеролога. Все антибиотики по риску развития инфекции C.difficile делятся на три группы:
1) высокий риск ― фторхинолоны (ципрофлоксацин и т.д.), цефалоспорины 2 и 3 поколений, клиндамицин, ампициллин, пенициллины широкого спектра действия с клавулановой кислотой;
2) умеренный риск ― макролиды, триметоприм/сульфаметоксазол, сульфаниламиды, другие пенициллины;
3) низкий риск ― аминогликозиды, бацитрацин, метронидазол, тейкопланин, ванкомицин, рифампицин, хлорамфеникол, тетрациклин, карбапенемы, даптомицин, тигециклин.
Пути заражения и патогенез.
C.difficile широко распространена в окружающей среде и передается фекально-оральным путем. Как уже говорилось выше, бактерия образует споры, которые в неактивном виде долго сохраняются в окружающей среде. Устойчивость спор к высоким температурам, ультрафиолетовому излучению и антибиотикам делает бактерии очень жизнеспособными.
Споры могут сохраняться в желудочно-кишечном тракте человека и быть причиной рецидива инфекции C.difficile после успешного лечения.
Вспышки инфекций в стационарах обусловлены передачей спор через руки медицинского персонала или ухаживающих лиц (в том числе родственников). Споры C.difficile найдены в палатах половины инфицированных лиц.
Патогенность C.difficile обусловлена наличием двух токсинов ― токсин А и токсин В. Бактерии, которые токсины не продуцируют, не вызывают развитие болезни. Часть бактерий продуцирует только токсин В, некоторые ― оба токсина. В последние годы описаны штаммы бактерий, которые могут также выделять двойной токсин (CDT).
После попадания спор в желудочно-кишечный тракт человека, они прорастают с образованием вегетативных форм бактерий. Далее происходит адгезия (прилипание) бактерий к клеткам эпителия толстой кишки и продукция токсинов. Важную роль играет нарушение конкуренции со стороны нормальной кишечной микробиоты, которая меняется после антибиотикотерапии.
Токсин А вызывает воспаление слизистой толстой кишки и секрецию жидкости, именно с ним связано развитие водянистой диареи при инфицировании C.difficile.
Токсин В токсичен в отношении клеток, причем не только кишечника. Повышенная продукция этого токсина может приводить к развитию осложнений и поражению других органов и систем (например, сердечно-сосудистой) при тяжелом течении болезни.
Классификация заболеваний, вызванных C.difficile.
Согласно международной классификации болезней 10 пересмотра (МКБ-10) заболевание кодируется как «энтероколит, вызванный C.difficile» (код А 04.7).
Российская гастроэнтерологическая ассоциация в своих рекомендациях от 2016 года выделяет следующие проявления C.difficile-ассоциированной болезни в зависимости от тяжести ее течения:
1) Легкое/среднетяжелое ― диарея (неоформленный стул 3 и более раз в сутки) в сочетании с болью в животе
4) Рецидив болезни ― повторное развитие симптомов менее чем через 8 недель после окончания терапии.
Представляется сомнительными следующие формулировки диагноза у пациента с инфекцией C.difficile:
1) «Антибиотик-ассоциированная диарея» ― лишь около 20% случаев нарушений стула после антибиотиков связаны с C.difficile»
2) «Псевдомембранозный колит» ― лишь в 50% случаев в кишке выявляются «псевдомембраны» и только при тяжелом колите.
До получения новых данных можно использовать термин, предложенный Российской гастроэнтерологической ассоциацией: «C.difficile-ассоциированная болезнь». Также логичным представляется описательный диагноз «C.difficile-ассоциированная диарея» или «C.difficile-ассоциированный колит» в зависимости от тяжести заболевания.
Клиническая картина C.difficile-ассоциированной болезни.
Диагностика C.difficile-ассоциированной болезни.
1. Исследование кала. Образец кала для наилучшей диагностики инфекции C.difficile ― неоформленный (лучше жидкий) свежий кал. Для лиц с кишечной непроходимостью с отсутствием стула ― кишечный мазок.
Современные методы диагностики инфекции C.difficile в кале включают:
А. Полимеразную цепную реакцию (ПЦР) для диагностики токсин-продуцирующих штаммов C.difficile.
Преимущества: метод с высокой специфичностью и чувствительностью, во многих рекомендациях рассматривается как «золотой стандарт» диагностики. Небольшие сроки выполнения.
Недостатки: требует специализированной лаборатории для молекулярно-генетической диагностики. Может быть причиной гипердиагностики, так как выявляет не сами токсины в кале, а только бактерии, которые могут их продуцировать.
Б. Иммуноферментный анализ (ИФА) кала для выявления токсинов А и В C.difficile.
Преимущества: наиболее доступный метод, достаточно высокая специфичность.
Недостатки: низкая чувствительность, т.е. не все случаи явной инфекции будут выявлены тестом. Чувствительность зависит от вида тест-системы. Не все коммерческие тест-системы определяют токсин В.
В. Исследование глутаматдегидрогеназы (ГДД) в кале.
ГДД ― фермент, продуцируемый C.difficile.
Преимущества: высокая чувствительность и специфичность метода. Очень быстрое исследование (до 30 минут).
Недостатки: ГДД продуцируется как токсигенными, так и нетоксичными штаммами C.difficile. В России этот метод пока практически недоступен.
2. Эндоскопическая диагностика толстой кишки (колоноскопия).
При C.difficile-ассоциированной диарее изменения со стороны слизистой оболочки толстой кишки обычно неспецифичны: отек, гиперемия (покраснение), иногда в виде очагов.
При C.difficile-ассоциированном колите, когда кишечное воспаление более выражено, могут выявляться эрозии и язвы. Тяжелое воспаление сопровождается образованием «псевдомембран». Это наложения на слизистой оболочке желто-зеленого, бело-желтого или розового цвета, которые с трудом отделяются. Псевдомембраны выявляются лишь в половине случаев колита, вызванного C.difficile, во всех остальных ситуациях эндоскопическая картина воспаления мало специфична. Это приводит к неверным диагнозам: язвенный колит, болезнь Крона, особенно если не было указания на прием антибиотиков.
Лечение C.difficile-ассоциированной болезни.
1. Процедуры по изоляции пациента и профилактике распространения инфекции (актуальны в стационаре):
2. Терапия заболевания включает:
* не зарегистрированы в Российской Федерации
Профилактика возникновения инфекции C.difficile.
1) Использование антибиотикотерапии только по показаниям
2) Использовать минимально эффективную продолжительность лечения антибиотиками