Proteus mirabilis в мазке у женщин что это
Протейная инфекция: причины, развитие, опасность для организма
Протейная инфекция: причины, развитие, опасность для организма
Возбудителями протейной инфекции являются грамотрицательные условно-патогенные микроорганизмы семейства энтеробактерий, которые присутствуют в нормальной микрофлоре кишечника, а также повсеместно распространены в воздухе, почве и воде. Бактерии рода Proteus в течение долгого времени не причислялись к возбудителям серьезных инфекционно-воспалительных заболеваний. Однако в связи с последними достижениями в области диагностики было обнаружено, что эти микроорганизмы способны вызывать трудно поддающиеся лечению патологии (протеозы), поражающие преимущественно ЖКТ и мочеполовую систему.
Причины протейной инфекции
Протейная палочка, присутствующая в кишечной микрофлоре в небольших количествах, не причиняет организму никакого вреда. При определенных обстоятельствах (снижение иммунитета, неправильное питание, длительный прием антибиотиков) она может активизироваться и начать интенсивно размножаться. Также инфицирующее количество этих бактерий способно проникнуть в организм из внешней среды.
Основными путями передачи инфекции являются пищевой и контактно-бытовой. Чаще всего заражение происходит при употреблении белковых продуктов (мяса, рыбы, молока, колбасы), которые хранились с нарушением надлежащих сроков и условий. Значительно реже инфицирование осуществляется через немытые руки, во время купания или при употреблении зараженной воды.
Развитие патологии
При непосредственном попадании протея в ЖКТ вместе с продуктами питания инфекционное заболевание развивается очень стремительно. Первые симптомы ярко выражены, а общая клиническая картина совпадает с проявлениями сильного пищевого отравления. При контактно-бытовом способе заражения развитие признаков инфекции обычно происходит медленнее.
Если инфекционный процесс протекает в легкой форме, больной испытывает слабость, у него отмечаются повышение температуры, рвота, боль в животе, частый водянистый стул, в котором могут обнаруживаться слизь и зеленые включения. При тяжелом течении заболевания приступы рвоты случаются около 10 раз за сутки и более, а температура обычно поднимается до 40°С.
При условии своевременного и адекватного лечения вся острая симптоматика протеоза легкой или средней степени тяжести исчезает спустя несколько дней, после чего больной быстро идет на поправку.
Опасность протейной инфекции
Тяжелые формы патологии могут осложняться состояниями, требующими срочной госпитализации больного, такими как сильное обезвоживание, судороги, инфекционно-токсический шок.
Помимо острых инфекций пищеварительной системы бактерии Proteus способны поражать другие органы, распространяясь через кровь или по лимфатическим сосудам. Очаг воспаления может локализоваться в мочеполовой системе, глазах, ушах, легких и даже в костной ткани или мозговых оболочках. Данные патологии достаточно часто переходят в хроническую форму с упорным рецидивирующим течением, которая тяжело поддается терапии.
Если протейная инфекция заносится на незажившие поверхности кожи и слизистых оболочек (послеоперационные раны, ожоги), вызванный ею воспалительный процесс значительно замедляет регенерацию тканей и снижает эффективность лечебных мероприятий.
Следует отметить, что даже незначительное превышение нормального количества протейной палочки в кишечной микрофлоре может негативно отразиться на состоянии здоровья. Так, если у человека имеются аутоиммунные болезни, существует высокий риск их обострения из-за возросшей активности протейной палочки. Атопический дерматит, астма, аллергические заболевания и другие иммунозависимые патологии могут впервые развиться или обостриться под воздействием бактерий Proteus.
Инфекции, вызываемые возбудителями рода PROTEUS (Протей)
В последние годы инфекционисты отмечают рост заболеваний, обусловленных нетрадиционными микроорганизмами. Особое место занимает протейная инфекция. Ее кишечная форма, вызванная бакетриями рода Протей — P. vulgaris протекает тяжелее у детей раннего возраста. Не менее опасны гнойно-воспалительные заболевания мочевыводящей системы, вызываемые P. mirabilis, P. rettgeri и P. morganii.
В греческой мифологии Протей – божество, способное менять облик. Отсюда название полиморфных, мелких, нитевидных палочек, отличающихся активной подвижностью. Размеры клеток составляют 0,5 — 3 мкм. P. morganii, P. rettgeri — менее полиморфны и малоподвижны.
Протейная инфекция: причины, развитие, опасность для организма
Возбудителями протейной инфекции являются грамотрицательные условно-патогенные микроорганизмы семейства энтеробактерий, которые присутствуют в нормальной микрофлоре кишечника, а также повсеместно распространены в воздухе, почве и воде. Бактерии рода Proteus в течение долгого времени не причислялись к возбудителям серьезных инфекционно-воспалительных заболеваний. Однако в связи с последними достижениями в области диагностики было обнаружено, что эти микроорганизмы способны вызывать трудно поддающиеся лечению патологии (протеозы), поражающие преимущественно ЖКТ и мочеполовую систему.
Протей – факультативный анаэроб, палочковидная, неспороносная, подвижная, грамотрицательная бактерия. В микробиологическом анализе кала протей встречается в комплексе с другими условно-патогенными бактериями семейства энтеробактерий. Кроме протея, в составе нормальной микрофлоры кишечника человека определяются: клебсиелла, энтеробактер, гафния, серратия, морганелла, провиденция, цитробактер. В 1 г кала должно быть меньше 10 4 общего количества этих бактерий. Большее количество перечисленных бактерий является признаком дисбактериоза.
В природе бактерии рода Proteus обнаруживаются: в сточных водах, в земле, в водоемах, на овощах, в разлагающихся органических веществах. Эти микроорганизмы — сапрофиты, они живут на слизистых оболочках, на коже, в кишечнике человека и животных. Протеи устойчивы во внешней среде и сохраняют жизнедеятельность в слабых растворах фенола и других средств. Выявлена также резистентность ко многим антибиотикам.
Причины протейной инфекции
Протейная палочка, присутствующая в кишечной микрофлоре в небольших количествах, не причиняет организму никакого вреда. При определенных обстоятельствах (снижение иммунитета, неправильное питание, длительный прием антибиотиков) она может активизироваться и начать интенсивно размножаться. Также инфицирующее количество этих бактерий способно проникнуть в организм из внешней среды.
Основными путями передачи инфекции являются пищевой и контактно-бытовой. Чаще всего заражение происходит при употреблении белковых продуктов (мяса, рыбы, молока, колбасы), которые хранились с нарушением надлежащих сроков и условий. Значительно реже инфицирование осуществляется через немытые руки, во время купания или при употреблении зараженной воды.
Инфицирование протеем может произойти через полуфабрикаты, сырые продукты или готовые блюда из мяса, рыбы, молока, колбасы, студня. В них происходит быстрое размножение бактерий с образованием токсинов. Реже отмечают водный путь передачи: при купании в загрязненных водоемах или употреблении инфицированной воды. Возможен и контактный путь передачи на инфицированных руках зараженного человека.
Развитие патологии
При непосредственном попадании протея в ЖКТ вместе с продуктами питания инфекционное заболевание развивается очень стремительно. Первые симптомы ярко выражены, а общая клиническая картина совпадает с проявлениями сильного пищевого отравления. При контактно-бытовом способе заражения развитие признаков инфекции обычно происходит медленнее.
Если инфекционный процесс протекает в легкой форме, больной испытывает слабость, у него отмечаются повышение температуры, рвота, боль в животе, частый водянистый стул, в котором могут обнаруживаться слизь и зеленые включения. При тяжелом течении заболевания приступы рвоты случаются около 10 раз за сутки и более, а температура обычно поднимается до 40°С.
При условии своевременного и адекватного лечения вся острая симптоматика протеоза легкой или средней степени тяжести исчезает спустя несколько дней, после чего больной быстро идет на поправку.
Протеи выделяют токсические вещества — эндотоксины с гемолитическими свойствами и с различной степенью биохимической активности. У штаммов P. vulgaris обнаружена лецитиназная активность. Протеи обладают способностью адгезии к уротелию при помощи ресничек. Отмечают, что резистентность к антибиотикам связана с адгезивной способностью уропатогенных протеев.
Острой кишечной протейной инфекцией, протекающей по типу гастроэнтерита, гастрита и колиэнтерита часто болеют дети раннего возраста с пониженным иммунитетом и после бесконтрольного назначения антибиотиков. Заболевание сопровождается симптомами токсикоза — повышением температуры, рвотой, метеоризмом, схваткообразными болями в животе, нарушением аппетита, кратковременными судорогами, появлением водянистого, зловонного, учащенного стула.
В тяжелых случаях могут развиться осложнения: гемолитико-уремический синдром, а также симптомы острой гемолитической тромбопении, анемии или острой почечной недостаточности.
Клинические проявления внутрибольничной инфекции протейной этиологии весьма разнообразны: поражения мочевыводящей системы, отиты, холециститы, нагноения ран и септические состояния. Попадание протеев в пупочную ранку новорожденного может привести к бактериемии или развитию менингита.
Данные заболевания могут развиться: при передаче возбудителя контактно-бытовым или воздушно-капельным путями, при заносе с катетером, другими урологическими инструментами.
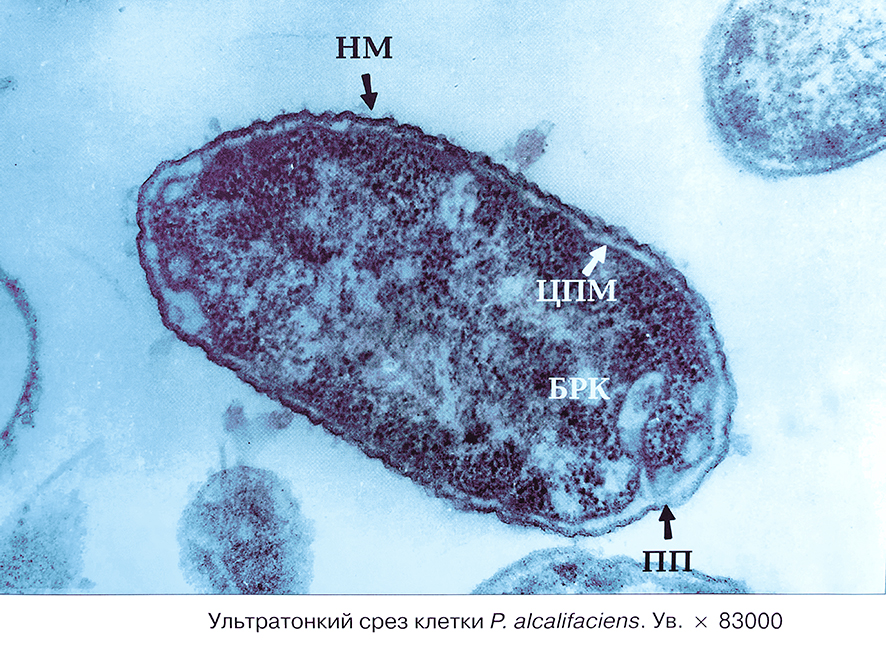
Если в мазках исследуемого материала (участки ожоговой ткани, гной, раневое отделяемое, испражнения) обнаруживаются грамотрицательные палочки, то бактериоскопический метод позволяет сделать предварительное заключение. Бактериологическим методом на средах определяют колонии протея в виде тонкого стелющегося налета. Активно размножаются протеи на белковой питательной среде вызывают гниение мяса, рыбы, других белковых продуктов.
Важнейшие профилактические меры — это соблюдение санитарного режима в детских учреждениях и стационарах, проведение общесанитарных мероприятий. Для профилактики протея каждому необходимо соблюдать правила личной гигиены, исключить потребление подозрительных продуктов в питании, избегать контактов с больными детьми и взрослыми.
При лечении протейной инфекции следует придерживаться лечебной щадящей диеты с исключением жареных, острых блюд, белковых продуктов. В острый период протейного инфицирования, при поражении желудочно-кишечного тракта — необходимо обеспечить восполнение потерянной жидкости. Полезно употреблять отвары трав – тысячелистника, алтея, зверобоя, ромашки, календулы; морсы, компоты с клюквой, черной смородиной, абрикосами, черникой, яблоками. Применять антибиотики можно только по назначению врача, в соответствии с данными анализов чувствительности бактерии протея к ним.
Обязательно нужно принимать препараты – пробиотики, пребиотики, синбиотики для восстановления нормальной флоры кишечника.
Синбиотические комплексы Нормофлорины, содержащий живые активные лакто- и бифидобактерии, секретирующие молочную, уксусную, масляную, пропионовую кислоты, оказывающие защитное, антисептическое, противовоспалительное, сорбционное действие – уменьшает интоксикацию, улучшает моторику кишечника, функцию печени, повышает иммунную реактивность. Это помогает в борьбе с протейной инфекцией, восстанавливает работу желудочно-кишечного тракта, общее самочувствие, повышает иммунитет.
Схема (возрастные дозировки для детей или взрослых): (взрослый) нормофлорин Л – 20 мл (при диарее) – 40 (при запорах) мл утром перед едой, Д — 40 мл вечером за 20 мин до еды, Б – 20-30 мл на ночь в клизме. При диарее в обед можно добавить Д – 30-40 мл, при запорах в обед + Л – 30-40 мл.
Курс приема нормофлоринов — 1 — 1,5 месяца, для выведения токсинов, патогенной микрофлоры, восстановления полезных собственных бактерий. Уникальный состав нормофлоринов, не содержащих белков коровьего молока, молочного сахара, консервантов позволяет при протейной инфекции успешно применять его у детей с первых дней жизни, беременных, кормящих, больных сахарным диабетом, аллергическими заболеваниями, т.е. у взрослых при любой сопутствующей патологии.
Опасность протейной инфекции

Тяжелые формы патологии могут осложняться состояниями, требующими срочной госпитализации больного, такими как сильное обезвоживание, судороги, инфекционно-токсический шок.
protey_mirabilis
Помимо острых инфекций пищеварительной системы бактерии Proteus способны поражать другие органы, распространяясь через кровь или по лимфатическим сосудам. Очаг воспаления может локализоваться в мочеполовой системе, глазах, ушах, легких и даже в костной ткани или мозговых оболочках. Данные патологии достаточно часто переходят в хроническую форму с упорным рецидивирующим течением, которая тяжело поддается терапии.
Если протейная инфекция заносится на незажившие поверхности кожи и слизистых оболочек (послеоперационные раны, ожоги), вызванный ею воспалительный процесс значительно замедляет регенерацию тканей и снижает эффективность лечебных мероприятий.
Следует отметить, что даже незначительное превышение нормального количества протейной палочки в кишечной микрофлоре может негативно отразиться на состоянии здоровья. Так, если у человека имеются аутоиммунные болезни, существует высокий риск их обострения из-за возросшей активности протейной палочки. Атопический дерматит, астма, аллергические заболевания и другие иммунозависимые патологии могут впервые развиться или обостриться под воздействием бактерий Proteus.
Бактериальный вагиноз
Нормальная микрофлора влагалища женщин репродуктивного возраста является одним из показателей здоровья, так как играет большую роль в поддержании микроэкологического статуса. Взаимодействие между представителями нормальной микрофлоры и клетками вагиналь
Нормальная микрофлора влагалища женщин репродуктивного возраста является одним из показателей здоровья, так как играет большую роль в поддержании микроэкологического статуса. Взаимодействие между представителями нормальной микрофлоры и клетками вагинального эпителия осуществляется на клеточном и молекулярном уровнях и постоянно контролируется со стороны ряда систем макроорганизма. Результатом этого взаимодействия являются создание и поддержание высокой колонизационной резистентности вагинального эпителия к внедрению патогенных и условно-патогенных микроорганизмов [1–6].
Бактериальный вагиноз выделен из категории неспецифических вагинитов в отдельную нозологическую форму. К нему относят патологические состояния во влагалище, сопровождающиеся нарушениями качественного и количественного состава нормальной микрофлоры и не связанные с бактериальными инфекциями, передаваемыми половым путем (ИППП), грибами или простейшими.
Согласно современным представлениям, бактериальный вагиноз — инфекционный невоспалительный синдром полимикробной этиологии, который связан с дисбиозом вагинального биотопа. Нарушение микроэкологии влагалища при бактериальном вагинозе характеризуется резким снижением количества или отсутствием лактобактерий, продуцирующих перекись водорода и увеличением количества Gardnerella vaginalis, грамотрицательных анаэробных бактерий (Bacteroides spp., Mobiluncus spp., Fusobacterium spp., Peptostreptoicoccus spp., M. hominis, U. urealyticum).
Гарднереллы, как и лактобациллы, обладают выраженной способностью к адгезии на поверхности вагинальных эпителиоцитов. Gardnerella vaginalis могут продуцировать токсические биопродукты, к которым относятся муколитические ферменты и гемолизин, являющийся лейкотоксическим фактором. Гемолизин, воздействуя на эритроциты, вызывает образование многочисленных пор в эритроцитарной мембране, а также оказывает влияние на лейкоциты, вызывая их структурные и функциональные нарушения. Этим и объясняется отсутствие существенной лейкоцитарной инфильтрации, т. е. активности лейкоцитов в присутствии Gardnerella vaginalis.
Определенную роль в патогенезе бактериального вагиноза играют представители семейства Mycoplasmataceae — Mycoplasma hominis и Ureaplasma urealyticum. 70% выделенных штаммов Ureaplasma urealyticum относятся к биовару Parvo, 23,3% — к биовару Т960. Большинство пациенток, у которых была выделена Ureaplasma urealyticum, относящаяся к биовару Parvo, имели в прошлом раннее начало половой жизни, частую смену половых партнеров, наличие одновременно нескольких половых партнеров, большое количество беременностей и абортов, а также сопутствующие гинекологические заболевания и ИППП.
При обследовании половых партнеров пациенток с бактериальным вагинозом морфотипы ассоциированных с бактериальным вагинозом микроорганизмов выявлялись у 25% мужчин, при этом клинические проявления (баланопостит) наблюдались только у 3,1% [2].
В результате субмикроскопического исследования вагинального экссудата пациенток с бактериальным вагинозом определены структурно-функциональные особенности микробных клеток, участвующих во взаимодействии друг с другом, при этом клетки организма-хозяина представлены преимущественно плоским эпителием. Установлена грамвариабельность Gardnerella vaginalis вне зависимости от характера микробных ассоциаций. Анализ электронограмм продемонстрировал, что структурная организация Gardnerella vaginalis, адгезированных на поверхности эпителиальных клеток, не зависела от сочетания бактериального вагиноза с другими инфекционными агентами.
При сочетании бактериального вагиноза с Chlamydia trachomatis, Mycoplasma hominis, Ureaplasma urealyticum наблюдали значительное количество микроорганизмов в межклеточном пространстве и бактерий, морфологически идентичных микоплазмам [2].
Пациентки предъявляют жалобы на обильные выделения из половых путей белого или серого цвета, часто с неприятным запахом, особенно после полового акта или во время менструации. При длительно текущем процессе выделения приобретают желтовато-зеленую окраску, становятся более густыми, нередко напоминают творожистую массу, обладают свойством пениться; слегка тягучие и липкие, они равномерно распределяются по стенкам влагалища. Количество белей варьирует от умеренных до весьма обильных, составляя в среднем 20 мл в сутки. Жалобы на зуд и дизурические расстройства встречаются редко: они могут совсем отсутствовать или появляться периодически. Эти симптомы обнаруживаются у 16–23% пациенток с нарушениями микрофлоры влагалища. Характерным признаком бактериального вагиноза является отсутствие воспалительного процесса стенок влагалища. Нередко женщины с бактериальным вагинозом жалуются на обильное менструальное кровотечение, боли в низу живота. В то же время у части пациенток какие-либо субъективные ощущения отсутствуют.
Диагностика бактериального вагиноза основана на данных анамнеза, оценке субъективных и объективных симптомов заболевания, результатах лабораторных тестов — микроскопического исследования материала, аминного теста и рН вагинального экссудата [3].
При сборе анамнеза выясняют:
Диагноз бактериального вагиноза устанавливается на основании наличия трех критериев из нижеперечисленных:
Обследование пациентки следует проводить не ранее, чем через 72 ч после последнего полового контакта (без использования презерватива); оно не проводится также во время менструации. В течение 3 нед до обследования женщина не должна получать терапию системными и местнодействующими антибактериальными препаратами [3].
При микроскопическом исследовании нативного и окрашенного по Граму вагинального мазка определяются следующие признаки:
Оценка общей микробной обсемененности вагинального отделяемого проводится по 4-балльной системе — по числу микробных клеток, обнаруживаемых в одном поле зрения при иммерсионной микроскопии:
1 балл (+) — до 10 микробных клеток в поле зрения, незначительное их количество (скудный рост);
2 балла (++) — от 11 до 100 микробных клеток в поле зрения, умеренное их количество;
3 балла (+++) — от 100 до 1000 микробных клеток в поле зрения, большое их количество;
4 балла (++++) — более 1000 микробных клеток в поле зрения, массивное их количество.
Так как Gardnerella vaginalis может быть обнаружена у здоровых женщин, культуральное исследование и ПЦР-диагностику для идентификации Gardnerella vaginalis не проводят. Культуральное исследование проводят при наличии показаний для определения видового и количественного состава вагинального микроценоза и исключения возбудителей ИППП.
При культуральном исследовании могут быть обнаружены изменения, характерные для бактериального вагиноза: общая микробная обсемененность превышает 10 9 КОЕ/мл; при использовании только аэробных условий культивирования рост микроорганизмов отсутствует или наблюдается рост сопутствующих условно-патогенных микроорганизмов (чаще в небольшом титре); полимикробный характер микрофлоры с абсолютным преобладанием облигатно-анаэробных видов и Gardnerella vaginalis; отсутствие роста лактобацилл или резкое снижение их титра ( 4 КОЕ/мл).
На основании проведенных исследований в настоящее время рекомендуется в план ведения пациенток включать:
Целью лечения является уменьшение выраженности клинических симптомов, нормализация лабораторных показателей, предотвращение развития возможных осложнений в период беременности, а также в послеродовом периоде и при выполнении инвазивных гинекологических процедур.
Результаты лабораторных исследований в норме следующие.
Лечение
Основное направление терапии — применение местных или системных антибактериальных препаратов с антианаэробным эффектом.
Показано применение клиндамицина. Препарат является 7-дезоксипроизводным линкомицина, ингибирует синтез белков в микроорганизмах, оказывает бактериостатическое или бактерицидное действие в зависимости от концентрации в макроорганизме и чувствительности микроорганизма. Препарат эффективен в отношении грамположительных микроорганизмов (стафилококков, стрептококков, пневмококков, палочки дифтерии), гарднерелл, микоплазм. Устойчивость микроорганизмов к клиндамицину вырабатывается медленно. При приеме внутрь клиндамицин всасывается лучше, чем линкомицин. После внутримышечного введения максимум его концентрации в крови отмечается через 2–2,5 ч. Препарат хорошо проникает в жидкости и ткани организма, выводится с мочой и желчью. При нарушении функции почек и печени выведение клиндамицина замедляется. При бактериальном вагинозе можно назначать одну из лекарственных форм клиндамицина: крем 2%-ный 5 г в аппликаторе (разовая доза) интравагинально 1 раз в день (на ночь) в течение 6 дней; овули 100 мг интравагинально на ночь в течение 3 дней; капсулы 300 мг внутрь 2 раза/сут в течение 7 дней.
Клиндамицин разрешенн к применению у беременных в виде 2%-го крема 5 г (разовая доза) интравагинально 2 раза/сут в течение 5 дней.
Также при бактериальном вагинозе можно назначать метронидазол. Он обладает широким спектром действия в отношении простейших, подавляет развитие Trichomonas vaginalis, Entamoeba histolytica и лямблий. В отношении анаэробных бактерий препарат высокоэффективен. Метронидазол хорошо всасывается при приеме внутрь, проникает в органы и ткани, проходит через плаценту и гематоэнцефалический барьер, накапливается в печени. Период полувыведения препарата составляет 8–10 ч, полностью выводится из организма через 1–2 сут после введения. Метронидазол в основном выводится с мочой в неизмененном виде и в виде метаболитов, частично — с калом. При применении метронидазола могут отмечаться потеря аппетита, сухость и неприятный вкус во рту, тошнота, рвота, диарея, головная боль, крапивница, зуд. Эти явления проходят после окончания лечения или отмены препарата. Возможна лейкопения. Препарат противопоказан при беременности и кормлении грудью, нарушениях кроветворения, остром течении заболеваний центральной нервной системы. Во избежание развития тяжелых побочных реакций следует предупреждать пациентов о недопустимости приема алкоголя и содержащих его продуктов как в ходе терапии метронидазолом, так и в течение 24 ч после ее окончания. При бактериальном вагинозе можно применять одну из следующих схем лечения с использованием метронидазола:
Также используют и другие производные метронидазола:
Ранее было проведено сравнительное изучение эффективности местнодействующих пробиотиков. Поскольку не было выявлено достоверных отличий в результатах лечения у пациенток, получавших и не получавших эти средства, в настоящее время их не рекомендуют при лечении бактериального вагиноза [3].
При сочетании бактериального вагиноза с ИППП, одновременно применяют антибактериальные препараты в соответствии с нозологической формой заболевания [2]. При неосложненной гонорейной инфекции назначают цефтриаксон однократно внутримышечно в дозе 250 мг (препарат является цефалоспориновым антибиотиком III поколения; после внутримышечного введения пик концентрации в крови отмечается через 1,5 ч; из организма выводится медленно). При обнаружении хламидий и/или микоплазм показано применение антибиотиков — макролидов, тетрациклинов.
Высокий терапевтический эффект, хорошая переносимость способствовали значительному распространению применения макролидов. Их антимикробный эффект обусловлен нарушением синтеза белка в рибосомах микробной клетки. Как правило, макролиды оказывают бактериостатическое действие, но в высоких концентрациях способны вызывать и бактерицидный эффект. Кроме антибактериального действия, макролиды обладают умеренной иммуномодулирующей и противовоспалительной активностью. Представителем III поколения макролидов является джозамицин (Вильпрафен). Этот антибиотик быстро абсорбируется из желудочно-кишечного тракта (ЖКТ), хорошо проникает через биологические мембраны и накапливается в тканях. Максимальная концентрация достигается через 1–2 ч после приема. Через 45 мин после приема дозы 1 г средняя концентрация джозамицина в плазме составляет 2,41 мг/л; связывание с белками плазмы не превышает 15%. Прием препарата с интервалом в 12 ч обеспечивает сохранение эффективной концентрации джозамицина в тканях в течение суток. Равновесное состояние достигается через 2–4 дня регулярного приема. Концентрация джозамицина в полиморфонуклеарных лейкоцитах человека, моноцитах и альвеолярных макрофагах примерно в 20 раз выше, чем в других клетках организма. Препарат биотрансформируется в печени до менее активных метаболитов. Джозамицин выводится главным образом с желчью, выведение же с мочой составляет менее 20%. Препарат назначается по 500 мг 2 раза в день в течение 10 дней.
Из группы тетрациклинов при ИППП наиболее эффективен доксициклин; в последние годы широко применяется Юнидокс Солютаб. Препарат отличается от Доксициклина гидрохлорида нейтральной реакцией, оказывает меньшее раздражающее действие на слизистую оболочку пищеварительного тракта и обладает улучшенными противомикробными и фармакокинетическими свойствами. Юнидокс Солютаб блокирует рибосомальную полимеразу и тормозит синтез белка в микроорганизмах.
Таблетки Юнидокс Солютаб обладают контролируемой растворимостью. Их можно не только принимать внутрь целиком или по частям, но и быстро приготовить из них сироп, суспензию (растворив таблетку в 20 мл воды) или раствор (растворив таблетку в 100 мл воды), которые обладают приятным вкусом. Таблетки растворяются в воде в течение 5–10 с, в биологических жидкостях — в течение 1 мин, превращаясь в равномерную суспензию.
Юнидокс Солютаб всасывается полностью. Биодоступность препарата составляет 95%. Через 2 ч после приема (200 мг в первый день и 100 мг в последующие дни) уровень в сыворотке составляет от 1,5 до 3 мг/мл. Препарат на 80–90% связывается с белками плазмы, хорошо проникает в ткани, накапливается в ретикулоэндотелиальной системе. Период полувыведения составляет 16–18 ч, после приема повторных доз — 22–23 ч.
Ранее были отмечены преимущества, заключающиеся в отсутствии побочных эффектов по типу эзофагитов, встречающихся при применении обычных форм Доксициклина гидрохлорида, способности накапливаться в высоких концентрациях в репродуктивных органах и активно воздействовать на инфекционный агент.
Юнидокс Солютаб назначают в дозе 200 мг в течение 10 дней.
Лабораторный контроль эффективности терапии следует проводить непосредственно по окончании этиотропного лечения: при микроскопии вагинальных мазков, окрашенных по Граму, необходимо констатировать степень эрадикации микроорганизмов, ассоциированных с бактериальным вагинозом; при посеве вагинального отделяемого — выявлять случаи колонизации факультативно анаэробными условно-патогенными микроорганизмами.
При сочетании бактериального вагиноза с урогенитальным хламидиозом и/или микоплазмозом лабораторный контроль необходимо повторить через 3 нед по окончании терапии.
По вопросам литературы обращайтесь в редакцию.
И. В. Хамаганова, доктор медицинских наук, профессор
РГМУ, Москва
