Proteus spp что это в моче
Proteus spp. (качественный метод)
Описание исследования
Proteus spp. – это род грамотрицательный факультативных анаэробных не образующих спор бактерий, представляющих нормальную, условно-патогенную флору кишечника. Патогенными для человека являются три вида протей – Proteus mirabilis, Proteus vulgaris и Proteus penneri, причем наиболее часто заболевания вызывает Proteus mirabilis.
Протеи похожи на мелкие нитевидные палочки, которые очень активно двигаются. Патогенное действие бактерий объясняется способностью вырабатывать эндотоксин и разрушать красные клетки крови (эритроциты). Кроме того, протеи обладают способностью вырабатывать уреазу – фермент, разлагающий мочевину (уреаза продуцируется также Хеликобактер пилори, что, при заселении протеями верхних отделов желудочно-кишечного тракта, может стать причиной ложноположительного результата при обследовании на инфицирование Helicobacter pylori). В результате реакции выделяется аммиак, способствующий образованию в почках фосфатных камней, микрогнойников, вызывающий некроз (отмирание) почечных тканей, снижение местного иммунитета. Поражение протеями происходит только в случае выхода бактерий за пределы нормальной среды обитания (желудочно-кишечного тракта). Они провоцируют развитие острых кишечных инфекций, которые протекают в форме:
Характерными признаками кишечных инфекций являются следующие симптомы:
Чаще всего кишечные инфекции развиваются у маленьких детей с пониженным иммунитетом. Также заболевание может возникнуть при бесконтрольном приеме антибиотиков.
Поражение протеем урогенитальных путей и почек может привести к развитию:
Кроме вышеперечисленного, Proteus spp. может стать причиной:
Заражение инфекцией может произойти:
Количество протей является показателем санитарного состояния среды. Наличие Proteus mirabilis рассматривают как показатель фекального загрязнения, а Proteus vulgaris —загрязнения объекта органическими веществами.
Данное исследование проводится методом полимеразной цепной реакции в режиме реального времени. В рамках теста исследуется соскоб эпителиальных клеток урогенитального тракта, задней стенки глотки, сперма, моча.
Подготовка к исследованию
Соскоб урогенитальный (цервикальный канал, влагалище, уретра)
Соскобы у женщин отбираются не ранее пятого дня от начала менструального цикла и не позже пятого дня до предполагаемой даты следующей менструации. Если наблюдаются явные признаки заболевания, отбор пробы проводится непосредственно в день обращения.
Требования по подготовке к тестированию:
Проба не отбирается:
Мочеиспускательный канал (уретра)
У лиц обоего пола проба отбирается не ранее чем через 14 дней после применения антибиотиков местного действия и 30 дней после перорального приема противобактериальных средств.
За неделю до манипуляции рекомендуется прекратить прием всех медицинских препаратов. Если отказ от лечения невозможен, то пациенту необходимо поставить об этом в известность специалиста, направляющего его на обследование.
При отборе эпителиальных клеток из мочеиспускательного канала, манипуляция проводится перед мочеиспусканием или через 2-3 часа после него (при обильных выделениях из уретры у мужчин – через 1 час).
Соскоб с задней стенки глотки
Перед отбором биологического материала необходимо учесть следующее:
При подготовке к взятию соскоба:
Перед проведением соскоба необходимо прополоскать рот, используя для этого воду комнатной температуры.
Для получения корректного результата тестирования все эти условия необходимо соблюсти в точности. Лечащий врач может рекомендовать иные условия проведения обследования.
Сперма
Отбор материала с целью диагностики проводится до начала противобактериального, антивирусного и противопаразитарного лечения, химиотерапии, а также до лечебных или диагностических мероприятий в месте предполагаемой локализации агента инфекции. После курса лечения проба отбирается не ранее, чем через 10-14 дней при проведении локальной терапии и через 30 дней после перорального приема антибиотиков.
На анализ собирается порция первой утренней мочи, выделенной не ранее, чем через 2-3 часа после предыдущего (ночного) мочеиспускания. Ее объем должен составлять порядка 20-30 мл. Емкость, используемая для сбора биоматериала – стерильный медицинский контейнер.
Моча собирается либо до проведения химиотерапии или лечения антибиотиками, либо через месяц после окончания курса лечения.
Перед началом манипуляции необходимо тщательно обмыть гениталии. Женщинам желательно воспользоваться гигиеническим тампоном во избежание попадания в пробу слизи из влагалища. Во время менструации материал не собирается.
После наполнения контейнера на треть-половину объема, емкость с мочой плотно закрывается крышкой, дабы избежать ее вытекания.
Доставка биоматериала должна быть организована в течение максимум 6 часов. До отправки в лабораторию моча может храниться как в холодильнике (при t⁰ от +2⁰С – замораживать ее нельзя), так и в комнате, но при этом температура не должна быть выше +25⁰С.
Показания к исследованию
Интерпретация исследования
Данный тест – качественный, результат выдается в формулировках «обнаружено» или «не обнаружено».
Нормой является отсутствие в исследуемой пробе специфических фрагментов ДНК Proteus spp.
Результат анализа выдается на бланке лаборатории медицинской компании «Наука». Пример результата по данному анализу представлен ниже:
Ф.И.О.: Иванов Иван Иванович Пол: м Год рождения: 01.01.0000
Дата исследования: 12.12.0000
Proteus spp. как предполагаемый патоген желудочно-кишечного тракта
Виды Proteus являются членами семейства бактерий Enterobacteriaceae. Чаще всего они распознаются клинически как причина инфекций мочевыводящих путей. Хотя Proteus spp. обычно считаются комменсалами желудочно-кишечного тракта (ЖКТ), их численность в процентном отношении к микробному сообществу очень низка (± 0,05%). В результате их обнаружение при болезненных состояниях с использованием профилей 16S и, возможно, метагеномики, возможно, привело к появлению Proteus spp. невозможно обнаружить из-за пороговых значений биоинформатической численности.
Недавняя идентификация Proteus spp. в качестве потенциальных патогенов при рецидиве болезни Крона после резекции кишечника служит стимулом для изучения их потенциальной роли в качестве кишечных патогенов. Этот обзор направлен на предоставление обзора рода Proteus с точки зрения его известных факторов вирулентности, а также на сопоставление доказательств, касающихся роли Proteus spp. в патофизиологии желудочно-кишечных заболеваний.
Характеристика рода Proteus.
Proteus spp. грамотрицательные бактерии, принадлежащие к семейству Enterobacteriaceae.и являются общими комменсалами микробиоты желудочно-кишечного тракта. Первые изоляты были описаны и охарактеризованы Хаузером в конце 19 века. В настоящее время род состоит из Proteus mirabilis, P. vulgaris, P. penneri, P. hauseri, P. terrae и P. cibarius, а также безымянных геномовидов 4, 5 и 6. У человека все нынешние представители этого рода, за исключением P. cibarius и P. terrae, были выделены из клинических образцов. Обычно кишечник человека заселен различными комбинациями P. vulgaris, P. mirabilis и P. penneri, но они составляют менее 0,05% кишечной микробиоты здоровых людей. В то время как Proteus spp. широко признаны патобионтами, а кишечник является резервуаром этих бактерий, исследования этого рода были сосредоточены на их роли в инфекциях мочевыводящих путей, а не в кишечных проявлениях.
Многие недавние исследования кишечного «микробиома» в отношении здоровья и болезней показали, что есть серьезные изменения в относительных пропорциях ключевых бактериальных таксонов, связанных с активным заболеванием, которое обычно называют «дисбактериозом». Одним из отличительных признаков дисбактериоза при воспалительных заболеваниях кишечника (ВЗК) является увеличение популяции типа Proteobacteria, в частности Enterobacteriaceae. Другим родам семейства Enterobacteriaceae, таким как Escherichia, Shigella, Salmonella и Klebsiella, уделялось должное внимание в этом отношении, а Proteus не был всесторонне исследован.
Виды Proteus представляют собой короткие (1,5–2 мкм) прямые стержни, которые демонстрируют диморфизм в виде «плавающих» и «роящихся» форм, как и некоторые другие представители семейства Enterobacteriaceae.
Proteus spp. в верхних отделах желудочно-кишечного тракта
Колонизация верхних отделов желудочно-кишечного тракта, включая пищевод и желудок.
Ач, вызванные видами Proteus у младенцев и пожилых людей, часто связаны с инструментарием ротоглотки. У 13 младенцев с зондами для кормления без желудочно-кишечных симптомов Proteus был изолирован из горла у 8% пациентов, из желудочного сока у 15% пациентов и из двенадцатиперстной кишки у 8% пациентов. У пожилых пациентов с назогастральным питательным зондом (NGT) виды Proteus были изолированы из ротоглотки у 24% пациентов и из желудочной жидкости у 26% пациентов. В другом исследовании колонизация ротоглотки видами Proteus присутствовала у 13% пациентов с чрескожной эндоскопической гастростомией (PEG) и 21% пациентов с NGT, а колонизация желудка присутствовала у 4% и 23% тех же пациентов. соответственно
Связь с гепатобилиарной болезнью.
Ранние культуральные исследования пациентов, перенесших хирургические операции на желчных путях, показали случайную изоляцию видов Proteus из желчных путей (13% образцов желчи). P. mirabilis также был выделен из желчи, полученной во время эндоскопической ретроградной холангиопанкреатографии (ERCP) в 6% культивированных образцов.
В метагеномном анализе с использованием многоточечного пиросеквенирования ректосигмоидное слизистое сообщество здоровых людей сравнивалось с таковым у пациентов с циррозом печени. Пациенты с циррозом имели повышенную долю видов Proteus по сравнению с контрольной группой; относительное количество у здоровых контролей составляло 0,0% по сравнению с 0,1% у пациентов с циррозом печени (P 0,00001). Микробы, продуцирующие уреазу, такие как Proteus spp., В кишечнике, как известно, вносят вклад в патогенез печеночной энцефалопатии за счет разложения мочевины до аммиака и угольной кислоты.
Виды Proteus являются выносливыми, адаптируемыми и потенциально патогенными обитателями желудочно-кишечного тракта человека и недооцениваются как причина желудочно-кишечных заболеваний. Взаимодействие микробов-хозяев и микробов-микробов с помощью Proteus spp., А также патогенность этого рода, которая может быть результатом увеличения популяции в ответ на изменения окружающей среды, становятся важными аспектами болезней, связанных с этим родом. Возможный вклад Proteus spp. кишечным заболеваниям и инфекциям уделяется некоторое внимание. Исследование вирулентности Proteus spp. в мочевыводящих путях, используя бактериологию подвздошных каналов и сегментов кишечника для увеличения мочевого пузыря, позволяет предположить, что Proteus spp. следует более внимательно изучить их потенциал в качестве возбудителей заболеваний желудочно-кишечного тракта.
Появляется все больше свидетельств того, что виды Proteus могут играть роль в воспалительных заболеваниях кишечника через прямое действие бактерий, усугубляемое уклонением и нарушением иммунной системы хозяина. Как грамотрицательные организмы, виды Proteus по своей природе обладают провоспалительным действием в результате продукции липополисахаридов (ЛПС) и иммуностимулирующих белков флагеллина. Может быть связь между видами Proteus и воспалительным заболеванием кишечника, особенно болезнью Крона, в основном за счет роста популяции и активации иммунной системы. Их низкая численность популяции не исключает потенциально большого патогенного воздействия.
Генетическая характеристика кишечных изолятов по сравнению с изолятами мочевыводящих путей будет важна для определения влияния факторов вирулентности на патогенез желудочно-кишечного тракта.
Исследования микробиома кишечника как экосистемы дают нам представление о видах Proteus, но все еще остаются без ответа вопросы. К ним относятся получение подтверждения того, что виды Proteus могут роиться в кишечнике человека, и устранение влияния индивидуальных изменений окружающей среды (например, хирургическое вмешательство, pH или концентрация кислорода) на популяцию Proteus, связанную со слизистой оболочкой.
Proteus (протей, род бактерий)

Протей. Общие сведения
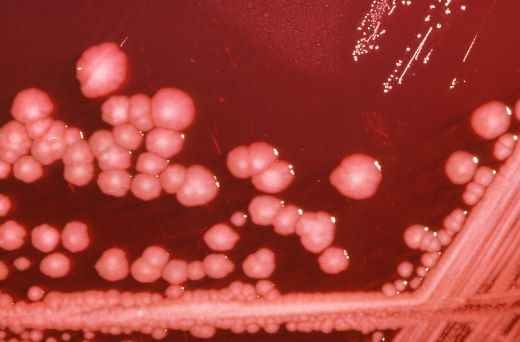
Протеи имеют вид мелких, 0,3 на 3 мкм, нитевидных палочек. Они отличаются очень активной подвижностью. Протеи обладают токсическими (вырабатывают эндотоксин) и гемолитическими свойствами.
Протеи считаются санитарно-показательными бактериями. Количество обнаруживаемых Proteus mirabilis рассматривают как показатель фекального загрязнения, а Proteus vulgaris — как показатель загрязнения объекта органическими веществами.
В зависимости от способности продуцировать индол, протеи делятся на индол-отрицательные (Proteus mirabilis, Proteus hauseri, Proteus penneri) и индол-положительные (Proteus vulgaris, Proteus inconstans и другие).
Протеи способны продуцировать уреазу, в связи с чем при заселении верхних отделов желудочно-кишечного тракта протеем увеличивается вероятность ложноположительных результатов при дыхательных уреазных тестах с изотопом 1ЗС и других с целью выявления Helicobacter pylori-инфекции (Стандарты диагностики и лечения. ).
Протей и заболевания человека
Три вида из рода протей — Proteus mirabilis, Proteus vulgaris и Proteus penneri являются патогенными для человека, причем 75–90 % инфекций вызывает Proteus mirabilis.
Наиболее часто острые кишечные инфекции, вызываемые протеем, встречаются у детей раннего возраста: ослабленных или с пониженным иммунитетом. Причиной протейной инфекции также может быть бесконтрольный прием антибиотиков. Заболевание обычно протекает в виде гастроэнтерита, гастрита и колиэнтерита. Очень часто острые кишечные протейные инфекции сопровождается повышением температуры, рвотой, нарушением аппетита, кратковременными судорогами, наблюдается также изменение характера стула и его учащение.
Бактерии рода протей, наряду с другими микроорганизмами, могут вызывать заболевания мочевыводящих путей и почек человека, в частности, острый и хронический простатит, цистит, пиелонефрит, в том числе большинство ксантогранулематозных пиелонефритов. Proteus mirabilis является причиной раневых инфекций. Proteus vulgaris присутствует в кишечнике здорового человека и многих животных, он обнаруживается в навозе, почве и загрязненных водах.
Proteus spp. высевается из тканей анального канала у больных с хронической анальной трещиной (Адиев Р.Ф., Малеева Е.А.).
Proteus spp. ассоциируются с воспалительными заболеваниями кишечника (ВЗК) и целиакией (Proteus mirabilis), острым гастроэнтеритом, хронической анальной трещиной, простатитом, циститом, пиелонефритом (Карпеева Ю.С. и др.).
Протей в результатах анализа кала на дисбактериоз
Протей обнаруживается в кале у 2,0±0,5 % здоровых людей, причем среднее содержание в 1 г кала от 1600 до 4000 КОЕ протея (М.Д.Ардатская, О.Н.Минушкин).
Терапия при избыточном росте протея
Приказом Минздрава РФ № 231 от 9 июня 2003 г. Об утверждении отраслевого стандарта «Протокол ведения больных. Дисбактериоз кишечника» при избыточном росте протея (proteus mirabilis, proteus vulgaris) детям рекомендованы бактериофаги «Интести-бактериофаг жидкий», «Бактериофаг протейный жидкий», «Бактериофаг колипротейный жидкий», «Колипротеофаг в таблетках», «Пиобактериофаг комбинированный жидкий», «Пиополифаг в таблетках», «Пиобактериофаг поливалентный очищенный жидкий».
На сайте GastroScan.ru в разделе «Литература» имеется подраздел «Микрофлора, микробиоценоз, дисбиоз (дисбактериоз)», содержащий статьи, затрагивающие проблемы микробиоценоза и дисбиоза отделов ЖКТ человека.
Протей в анализе мочи
Бактериурия — наличие бактерий в моче может является признаком воспаления в мочевыводящих путях, мочевом пузыре, почках. При отсутствии каких-либо симптомов, истинная бактериурия (инфекция мочевых путей) диагностируется при наличии не менее 10 5 микробных тел протеев (или других энтеробактерий) в 1 мл свежевыпущенной мочи, иначе предполагается, что загрязнение мочи происходит при ее заборе. Если бактериурия не сопровождается какими-либо симптомами, тогда она называется бессимптомной бактериурией. Бессимптомная бактериурия не всегда требует немедленного лечения.
При наличии симптомов или при заборе мочи катетером диагностический порог может быть значительно уменьшен. В частности, при наличии соответствующей клинической симптоматики (лихорадка, озноб, тошнота, рвота, боли в поясничной области, дизурия) и выделении не менее 10 лейкоцитов в 1 мкл мочи, критерием для диагностики острого пиелонефрита является наличие не менее 10 4 протеев (или других патогенных энтеробактерий) в 1 мл свежевыпущенной мочи.
Активность антибиотиков в отношении протея
Протей в систематике бактерий
Род протей (Proteus) входит в семейство Morganellaceae, порядок Enterobacteriales, класс γ proteobacteria), тип Proteobacteria, царство Бактерии.
Род протей включает следующие виды: Proteus cibarius, Proteus hauseri, Proteus inconstans, Proteus mirabilis, Proteus penneri, Proteus terrae, Proteus vulgaris.
До недавнего времени род протей входил в семейство энтеробактерии (Enterobacteriaceae), которое также относиться к порядку энтеробактерии (Enterobacteriales).
Ранее относящиеся к роду протей бактерии вида Proteus morganii реклассифицированы в Morganella morganii, Proteus myxofaciens — в Cosenzaea myxofaciens, а Proteus rettgeri реклассифицирован в Providencia stuartii и Providencia rettgeri (всё в пределах семейства Morganellaceae).
На верхней иллюстрации — протей вида Proteus penneri.
Дисбиоз мочеполовой системы (уретрит)
Описание исследования
На момент рождения мочеиспускательный тракт мальчиков стерилен. Однако его заселение начинается буквально с первых минут жизни. «Стартовой площадкой» для проникновения представителей микрофлоры внутрь являются кожа и слизистые оболочки.
Микроорганизмы, составляющие нормальную микрофлору мочеиспускательного канала, заселяют его начальный отрезок (порядка 5 см от наружного отверстия). Особенно большое количество микроорганизмов скапливается в области ладьевидной ямки, промываемой мочой хуже, чем весь остальной урогенитальный тракт.
Как показывают мазки на микрофлору, в уретре здоровых мужчин могут присутствовать следующие микроорганизмы:
Количество представителей нормальной микрофлоры в нижних отделах мочеиспускательного канала невелико. Однако ряд факторов могут спровоцировать их патологический рост, а также рост патогенных бактерий. Данное состояние определяется как дисбиоз половых органов мужчин.
Причинами его возникновения могут быть:
1. Проникновение в уретру при половых контактах болезнетворных микроорганизмов. Особенно велика опасность заражения для лиц, ведущих беспорядочную половую жизнь. Риск развития дисбиоза велик также для тех мужчин, чьи постоянные половые партнерши имеют нарушение в микрофлоре влагалища.
2. Резкое и значительное ослабление иммунитета. Иммунная система организма четко контролирует количество микробов. При их усиленном размножении специальные защитные клетки стабилизируют число бактерий, приводя их в норму. Однако различные инфекции, травмы, переохлаждение, применение ряда лекарственных средств ослабляют иммунную защиту, что становится причиной неконтролируемого размножения бактерий и, как следствие, развития дисбиоза.
3. Повышение температуры в мужских половых органах. Обычно температура в них относительно низкая. Однако воспалительные процессы в малом тазу могут привести к повышению местной температуры, что вызывает стремительный рост кокков и палочек.
4. Нарушение функций предстательной железы. Секрет простаты содержит ряд веществ, обладающих антибактериальными свойствами. При снижении функциональности простаты (например, гормональной недостаточности), нерегулярной половой жизни и влиянии прочих факторов нарушается процесс естественного очищения мочеиспускательного канала от лишних микроорганизмов, что становится причиной нарушения микрофлоры уретры.
5. Нарушение кровообращения в малом тазу. Снижение скорости тока крови и ее застой также вызывает местное повышение температуры, создавая тем самым благоприятные условия для усиленного размножения микробов. Это может наблюдаться:
6. Травма стенок уретры. Она может быть получена при неквалифицированном отборе мазков или введении катетера, при мочекаменной болезни во время прохождения по каналу песка и камней.
7. Несбалансированное питание и неправильный питьевой режим. Избыток кислой, острой пищи, алкоголя может стать причиной химического поражения стенок мочеиспускательного канала, что служит причиной для развития болезни. Недостаток жидкости приводит к тому, что мочеиспускание происходит реже, а, следовательно, бактерии, которые могли бы вымыться струей мочи, остаются в уретре.
8. Отсутствие полноценного отдыха. Усиленные физические нагрузки, вызывающие хроническую усталость, могут стать причиной снижения иммунной защиты организма в целом, и уретры в частности.
9. Наличие хронических заболеваний. Возбудители болезни могут попадать в уретру с кровотоком из любой части организма, что может послужить причиной развития инфекции в ней.
Основными симптомами уретрита являются:
У мужчин они проявляются значительно чаще, чем у женщин. Проявления заболевания могут быть острыми или носить «смазанных» характер (что свойственно хронической формы инфекции).
Само по себе заболевание не является опасным, однако отсутствие лечения может привести к весьма неприятным осложнениям:
В рамках данного теста проводится выявление в микрофлоре уретры следующих микроорганизмов:
Исследование проводится методом полимеразной цепной реакции в режиме реального времени. Цель тестирования – выявление в пробе мочи специфических фрагментов ДНК перечисленных выше микроорганизмов.
Подготовка к исследованию
Для проведения анализа отбирается первая утренняя моча в объеме 10-15 мл. Пациенту необходимо получить в пункте забора проб медицинской компании «Наука» или приобрести в аптеке одноразовый пластиковый контейнер.
Перед сбором мочи необходимо провести тщательную гигиену половых органов. Накануне необходимо исключить из рациона питания фрукты и овощи, изменяющие цвет мочи (морковь, свеклу).
Для получения корректных результатов исследования необходимо исключить прием витаминов. Перед проведением тестирования запрещено принимать мочегонные препараты.
Показания к исследованию
Интерпретация исследования
Результаты обследования выдаются на бланке лаборатории медицинской компании «Наука». В столбце «результат» в формулировках «обнаружено» или «не обнаружено» указывается наличие/отсутствие в исследуемой пробе следующих видов бактерий:
В столбце «Нормы интерпретации» содержится информация о референсных для данного исследования значениях. Нормой является отсутствие всех перечисленных видов микроорганизмов (результат «не выявлено»).
Положительный ответ свидетельствует о наличии в моче специфических фрагментов ДНК микроорганизмов и заражении выявленными бактериями.
Отрицательный результат может означать, что:
Пример по данному анализу представлен ниже:
Ф.И.О.: Иванов Иван Иванович Пол: м Год рождения: 01.01.0000
Дата исследования: 12.12.0000
Семейство Enterobacteriaceae. Часть 1
Автор: врач – клинический фармаколог Трубачева Е.С.
.jpg)
Автор: врач – клинический фармаколог Трубачева Е.С.
Morganella spp. и Proteus spp.
Особо выдающихся представителей семейства Enterobacteriaceae мы уже разбирали в отдельных статьях, а именно представительницу рода Esherichia — кишечную палочку E.coli, а также одну из представительниц клебсиелл — Klebsiella pneumonia. В ближайших статьях мы постараемся осветить все оставшееся семейство, как, во-первых, одно из самых проблемных в плане развития резистентности к антимикробным препаратам, а во-вторых — как возбудителей, наиболее часто являющихся причиной внутрибольничных инфекций.
Микробиологические аспекты
Основными клинически значимыми представителями родов семейства Enterobacteriaceae, вызывающими заболевания у человека, являются:
Естественно совсем уж экзотику мы рассматривать не станем, но по наиболее часто встречающимся представителям обязательно пробежимся.
Клинические аспекты
Почему данное семейство так актуально? Наверное, потому, что почти ни одна нозология не обходится без его представителей. В самом широком смысле семейство Enterobacteriaceae является причиной следующих заболеваний:
Как мы видим, наши знакомые отметились практически везде. Но надо обязательно помнить, что выявление вышеуказанных представителей у здоровых людей из респираторного тракта, урогенитального и уж тем более желудочно-кишечного ни в коем случае не говорит о том, что человек чем-то болен, так как в большинстве своем эти микробы являются представителями нормальной микрофлоры, а не все люди умеют мыть руки, особенно летом.
Когда можно думать о наличии бактериальной патологии? Во-первых, когда имеется четкая клиника, во-вторых, когда микробы выделены из стерильных в норме сред, таких как кровь и ликвор, брюшная или плевральная полость, точнее, экссудат оттуда и, в-третьих, когда микроорганизмы выделены в клинически значимых концентрациях (тут в помощь будет ваша бак. лаборатория).
Стоит отметить еще один немаловажный момент — не все представители семейства Enterobacteriaceae умеют жить вне организма человека, и поэтому не размножаются во внешней среде, а потому обнаружение оных на пищевых продуктах и всевозможных поверхностях в лечебных учреждениях говорит о фекальном загрязнении, проще говоря, о неумении обрабатывать руки после посещения туалетной комнаты. Одним из таких микробов-детекторов является кишечная палочка, и стоит ее поймать даже не на руках персонала, а, например, на компьютерной мышке, как дальше можно уже ничего не искать, а начинать очередной этап избиения младенцев, пардон, обучения правилам асептики и антисептики, в частности, обработки рук.
Но давайте перейдем к частностям — и первым микроорганизмом, который будем сегодня рассматривать, станет:
Morganella spp.
Зверюшка названа так в честь своего первооткрывателя Гарри Р. Моргана.
Начнем традиционно с микробиологических аспектов
Семейство морганелл включает единственный вид M. morganii, включающий два подвида M. morganii и M. sibonii, которые различаются только ферментацией трегалозы.
Морганеллы являются представителями нормальной микрофлоры как человека, так и животных, а потому могут присутствовать в качестве сапрофитов в окружающей (внебольничной!) среде.
Морганеллы имеют довольно сложные отношения с антибактериальными препаратами и обладают природной резистентностью к:
Проявляют высокую чувствительность к:
Клинические аспекты
Как говорилось выше, морганеллы являются частью нормальной микрофлоры человека, крайне редко вызывая инфекционные заболевания. Чаще всего они являются возбудителями осложненных инфекций мочевыводящих путей.
Факторами риска развития инфекции являются:
В качестве механизмов резистентности морганеллы способны продуцировать бета-лактамазы, чем и объясняется их природная устойчивость к пенициллинам и цефалоспоринам 1-2 поколений. При нерациональном использовании антибиотиков они начинают вырабатывать бета-лактамазы расширенного спектра и факторы устойчивости к фторхинолонам, которыми довольно бодро делятся с соседями по семейству Enterobacteriaceae. Отдельно стоит отметить способность отдельных штаммов морганелл к резистентности к имипенему.
Какие заболевания вызывают чаще всего:
Терапевтические аспекты
Антибактериальная терапия будет полностью зависеть от результата из микробиологической лаборатории. Повторимся еще раз, микроб изначально умеет вырабатывать бета-лактамазы, а потому в случае развития осложненных инфекции мочевыводящих путей, которые чаще всего уже не связанны с кишечной палочкой, препаратами выбора становятся карбопенемы (имипенем, если штамм к нему чувствителен, или меропенем), дозирование которых проводится с учетом клиренса креатинина. Длительность лечения должна быть не менее 7 дней. В качестве альтернативы можно использовать цефалоспорин 4-го поколения Цефипим каждые 8 часов или фторхинолоны.
Аминогликозиды, несмотря на чувствительность к оным, при лечении заболеваний мочевыводящих путей лучше не применять в виду их нефро- и отоксичности, и по этой же причине их невозможно будет использовать около трех месяцев после проведенной терапии, например, в лечении синегнойной инфекции. Цефалоспорины третьего поколения тоже применять не стоит, так как морганеллы довольно быстро обзаводятся бета-лактамазами расширенного спектра, которые, как мы помним, эту генерацию препаратов быстро инактивируют.
Proteus spp.
Микробиологические аспекты
Протей долгое время был практически родным отцом морганеллы, так как последняя рассматривалась как один из видов рода протей. Этот род примечателен тем, что занимает почетное второе место по выявляемости после кишечной палочки в семействе Enterobacteriaceae.
В данный момент представителями рода протей являются P. mirabilis, вызывающий порядка 90% инфекционных заболеваний, а также P. vulgaris и P. penneri.
Клинические аспекты
Протеи выступают возбудителями порядка 10% неосложненных инфекций мочевыводящих путей, с чем могут быть связаны неудачи в лечении последних с использованием аминопенициллинов.
Как и все клинически значимые возбудители семейства Enterobacteriaceae, протей является возбудителем нозокомиальных инфекций, таких как пневмония, вплоть до сепсиса. Кроме того выступает возбудителем интраабдоминальных, а также хирургических инфекций кожи и мягких тканей, сепсиса, связанного с медицинскими вмешательствами как последствий нозокомиальной пневмонии в результате недостаточной дезинфекции, например, бронхоскопов.
Таким образом, мы видим, что, как и в предыдущем случае, проще правильно помыть руки и обработать инструменты, чем лечить это все с учетом природной и приобретенной резистентности.
Терапевтические аспекты
Как и в случае с морганеллой, нам просто необходим результат микробиологического исследования с определением чувствительности по МПК возбудителя либо результаты микробиологического мониторинга, которые помогут предположить зверей в случае неудачи ранее проводимого лечения.
В случае ампициллин-чувствительного P.mirabilis именно ампициллин может выступать препаратом первой линии. Кроме того, возможно использование цефуроксима и фторхинолонов. Обязательным аспектом лечения является его длительность. В случае неосложненных инфекций мочевыводящих путей (цистита) — не менее 3 дней, пиелонефрита — 10–14 дней, осложненных инфекций — 10–21 день. Сепсис является состоянием, требующим индивидуального подхода, но лечим не менее 14 дней.
На этом на сегодня мы закончим, но повторим одну базовую и, чего уж, наиважнейшую истину: в лечении инфекций, связанных с любым представителем семейства Enterobacteriaceae, самым главным будет являться профилактика. А именно правильное и тщательное мытье рук. Обеспечим мытье рук, не будет большинства проблем с инфекциями, вызванными указанным семейством.