R75 диагноз у ребенка что это
Иммунодефицит у ребенка
Содержание статьи
Такой диагноз у детей означает, что поражен один или несколько элементов системы иммунитета. При такой патологии тяжело протекают инфекционные заболевания, часто проявляются аутоиммунные болезни, возникают опухоли, могут быть аллергии.
Виды заболеваний
Данный синдром может быть как первичным (генетически обусловленным), так и вторичным (появляется ввиду внешних факторов или заболеваний).
Первичный иммунодефицит у детей – что это и откуда берется?
Врожденный иммунодефицит (ИД) у ребенка – это то, что развивается из-за генетических факторов, это первичные нарушения работы иммунной системы. В результате развиваются тяжелые инфекции, быстро переходящие в хроническую форму, а органы и ткани поражаются воспалительными процессами. Без лечения первичный иммунодефицит приводит к смертности детей от осложнений различных инфекционных болезней.
Симптомы первичного иммунодефицита могут не обнаруживаться у детей, потому что болезнь не имеет уникальных признаков. Это может быть простая, но часто повторяющаяся инфекция, например легких или ЛОР-органов, или проблемы с ЖКТ, воспаления суставов. Часто ни родители, ни врачи не осознают, что все эти проблемы – результат дефекта иммунной системы ребенка. Инфекционные заболевания становятся хроническими, проявляются осложнения, нет реакции на курс антибиотиков. Обычно тяжелые формы иммунодефицита видны сразу после рождения младенца или через некоторое время. Источник:
Доан Тхи Май
Рецидивирующие инфекции у детей – риск иммунодефицита
// Педиатр, 2017, т.8, спецвыпуск, с.109-110
Важно отличать первичный иммунодефицит от СПИДа. Второй – это вирусное, приобретенное заболевание, а первичная форма уже «вживлена» в тело из-за генетических дефектов.
Почему у ребенка появляется вторичный иммунодефицит, и что это такое?
Такое заболевание – это тоже нарушение в работе иммунной системы, оно появляется у детей и взрослых и не является результатом дефектов в генах. Вторичный иммунодефицит может вызывать ряд факторов – внешних и внутренних. Любые внешние неблагоприятные факторы, которые нарушают процесс обмена веществ в организме, могут привести к развитию такой патологии. Самые распространенные из них:
Все эти факторы комплексно воздействуют на организм и все его системы, включая иммунную. А такие, как ионизирующее излучение, избирательно угнетают систему кроветворения. У людей, живущих в условиях загрязненности окружающей среды, снижен иммунитет, они чаще переносят инфекции, увеличиваются риски развития онкологии.
Диагностика ИД
Проводится сбор семейного анамнеза и жалоб ребенка (если он не новорожденный), осмотр, а также ряд лабораторных исследований: молекулярно-генетическое, клинический анализ крови и др.
Важно! Если в семье уже есть ребенок с первичной иммунной недостаточностью, то при вынашивании второго крайне важна пренатальная диагностика.
Признаки и симптомы первичного иммунодефицита обнаруживаются у детей уже в первые недели жизни. Когда врач собирает анамнез, особое внимание он обращает на частую заболеваемость вирусами и бактериальными инфекциями, на наследственность, отягощенную нарушениями работы иммунитета, на врожденные пороки развития.
Нередко такую патологию выявляют намного позже и случайно, когда проводят другие анализы.
Основные методы диагностики как врожденных, так и приобретенных нарушений работы иммунитета:
Лечение заболевания
Первичная форма заболевания предполагает:
Скорректировать иммунодефицит можно, применяя иммунореконструкцию, заместительное лечение, иммуномодуляторы. При первичной форме патологии применяют иммуноглобулины, при вторичной используют иммунотропы, заместительную терапию, иммунизацию.
Крайне важна при первичной патологии изоляция ребенка от всех источников заражения. Когда нет обострений инфекций, ребенок может вести нормальный образ жизни. При первичном иммунодефиците на фоне общей недостаточности антител детей нельзя прививать от:
Проживающим вместе с ребенком можно делать прививки только инактивированными вакцинами.
Противомикробное лечение заключается в приеме антибиотиков широкого спектра. При отсутствии быстрого ответа на терапию препарат меняют. Если же эффект есть, то принимать антибиотик ребенок должен минимум 3-4 недели. Лекарства вводятся внутривенно или парентерально. Одновременно назначают противогрибковые препараты и при показаниях – противовирусные, антипротозойные, антимикобактериальные лекарства. Противомикробная терапия может быть даже пожизненной.
При гриппе на фоне ИД обычно прописывают озельтамивир, ремантадин, занамивир, амантадин, ингибиторы нейраминидазы. Если ребенок заболел «ветрянкой» или герпесом, назначают ацикловир, парагрипп требует приема рибавирина. Перед стоматологическим лечением и операциями ребенок должен пройти курс антибиотиков для профилактики инфекции.
При серьезном вторичном или первичном Т-клеточном ИД нужно профилактировать пневмоцистовую пневмонию, в зависимости от показателей анализов крови. Для этого врачи обычно прописывают триметопримсульфометаксозол.
Важно! Любые лекарства должен назначать только врач, самолечение смертельно опасно для ребенка!
Способы коррекции недостаточности иммунитета:
Иммунореконструкция предполагает пересадку костного мозга или стволовых клеток, которые получают из пуповинной крови. При первичном ИД заместительная терапия – это чаще всего прием аллогенного иммуноглобулина, который в последние годы принято вводить внутривенно.
Лечение детей с первичным ИД с общими дефектами выработки антител
В этом случае проводится заместительная терапия иммуноглобулинами, которые вводятся внутривенно, и антибиотиками. Иммуноглобулины вводятся один раз в три-четыре недели пожизненно. Постоянная терапия антибиотиками нужна для профилактики бактериальных инфекций.
При обострении бактериальной инфекции назначаются антибиотики широкого спектра, вводимые парентерально. При гипер IgM-синдроме и общей вариабельной иммунной недостаточности (ОВИН) нужно постоянно принимать противогрибковые и противовирусные препараты. Они могут назначаться курсами. Это определяется врачом индивидуально. Если у ребенка Х-сцепленный гипер IgM-синдром, то ему показана пересадка костного мозга от HLA-идентичного донора.
Методы лечения вторичного ИД
В основном применяется иммунотропная терапия, которая может быть разных направлений:
Выбор иммунотропной терапии зависит от того, насколько остро выражен воспалительно-инфекционный процесс и какой иммунологический дефект выявлен. Когда симптомы болезни отступают, для профилактики может проводиться вакцинотерапия.
В качестве заместительной терапии применяются иммуноглобулины, вводимые внутривенно. Основное их действующее вещество – специальные антитела, получаемые от доноров. Часто назначаются иммуноглобулины, содержащие только IgG.
Иммунотропное лечение вторичного ИД
С помощью иммуномодуляторов можно повысить эффективность антимикробной терапии. Иммуномодуляторы должны быть частью комплексной терапии совместно с этиотропным лечением инфекции. Схемы и дозировку рассчитывает врач индивидуально.
Во время приема иммуномодуляторов должен проводиться иммунологический мониторинг. Если инфекция находится в острой стадии, иммуномодуляторы применяют с осторожностью. Иначе можно вызывать тяжелый общий воспалительный ответ и септический шок в результате него. Источник:
Г.А. Самсыгина, Г.С. Коваль
Проблемы диагностики и лечения часто болеющих детей на современном этапе
// Педиатрия, 2010, т.89, №2, с.137-145
Способы профилактики
ИД проще предупредить, чем лечить. Важно помнить, что состояние ребенка напрямую зависит от того, насколько правильно планировалась беременность. Если у одного из родителей есть проблемы с иммунитетом, он должен пройти специальные процедуры, чтобы исключить подобную патологию у ребенка.
В первые шесть месяцев жизни рекомендуется только грудное вскармливание, потому что в материнском молоке есть все нужные элементы, способствующие выработке полноценного иммунитета. Если нет лактации, нужны качественные искусственные смеси, но обязательно дополняемые поливитаминами.
Источники:
Врожденная ВИЧ-инфекция: клиника, диагностика, лечение
В настоящее время ВИЧ-инфекция у детей является одной из актуальнейших проблем во всем мире.
В настоящее время ВИЧ-инфекция у детей является одной из актуальнейших проблем во всем мире. Первоначально в нашей стране она была обусловлена внутрибольничной заболеваемостью, а в последние годы — рождением детей ВИЧ-инфицированными женщинами. Более 90% детской ВИЧ-инфекции является результатом именно перинатальной трансмиссии вируса.
Больные ВИЧ-инфекцией дети и их близкие нуждаются в профессиональной лечебно-реабилитационной поддержке их социального функционирования и оптимального качества жизни. Эта работа должна быть прежде всего направлена на «обновление взглядов» как на больных детей, так и их родителей. Очень важно не оставлять их в социальной изоляции, ведь порой вторичные проблемы негативно действуют на больного и его родственников не меньше, чем само заболевание.
По данным Федерального научно-методического центра по профилактике и борьбе со СПИДом, в России на 31 декабря 2006 г. зарегистрировано 2093 ребенка с подтвержденным диагнозом «ВИЧ-инфекция», из них 169 детей — в Москве [4].
По данным МГЦ СПИД за последние 10 лет произошло уменьшение числа детей с врожденной ВИЧ-инфекцией. Так, если в 2001 году, когда химиопрофилактика вертикальной трансмиссии ВИЧ-инфекции только начинала проводиться, число ВИЧ-инфицированных детей составляло 8%, то в 2006 году — всего 1,5%. Таких результатов удалось добиться благодаря введению в практику схемы профилактики согласно протоколу от 1996 г. PACTG 076 (Pediatric AIDS Clinical Trial Group), который основан на назначении беременной женщине Азидотимидина — антиретровирусного препарата из группы нуклеозидных ингибиторов обратной транскриптазы.
Однако даже своевременное проведение химиопрофилактики не исключает полностью возможность перинатальной передачи ВИЧ-инфекции от матери плоду.
К факторам, повышающим риск передачи ВИЧ от матери к ребенку, относятся:
При отсутствии профилактики перинатальной передачи ВИЧ, риск заражения составляет 30–40% [3].
Причинами отсутствия химиопрофилактики во время беременности и родов могут быть: диагностика ВИЧ-инфекции только во время родов, употребление наркотических веществ во время беременности, добровольный отказ от профилактики, в т. ч. по религиозным убеждениям, беременность до внедрения в практику профилактики вертикальной передачи ВИЧ и домашние роды.
Особенности клинических проявлений ВИЧ-инфекции у детей определяются стадией онтогенеза, на которой произошло инфицирование плода ВИЧ в организм (внутриутробно или интранатально) и от возраста ребенка в случае постнатального заражения.
При заражении плода в позднем перинатальном периоде или ребенка после рождения течение ВИЧ-инфекции почти не отличается от взрослых.
Целью данной работы является оценка эффективности общей и высокоактивной антиретровирусной терапии (ВААРТ) у детей с врожденной ВИЧ-инфекцией.
Задачи
Нами проанализированы 60 случаев врожденной ВИЧ-инфекции у детей в возрасте от 1 месяца до 7 лет, в т. ч.: 30 амбулаторных карт детей, состоящих на диспансерном учете в московском городском центре СПИД (МГЦ СПИД); 30 историй болезни детей, находящихся на стационарном лечении в МГЦ СПИД.
По результатам анализа амбулаторных карт и историй болезни нами были выявлены следующие наиболее часто встречающиеся клинические проявления врожденной ВИЧ-инфекции у детей: поражение ЦНС, лимфаденопатия, гепатолиенальный синдром, интерстициальные изменения в легких, анемия, гипотрофия, недоношенность.
Поражение ЦНС в нашем исследовании наблюдалось у 75% детей. Установлено, что ВИЧ является не только иммунотропным, но и нейротропным вирусом и проникает через гематоэнцефалический барьер на ранних этапах инфекционного процесса в организме, поражая олигодендроциты и астроциты, нейроциты, микроглию, макрофаги, клетки эндотелия кровеносных сосудов, фибробластоподобные клетки мозга. Указанные клетки имеют рецептор CD4 и считаются прямыми клетками-мишенями для ВИЧ. Патоморфологические изменения головного мозга при ВИЧ-инфекции могут быть охарактеризованы как альтернативно-дистрофические, с периваскулярным отеком, дистрофией нейронов, очаговой демиелинизацией и циркуляторными нарушениями.
У обследованных нами ВИЧ-инфицированных детей наблюдался полиморфизм клинических неврологических проявлений.
В начале заболевания отмечались астеноневротический и цереброастенический синдромы. Для этой стадии СПИДа характерной была ВИЧ-энцефалопатия. Также было установлено, что тяжесть поражения нервной системы более выражена у детей первого года жизни.
ВИЧ-энцефалопатия — тяжелое заболевание, затрагивающее все функции ЦНС. При подострой прогрессирующей энцефалопатии утрачиваются ранее приобретенные умения и навыки. Вялотекущая прогрессирующая энцефалопатия замедляет или прекращает формирование новых навыков, не затрагивая при этом старых. Обе формы прогрессирующей энцефалопатии резко замедляют психомоторное развитие. Дети с непрогрессирующей энцефалопатией продолжают приобретать новые навыки, но медленнее, чем здоровые сверстники.
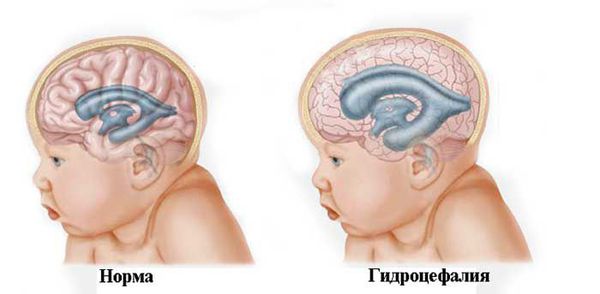
Одновременно поражение ЦНС проявлялось грубой задержкой психомоторного развития, синдромом гипервозбудимости и гидроцефальным синдромом.
Клиническая манифестация ВИЧ-инфекции у детей разнообразна и зачастую неспецифична. Нами установлено, что лимфаденопатия, ассоциированная с гепатоспленомегалией, является одним из наиболее ранних признаков врожденной ВИЧ-инфекции. Так, персистирующая генерализованная лимфаденопатия выявлена в 64% случаев, а гепатолиенальный синдром — в 38% случаев. Сочетание обоих синдромов наблюдалось у 36% детей.
Интерстициальные изменения в легких были у 25% детей, они развивались в результате многократно перенесенных ранее пневмоний различной этиологии.
Из гематологических проявлений чаще всего отмечалась анемия (24% больных), что было связано с приемом антиретровирусного препарата из группы нуклеозидных ингибиторов обратной транскриптазы ВИЧ — «Зидовудина».
Гипотрофия (от I до III степени) была выявлена у 18% больных, недоношенность отмечалась в 14% случаев.
Из сопутствующих заболеваний чаще встречались хронический вирусный гепатит С и туберкулез, а из оппортунистических заболеваний — грибковые поражения кожи и слизистых, пневмоцистная пневмония, герпетическая инфекция, цитомегаловирусная инфекция.
Грибковые поражения кожи и слизистых отмечались у 38% детей.
Чаще всего наблюдался оральный кандидоз, которому сопутствовал ангулярный хейлит, когда в углах рта возникали мацерации, эрозии, трещины. По краям трещин иногда отмечался гиперкератоз. Для детей, больных ВИЧ/СПИДом, характерно рецидивирующее течение орофарингеального кандидоза. В зависимости от степени иммунодефицита (определяется по количеству CD4-лимфоциов), было отмечено возникновение рецидивов через несколько месяцев, недель, а иногда и дней после отмены антимикотической терапии. Продолжительность периодов ремиссии была индивидуальна у каждого больного.
Наиболее опасная оппортунистическая инфекция, пневмоцистная пневмония, наблюдалась у 26% детей. Пневмоцистная пневмония может развиться в любом возрасте, но у наблюдавшихся нами больных почти в половине случаев приходилась на первые 6 месяцев жизни.
Обычно она развивалась остро, проявляясь одышкой и кашлем. Однако в некоторых случаях сначала появлялся кашель, и в течение нескольких дней к нему присоединялось постепенно нарастающее тахипноэ. Вначале появлялось навязчивое покашливание, затем кашель становился коклюшеподобным, особенно в ночное время. У ребенка отмечалась прогрессирующая слабость, снижение аппетита, бледность кожного покрова, цианоз носогубного треугольника. Температура тела в начале заболевания была нормальной или субфебрильной [1, 5].
При физикальном исследовании выявлялись тахипноэ, одышка, влажные и сухие хрипы. При прогрессировании пневмонии, возможно, возникала легочно-сердечная недостаточность.
Рентгенологические изменения, характерные для пневмоцистной пневмонии в виде снижения прозрачности легких, появления симметричных теней в виде крыльев бабочки, «ватных легких», определялись менее чем у половины больных.
Диагноз пневмоцистной пневмонии был основан на обнаружении возбудителя в мокроте, в материале, полученном при бронхоальвеолярном лаваже или биопсии легкого. У большинства детей пневмоцистная пневмония сочеталась с другими оппортунистическими заболеваниями.
Для лечения применялся Бисептол (сульфаметоксазол + триметоприм), который назначался при первом подозрении на пневмоцистную пневмонию до получения результатов микробиологического исследования. Профилактика пневмоцистной пневмонии проводилась тем же препаратом всем детям, рожденным ВИЧ-инфицированными женщинами в возрасте от 6 недель до 4 месяцев до исключения диагноза «ВИЧ-инфекция». ВИЧ-инфицированным детям первичная профилактика пневмоцистной пневмонии проводилась в течение первого года жизни. Дальнейшее проведение профилактики рекомендуется детям при уровне CD4-лимфоцитов 5 лет, независимо от клинических симптомов и уровня вирусной нагрузки;
Антиретровирусную терапию можно временно не назначать детям, у которых нет клинических проявлений ВИЧ-инфекции или они слабо выражены, при уровне CD4-лимфоцитов ≥ 25% у детей от 1 года до 5 лет или уровне CD4-лимфоцитов ≥ 350 клеток/мм3 у детей > 5 лет и уровне вирусной нагрузки
Н. О. Голохвастова, студентка 6 курса МГМСУ, Москва
Что такое перинатальная энцефалопатия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Гавриловой Татьяны Алексеевны, детского невролога со стажем в 20 лет.
Определение болезни. Причины заболевания
Перинатальная энцефалопатия (перинатальное поражение центральной нервной системы) — это заболевание, которое характеризуется повреждением нервной системы ребёнка в перинатальный период.
Перинатальная энцефалопатия (ПЭП) и перинатальное поражение ЦНС — это равнозначные термины, однако детские неврологи чаще применяют второй вариант при постановке диагноза.
В РФ принято объединять всевозможные варианты поражения нервной системы под одним общим диагнозом – «перинатальная энцефалопатия», а в международной классификации, наоборот, максимально уточнять его название и код.
То есть российскому обобщённому диагнозу «перинатальная энцефалопатия» в МКБ-10 может соответствовать несколько уточнённых диагнозов, например:
Основные факторы, приводящие к повреждению нервной системы во время беременности:
Основные факторы, приводящие к повреждению нервной системы в родах:
Основные факторы, приводящие к повреждению головного мозга после родов:
Симптомы перинатальной энцефалопатии
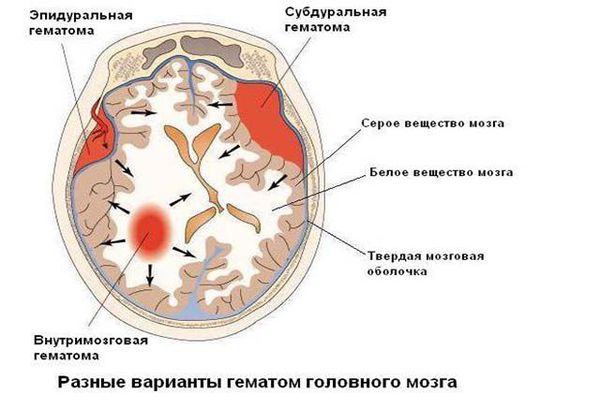
Уже при рождении при наличии тяжёлой родовой травмы с внутричерепным или внутрижелудочковым кровоизлиянием, асфиксией в родах и т. д. у детей отмечаются такие проявления, как угнетение или возбуждение ЦНС, внутричерепная гипертензия (повышенное давление), судороги и даже кома. В таком случае дети экстренно госпитализируются в отделение неонатологии, где получают интенсивное лечение под постоянным наблюдением врачей с внутривенным введением лекарственных препаратов. При необходимости детей временно подключают к аппарату ИВЛ (искусственной вентиляции лёгких).
У детей до года с перинатальной энцефалопатией клинические проявления делят на несколько групп.
Синдром двигательных нарушений:
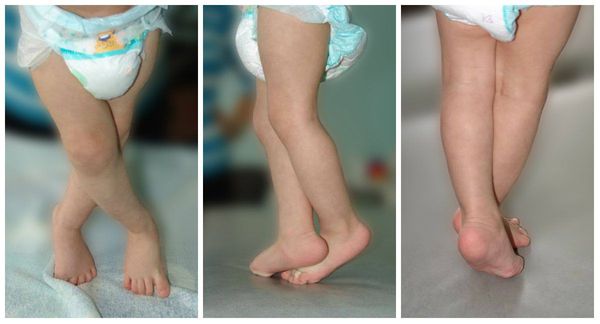
Мышечный тонус при этом может быть повышен либо снижен. При повышении тонуса мышц в руках преобладает тонус в сгибателях (ребёнок держит ручки в кулачках), в ногах преобладает тонус в икроножных мышцах и приводящей группе мышц бедра (при попытке поставить на поверхность ребёнок поджимает пальцы стоп, опора на носочки с перекрёстом).
Также у многих детей с перинатальным поражением ЦНС отмечается задержка психомоторного развития. В связи с чем детский невролог должен чётко знать календарь психомоторного развития у детей до года. При нормальном психомоторном развитии дети начинают:
Существуют индивидуальные особенности развития, небольшие отклонения в развитии могут проходить самостоятельно, но отставание в психомоторном развитии доношенного ребёнка на 2 месяца и более требует осмотра детского невролога для решения вопроса: нуждается ли ребёнок в лечении и назначении комплексной реабилитации.
Не стоит заниматься самолечением, обследование и лечение ребёнку должен назначить детский невролог.
Патогенез перинатальной энцефалопатии
При неблагополучном течении беременности и родов универсальным патогенетическим фактором, повреждающим головной мозг, является гипоксия — это недостаточное поступление кислорода к клеткам головного мозга.
Существует два основных варианта повреждения головного мозга:
Поражение нервной системы при внутриутробных инфекциях сопровождается вовлечением в воспалительный процесс тканей головного мозга и его оболочек (энцефалит, менингит), повышением внутричерепного давления и присоединением судорог.
Возможен также механический перелом ключицы, с повреждением нервного сплетения, расположенного вблизи, возможно механическое повреждение лицевого нерва с формированием в дальнейшем пареза (ослабления) лицевого нерва. При тяжёлых родах возможно формирование ротационного подвывиха шейных позвонков.
Классификация и стадии развития перинатальной энцефалопатии
Перинатальные поражения ЦНС в зависимости от основного повреждающего фактора:
Длительность острого периода:
Восстановительный период длится от месяца до года, у недоношенных детей этот период удлиняется до 2 лет.
Осложнения перинатальной энцефалопатии
В случае тяжёлого поражения нервной системы и несвоевременного начала комплексного лечения впоследствии возможно формирование серьёзных нарушений:
Диагностика перинатальной энцефалопатии
В тех случаях, когда неврологические нарушения были ярко выражены изначально, диагноз перинатальной энцефалопатии устанавливается непосредственно в роддоме и ребёнок своевременно направляется в отделение неонатологии для интенсивной терапии.
В таком случае диагноз ставится на основании:
Далее невролог назначает ребёнку обследование:
При осмотре глазного дна отмечается ангиопатия сосудов глазного дна: сужение артерий, расширение и патологическая извитость вен. Однако провести осмотр глазного дна у маленького ребёнка не всегда удаётся, так как он не может зафиксировать взор в нужную для осмотра точку.
Лечение перинатальной энцефалопатии
Лечение перинатальной патологии в острый период проводится в отделении неонатологии.
Оперативное лечение может понадобиться при наличии у ребёнка большой гематомы внутри полости черепа — её удаление возможно только хирургическим путём.
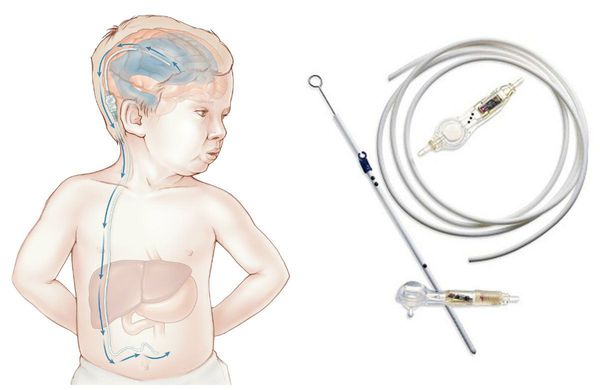
При нарастающей закрытой гидроцефалии, чтобы избежать атрофии головного мозга от сдавления его жидкостью, детям проводят шунтирующую операцию — устанавливают шунт (пластиковую трубочку, по которой лишняя жидкость из полости черепа отводится в брюшную полость и там всасывается).
Однако большинство родителей сталкивается с необходимостью лечения ребёнка с перинатальной энцефалопатией в восстановительный период до 1 года в связи с нарушением мышечного тонуса, задержкой развития, гипертензионно-гидроцефальным синдромом и прочими проявлениями.
Наибольшего эффекта можно добиться с помощью комплексного лечебного подхода.
ЛФК — лечебная физкультура. Может включать различные виды:
Микротоковая рефлексотерапия (МТРТ) — новая медицинская технология, разрешённая Минздравом РФ и рекомендованная для лечения детей с органическим поражением головного мозга, с задержками развития двигательного, речевого, психического развития и ДЦП. Лечение проводится в амбулаторном режиме в реабилитационных центрах в различных регионах РФ.
Лечебное воздействие физиологичное и безболезненное, оказывается токами микроамперного диапазона на нейрорефлекторные зоны на различных участках кожного покрова. Микротоки в 10 раз меньшие, чем при стандартной физиотерапии. Лечение проводится по индивидуальной схеме с учётом всех имеющихся у ребёнка проявлений перинатальной энцефалопатии.
В процессе лечения восстанавливается нормальная рефлекторная деятельность головного мозга, нормализуется мышечный тонус: спастичные (напряжённые) мышцы — расслабляются, гипотоничные (ослабленные) — стимулируются. МТРТ стабилизирует тонус сосудов головного мозга, что позволяет скомпенсировать внутричерепное давление.
Мочегонные препараты целесообразно использовать только при повышении внутричерепного давления (расширение ликворных пространств на НСГ, наличие клинических проявлений гипертензионно-гидроцефального синдрома).
Прогноз. Профилактика
В качестве профилактики необходимо минимизировать факторы риска при беременности и родоразрешении. Важнейшей задачей является предупреждение внутриутробной гипоксии. Для этого важно провести адекватную терапию имеющихся хронических заболеваний и своевременную коррекцию течения осложнённой беременности.