Svo2 что это такое в медицине
Какая норма сатурации кислорода в крови у взрослых
Кислород участвует в образовании 90 % энергии, производимой организмом. Он необходим для химических реакций расщепления молекул пищи и высвобождения из них энергии для функционирования всех органов и систем нашего тела. Сатурация — это показатель, определяющий уровень насыщения крови кислородом. Норма сатурации кислорода в крови у взрослых — 94-99 %. Если значение опускается ниже, человек испытывает симптомы гипоксии, или кислородной недостаточности. В этой статье мы рассмотрим, как определить уровень сатурации кислорода и что предпринимают врачи при критически низких показателях.
Сатурация измеряется в процентах. Они означают соотношение количества молекул гемоглобина к общему числу молекул, находящихся в соединении с кислородом. Существуют два способа измерения:
SaO2 — это обозначение истинной сатурации, которая измеряется путем анализа артериальной крови.
Как измеряют сатурацию
Уровень кислорода в крови — один из ключевых показателей при проведении диагностики во всем мире. Сатурацию легко и быстро измерить: процедура занимает от 10 секунд до минуты, а используются для этого недорогие и компактные пульсоксиметры. Понижение уровня кислорода в крови может свидетельствовать о:
Среди причин низкой сатурации кислорода в крови у взрослых также называют лишний вес и курение.
Как работают пульсоксиметры
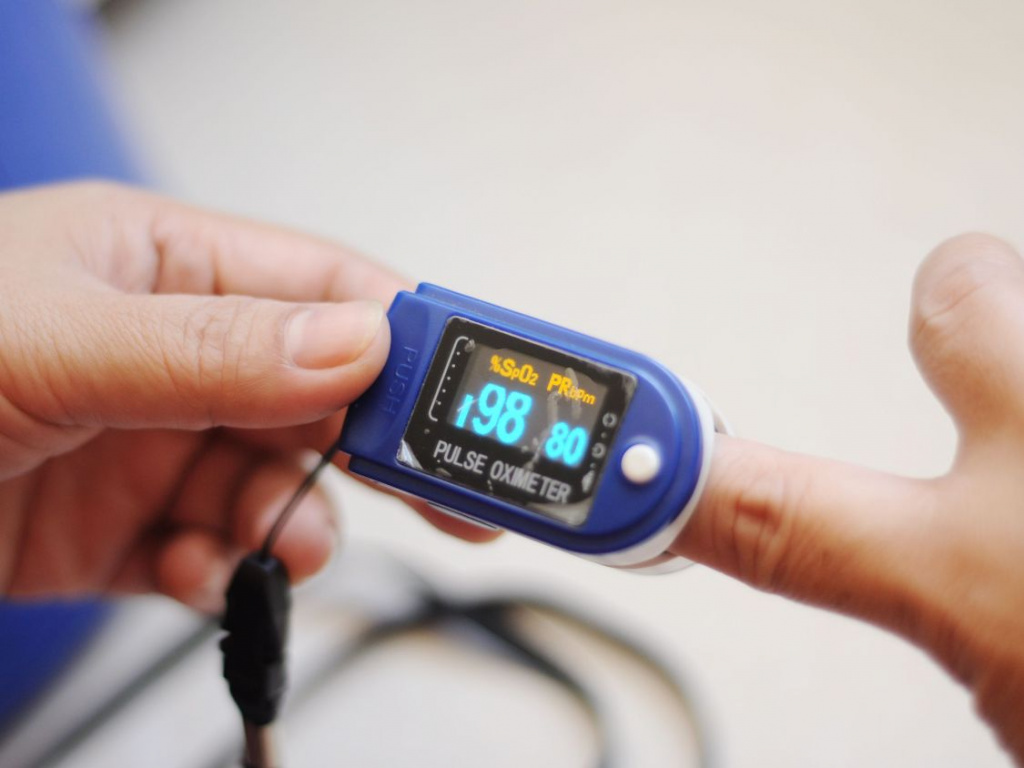
Чтобы определить, в норме ли сатурация кислорода в крови, используют контрольно-диагностический прибор, похожий на прищепку. Пульсоксиметр цепляют на палец, после чего устройство пропускает через него луч света. На одном конце прибора находятся светоизлучающие диоды, а на другом — измерители. Благодаря способности гемоглобина поглощать свет кровь, насыщенная кислородом, имеет иной оттенок. Фотодетектор фиксирует измерения и мгновенно выводит их на экран. Убедиться, что уровень сатурации кислорода у взрослого в норме, можно с помощью последних версий фитнес-браслетов и умных часов: они схожим образом проводят измерения, но менее точны.
Чтобы получить достоверные показания, необходимо сесть и расслабиться. Датчик пульсоксиметра должен находиться у основания ногтя. Шевелить рукой во время определения сатурации нельзя. О том, что прибор закончил диагностику, сообщает звуковой сигнал. Чтобы диагностика была максимально точной в критичный момент, желательно знать свою норму сатурации кислорода — например, произвести измерения в разное время суток: сразу после сна, после еды, во время работы и т.д.
Оптимальные показатели сатурации кислорода
Есть усредненная норма сатурации кислорода у взрослых при измерении пульсоксиметром. Средние значения приведены в таблице:
Нормальная сатурация кислорода у взрослого
Дыхательная недостаточность 1-й степени
Дыхательная недостаточность 2-й степени
Дыхательная недостаточность 3-й степени
Важно отметить, что для новорожденных детей ситуация будет отличаться. У младенцев слабо развиты легкие, а в организме мало железа, поэтому сатурация кислорода 98 % и ниже вплоть до 92 % считается нормой. У недоношенных детей сатурация может опускаться до 82 %: в этом случае используют искусственную вентиляцию легких.
Что делать, если сатурация кислорода низкая
Не всегда причины низкой сатурации кислорода связаны с какими-либо заболеваниями. Например, показатель может опускаться до 92-94 % при интенсивных занятиях спортом, когда кислорода банально не хватает из-за высоких нагрузок.
Помимо низкой сатурации гипоксемия может проявляться учащенным сердцебиение и дыханием, сонливостью, бледными кожными покровами, снижением артериального давления, слабостью и головокружением. Человек может заметить повышенный уровень тревожности, бессонницу. Если гипоксемия ухудшается, то начинаются анаэробные процессы в клетках, сопровождающиеся выделением большого количества вредных веществ. Проявляются одышка, дыхательная недостаточность, тахикардия, отеки нижних конечностей, обмороки, тремор, синюшность кожных покровов.
Если известны причины снижения сатурации кислорода, то в первую очередь врачи работают над лечением данного состояния. При незначительной гипоксии используются кислородные баллончики: они позволяют быстро насытить кровь кислородом и сразу же улучшить самочувствие, однако никак не воздействуют на первопричину кислородной недостаточности. Как правило, такую терапию используют, если дефицит вызван высокими физическими нагрузками, хроническими заболеваниями бронхов и легких, восстановлением после инфекционных болезней.
Если показатели сатурации кислорода падают до 94 %, это повод обратиться к врачу. Однако принимать решение о лечении доктора будут с учетом других симптомов. Например, при легкой форме COVID-19 пульмонологи порекомендуют домашнее лечение с использованием кислородных баллончиков и укладыванием пациента на живот в прон-позицию для облегчения симптомов гипоксемии. Однако если сатурация ниже 95 % и одновременно у больного высокая температура, одышка, хрипы, ему требуется госпитализация и, возможно, оксигенотерапия.
Какой уровень сатурации кислорода в крови критичный
Поскольку низкая сатурация кислорода может быть вызвана целым рядом заболеваний, нет единых требований, когда нужно начинать кислородотерапию. Доктора оценивают состояние пациента, и если видят медицинскую необходимость, то помогают ему при помощи лекарств или оксигенотерапии.
При какой сатурации дают кислород? Правильный ответ зависит от того, по какой именно причине наблюдается его дефицит. Давайте рассмотрим рекомендации специалистов для лечения больных с коронавирусом.
Предпринимаемые врачом меры
Пациент получает кислород при помощи кислородного концентратора. Для подачи газовой смеси используются маски или носовые катетеры/канюли.
Пациента забирают в реанимацию. Используется неинвазивная или инвазивная вентиляция легких.
Пациента подключают к ИВЛ. Если возникают проблемы с аппаратным дыханием, пациента могут ввести в искусственную кому.
Важно отметить, что при угрожающих жизни состояниях сатурация не является основным критерием при принятии решения о подключении пациента к ИВЛ. Намного важнее показатели газообмена в крови, степень повреждения легких и др.
Методы оксигенотерапии
Все способы подачи кислорода делят на две группы.
Поликлиника №10
Сатурация. Почему норма кислорода в крови бывает низкой?
С началом пандемии отдельные слова если не прочно вошли в наш обиход, то довольно часто звучат в новостях и из уст знакомых. Одно из таких слов – «сатурация». Давайте разберемся, что это за показатель и каким он должен быть.
1. Чем измерить сатурацию?
Самый доступный вариант определить, в норме ли сатурация, – использовать пульсоксиметр. Это маленький прибор, который за секунды считает процент оксигемоглобина в крови.
В больнице также используют пульсоксиметр или могут определить газовый состав крови в лаборатории. Для этого берется образец крови из артерии или вены. Это не рутинный анализ и обычно его делают при серьезных заболеваниях.
2. Что такое сатурация?
Сатурация – это показатель насыщения крови кислородом. По сниженному уровню сатурации можно заподозрить проблемы с легкими. Это стало особенно актуальным после появления новой коронавирусной инфекции. Одним из основных осложнений COVID-19 становится вирусная пневмония. Если вовремя заметить, что человеку не хватает кислорода, помочь ему будет легче.
3. Какой уровень кислорода в крови у взрослых считается нормой?
Нормой сатурации для здорового человека считается, когда 95% и больше гемоглобина связано с кислородом. Это и есть сатурация – процент оксигемоглобина в крови.
При COVID-19 вызывать врача рекомендуют, когда сатурация снижается до 94%. Сатурация 92% и ниже обычно считается критической. Человеку с таким низким показателем кислорода в крови требуется срочное медицинское вмешательство.
Есть исключения. Например, при тяжелой хронической обструктивной болезни легких, которая часто встречается у курильщиков, показатель сатурации может быть от 88 % до 92%. Обычно организм таких людей адаптирован к более низкому уровню кислорода. Если у вас есть пульмонологическое заболевание, ваш врач сообщит, какой показатель сатурации должен стать сигналом тревоги именно для вас.
4. Почему норма кислорода в крови бывает низкой?
Это может случиться по разным причинам. Например, проблемы могут возникнуть при болезнях крови или дыхательной системы.
Последнее как раз характерно для КОВИД-19. После пневмонии нередко возникает фиброз легких, когда из-за болезни «дышащая» легочная ткань заменяется соединительной. Это можно сравнить с закрытыми форточками. Вы бы рады подышать, но свежий воздух не проходит через плотно закрытые окна.
Другая причина – заболевания крови. Например, часто встречающаяся анемия. Когда не хватает эритроцитов или самого гемоглобина, то кислороду просто не на чем перемещаться по организму. В этом случае сатурация тоже падает ниже нормы.
5. Что происходит, когда кислорода становится мало?
Одышка, боль в груди, спутанность сознания, головная боль и быстрое сердцебиение, синюшность носогубного треугольника и кончиков пальцев – такие неприятные симптомы могут появиться, если уровень кислорода в крови начнет падать.
6. Надо ли знать свою сатурацию?
Как правило, нет. Исключение, если у вас больные легкие и вы наблюдаете за динамикой болезни.
Измерение газообмена
, MD, Grant Medical Center, Ohio Health
Газообмен измеряется несколькими способами, включая
Диффузионная способность легких для монооксида углерода
Исследование газового состава артериальной крови
Диффузионная способность легких по монооксиду углерода
Диффузионная способность легких по монооксиду углерода (DLCO) – мера способности газа переходить из альвеол через альвеолярный эпителий и капиллярный эндотелий в эритроциты. DLCO зависит не только от области и толщины альвеолярно-капиллярной мембраны, но также от объема крови в легочных капиллярах. Распределение альвеолярного объема и вентиляции также вызывает изменение показателя.
DLCO определяется с помощью анализа воздуха на содержание монооксида кислорода (СО) в конце выдоха, после того как пациент вдыхает незначительное количество СО, задерживает дыхание и выдыхает. Определяемые показатели DLCO должны быть соотнесены с альвеолярным объемом (который оценивается разведением гелия Легочные объемы Определение скорости потока и легочных объемов используют для дифференцировки обструктивных и рестриктивных пульмональных нарушений, определения тяжести заболевания и оценки эффективности лечения. Прочитайте дополнительные сведения ) и уровнем гематокрита пациента. DLCO измеряется в мл/минуту/мм.рт.ст. и в процентах от должного.
Причины снижения DLCO
Причины повышения DLCO
Условия, при которых значения DLCO будут выше, чем прогнозировалось, включают
Во время сердечной недостаточности DLCO увеличивается предположительно вследствие повышения объема крови в легочных капиллярах из-за повышенных легочных венозного и артериального давлений. При эритроцитемии увеличение DLCO обусловлено увеличением количества эритроцитов, а также из-за сосудистого наполнения вследствие возрастания легочного давления, обусловленного повышенной вязкостью крови. При альвеолярном кровотечении эритроциты также могут связывать монооксид углерода в альвеолярном пространстве, увеличивая DLCO. При астме увеличение DLCO связывают с увеличением перфузируемых сосудов, однако согласно некоторым данным, не исключено влияние различных факторов роста, индуцирующих неоангиогенез.
Пульсоксиметрия
Чрескожная пульсоксиметрия оценивает сатурацию кислорода (SpО2) капиллярной крови по поглощению света от светоиспускающих диодов, помещенных в клипсу для пальца или датчик на пластыре. В целом результаты чрезвычайно точные и коррелируют с сатурацией кислорода с погрешностью в пределах 5% (SaО2). Результаты могут быть менее точными у пациентов с
Очень пигментированная кожа
Выраженной системной вазоконстрикцией
Результаты пульсоксиметрии также менее точны при наличии накрашенных ногтей у пациентов.
Пульсоксиметрия способна определять содержание только оксигемоглобина или дезоксигемоглобина, но не другие формы гемоглобина (например, карбоксигемоглобин, метгемоглобин); данные фракции завышают показатели SpO2, когда их ошибочно принимают за оксигемоглобин.
Исследование газового состава артериальной крови (ГСАК)
Исследование газового состава артериальной крови проводится для получения точных значений парциального давления кислорода в артериальной крови (PaO2), парциального давления углекислого газа в артериальной крови (PaCO2) и pH артериальной крови; эти показатели, откорректированные с учетом температуры пациента, позволяют рассчитать уровень бикарбоната (который может также быть измерен непосредственно в венозной крови) и SaO2. С помощью исследования газового состава также можно точно измерить уровень карбоксигемоглобина и метгемоглобина.
Обычно для взятия образцов артериальной крови используется лучевая артерия. Поскольку артериальная пункция может в редких случаях приводить к тромбозу и ухудшению перфузии дистальных отделов, вначале выполняется тест Аллена. Он позволяет оценить адекватность коллатерального кровообращения. При выполнении этой пробы одновременно пережимаются лучевая и локтевая артерии до тех пор, пока рука пациента не станет бледной. После этого локтевую артерию отпускают, в то время как давление на лучевую артерию продолжается. Появление розовой окраски во всей руке в течение 7 секунд после ослабления давления указывает на адекватный кровоток через локтевую артерию.
В стерильных условиях игла калибром 22–25G, присоединенная к гепаринизированному шприцу, вводится проксимальнее места максимальной пульсации лучевой артерии и продвигается немного дистальнее в артерию, пока не восстановится пульсация. Систолическое артериальное давление обычно является достаточным, чтобы выдвинуть поршень шприца обратно. После забора 3–5 мл крови игла быстро извлекается, и место пункции сильно прижимается для осуществления гемостаза. Одновременно образец артериальной крови помещается в лед (для уменьшения потребления кислорода и продукции углекислого газа лейкоцитами) и посылается в лабораторию.
Оксигенация
Гипоксемия – это снижение парциального давления кислорода (PO2) в артериальной крови; гипоксия – это снижение РO2 в тканях. Исследование газового состава точно определяет наличие гипоксемии, которая обычно определяется как достаточно низкое значение РаO2, способное уменьшить SaO2 ниже 90% (т.е. РаO2 60 мм.рт.ст.). Патологические формы гемоглобина (например, метгемоглобин), более высокая температура, низкий pH и высокий уровень 2,3-дифосфоглицерата уменьшают гемоглобин SaO2, несмотря на адекватный РаO2, как показано на кривой диссоциации оксигемоглобина ( Кривая диссоциация оксигемоглобина Кривая диссоциация оксигемоглобина Газообмен измеряется несколькими способами, включая Диффузионная способность легких для монооксида углерода Пульсоксиметрия Исследование газового состава артериальной крови Диффузионная способность. Прочитайте дополнительные сведения ).
Кривая диссоциация оксигемоглобина
Насыщение артериальной крови оксигемоглобином соответствует P o 2. P o 2 при сатурации 50% (P 50) обычно соответствует 27 мм.рт.ст.
Кривая диссоциации смещается вправо при увеличении концентрации ионов водорода (Н + ), увеличении в эритроцитах 2,3-дифосфоглицерата, повышении температуры (Т) и увеличении P co 2.
Гемоглобин, характеризующийся смещением кривой вправо, имеет пониженное сродство к кислороду, а гемоглобин, характеризующийся смещением кривой влево, имеет повышенное сродство к кислороду.
Причины гипоксемии классифицируют в зависимости от значения (повышение или норма) альвеолярно-артериального градиента PО2 по кислороду ([A-а]DО2), который определяется как разница между альвеолярным напряжением кислорода (PAО2) и PaО2. РAO2 рассчитывается следующим образом:
где FIO2 – содержание кислорода во вдыхаемом воздухе (например, в комнатном воздухе – 0,21), Patm – барометрическое атмосферное давление (например, 760 мм.рт.ст. на уровне моря), PH2O – парциальное давление водяного пара (обычно 47 мм.рт.ст.), PaСО2 – измеренное парциальное давление углекислого газа в артериальной крови, R – дыхательный коэффициент, который принимают за 0,8 у пациента в состоянии покоя при обычном питании.
Для пациентов, находящихся на уровне моря при дыхания комнатным воздухом, FIO2 = 0,21 и (A-а) DO2 можно упростить следующим образом:
где (A-a)DО2 обычно 20, но увеличивается с возрастом (из-за снижения функции легких с возрастом) и с увеличением FIO2 (несмотря на то, что насыщение гемоглобина достигает 100% при PaО2 около 150 мм.рт.ст., кислород растворим в крови и кислород плазмы продолжает увеличиваться при повышении FIO2 ). Оценки нормального (А-а) DO2 значения как (2,5 + [FIO2 × возраст в годах]) или как менее абсолютного значения Fio2 (например, 21 при комнатной температуре; 30 на 30% FIO2) корректируют эти эффекты.
Гипоксемия с повышенным (А-а) DO2
Гипоксемия с повышенным (Aa)DO2 вызвана
Низкое вентиляционно-перфузионное (V/Q) соотношение (разновидность вентиляционно-перфузионного несоответствия)
Шунтирование крови справа налево
Серьезное нарушение диффузионной способности
Шунтирование крови справа налево является ярким примером низкого вентиляционно-перфузионного соотношения. При шунтировании дезоксигенированная легочная артериальная кровь поступает в левую половину сердца, не пройдя через вентилируемые сегменты легкого. Шунтирование может проходить через паренхиму легкого, через патологические связи между легочными артериальными и венозными сосудами или через патологические анатомические структуры в сердце (например, открытое овальное отверстие). При наличии подобного шунтирования справа налево устранить гипоксемию с помощью кислородотерапии не представляется возможным.
Сниженная диффузионная способность редко встречается изолированно; обычно она сопровождается низким вентиляционно-перфузионным соотношениями. Поскольку кислород полностью насыщает гемоглобин только после контакта крови с воздухом, гипоксемия из-за сниженной диффузионной способности встречается только при увеличенном сердечном выбросе (например, во время физической нагрузки), при низком атмосферном давлении (например, на высоте в горах) или при разрушении > 50% легочной паренхимы. Как при низким вентиляционно-перфузионном соотношении, (A-a)DO2 увеличен, но PaO2 может быть быстро увеличен благодаря увеличению FIO2. Гипоксемия, развивающаяся вследствие нарушения диффузионной способности, корректируется с помощью кислородотерапии.
Венозная сатурация
Определение насыщения (сатурации) венозной крови кислородом (SvO2) является одним из современных направлений инвазивного мониторинга. Этот параметр сравнивают со «сторожевым псом» кислородного баланса и иногда называют «пятым витальным показателем», позволяющим косвенно судить о глобальном балансе между доставкой и потреблением кислорода. Следует помнить, что периодическое или непрерывное измерение СВ и SaO 2 (SpO 2 ) дает возможность отслеживать доставку O 2 , но в то же время ничего не говорит о потребности в нем в рамках иерархической обратной связи, описанной Pflüger E.F., – «потребность – потребление – доставка».
Потребление кислорода может быть рассчитано согласно принципу Фика:
Путем математического преобразования этого уравнения можно определить, что при данном значении VO2 показатель SvO2 пропорционален соотношению между доставкой и потребностью в кислороде:
где SvO2 – насыщение (сатурация) венозной крови кислородом (%); SaO2 – насыщение артериальной крови кислородом (%); Hb – концентрация гемоглобина (г/л); VO2 – потребление кислорода тканями (мл/мин); СВ – сердечный выброс (л/мин).
Таким образом, насыщение гемоглобина венозной крови кислородом будет пропорционально усредненному значению экстракции O2 (VO2/DO2, O2ER) и в случае снижения может быть следствием критического дисбаланса между доставкой кислорода и потребностью в нем. Исследования показали, что, при сравнении со значениями АДСРЕД и ЧСС, показатель SvO2 демонстрирует наиболее четкую связь с O2ER.
Действительно, перфузионное АД, хотя и является наиболее часто измеряемым гемодинамическим показателем, обладает при этом наименьшей значимостью в оценке адекватности транспорта кислорода и тканевой оксигенации. Несмотря на нормализацию АД и СВ, неадекватное распределение кровотока или блокада потребления O2 могут сопровождаться явлениями тканевой гипоксии и прогрессированием ПОН.
Классической точкой измерения венозной сатурации (SvO2) считается легочнаяартерия, содержащая смешанную венозную кровь из бассейна нижней и верхней полой вен, а также коронарного синуса. Соответственно, исследование этого параметра требует выполнения катетеризации легочной артерии. Нормальные значения
показателя могут варьировать в диапазоне 65–75%. При критических состояниях интерпретация динамических изменений SvO2 имеет большее значение, нежели одномоментная оценка его абсолютного значения (таблица 1).

Таблица 1. Сатурация смешанной венозной крови: диапазоны значений
Показатель SvO2 представляет нам усредненное значение SO2 крови, оттекающей от различных органов и тканей. Однако на уровне отдельно взятого органа или сектора организма насыщение венозной крови кислородом может значимо варьировать, что определяется характером и интенсивностью работы органа (таблица 2).
Например, потребление O2 мышцами может существенно возрастать при физической нагрузке за счет роста его экстракции, что ведет к снижению SO2 оттекающей крови.
При физической нагрузке значения CvO2 и SvO2 снижаются, несмотря на повышение DO2. Показатель SvO2 для почек высок и составляет 90–92%. Относительно большой объем почечного кровотока не связан с собственными потребностями органа и отражает его экскреторную функцию.
Таблица 2. Относительный объем перфузии, потребление кислорода и насыще-
ние кислородом венозной крови, оттекающей от различных органова
Необходимо учитывать, что при критических состояниях, сопровождающихся повреждением легких, прослеживается четкая корреляция между изменениями SvO2 (ΔSvO2) и SaO2 (ΔSaO2). Помимо состояния внешнего газообмена, существует большое число факторов, определяющих результирующее значение SvO2. Так, снижение SvO2 может быть вызвано не только тканевой гипоперфузией (снижение СВ), но и артериальной десатурацией, а также снижением концентрации гемоглобина, в том числе в результате гемодилюции на фоне проводимой инфузионной терапии (таблица 3).
По данным Ho K.M. et al.21 (2008), оксигенация артериальной крови (PaO2) может оказывать даже большее влияние на значение венозной сатурации, чем величина сердечного выброса. Таким образом, оценка и интерпретация SvO2 должны быть основаны на комплексном подходе, учитывающем такие важные детерминанты, как SaO2, ЧСС, АД, ЦВД, СВ, темп диуреза, а также концентрации гемоглобина и лактата в венозной крови. Наличие большого числа факторов, определяющих результирующее значение SvO2, и их быстрое изменение при критических состояниях создают предпосылки для непрерывного мониторинга венозной сатурации в интенсивной терапии и анестезиологии.

Таблица 3. Причины изменений сатурации смешанной и центральной венозной крови
ScvO2 – сатурация центральной венозной крови; SvO2 – сатурация смешанной венозной крови; СВ – сердеч-
ный выброс; Hb – концентрация гемоглобина; SaO2 – насыщение артериальной крови кислородом; ОПЛ –
острое повреждение легких
Несмотря на эти ограничения, оценка SvO2 остается удобным подходом, направленным на раннее выявление шока, в частности его «скрытых» форм («cryptic shock»), не проявляющихся ростом плазменной концентрации лактата и признаками развернутой полиорганной недостаточности. Диагностическая, прогностическая и тера-
певтическая значимость снижения SvO2 была продемонстрирована у различных групп реанимационных больных.28 Вместе с тем ряд критических состояний могут сопровождаться гетерогенным распределением перфузии, шунтированием крови на прекапиллярном уровне, диспропорциональным угнетением циркуляции и митохондриальной активности (блокада экстракции кислорода). На фоне подобных нарушений, в частности при септическом шоке, может наблюдаться повышение SvO2, что связано с подавлением захвата кислорода клетками на фоне дисфункции митохондрий и расстройств микроциркуляции. Неслучайно септический шок иногда характеризуется как «микроциркуляторный и митохондриальный дистресс-синдром».
«Супранормальные» значения SvO2, наблюдающиеся в ряде случаев на фоне ПОН, не должны рассматриваться как признак избыточной доставки кислорода или «шикарная перфузия». Напротив, рост SvO2 может указывать на подавление митохондрий и «обкрадывание» тех областей, где потребность в кислороде особенно высока, со всеми вытекающими отсюда последствиями.7 Схожая картина наблюдается при блокаде митохондриальной дыхательной цепи цианидами. Нередко повышение SvO2 может быть следствием гипердинамической реакции кровообращения на фоне сепсиса, вазодилатации и инотропной поддержки.
По данным Varpula M. et al.51 (2005), исход у пациентов с септическим шоком помимо прочих переменных (АДСРЕД, концентрация лактата и ЦВД) связан с показателем SvO2, при этом значение SvO2 > 70% ассоциировалось с улучшением исхода. Тем не менее в исследовании Dahn M.S. et al. указывается, что у пациентов с сепсисом час-
то не удается зарегистрировать значимого снижения SvO2, что может быть следствием регионарных нарушений потребления кислорода. В связи с этим некоторые авторы не рекомендуют использовать SvO2 в качестве маркера тканевой гипоперфузии.
В рандомизированном исследовании Gattinoni L. et al. повышение SvO2 > 70% в течение 5 суток у пациентов с септическим шоком не сопровождалось значимым снижением летальности. Однако шесть лет спустя Rivers E.P. et al.37 (2001) продемонстрировали значимое улучшение исхода при использовании протокола целенаправленной терапии, который включал функциональный аналог SvO2 – сатурацию центральной венозной крови (ScvO2).
Измерение сатурации центральной венозной крови (ScvO2)
Для дискретного измерения сатурации «центральной» венозной крови (ScvO2) необходим забор крови из верхней полой вены с последующим исследованием газового состава образца. Непрерывное измерение ScvO2 требует установки фиброоптического датчика и основано на принципе отражательной фотометрии.
Основное преимущество измерения SсvO2 по сравнению с SvO2 заключается в том, что в этом случае не требуется катетеризация легочной артерии. Действительно, ранняя установка катетера Сван–Ганца для проведения начальной терапии шока и ПОН может быть технически затруднена и нецелесообразна, в то время как цен-
тральный венозный катетер устанавливается у большинства пациентов, поступающих в ОИТ. Известно, что помимо диагностических целей (измерение ЦВД и ScvO2), катетеризация центрального венозного русла необходима для проведения инфузионной и заместительной почечной терапии, парентерального питания, а также введения препаратов вазопрессорного и инотропного ряда. Примечательно, что, по мнению Bauer P. и Reinhart K., именно необходимость измерения ScvO2 может рассматриваться как решающее показание к катетеризации центрального венозного русла при критических состояниях.
Необходимо отметить, что в 10–30% случаев кончик центрального венозного катетера находится в правом предсердии и, в частности, в его нижней части. В этой ситуации значение сатурации венозной крови будет близко к таковому для смешанной венозной крови.
Очевидно, что на сегодняшний день мониторинг ScvO2 превосходит по своей популярности измерение SvO2. Кроме того, несмотря на возможность периодического измерения SvO2/ScvO2 путем лабораторного анализа газового состава крови, определенный интерес представляет непрерывный мониторинг показателя методом фотометрии. Теоретическим обоснованием целесообразности непрерывного измерения ScvO2 может быть тот факт, что при нестабильном состоянии больного баланс VO2/DO2 зависит от ряда условий (таблица 3) и подвержен быстрым изменениям, требующим незамедлительной коррекции. Обращает на себя внимание тот факт, что эффективность мониторинга ScvO2 доказана в известном исследовании Rivers E.P. et al. именно с использованием метода непрерывной венозной оксиметрии.
Согласно литературным данным, до 50% пациентов с шоком имеют сохраняющуюся тканевую гипоксию (повышение уровня лактата и снижение ScvO2) даже на фоне нормализации витальных показателей и ЦВД. Более того, в связи со стабильными значениями витальных параметров (ЧСС, АДСРЕД, темп диуреза и др.) пациенты, поступающие на приемный покой, часто не обследуются в полном объеме на предмет расстройств тканевого кровотока и не получают адекватной терапии на протяжении «золотых часов» – периода, когда органная дисфункция является обратимой. Это подтверждает необходимость адекватной терапии реанимационных больных уже с первых минут их поступления в стационар. Выбор исходно ошибочной тактики ранней терапии, в узких пределах «золотых» 6 часов после поступления в стационар, крайне неблагоприятно влияет на исход, даже при последующей коррекции лечебных мероприятий. Так, в исследовании пациентов с тяжелым сепсисом было показано, что раннее (в течение первых 6 часов после поступления) применение протокола целенаправленной терапии (EGDT), ориентированного в том числе на достижение целевого значения ScvO2, привело к следующим результатам:
1) снижение летальности на 15% (с 46,5% до 30,5%; p = 0,009);
2) снижение длительности пребывания в ОИТ на 3,8 суток;
3) снижение расходов на терапию на 12 000 долларов США.
Предложенный Rivers E.P. etal. протокол EGDT (EarlyGoal—DirectedTherapy –ранняя целенаправленная терапия) (рисунок 9.4) устанавливает целевые критерии, позволяющие на раннем этапе выявить пациентов высокого риска, и определяет тактику ранней инфузионной и/или трансфузионной, и/или инотропной терапии
на основании следующих целевых показателей:
– ЦВД = 8–12 мм рт. ст.;
– АДСРЕД > 65 мм рт. ст.;
– темп диуреза > 0,5 мл/кг/час;
– ScvO2 > 70% (непрерывная оксиметрия).

правленной терапии Rivers E.P.
et al. (2001)
ЦВД – центральное венозное дав-
ление; АДСРЕД – среднее артериаль-
ное давление; ScvO2 – насыщение
центральной венозной крови ки-
слородом; ИВЛ – искусственная
вентиляция легких
Рекомендации Surviving Sepsis Campaign 2008 включают нормализацию показателя ScvO2 (> 70%), что подразумевает мониторинг этого показателя на начальной стадии лечебных мероприятий у пациентов с тяжелым сепсисом и септическим шоком.
Однако в некоторых ситуациях, в том числе при септическом шоке, может наблюдаться повышение ScvO2, что обусловлено «уклонением» кровотока от тканей в результате шунтирования, уменьшением экстракции O2 и гипердинамией, а также прочими факторами и их сочетанием. В этом контексте представляют интерес данные
Bauer P. et al. (2008), которые демонстрируют, что как снижение ( 75%) при плановых кардиоторакальных вмешательствах сопровождаются значимым ростом частоты осложнений и летальности параллельно с повышением концентрации лактата > 4 ммоль/л. Эти результаты позволили авторам сделать заключение, что для показателя ScvO2 «коридор безопасности» пролегает
в интервале между 65% и 75% (70 ± 5%).
Вместе с тем снижение ScvO2 также не обязательно указывает на критическую тканевую гипоксию. Метаболический стресс, наблюдающийся при физической нагрузке или компенсаторном повышении O2ER на фоне хронической сердечной недостаточности, будет сопровождаться компенсаторным снижением SvO2/ScvO2, что, впрочем, является относительно доброкачественным признаком и не сопровождается развитием ПОН. Следует подчеркнуть, что чувствительность показателя ScvO2, скорее всего, недостаточно высока для оценки потребления O2 отдельными органами при их изолированном поражении. Согласно данным Weinrich M. et al. (2008), при обширных абдоминальных вмешательствах показатель ScvO2 не коррелирует с насыщением кислородом венозной крови, оттекающей непосредственно от органа/области вмешательства.
Тем не менее, результаты ряда рандомизированных исследований показывают, что применение протоколов целенаправленной терапии, основанных на целевых значениях ScvO2, при обширных хирургических вмешательствах может сопровождаться снижением частоты послеоперационных осложнений и летальности. По нашим данным, сочетанный мониторинг ScvO2 и внутригрудного объема крови (ВГОК) при аортокоронарном шунтировании на работающем сердце ведет к увеличению интраоперационного гидробаланса, снижению частоты использования вазопрессоров и уменьшению длительности пребывания пациентов в стационаре. У кар-
диохирургических пациентов могут наблюдаться разнонаправленные изменения ScvO2 и SvO2: Sander M. et al. (2007) утверждают, что одновременный мониторингобоих показателей может повысить частоту выявления глобальной и локальной гипоперфузии. Мониторинг венозной сатурации может также оказаться полезным у
пациентов с травмой, при остром инфаркте миокарда и кардиогенном шоке, облегчая раннюю диагностику критического дисбаланса транспорта кислорода при этих состояниях. Кроме того, наряду с такими индикаторами, как концентрация гемоглобина, гематокрит и избыток оснований (BE), показатель ScvO2 в случае адекватной артериальной оксигенации и нормализации СВ может рассматриваться как удобный маркер, указывающий на необходимость гемотрансфузии.
Различия ScvO2 и SvO2
Следует признать, что прикладные клинические исследования сатурации центральной венозной крови начались до введения в широкую клиническую практику катетера Сван–Ганца, а следовательно, и возможности измерения SvO2. Вопрос о различиях между абсолютными значениями ScvO2 и SvO2 носит, главным образом,
академический интерес. В отличие от смешанной венозной крови, газовый состав центральной венозной крови отражает экстракцию O2 головным мозгом и верхними конечностями/плечевым поясом. В клинических условиях ScvO2 расценивается как «функциональный аналог» (или «суррогат») показателя сатурации смешанной венозной крови. Сатурация центральной венозной крови менее точно отражает глобальное среднее значение O2ER, но является доступной и удобной альтернативой SvO2.
У здорового человека, находящегося в состоянии покоя, ScvO2 обычно на 2–4% ниже SvO2, что связано с более высокой экстракцией O2 в органах верхней половины тела, в том числе в головном мозге, который при весе, составляющем всего 2% от массы тела, может получать до 20–22% от объема сердечного выброса. Несмотря на
эти различия, глобальные изменения O2ER сопровождаются однонаправленными и близкими по амплитуде сдвигами значений ScvO2 и SvO2.
При развитии шока картина диаметрально меняется: ScvO2 всегда превышает SvO2, при этом различия достигают 5–18%. По данным Reinhart K. et al., при септическом шоке ScvO2 превышает SvO2 на 8%. Кардиогенный и гиповолемический шок ведут к подавлению спланхнической перфузии, что сопровождается ростом O2ER с
неизбежным снижением SvO2. Таким образом, различия между ScvO2 и SvO2 могут варьировать в зависимости от ряда факторов (таблица 4). Так, во время анестезии показатель ScvO2 превышает SvO2 на 6%. Схожие изменения наблюдаются при седации и внутричерепной гипертензии.

Таблица 4. Различия сатурации центральной и смешанной венозной крови
Выводы клинических и экспериментальных исследований в отношении использования ScvO2 в качестве альтернативы SvO2 варьируют. Ряд исследователей указывают на соответствие изменений SvO2 и ScvO2 при различных критических состояниях. Некоторые авторы полагают, что значения ScvO2 не показывают тесной
корреляции с SvO2, при этом мониторинг показателя не позволяет с приемлемой точностью оценить глобальный баланс VO2/DO2. Особенно остро несоответствие значений ScvO2 и SvO2 проявляется при септическом шоке, который сопровождается явлениями митохондриального дистресса. Выраженность шунтирования и
тяжесть митохондриальной дисфункции в бассейне верхней и нижней полых вен могут различаться; в подобной ситуации ScvO2 не может служить адекватным заменителем SvO2.50 Недавние исследования показали, что на момент поступления в ОИТ снижение ScvO2 наблюдается лишь у небольшой части пациентов с тяжелым сепси-
сом. В связи с этим некоторые эксперты считают включение ScvO2 в стандартизованные рекомендации по ведению этой категории больных преждевременным.
Тем не менее резкое снижение ScvO2 практически всегда сопряжено со снижением SvO2. Таким образом, ScvO2 остается важным клиническим параметром и может рассматриваться как надежный показатель дисбаланса между доставкой и потреблением кислорода.

менения сатурации смешанной
и центральной венозной крови:
1 – нормоксия; 2 – кровопотеря; 3 –
инфузионная терапия (HAES); 4 –
гипоксия; 5 – нормоксия; 6 – гипе-
роксия; 7 – кровопотеря.
Из: Reinhart K., Bloos F. Central Venous
Oxygen Saturation (ScvO2).
Yearbook of Intensive Care Medicine
2002: Ed.: Vincent J.-L.:241–250
ТЕХНИЧЕСКОЕ ОБЕСПЕЧЕНИЕ МОНИТОРИНГА ВЕНОЗНОЙ САТУРАЦИИ
Показатели ScvO2 и SvO2 могут измеряться дискретно, путем анализа газового состава образцов венозной крови, забранных, соответственно, из центрального венозного катетера или дистального просвета катетера Сван–Ганца. Однако по ряду причин, указанных выше, непрерывное измерение ScvO2/SvO2 может иметь ряд преимуществ, в частности, на фоне быстрых и трудно прогнозируемых изменений тканевого кровотока и прочих детерминант доставки кислорода. В настоящее время существует несколько систем для непрерывного измерения ScvO2/SvO2, действующих по принципу венозной фотометрии (оксиметрия). Метод непрерывного измерения основан на использовании катетера малого диаметра, в который интегрированы фиброоптические проводники, один из которых излучает свет определенной волны в поток венозной крови, а второй передает отраженный сигнал на оптический датчик монитора (рисунок 3).

рывной отражательной веноз-
ной оксиметрии
1. Системы мониторинга CeVOX и PiCCO2 (Pulsion Medical Systems, Германия). Датчик для венозной оксиметрии устанавливается через один из просветов центрального венозного катетера. Для непрерывного измерения ScvO2 необходимы центральные блоки CeVOX (PC3000) или PiCCO2, снабженные оптическим модулем (PC3100) и одноразовым фиброоптическим датчиком (PV2022-XX, 2F (0,67 мм), 30–38 см). Для начальной калибровки монитора in vivo необходимо введение датчика в верхнюю полую вену. После подтверждения качественного сигнала забирают образец венозной крови с определением ее насыщения кислородом и концентрации гемоглобина. Введение этих показателей в меню монитора завершает процедуру калибровки. Удобство системы состоит в том, что изменение положения, удаление или замена оксиметрического датчика не требуют смены положения или извлечения центрального венозного катетера. По данным недавнего исследования Baulig W. et al.6 (2008), ScvO2, измеренная при помощи системы CeVOX, характеризуется приемлемыми значениями чувствительности и специфичности в отношении прогнозирования значимых изменений показателя. Система PiCCO2 позволяет осуществлять непрерывный мониторинг значений DO2 и VO2.
2. Система PreSepTM (Edwards Lifesciences, Ирвин, США) включает трехпросветный центральный венозный катетер с заранее интегрированным фиброоптическим проводником для непрерывного мониторинга ScvO2. Катетер может быть подключен к ряду систем компании Edwards Lifesciences, в частности Vigilance-I, Vigilance-II и VigileoTM. При длине 20 см диаметр катетера составляет 8,5F (2,8 мм). Перед установкой требуется калибровка in vitro и in vivo. Качество сигнала ScvO2 может быть нарушено при пульсации в области кончика катетера, периодическом контакте со стенкой сосуда (заклинивание катетера), перегибе и формировании сгустка крови, гемодилюции. Обновление в меню монитора значений гемоглобина и гематокрита необходимо при изменении этих величин на 6% и более. Модели с маркером «H» имеют традиционное антибактериальное и гепариновое по-
крытие AMC Thromboshield. В настоящее время катетеры PreSepTM защищены от бактериальной контаминации патентованным комплексом OligonTM (комплексное покрытие, включающее атомы серебра, платины и углерода), действие которого основано на выделении активных ионов серебра.
3. Система CCOmbo (Edwards Lifesciences, Ирвин, США) представляет собой катетер Сван–Ганца с интегрированным фиброоптическим элементом. При подключении к системам мониторинга Vigilance дает возможность непрерывного измерения SvO2, СВ, а также конечно-диастолического объема и фракции изгнания правого желудочка. Стоимость катетера относительно высока.
ПОКАЗАНИЯ К МОНИТОРИНГУ ВЕНОЗНОЙ САТУРАЦИИ
По данным ряда клинических исследований, мониторинг центральной и/или смешанной венозной сатурации может быть показан в следующих ситуациях:
– тяжелый сепсис и септический шок;
– периоперационный период кардиоторакальных вмешательств;
– инфаркт миокарда, кардиогенный шок и остановка кровообращения;
– тяжелая травма и кровопотеря.
Алгоритмы целенаправленной терапии, основанные на определенном значении SvO2/ScvO2, в большинстве случаев направлены на увеличение детерминант доставки кислорода:
– повышение сердечного выброса (инфузионная терапия и инотропная поддержка);
– нормализация концентрации гемоглобина (гемотрансфузия);
– нормализация внешнего дыхания (SaO2) – методы респираторной терапии.
Вместе с тем с учетом характера компенсаторных изменений, наблюдающихся при неадекватном распределении тканевого кровотока, могут быть целесообразны методы, способствующие перераспределению капиллярного кровотока (микроциркуляторный рекрутмент) и повышению экстракции O2 тканями («метаболическая терапия»).
В заключение необходимо еще раз напомнить, что поддержание адекватной перфузии и оксигенации тканей является основной целью терапии реанимационных больных. Целесообразность мониторинга сатурации центральной венозной крови состоит в том, что этот метод не требует проведения дополнительных инвазивных
вмешательств и имеет явные преимущества на раннем этапе диагностики шока. При дистрибутивном шоке ScvO2 не всегда точно отражает глобальную экстракцию кислорода, однако изменения ScvO2 в результате лечебных мероприятий достоверно коррелируют с динамикой SvO2. В такой ситуации представляется рациональным говорить о «коридоре безопасных значений» показателя, а не только о его нижней границе. Мониторинг ScvO2 может быть полезен при обширных хирургических вмешательствах, кардиогенном шоке различного генеза, кровопотере и остановке кровообращения.
Показатели центральной и смешанной венозной сатурации следует интерпретировать с учетом других гемодинамических показателей (ЧСС, АД, ЦВД, СВ, ГКДО) и маркеров метаболической активности органов (темп диуреза, PvCO2, градиент тканевого или гастрального PCO2 и PaCO2, концентрация лактата и др.). Измерение венозной сатурации может быть полезным «скрининговым тестом» для дальнейшей детальной оценки гемодинамики, в частности исследования преднагрузки, сердечного выброса и прочих показателей. При критических состояниях использование этих показателей и ранняя целенаправленная терапия нарушений могут способствовать выявлению метаболического стресса и тканевой гипоксии и, следовательно, выбору адекватной лечебной тактики. Кроме того, показатель венозной сатурации, как и прочие «метаболические маркеры», может быть использован для оценки эффективности и безопасности ряда лечебных мероприятий, например, отлучения от ИВЛ или прекращения инотропной поддержки.