т лимфоциты это какой иммунитет
Т лимфоциты это какой иммунитет
Оба типа лимфоцитов образуются у эмбриона из полипотентных гемопоэтических стволовых клеток, формирующих лимфоциты как один из наиболее важных результатов их дифференцировки. Почти все сформированные лимфоциты в результате заселяют лимфоидную ткань, однако прежде чем это произойдет, они дополнительно дифференцируются или проходят предварительную обработку.
Лимфоциты, которые в итоге станут активированными Т-лимфоцитами, сначала мигрируют к тимусу, где подвергаются предварительной обработке. Эти ответственные за клеточно-опо-средованный иммунитет лимфоциты называют Т-лимфоцитами, что подчеркивает роль тимуса.
Другая популяция лимфоцитов, В-лимфоциты, предназначенные для формирования антител, проходят предварительную обработку в печени плода в середине периода внутриутробной жизни, а также в костном мозге в конце внутриутробной жизни плода и после рождения. Эта популяция клеток впервые была открыта у птиц, имеющих специальный орган для их предварительной обработки, который называют бурсой Фабриция (фабрициевой сумкой). Ответственные за гуморальный иммунитет лимфоциты называют В-лимфоцитами, что подчеркивает роль бурсы.
На рисунке ниже показаны две лимфоцитарные системы для формирования: (1) активированных Т-лимфоцитов; (2) антител.
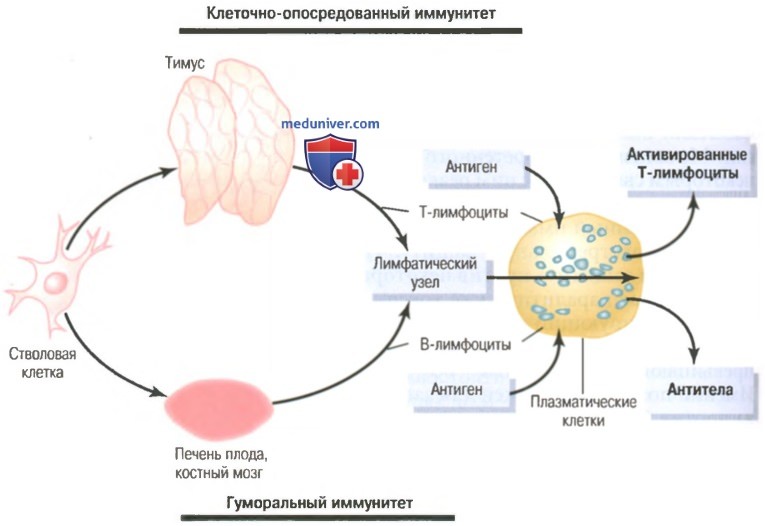
Этот рисунок также демонстрирует происхождение лимфоцитов тимуса (Т-лимфоцитов) и бурсы (В-лимфоцитов), ответственных за клеточно-опосредованные и гуморальные иммунные процессы, соответственно
Предварительная обработка Т- и В-лимфоцитов
Все лимфоциты организма происходят от коммитированных в лимфоцитарном направлении стволовых клеток эмбриона, но эти клетки не могут непосредственно превратиться в активированные Т-лимфоциты или антитела. Прежде чем это станет возможным, клетки должны подвергнуться дальнейшей дифференцировке в соответствующих областях, где они проходят специфическую обработку.
а) Т-лимфоциты проходят предварительную обработку в тимусе (вилочковой железе). После образования в костном мозге Т-лимфоциты сначала мигрируют к вилочковой железе. Здесь они быстро делятся, одновременно становясь чрезвычайно разнообразными, т.е. предназначенными для реакции против разных специфических антигенов. Это значит, что один лимфоцит, обработанный в тимусе, проявляет специфическую реактивность в отношении одного антигена. Следующий лимфоцит специфически реагирует на другой антиген. Это продолжается до тех пор, пока в тимусе не появятся тысячи разных типов лимфоцитов со специфической реактивностью в отношении тысяч разных антигенов. Эти разные типы предварительно обработанных Т-лимфоцитов оставляют тимус и распространяются кровью по всему телу, временно оседая в лимфоидной ткани.
Кроме того, благодаря обработке в тимусе любой оставляющий его Т-лимфоцит не реагирует с белками или другими антигенами собственных тканей организма (иначе Т-лимфоциты погубили бы собственное тело человека в течение всего нескольких дней). Тимус выбирает, какие Т-лимфоциты могут его покинуть, сначала смешивая их практически со всеми специфическими аутоантигенами собственных тканей тела. Если Т-лимфоцит реагирует, он разрушается и фагоцитируется, вместо того, чтобы выделяться. Это происходит с основной частью клеток (вплоть до 90%). Таким образом, клетки, выделяющиеся из тимуса, не реагируют против собственных антигенов тела; они реагируют лишь на антигены внешних источников, например бактерий, токсинов или тканей, пересаженных от другого человека.
Основная часть предобработки Т-лимфоцитов в тимусе происходит перед рождением ребенка и в течение нескольких месяцев после рождения. Удаление вилочковой железы после этого периода ослабляет (но не исключает) Т-лимфоцитарную иммунную систему. Однако удаление тимуса за несколько месяцев до рождения может нарушить развитие всего клеточно-опосредован-ного иммунитета. Поскольку именно клеточный тип иммунитета в основном отвечает за отторжение трансплантированных органов, например сердца или почек, органы можно пересаживать с меньшей вероятностью отторжения, если у животного в соответствующее время до его рождения удалить тимус.
б) В-лимфоциты проходят предварительную обработку в печени и костном мозге. О деталях предварительной обработки В-лимфоцитов известно гораздо меньше, чем о предобработке Т-лимфоцитов. Известно, что у человека предварительная обработка В-лимфоцитов осуществляется в печени в середине внутриутробного периода развития, а также в костном мозге в конце внутриутробного периода и после рождения.
Существуют два важных различия между В- и Т-лимфоцитами. Во-первых, В-лимфоциты активно секретируют реактивные агенты, называемые антителами, в отличие от Т-лимфоцитов, реагирующих с антигеном непосредственно. Антитела — это крупные белковые молекулы, способные соединяться с антигенной субстанцией и разрушать ее. Во-вторых, разнообразие В-лимфоцитов выражено больше, чем у Т-лимфоцитов, т.е. формируются миллионы типов В-лимфоцитарных антител с разными специфическими реактивностями. После предобработки В-лимфоциты, как и Т-лимфоциты, мигрируют к лимфоидной ткани по всему телу, где временно располагаются рядом, но несколько обособленно от областей локализации Т-лимфоцитов.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
ЗдоровьеКак Т-лимфоциты спасут нас от коронавируса и почему они лучше, чем антитела
В пандемию мы все научились немного больше заботиться о своём здоровье. И точно так же стали немного лучше разбираться в том, о чём раньше даже не подозревали: устройстве иммунной системы человека, взаимодействии её с вирусами разных типов и антителах. Последние особенно интересны в контексте приобретённого иммунитета, который позволяет переболевшим COVID-19 (кому-то больше, кому-то меньше) оставаться защищёнными от коронавируса.
Но вот в чём проблема: не у всех людей с симптомами коронавируса обнаруживаются антитела. Как такое возможно? Ответом на задачу со звёздочкой стали Т-лимфоциты. Учёные уже доказали, что сформированная ими защита может быть прочнее и совершеннее. Обо всём этом давайте немного подробнее.
ТЕКСТ: Марина Левичева
Иммунитет врождённый и адаптивный
Иммунная система представляет собой сложную сеть связанных между собой клеток, которая защищает организм от внутренних и внешних угроз. Сам иммунитет при этом бывает двух типов: врождённый (естественный) и адаптивный (приобретённый). В основном они отличаются друг от друга специфичностью и оперативностью реагирования на врага.
Врождённый иммунитет — наша первая линия защиты. Она может обнаружить многие патогены, как только они попадают в организм. Но, во-первых, она не всегда делает это достаточно быстро, чтобы мы успели не заболеть, во-вторых, она всё-таки не может распознать все потенциально опасные молекулы.
Если что-то идёт не так и врождённый иммунитет не справляется, система посылает сигналы, чтобы активировать адаптивную иммунную систему. Этот процесс называется презентацией антигена, потому что компоненты системы естественного иммунитета буквально представляют Т-лимфоцитам захваченный ими антиген (разве что без слов «Теперь это ваша проблема»).
Адаптивная иммунная система развивалась, чтобы обеспечить организму лучшую защиту. Но её полноценный запуск довольно медленный, так что может пройти несколько дней, прежде чем в игру вступят звёзды этой вечеринки — Т-клетки.
Т-клетки и что о них нужно знать
Из школьной программы многие помнят, что за иммунитет у нас ответственны лимфоциты. Существует два типа лимфоцитов: В-клетки, которые образуются и созревают в костном мозге, и Т-клетки, которые также образуются в костном мозге, но созревают в вилочковой железе (тимусе), расположенной в верхнем отделе грудной клетки. В организме они работают вместе, но Т-клетки всё равно круче.
Дело в том, что Т-клетки нацелены на выявление и устранение специфических инородных частиц. Вместо того, чтобы атаковать все антигены подряд (а это бактерии, вирусы, токсины и даже пыльца — всё, что заставляет организм вырабатывать антитела), Т-клетки циркулируют до тех пор, пока не столкнутся со «своим» антигеном. Они определяют его с помощью белков на поверхности, которые могут связываться с белками на поверхности антигенов. Существуют триллионы вариантов этих поверхностных белков, каждый из которых может распознать собственную мишень.
Роль Т-клеток немного меняется на протяжении жизни. В детстве с их помощью у нас формируется иммунитет к общим патогенам и создаётся запас Т-клеток памяти. Они буквально запоминают реакцию на те или другие антигены, поэтому, встречая их в будущем, реагируют быстрее и эффективнее (это называется вторичным иммунным ответом). Дальше
Т-клетки в основном занимаются иммунорегуляцией и работой с повторяющимися или постоянно присутствующими (при наличии хронических заболеваний) в организме антигенами. С возрастом их количество снижается, так что чем мы старше, тем слабее становится наш иммунитет.
Т-клетки тоже бывают разных типов. Т-хелперы, например, помогают активности других иммунных клеток, высвобождая информационные молекулы цитокины. Они стимулируют созревание В-клеток, которые уже начинают вырабатывать антитела для нейтрализации патогена. А
Т-киллеры (цитотоксические T-лимфоциты) самостоятельно убивают повреждённые или инфицированные клетки организма.
Хотя Т-клетки в основном наши друзья и защитники, иногда они могут стать причиной аутоиммунных заболеваний. Это происходит, когда путешествующие в поисках своего антигена клетки начинают атаковать собственные клеточные белки человека.
Что не так с антителами
Основная проблема антител в том, что они не очень долго сохраняются в организме. Есть данные, что уровень антител у людей, инфицированных SARS-CoV-2, снижается в течение 2–3 месяцев. Это справедливо, что так бывает не всегда, потому что срок жизни антител, по всей видимости, зависит от патогена.
Антитела к другим коронавирусам могут, постепенно уменьшаясь, сохраняться от 12 до 52 недель с момента заражения. Но в случае
с COVID-19 это может продолжаться до семи недель, а может и больше. Другое недавнее исследование показало, что при бессимптомном течении заболевания уровень антител значительно ниже и в 40 % случаев они полностью исчезают через восемь недель.
Получается, что с антителами пусть и всё так, но защита, которую они обеспечивают, не настолько продолжительная и мощная, как того хотелось бы.
Т-клетки и коронавирус
Так как большинство людей раньше не подвергались воздействию нового коронавируса (на то он и новый), у них нет Т-клеток памяти и, соответственно, защиты от инфекции. Хорошая новость в том, что инфицированные люди при этом могут генерировать COVID-специфические Т-клетки. Причём, как показало исследование шведских учёных, это происходит также у пациентов со слабыми симптомами или вообще без них. И даже в том случае, если в организме нет антител.
А ещё обнаружилось, что некоторые неинфицированные люди имеют
Т-клетки к COVID-19. Это, вероятнее всего, является перекрёстной реактивностью — совпадением с реакцией организма на предыдущие коронавирусные инфекции. Когда учёные посмотрели на образцы крови, взятые за несколько лет до начала пандемии, и обнаружили в них Т-клетки, приспособленные к обнаружению белков на поверхности COVID-19, теория подтвердилась.
Почему это всех так радует? Потому что Т-клеточные реакции могут быть довольно длительными. Когда учёные из Сингапура проанализировали показатели людей, перенёсших атипичную пневмонию в 2003 году, они увидели, что даже спустя семнадцать лет у них остались специфические
Т-клетки. Не говоря уже о том, что наличие Т-клеток более точно показывает, переболел человек коронавирусом или нет.
Что выяснили российские учёные
Совсем недавно в авторитетном научном журнале Immunity опубликовали исследование российских учёных на тему Т-клеток и коронавируса, в котором приняли участие 34 переболевших коронавирусом добровольца и две контрольные группы здоровых доноров.
«Действительно, не у всех переболевших коронавирусом обнаруживаются антитела. У части выздоровевших иммунный ответ обеспечивается только за счёт Т-клеток, чего, по всей видимости, оказывается достаточно», — объясняет Григорий Ефимов, заведующий лабораторией трансплантационной иммунологии Национального медицинского исследовательского центра (НМИЦ) гематологии Минздрава и один из авторов исследования.
Учёные также отметили, что ответ на фрагменты коронавируса есть не только у тех, кто им переболел, что может объясняться сезонными простудными заболеваниями в прошлом, которые были вызваны коронавирусами других типов. «При этом здоровые доноры, которых мы набирали во время пандемии, в среднем имели более высокий уровень ответа, чем те, образцы которых хранились в биобанке и были получены раньше. Скорее всего, это значит, что часть доноров имела контакт с вирусом, вызывающим COVID-19, не подозревая об этом», — добавляет Григорий Ефимов.
Одно из самых интересных открытий — обнаружение фрагментов вируса,
Т-клеточный ответ на которые у людей возникает особенно часто. По словам исследователей, прямо сейчас они заняты изучением этих фрагментов, так как лучшее их понимание даст информацию для разработки теста
на Т-клеточный иммунитет. Пока он используется только как научный инструмент, но если всё пойдёт хорошо, в ближайшее время может стать доступным и для диагностики тоже.
Диагностика Т-клеточного иммунитета: пандемия как драйвер инновации
Диагностика Т-клеточного иммунитета: пандемия как драйвер инновации
Т-клеточный стартап TScan Therapeutics начал коллаборацию с компанией Qiagen для разработки теста на Т-клеточный иммунитет к COVID-19
Автор
Редакторы
Статья на конкурс «Био/Мол/Текст»: Споры о вакцинах и иммунитете против нового коронавируса кажутся бесконечными! От обсуждения ПЦР-диагностики и тестов на антитела дискуссии постепенно смещаются в сторону стойкости иммунитета: но измерить иммунитет человека по-прежнему сложно. Узнаем о том, как пандемия вдохнула новую жизнь в старую технологию и станет ли диагностика клеточного иммунитета доступной, в статье специалиста по Т-клеткам Софьи Касацкой.
Конкурс «Био/Мол/Текст»-2020/2021

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Вакцинация от коронавирусной инфекции SARS-CoV-2 — одна из самых горячих тем на границе 2020 и 2021 гг. Не утихают споры о безопасности вакцин, разработанных в сжатые сроки, о принципах производства и об основных принципах иммуногенности. Много спорят и о том, стоит ли добровольно прививаться тем, кто уже успел переболеть COVID-19, или, по крайней мере, подозревает об этом. Достаточно ли привиться один раз, а если вирус будет мутировать, как действовать дальше? Достаточно ли переболеть один раз или стоит бояться заболеть одной и той же инфекцией раз в сезон?
Для того чтобы ответить на эти вопросы и понять историю прошлых болезней, нужно изучить иммунную память (также ее называют иммунологической). Как правило, для проверки иммунной памяти на конкретную инфекцию проверяют наличие антител в плазме крови: ИФА-тест на антитела класса IgG (ИФА — иммуноферментный анализ). В этом тесте подсчитывается количество антител, которые сорбируются (прилипают) к стандартизированным антигенам, то есть молекулам, встречающимся именно у возбудителя данной инфекции и нигде больше. Антитела, в особенности класса IgG, поразительно точно и выборочно контактируют с однажды «выбранной» молекулой: мало где в биологии можно найти более точные и постоянные молекулярные контакты. Тем не менее тест на антитела — по большей части дань историческому процессу, а не «золотой стандарт» тестирования иммунной памяти. Пандемия стремительно изменила многие аспекты нашей жизни — может ли она поменять и то, что мы считаем стандартом в диагностике иммунитета?
Увидеть адаптивный иммунитет
«Биомолекула» неоднократно писала об уникальных механизмах, которые обеспечивают работу этой удивительной регуляторной системы — системы адаптивного иммунитета человека [1–3].
Чтобы увидеть Т-клетки и В-клетки разных типов, иммунологи чаще всего используют проточную цитометрию (FACS) [4]. Например, если мы хотим увидеть клетки памяти, то крепим флуоресцентную метку на молекулу, присутствующую только на поверхности клеток иммунной памяти, и подсчитываем клетки, пролетающие по одной через лазер и детектор флуоресценции.
Так можно узнать процент клеток, выполняющих определенную функцию, например, весь объем клеток памяти в крови на все прошлые инфекции. Теперь усложним задачу и выделим только клетки памяти на конкретную инфекцию — например, интересующий всех SARS-CoV-2, — как это сделать? Мы можем увидеть недавно активированные клетки среди клеток памяти. Лимфоциты из образца крови пациента смешиваются и инкубируются с молекулами, принадлежащими вирусу, чаще всего, — с очищенными белками, нарезанными на фрагменты. Т- и В-клетки, способные узнать и связать вирусный антиген, активируются, станут активированными эффекторными клетками, и мы сможем их различить среди всей иммунной памяти на FACS-анализе. Такие тесты проводятся в качестве дополнительных научных исследований.
Тест требует не только несколько часов на выделение клеток и их активацию вирусными белками либо пептидами, но и время дорогостоящего специалиста по проточной цитометрии, у которого прибор для FACS всегда работает и настроен, а не простаивает. Сочетание сразу двух факторов приводит к тому, что метод далеко не массовый. Можно представить метод рутинным в нескольких ведущих медицинских центрах, но сложно распространить: на порядки сложнее, чем внедрить регулярное ПЦР-тестирование.
Антитела или Т-лимфоциты
В качестве гораздо более дешевого и доступного теста, чем FACS, иммунологи смотрят не на сами клетки, а на то, что иммунные клетки производят [5]. Вспомним рецепторы, которые служат для решения задачи точного, прочного и выборочного связывания вирусных белков-антигенов. Т-клетки держат рецепторы на поверхности, на клеточной мембране. А вот В-лимфоциты свои уникальные рецепторы синтезируют как в мембранной, так и в растворимой форме — эти растворимые В-клеточные рецепторы и есть антитела. Получается, что вместо флуоресцентных меток и В-клеток памяти можно просто измерить концентрацию антител? Вдобавок, учебник иммунологии рассказывает, что В-клетки формируют память с помощью Т-клеток. Значит ли это, что если антитела есть, то уже произошло формирование памяти: сначала на уровне Т-клеток, затем на уровне В-клеток?
Да, текущие представления об иммунологии человека говорят: высокий уровень антител подразумевает, что Т-клеточный иммунный ответ тоже есть. Тем не менее известны и неклассические механизмы, при которых В-клетки быстро начинают производить антитела (чаще классов IgD, IgM) вне особых зон лимфоузла и при меньшем контроле со стороны Т-клеток. Обратная логика оказывается неверной: Т-клеточная иммунная память не зависит от наличия антител в крови, формируется независимо и сохраняется дольше.
Интуитивно кажется, что было бы отлично сохранять в крови антитела к коронавирусу после вакцинации или инфекции на всю жизнь. Некоторые инфекции формируют такой иммунный ответ, и это коррелирует с иммунной защитой, то есть вероятностью не заболеть при повторном заражении [6]. Но для других инфекций уровень антител в крови достаточно быстро, за несколько месяцев, снижается. Так происходит потому, что за свою жизнь человек встречает сотни тысяч типов вирусов, и производить антитела на все вирусные антигены просто невозможно. Приходится выбирать, происходит конкуренция с защитой от других инфекций, а также конкуренция с антителами, которые нужны для регуляции собственной физиологии организма. Антитела постепенно снижают концентрацию и пропадают из крови, но сохраняются В-клетки памяти, которые смогут вновь производить нужные антитела при необходимости.
Было бы идеально, чтобы организм производил антитела и держал их в оптимальной концентрации в крови не во время повторной болезни, а чуть заранее: до заражения. Именно для этого существуют сезонные ревакцинации: небольшая бустерная доза антигена поступает заранее и через 9–14 дней иммунитет снова подготовлен к сезонному контакту с большим количеством вирусных частиц вокруг. А постоянное, круглогодичное производство антител на высоком уровне можно оставить тем В-лимфоцитам, которые действительно каждый день сталкиваются с одними и теми же бактериями и вирусами: например, В-лимфоцитам слизистой ЖКТ, работающим с кишечными симбионтами.
ELISPOT: ИФА для Т-клеток?
Антитела оказались удобным для измерения косвенным маркером иммунной памяти, но отсутствие антител еще не говорит об отсутствии Т-клеточной памяти. Специфичную иммунную память Т-клеток, к сожалению, нельзя измерить так же легко, по нескольким миллилитрам плазмы крови. Как упоминалось выше, Т-клетки не секретируют свои рецепторы в растворимом виде. Зато Т-лимфоциты, в соответствии со своей ролью дирижеров всего иммунного ответа, вырабатывают множество сигнальных молекул — цитокинов. Цитокины, в большинстве своем, — тоже растворимые молекулы, и их концентрацию можно измерить в объеме (суммарно), либо «подсветить» с помощью флуоресцентных меток сразу при их секреции из специфичных Т-клеток (и увидеть соответствие клетка—сигнал). На этом принципе основан иммуноферментный анализ на клональных отпечатках Т-клеток, или ELISPOT (enzyme-linked immunosorbent spot).
Как правило, Т-хелперы секретируют сигнальные цитокины, чья основная задача — активировать нужную ветвь иммунного ответа, привлечь клетки врожденного иммунитета и подавить конкурирующие сигналы. Среди функций цитокинов — подача сигналов внутри иммунной системы — от Т-клеток и для Т-клеток для уточнения принятия решений. Подобная информация «для внутреннего использования» передается и от Т-хелперов Т-киллерам, и в обратном направлении. Яркий пример такого сигнала — интерферон-гамма: активированные Т-киллеры секретируют IFNγ наравне с Т-хелперами. Массовая выработка интерферона позволяет быстро распространить информацию на уровне всего организма. На основе измерения продукции IFNγ Т-клетками разработан самый надежный из ELISPOT-тестов на антиген-специфичный Т-клеточный ответ [7], [8].
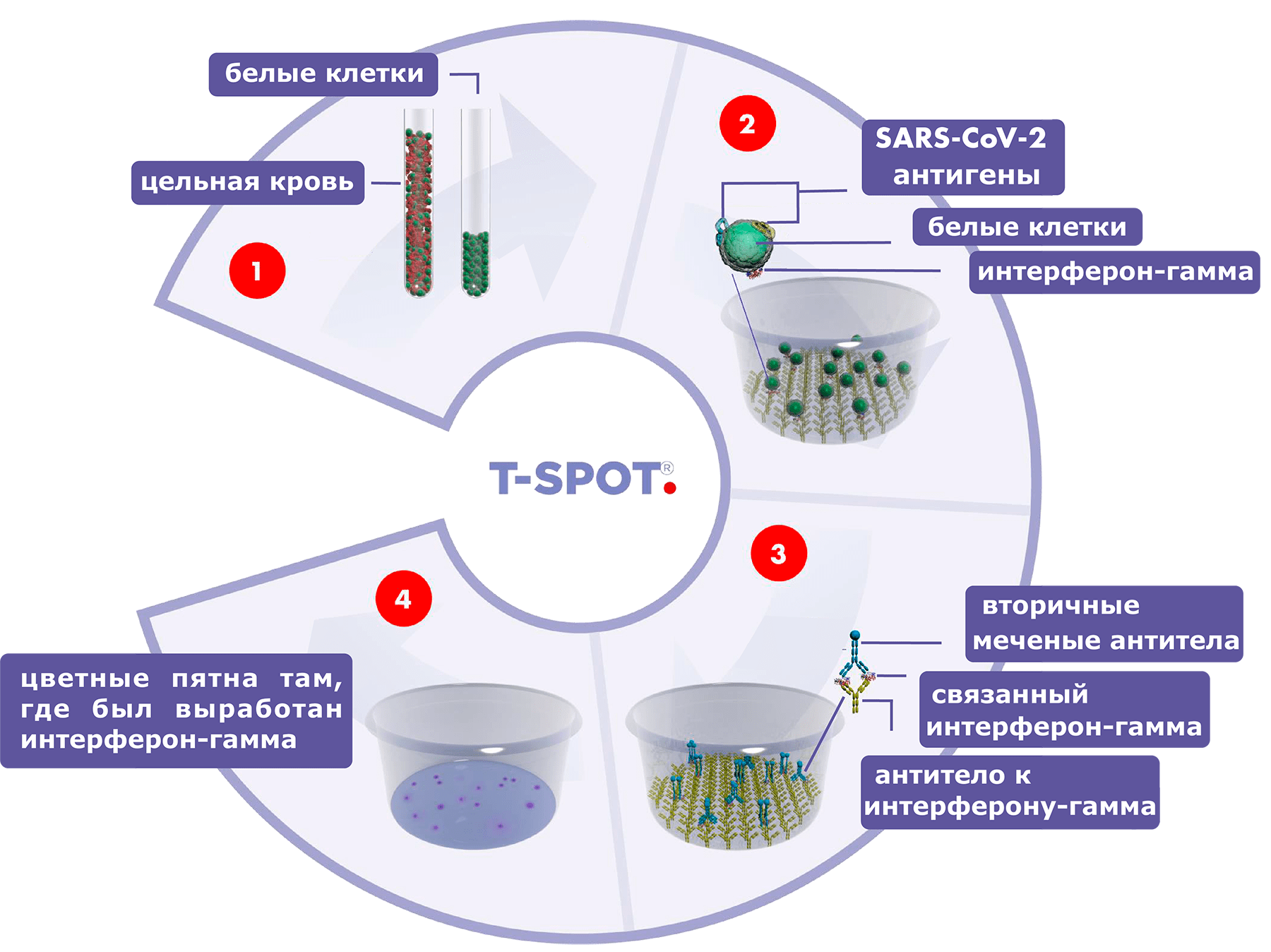
Для ELISPOT живые изолированные Т-клетки периферической крови инкубируются с антигенами, как правило, белковыми либо пептидными. Этот процесс должен имитировать то, как в организме Т-клетки в лимфоузлах узнают антигены и активируются: процесс презентации антигена. Небольшая доля специфичных клеток узнает антигены и производит IFNγ, причем интерферон сразу фиксируется и позже визуализируется в точке секреции. В процессе активации Т-клетки делятся: из одной клетки образуется целый клон антигенспецифичных клеток, все они производят интерферон, и при визуализации «пятно» продукции интерферона растет в диаметре (рис. 1). При ELISPOT сложно точно сказать, сколько антигенспецифичных клонов было изначально в образце до активации, размножения и формирования пятна. Остается неясным, сколько Т-клеток узнают антиген in vivo, но не прореагировали из-за искусственной формы презентации антигена, не похожей на то, как Т-клетки обычно активируются в лимфоузлах. С другой стороны, метод немного проще оптимизировать в лаборатории и проще делать для многих пациентов одновременно, чем более дорогостоящий FACS-анализ; требующиеся приборы и реагенты дешевле.
Рисунок 1. Схема работы теста ELISPOT, определяющего активацию Т-лимфоцитов при взаимодействии с антигенами нового коронавируса SARS-CoV-2
[11], рисунок с изменениями
Поиск коронавирусных Т-клеток. Инновация TScan
ELISPOT используется во всех лабораториях, которые исследуют иммунитет человека. Метод ELISPOT и его модификации на пересекающихся пулах пептидов (наборах фрагментов, на которые нарезается белковый антиген) использовались в исследованиях эффективности вакцин от ВИЧ, и позже медленно распространились на исследования и других вакцин. В диагностических лабораториях метод стал популярен потому, что для более точной диагностики туберкулеза необходимо оценивать Т-клеточный иммунный ответ. Коммерческий тест получил название T-SPOT. Кроме туберкулеза, для других инфекций аналогичная диагностика не применялась — до 2020 года и кризиса, вызванного новой коронавирусной инфекцией SARS-CoV-2. Необходимость широкой диагностики самой инфекции и иммунной памяти к ней подтолкнула одновременно исследователей и производителей диагностических тестов к разработке новых методов и оптимизации старых и привычных. Интерес к быстрому и дешевому измерению Т-клеточной памяти растет параллельно с популярными в медиа опасениями, что у переболевших COVID-19 быстро пропадают антитела в крови.
Очень многие академические коллективы, которые работают на стыке биохимии, иммунологии человека и прикладных биотехнологий, весной 2020 года стали заниматься разработками для борьбы с пандемией, в том числе разрабатывать и налаживать диагностику инфекции. Нельзя не упомянуть пример коллектива Григория Ефимова из НМИЦ гематологии в Москве, активно работающий как над диагностикой Т-клеточного иммунитета к новому коронавирусу на основе FACS, так и в коллаборации по созданию одного из ИФА-тестов для определения антител к антигенам SARS-CoV-2 [9], [10]. Тем не менее вернемся к теме масштабируемого производства быстрых ELISPOT-тестов на Т-клеточный иммунитет: откуда берутся такие разработки, тоже из фундаментальных и клинических академических лабораторий?
Первой ELISPOT-тест на ковид (T-SPOT Discovery SARS-CoV-2 assay) выпустила компания Oxford Immunotec, ранее создавшая одну из самых популярных версий теста на туберкулез [11]. Этот тест использует пул разнообразных антигенов коронавируса и активацию Т-клеток в смеси с другими лейкоцитами периферической крови: иначе говоря, дизайн теста даже несколько упрощен по сравнению с тестом на туберкулез (рис. 1).
Куда более интересную модификацию запустил небольшой биотех-стартап под названием TScan Therapeutics. Этот стартап переориентировался на инфекционную иммунологию во время пандемии. Как и многие другие коллективы, к примеру, BioNTech (разработчик вакцины от коронавируса совместно с Pfizer), до пандемии они занимались онкологией и задачей оптимальной активации противоопухолевого иммунитета.
Осенью 2020 года TScan Therapeutics подписали соглашение о совместной разработке диагностического теста ELISPOT-типа с компанией Qiagen — крупнейшим производителем лабораторных реагентов и универсальных наборов для типовых экспериментов в молекулярной и клеточной биологии [12], [13]. Эта диагностика Т-клеточной памяти во многом отличается от версии Oxford Immunotec, и в первую очередь отличается идеологически: оксфордская компания быстро и практично сделала аналог своего существующего продукта-бестселлера, сохранив всю платформу и протокол метода и изменив только антиген. TScan же демонстрирует почти идеальный инновационный подход: вначале провели исследования Т-клеточного иммунитета, опубликовали выводы в престижном журнале Immunity, затем появилась идея для диагностического теста и, наконец, возможность производства в партнерстве с Qiagen.
Исследование TScan раскрывает детали того, какие молекулы среди белков коронавируса вызывают наибольший «интерес» у Т-клеток человека [14]. Иммунная память Т-киллеров, согласно исследованию, формируется не только и не столько на фрагменты антигена (эпитопы) S-белка коронавируса, на котором сфокусировано большинство вакцин 2020 года [15]. Напротив, эпитопов гораздо больше в нуклеокапсидном основном белке [16]. Далее, специалисты TScan показали отсутствие перекрестного иммунитета: антигены «сезонных» неопасных человеческих коронавирусов формируют память Т-киллеров, но эти Т-киллеры не способны отреагировать на коронавирус SARS-CoV-2. Наоборот, между SARS-CoV-1 (вызвавшим вспышку атипичной пневмонии в 2003 году) и SARS-CoV-2 существует значительная кросс-реактивность Т-клеток (переболевшие атипичной пневмонией могут быть защищены от SARS-CoV-2).
Обнаружение важнейших участков вируса, вызывающих долгую Т-клеточную память — это поиск иммунодоминантных эпитопов. Если активировать Т-клетки именно такими пептидами, можно существенно повысить качество диагностического теста. Уникальные данные TScan позволяют вычесть фон иммунной памяти на родственные и далекие коронавирусы и поднять специфичность диагностики иммунной памяти. При этом используется платформа, сходная с ELISPOT, что позволяет объединять много образцов и делать тест быстрым и широко доступным. Сейчас исследования Т-клеточного иммунитета при коронавирусе проводится либо в рамках научных исследований, либо на коммерческой основе, но точность и интерпретация теста затруднена, клиент получает результат через 1–2 неделю после теста. Партнерство TScan с Qiagen вселяет оптимизм по поводу доступности теста: ведь продукцией этой компанией пользуются буквально в каждой молекулярной и биохимической лаборатории на планете.
Интересна еще одна деталь. Исследователи из TScan брали донорские Т-клетки у доноров с наиболее распространенными в США генотипами других важных иммунных молекул: молекул HLA (молекул главного комплекса гистосовместимости, Human Leukocyte Antigen) подтипов HLA-A*02:01, HLA-A*01:01, HLA-A*03:01, HLA-A*11:01, HLA-A*24:02 и HLA-B*07:02. В зависимости от типа молекул HLA Т-клетки будут распознавать разные эпитопы одного и того же вируса. А поскольку у разных людей максимально вариабельные молекулы HLA, то и иммунный ответ Т-клеток у каждого формируется максимально индивидуально. Именно с этим связаны и сложности/дороговизна изучения Т-клеточного иммунитета, и невозможность «перелить иммунную память» переливанием крови — такой эксперимент может получиться только внутри пары однояйцевых близнецов. С другой стороны, даже в этом огромном разнообразии реакций клеточного иммунитета Т-клетки разных доноров, отвечающие на новый коронавирус, обладают некоторыми общими характеристиками.
Данные об общих параметрах иммунного ответа, которые будут накапливаться в совместных исследованиях TScan/Qiagen, представляют несомненный интерес для оптимизации лечения пациентов и создания методов лечения, таргетно направленного на активный и безопасный Т-клеточный ответ. Здесь проявляется особая черта сильных deeptech-стартапов в области биологии, биоинформатики и биотехнологий: технологическая платформа может быть использована не только для одного применения и быстрого завоевания рынка, а для разных задач, и в процессе, по ходу решения прикладной задачи возникают ценные, качественные и заметные научные открытия. Конечно, новость о сотрудничестве TScan и Qiagen — всего лишь одна из множества историй о биотех-прорывах 2020 года, и легко могла затеряться среди других новостей и инноваций. Но в этой неприметной новости заложен мощный потенциал, способный изменить современные представления о клинической диагностике иммунной памяти.