тени боткина гумпрехта встречаются при каком заболевании
Тени боткина гумпрехта встречаются при каком заболевании
Актуальность темы
Хронический лимфолейкоз (ХЛЛ) является наиболее распространенным среди заболеваний кроветворной системы человека. В Европе и Северной Америке ХЛЛ очень распространенный вид лейкоза. На долю ХЛЛ приходится примерно тридцать процентов от всех видов лейкозов. Ежегодная заболеваемость составляет три случая на сто тысяч человек, увеличиваясь для лиц старше шестидесяти пяти лет до двадцати, а старше семидесяти – до пятидесяти случаев на сто тысяч человек. Больные ХЛЛ – это люди обычно старшей возрастной группы, которые имеют множество сопутствующих заболеваний с различной степенью недостаточности функции систем органов, которые затрудняют лечение основного заболевания [6]. Однако, в последние годы наметилась тенденция к увеличению больных молодого возраста. Чаще всего ХЛЛ можно встретить у мужчин, соотношение больных мужского и женского пола составляет два к одному. Осложнения инфекционной природы чаще всего являются главной причиной, приводящей к смерти больных с этим заболеванием [2]. Смертность от инфекций составляет от тридцати до пятидесяти процентов от всех случаев со смертельным исходом. Несмотря на прогресс в лечении и диагностики данного заболевания, ХЛЛ остается неизлечимым, поэтому так важно вовремя диагностировать ХЛЛ и осуществлять терапию, чтобы избежать серьезных осложнений и продлить жизнь.
Хронический лимфолейкоз, или хронический лимфоцитарный лейкоз (ХЛЛ) – злокачественное клональное лимфопролиферативное заболевание, которое характеризуется накоплением атипичных CD5/CD23-положительных В-лимфоцитов в крови, костном мозге, лимфатических узлах, печени и селезенке. В проявлении ХЛЛ важную роль играют наследственность и нарушения иммунологической реактивности. Клетка-предшественница лимфопоэза является источником опухоли. Чаще всего субстратом опухоли являются В-лимфоциты, но бывают и Т-лимфоциты. Cвойственен абсолютный лимфоцитоз в периферической крови (по данным гемограммы) и костном мозге (по данным миелограммы)[7]. На ранних стадиях лимфоцитоз может являться единственным проявлением заболевания. Больные могут жаловаться на так называемые «конституциональные симптомы» – хроническую усталость, сниженную работоспособность, повышенную потливость, спонтанную потерю веса. Cвойственно генерализованное увеличение лимфатических узлов – внутригрудных и внутрибрюшных. Обнаруживается при ультразвуковом или рентгенологическом исследовании, периферические лимфоузлы доступны для прощупывания. Достигают больших размеров, образовывают мягкие или плотноватые конгломераты. Сдавление внутренних органов обычно не наблюдается. На поздних стадиях ХЛЛ может наблюдаться увеличение печени и селезенки. Данная патология может проявляться чувством тяжести либо дискомфорта в области левого подреберья, феноменом раннего насыщения пищей. За счет того, что увеличивается количество опухолевых клеток в костном мозге и вытесняется нормальный гемопоэз, на поздних стадиях наблюдается анемия, снижение тромбоцитов, иногда встречается пониженный уровень нейтрофильных гранулоцитов. Поэтому больные могут жаловаться на общую слабость, головокружения, точечные кровоизлияния, экхимозы и спонтанную кровоточивость. Анемия и тромбоцитопения также могут иметь аутоиммунного происхождения. Для заболевания cвойственно выраженное подавление иммунитета, которое затрагивает в большей степени гуморальный иммунитет (гипогаммаглобулинемия). Поэтому имеется предрасположенность к инфекциям, например, рецидивирующим простудным заболеваниям.
Интересным клиническим проявлением заболевания может быть гиперреактивность на укусы насекомых [1]. В развитии хронического лимфолейкоза выделяют три стадии:
1.Начальная – умеренное увеличение лимфоузлов, умеренная спленомегалия, характерные изменения периферической крови и костного мозга (лимфоидная пролиферация).
2.Развернутая (выраженные клинико-гематологические проявления): увеличение лимфатических узлов и селезенки, типичные изменения периферической крови и костного мозга, иммунные нарушения.
3. Терминальная – слабость организма, истощение, невосприимчивость к проводимому лечению, развитие тяжелых осложнений, достаточно выраженная анемия, существенное увеличение лимфатических узлов и спленомегалия(увеличение селезенки).
Кроме данной стадийности заболевания выделяют такие клинические варианты ХЛЛ как: доброкачественная и прогрессирующая формы болезни. При доброкачественной форме можно увидеть несущественное увеличение количества лимфоцитов в крови, очаговый (не диффузный) рост лимфоидной ткани в костном мозге, незначительное увеличение количества пролимфоцитов. При прогрессирующей форме количество лимфоцитов в крови достаточно увеличено, в костном мозге имеется диффузная лимфоидная пролиферация[2].
Диагностика хронического лимфолейкоза
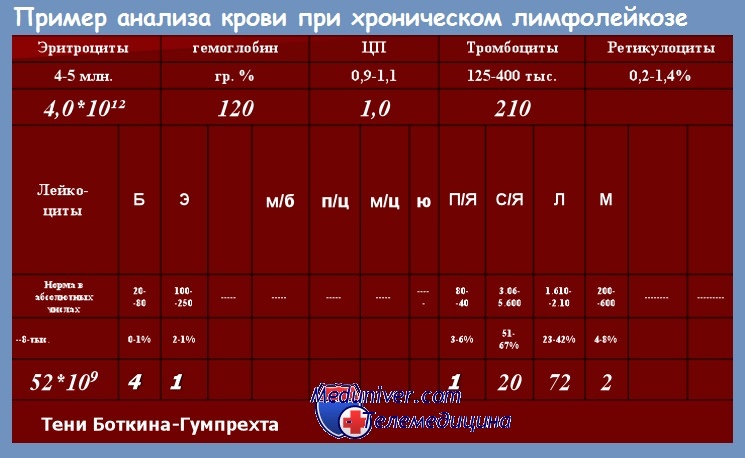
Главная роль принадлежит исследованию общего анализа крови и пунктата костного мозга. Первым лабораторным признаком ХЛЛ может являться лейкоцитоз с относительным и абсолютным лимфоцитозом. Морфологически лимфоциты не отличаются от нормальных. Пролимфоцитов обычно не более двух процентов.
Имеется редкий вариант хронического лимфолейкоза, где пролимфоцитов больше десяти процентов, но меньше 55% (при количестве пролимфоцитов больше 55% диагностируется пролимфоцитарный лейкоз). Течение данного варианта заболевания намного агрессивнее и приближается к пролимфоцитарному лейкозу [3]
Можно увидеть тени Боткина-Гумпрехта – это разрушенные ядра лейкемически измененных лимфоцитов (Во время приготовления мазка лимфоциты больного хроническим лимфолейкозом могут раздавливаться и повреждаться, что обуславливает появление «теней Боткина-Гумпрехта»). При прогрессировании нарастает лейкоцитоз и лимфоцитоз, анемия и тромбоцитопения. Анемия и тромбоцитопения могут иметь аутоиммунный характер, это подтверждается обнаружением антител и положительной реакцией на глюкокортикостероиды [5]
Диагностическое значение имеют обнаружение более тридцати процентов лимфоцитов в миелограмме (если аспират не разведен периферической кровью) и лимфоидная инфильтрация костного мозга по данным трепанобиопсии. Характер инфильтрации костного мозга имеет прогностическое значение: нодулярное и интерстициальное поражение более благоприятно, чем диффузное.
При хроническом течении лимфолейкоза отсутствуют патогномоничные изменения биохимических показателей. Однако, может часто наблюдаться увеличение содержания мочевой кислоты (при лейкоцитозе), количества общей ЛДГ, которая отражает объем опухолевой массы и является неблагоприятным прогностическим показателем, а также гипогаммаглобулинемия, коррелирующая с частотой инфекционных осложнений.
Первым маркером, который имеет корреляцию с мутационным статусом, стал CD38+. Пороговый уровень экспрессии CD38+ на лимфоцитах в периферической крови при ХЛЛ составляет тридцать процентов. Выявлена прямая зависимость между отсутствием мутаций IgVH-генов и экспрессией тирозинкиназы ZAP-70, липопротеинлипазы (LPL) и металлопротеазы (ADAM29). Кроме вышеуказанных факторов, имеется не менее десятка других прогностических факторов, к которым можно отнести, например, мутацию гена BCL6, экспрессию гена BCL2, уровень лактатдегидрогеназы (ЛДГ), β2-микроглобулин в сыворотке крови, экспрессию цитокинов (ИЛ-4, ИЛ-6) и фактора роста эндотелия сосудов (VEGF).
При проведении иммунофенотипирования рекомендуется оценивать экспрессию CD38, ZAP-70 и CD52. Экспрессия CD38 и/или ZAP-70 коррелирует с обнаружением «u-CLL» и является плохим прогностическим показателем. Маркер CD52 – «мишень» для лечения моноклональным анти-CD52 антителом (Campath-1) [3].
Цитогенетические и молекулярно-генетические исследования при хроническом лимфолейкозе. При рутинном цитогенетическом исследовании изменения кариотипа человека обнаруживаются более чем у половины больных ХЛЛ, при FISH-анализе – у 80%. К наиболее распространенным аномалиям относятся трисомия хромосомы 12 (20% случаев), делеция хромосом llq (20%), 13q и 14q (50%), 6q21 (5%) или 17р13 (локус р53 – 10% случаев). При изменениях кариотипа, особенно множественных, прогнозом является осложнение состояния пациента.
Диагноз В-клеточного хронического лимфолейкоза правомочен при наличии таких признаков как:
1) абсолютный лимфоцитоз периферической крови более 10 * 109/л;
2) при световой микроскопии лимфоциты имеют нормальную морфологию (меньше 10% атипичных лимфоцитов);
3) характерный иммунофенотип;
4) лимфоцитарная инфильтрация костного мозга (более 30% лимфоцитов при исследовании миелограммы, лимфоидная метаплазия костного мозга в трепанобиоптате)[4].
Дифференциальный диагноз проводится с заболеваниями, сопровождающимися увеличением лимфатических узлов и лимфоцитозом. К ним относятся другие лимфопролиферативные заболевания (неходжкинские лимфомы, волосатоклеточный лейкоз), вирусные (краснуха, корь, цитомегаловирус, ВИЧ-инфекция, герпес, инфекционный мононуклеоз) и такие бактериальные инфекции как токсоплазмоз, туберкулез.
Клиническая картина при реактивных и опухолевых лимфаденопатиях и лимфоцитозах не имеет главного значения для диагностики, но следует учитывать ряд некоторых гематологических показателей (во всех случаях отсутствуют тени Гумпрехта, при вирусных инфекциях возможно появление небольшого количества плазматических клеток, для неходжкинских лимфом и волосатоклеточного лейкоза cвойственен полиморфизм лимфоцитов и другой иммунофенотип) [3].
Проведение дифференциальной диагностики и постановка окончательного диагноза хронического лимфолейкоза основаны на результатах гистологического исследования лимфатического узла и трепанобиосии костного мозга, анализа миелограммы, иммунофенотипа лимфоцитов, данных серологических и культуральных обследований (для исключения инфекционных заболеваний).
Инструментальная диагностика направлена обчно на выявление изменений в селезенке и печени. Для этого обычно применяется ультразвуковое исследование [5].
Вывод
Анализ возможностей терапии и диагностики на протяжении времени показывает, что хронический лимфолейкоз из неизлечимого заболевания превратился в заболевание, которое очень часто при своевременном обнаружении можно успешно лечить, продлевая жизнь и благополучие больных, поддерживая качество жизни пациента. Ранняя диагностика заболевания имеет большое значение в этом вопросе. Большое значение для диагностики и дифференциального диагноза имеет определение иммунофенотипа.
Постановка данного диагноза может быть осуществлена при обнаружении: 1) абсолютный лимфоцитоз периферической крови более 10 • 109/л; 2) при световой микроскопии лимфоциты имеют нормальную морфологию (меньше 10% атипичных лимфоцитов); 3) характерный иммунофенотип;
4) лимфоцитарная инфильтрация костного мозга (более тридцати процентов лимфоцитов при исследовании миелограммы, лимфоидная метаплазия костного мозга в трепанобиоптате).
Тени боткина гумпрехта встречаются при каком заболевании
Лимфолейкоз – это злокачественное заболевание, при котором костный мозг вырабатывает большое количество незрелых, неспособных выполнять свои функции лимфоцитов. Лимфоциты являются разновидностью лейкоцитов и отвечают за иммунитет. Злокачественные лейкоциты не справляются с защитной функцией, при этом подавляют образование нормальных клеток крови и нарушают работу других органов.
Существует много разновидностей этого заболевания. Лимфолейкозы делят в зависимости от скорости развития патологического процесса, степени зрелости лимфоцитов, типа поврежденных лимфоцитов (Т- и В-лимфоциты). Однако чаще всего выделяют 2 основных типа: острый лимфобластный лейкоз и хронический лимфоцитарный лейкоз.
Лечение лейкозов обычно комплексное. На данный момент существует несколько вариантов терапии, и каждый год появляются новые, все более эффективные методы лечения лимфолейкозов. Прогноз при остром лимфолейкозе благоприятный – 95 % пациентов полностью излечиваются. Прогноз при хроническом лимфолейкозе зависит от скорости развития заболевания и сопутствующих патологий, он неуклонно прогрессирует, однако соответствующее лечение часто приводит к ремиссии и значительному улучшению состояния пациента.
Острый лимфолейкоз, острый лимфоцитарный лейкоз, острый лимфобластный лейкоз, хронический лимфолейкоз, хронический лимфоцитарный лейкоз.
Pediatric acute lymphoblastic leukemia, childhood acute lymphoblastic leukemia, acute lymphocytic leukemia, ALL, chronic lymphocytic leukemia, CLL.
Острый лимфобластный лейкоз развивается достаточно быстро – обычно в течение нескольких недель. Симптомами его являются:
Хронический лимфоцитарный лейкоз обычно никак не проявляется на начальной стадии. Он развивается годами, и постепенно возникают следующие симптомы:
Общая информация о заболевании
Лимфоциты – это разновидность лейкоцитов. Как и все остальные клетки крови, лимфоциты образуются из единой стволовой клетки, которая находится в костном мозге и дает начало лимфоидной и миелоидной стволовым клеткам. От лимфоидной стволовой клетки происходят лимфоциты, от миелоидной – другие виды лейкоцитов, эритроциты и тромбоциты.
Для того чтобы из лимфоидной стволовой клетки развились зрелые Т- и В-лимфоциты, она должна пройти через ряд последовательных делений. Сначала из лимфоидной стволовой клетки образуются лимфобласты, которые затем дают начало 2 типам клеток – предшественникам Т-лимфоцитов и предшественникам В-лимфоцитов. В процессе деления клетки становятся все более зрелыми и специализированными. Последние этапы созревания лимфоцитов проходят уже не в костном мозге, а в лимфоидных органах: тимусе, лимфатических узлах и селезенке. В результате формируются зрелые Т- и В-лимфоциты.
Лимфоциты, по сути, – клетки иммунитета. Это значит, что они участвуют в распознавании и уничтожении чужеродных тел (вирусов, бактерий) или патологически измененных тканей собственного организма (например, клеток опухоли). Т- и В- лимфоциты делают это по-разному. В-лимфоциты борются с чужеродными клетками (антигенами) с помощью иммуноглобулинов – белков, которые связывают антигены и запускают процесс их разрушения специальными белками. Т-лимфоциты распознают антигены, разрушают их самостоятельно или при взаимодействии с другими клетками крови, активируют выработку иммуноглобулинов В-лимфоцитами.
При лимфолейкозе нарушается формирование лимфоцитов. Появляется большое количество незрелых клеток, которые не способны выполнять свою работу. Это приводит к серьезным сбоям иммунитета. Человек становится более подвержен таким инфекционным заболеваниям, как туберкулез, кандидоз. Могут возникать серьезные осложнения от плановых прививок. Часто появляются так называемые аутоиммунные реакции – то есть иммунитет борется с нормальными клетками организма, например эритроцитами. В результате возникает анемия.
Злокачественные лимфоциты проникают в лимфатические узлы и селезенку, вызывая их увеличение, могут повреждать печень, легкие, головной мозг, кости.
При остром лимфолейкозе в костном мозге преобладают лимфобласты. Они очень быстро делятся, вытесняют из костного мозга и крови другие клетки, активно заселяют лимфатические узлы, селезенку. Чаще всего встречаются острые В-клеточные лейкозы, при которых образуется большое количество незрелых В-лимфоцитов. Острый В-клеточный лейкоз – самый распространенный вид лейкозов среди детей.
При хроническом лимфолейкозе в крови находят более зрелые формы лимфоцитов, которые способны некоторое время выполнять свои функции. Этот тип лейкоза характерен для людей старше 50-55 лет.
Кто в группе риска?
При остром лимфолейкозе в группе риска:
При хроническом лимфолейкозе в группе риска:
При хроническом лимфолейкозе лимфобласты обычно отсутствуют в крови. Характерным признаком хронического лейкоза является обнаружение в мазке крови клеток (или теней) Боткина – Гумпрехта. Они представляют собой остатки разрушенных лимфоцитов. Тени Боткина – Гумпрехта отсутствуют в жидкой крови и образуются в процессе приготовления мазка. Их количество определяет интенсивность разрушения лимфоцитов в крови.
При остром лимфобластном лейкозе прогноз благоприятный, особенно у детей. Большинство пациентов полностью излечиваются. Прогноз хронического лимфолейкоза зависит от скорости прогрессирования болезни и чувствительности к химиотерапии. Средняя продолжительность жизни пациентов с хроническим лимфолейкозом составляет 3-5 лет.
Специфической профилактики лимфолейкозов нет. Необходимо своевременно проходить профилактические осмотры, в ходе которых нередко выявляют заболевания крови.
Рекомендуемые анализы
Тени боткина гумпрехта встречаются при каком заболевании
Диагноз хронического лимфолейкоза (ХЛЛ) может быть установлен при абсолютном количестве лимфоцитов в крови более 5•10 9 /л, наличии в костно-мозговом пунктате не менее 30 % лимфоцитов и иммунологическом подтверждении клонового В-клеточного характера лимфоцитоза.
В подавляющем большинстве случаев предположение о наличии у больного хроническим лимфолейкозом (ХЛЛ) возникает в связи с изменениями картины крови: обнаружение абсолютного и относительного лимфоцитоза. Международное рабочее совещание в 1989 г. установило среди критериев для постановки диагноза хронического лимфолейкоза наличие абсолютного лимфоцитоза в крови не менее 10 • 109/л, однако позже это положение было пересмотрено. В настоящее время для предположения о заболевании ХЛЛ считается достаточным наличие абсолютного лимфоцитоза 5•10 9 /л.
Иногда на протяжении 2—3 лет при числе лейкоцитов, лишь незначительно превышающем норму или даже соответствующем нормальному показателю, наблюдается постепенно нарастающий лимфоцитоз — 50—60—70 %. Эти изменения лейкоцитарной формулы еще не являются оснаванием для постановки диагноза хронического лимфолейкоза без дополнительных исследований: пункции костного мозга и иммунологического исследования крови и костно-мозгового пунктата. Тем не менее такой пациент должен быть под пристальным наблюдением врача: обязательны осмотр и анализы крови каждые 3—4 мес, поскольку, как правило, такие изменения крови являются проявлением начала хронического лимфолейкоза.
В крови среди ядерных элементов обнаруживается преобладание зрелых лимфоцитов — клеток малого размера, округлых, с плотным ядром и узким ободком светлой или слегка базофильной цитоплазмы. В мазках крови обычно определяется то или иное количество клеток Гумпрехта—Боткина — полуразрушенных размытых ядер лимфоцитов. Их появление связано с повышенной ломкостью мембраны лимфоцитов при хроническом лимфолейкозе.
Количество клеток Гумпрехта — Боткина, как правило, больше у больных с высоким лейкоцитозом. Клетки, или, как их нередко называют, тени Гумпрехта — Боткина, образуются при приготовлении мазка, их наличие и количество не имеют прогностического значения.
Количество лейкоцитов при хроническом лимфолейкозе может быть различным, в большинстве случаев при установлении диагноза хронического лимфолейкоза оно составляет 20—50•10 9 /л, но нередко при первом обращении к врачу уже имеется гиперлейкоцитоз (100—500 • 10 9 /л), свидетельствующий о длительном недиагностированном периоде заболевания. Мы наблюдали больного, у которого при первом обращении к врачу по поводу длительно существующих увеличенных лимфатических узлов количество лейкоцитов оказалось 1200•10 9 /л.
При подсчете лейкоцитарной формулы содержание лимфоцитов обычно составляет 50—70 %, при высоком лейкоцитозе иногда достигает 95—99 %. Наряду со зрелыми лимфоцитами в крови обычно в очень небольшом количестве (как правило, не более 1—3 %) удается обнаружить пролимфоциты — более крупные клетки с отчетливой нуклеолой в ядре. Постепенное увеличение содержания пролимфоцитов в течение болезни, так же как их постоянное присутствие в количестве 10 % и более, является плохим прогностическим признаком.
Е. Matutes и соавт. на большом клиническом материале показали, что выживаемость больных хроническим лимфолейкозом прямо коррелирует с числом циркулирующих пролимфоцитов и значительно снижается уже при числе пролимфоцитов более 5 %.
На основании изучения морфологической картины крови почти 550 больных ХЛЛ Е. Matutes и соавт. выделили примерно 15 % больных с необычной морфологией клеток. Они предложили считать таких больных страдающими атипичным ХЛЛ, отметив два его подтипа: один с повышенным более 10 % количеством пролимфоцитов и второй — с лимфоплазмоцитоидной дифференцировкой лимфоцитов и/или наличием лимфоцитов с расщепленным (cleaved) ядром. Во втором случае одновременно имеются обычные лимфоциты, характерные для хронического лимфолейкоза, и переходные формы — более крупные лимфоциты с выраженной базофилией цитоплазмы или с намечающейся расщелиной ядра.
Течение болезни в этом случае обычно не отличается от характерного для типичного хронического лимфолейкоза, однако нередко при обоих указанных вариантах имеется трисомия хромосомы 12. При обоих подтипах: повышенном количестве пролимфоцитов и лимфоплазмоцитоидной морфологии лимфоцитов — течение болезни у больных с трисомией хромосомы 12 более агрессивное.
Костно-мозговой пунктат при хроническом лимфолейкозе обычно гиперклеточный, инфильтрация лимфоцитами чаще всего имеет диффузный характер, хотя иногда встречаются случаи нодулярной инфильтрации. В большинстве случаев процентное содержание лимфоцитов значительно превышает необходимые для установления диагноза 30 %, нередко достигая 90—95 %.
Лимфоциты в костном мозге морфологически не отличаются от лимфоцитов крови, но обычно имеется 3—5 % пролимфоцитов даже в тех случаях, когда они не обнаруживаются в крови.
При морфологическом исследовании лимфатического узла обнаруживают стирание нормального рисунка и мономорфную инфильтрацию лимфоцитами, морфологически сходными с лимфоцитами крови и костного мозга, иногда имеющими несколько большие размеры. В небольшом количестве встречаются пролимфоциты и клетки, названные параиммунобластами: клетки среднего размера с дисперсным хроматином и круглыми или овальными ядрышками. В селезенке преобладает инфильтрация белой пульпы, хотя красная пульпа обычно тоже оказывается в той или иной степени инфильтрированной малыми лимфоцитами.
Несмотря на характерную картину, результаты морфологического исследования не могут считаться достаточными для установления диагноза хронического лимфолейкоза (ХЛЛ), поскольку аналогичная морфологическая картина крови и костного мозга нередко наблюдается при фолликулярной и мантийно-клеточной лимфомах с поражением костного мозга. Согласно современным критериям, диагноз хронического лимфолейкоза может считаться установленным только после иммунологического исследования, подтверждающего диагноз. Патологические лимфоциты при хроническом лимфолейкозе имеют абсолютно характерный иммунофенотип.
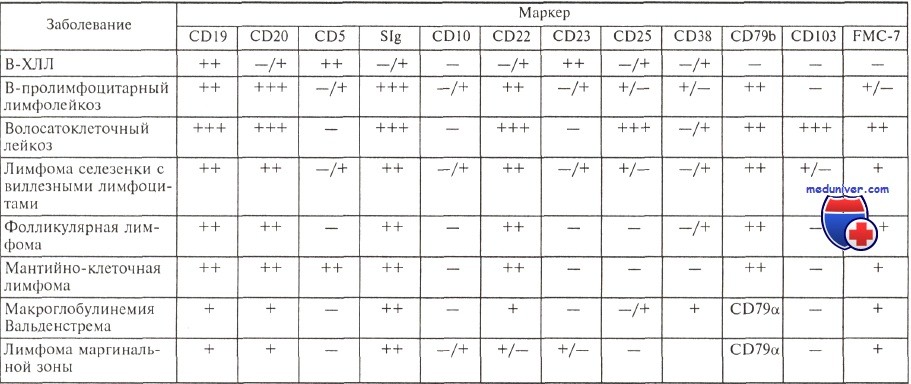
Они экспрессируют антигены CD19, CD5, CD23, отмечается слабая экспрессия на поверхности клеток иммуноглобулинов (экспрессируются IgM, нередко одновременно с IgD) с одной L-цепью, определяется слабая экспрессия антигенов CD20 и CD22, у ряда больных экспрессируется молекула FMC-7. Антиген CD79b, или Igb, являющийся частью В-клеточного рецептора, либо не экспрессируется, либо экспрессируется очень слабо в подавляющем большинстве случаев.
Характерный иммунофенотип опухолевых клеток позволяет отличить В-ХЛЛ от других лимфопролиферативных заболеваний.
Е. Matutes и соавт. предложили числовую систему, помогающую при дифференциальной диагностике В-ХЛЛ и других лимфопролиферативных заболеваний. По этой системе каждый иммунологический признак, характерный для В-ХЛЛ, расценивается как 1 балл, его противоположное значение — как 0.
Иммунофенотип опухолевых клеток при различных лимфопролиферативных заболеваниях
Иногда возникают трудности в дифференциальной диагностике хронического лимфолейкоза и так называемого монокло-нового В-лимфоцитоза неопределенного значения (MLUS — monoclonal lymphocytosis of undetermined significance), названного так по аналогии с моноклоновыми гаммапатиями неопределенного значения (MGUS). Термин был впервые введен еще в конце 80-х годов прошлого века для отличия непрогрессирующего моноклонового лимфоцитоза без признаков ХЛЛ от индолентного ХЛЛ с признаками заболевания. В настоящее время чаще употребляется термин CLUS (clonal lymphocytosis of undetermined significance).
При CLUS обычно на протяжении многих лет сохраняются умеренный и стабильный лейкоцитоз и лимфоцитоз (меньше необходимых для диагноза ХЛЛ 5•10 9 /л), нормальные показатели эритро- и тромбоцитопоэза, отсутствует увеличение лимфатических узлов и селезенки.
В наблюдениях С. Wang и соавт. клиническая картина и лабораторные показатели при CLUS оставались неизменными на протяжении 3—10 лет. Клоновая природа лимфоцитоза была подтверждена рестрикцией L-цепи экспрессируемых на поверхности лимфоцитов иммуноглобулинов. Никаких хромосомных аберраций на протяжении всего времени наблюдения выявлено не было. У всех пациентов исследование иммунофенотипа на протяжении всего времени наблюдения обнаруживало экспрессию лимфоцитами антигенов CD19, CD20 и слабую экспрессию поверхностных иммуноглобулинов, однако неизменно выявляло отсутствие экспрессии CD5 и CD23. Таким образом, данные наблюдения не отвечают всем признакам В-ХЛЛ. Однако в большинстве случаев иммунофенотип при CLUS не отличается от типичного иммунофенотипа В-ХЛЛ. A. Rowstron на основании анализа нескольких сотен наблюдений раннего стабильного хронического лимфолейкоза и сравнения их с CLUS указывает, что частота прогрессирования в этих случаях одинакова и не превышает 10 %.
Известно, что истинный хронический лимфолейкоз, имеющий все необходимые для установления диагноза черты, также может годами не проявлять признаков прогрессирования. В подобных случаях имеется характерный для данного заболевания иммунофенотип, а при длительном наблюдении (в одном нашем наблюдении спустя 22 года со времени постановки диагноза) во многих случаях появляются черты прогрессирующего хронического лимфолейкоза. В других наблюдениях клиническая картина сохраняется неизменной на протяжении всей жизни больного.
Мы наблюдали больную в течение 29 лет, которая не получала никакого лечения, поскольку все это время у нее была стабильная гематологическая и клиническая картина: отсутствие увеличенных лимфатических узлов и селезенки, количество лейкоцитов 15—20•10 9 /л, лимфоцитов 65—70 %. Это наблюдение похоже на наблюдения Т. Han и соавт., описавших 10 больных с лейкоцитозом более 10 • 109/л и моноклоновым В-клеточным лимфоцитозом, у которых в течение 6—24 лет не было признаков прогрессирования и которые не нуждались в терапии.
Возможно, эти наблюдения являются отражением возрастного изменения В-клеточного репертуара. Почти 10 лет назад было обнаружено, что у мышей с возрастом постепенно суживается разнообразие клонов В-клеток (В-клеточный репертуар) и одновременно происходит увеличение размеров (амплификация) отдельных клонов. N. Chiorazzi и М. Ferrarini указывают, что у здоровых людей старше 50 лет наличие таких клонов В-лимфоцитов является обычным. Возможно, отдельные клоны, возникшие под влиянием длительной стимуляции определенным антигеном, могут приобретать значительные размеры и определяться при рутинном иммунологическом исследовании.
Обнаруженная недавно в половине исследованных методом FISH случаев CLUS делеция 13ql4, являющаяся самой частой генетической аберрацией при ХЛЛ, подтверждает мнение о том, что CLUS следует расценивать как раннюю стадию хронического лимфолейкоза доброкачественного течения. В то же время P. Ghia и соавт., обследовав 500 здоровых людей старше 65 лет, обнаружили у части из них клоны клеток с иммунофенотипом, характерным для различных лимфопролиферативных заболеваний, иногда у одного и того же больного. Авторы полагают, что это, скорее всего, является не ранней стадией болезни, а отражением постепенно суживающегося с возрастом В-клеточного репертуара.
В 1982 г. описан постоянный поликлоновый В-лимфоцитоз у курящих женщин средних лет. У некоторых из них были частые респираторные заболевания. Это редкий феномен, и со времени первой публикации появилось не более 90 подобных описаний. Исследования с помощью ПЦР показали, что во всех изученных случаях имеется реаранжировка BCL-2/IgH, которая, однако, не всегда сопровождалась повышенной экспрессией BCL-2.
У некоторых курящих женщин с поликлоновым В-лимфоцитозом обнаружены незначительное увеличение размеров селезенки и поликлоновая гамма-патия, которые, как и лимфоцитоз, иногда исчезали после прекращения курения.
Несколько случаев поликлонового В-лимфоцитоза описаны у некурящих. С помощью ПЦР у некоторых пациентов в крови был обнаружен вирус Эпштейна—Барр. Неясно, играет ли этот вирус роль в развитии синдрома поликлонового В-лимфоцитоза.
Очевидно, в настоящее время подобные случаи не являются трудными для дифференциальной диагностики с хроническим лимфолейкозом (ХЛЛ), поскольку поликлоновый характер лимфоцитоза обнаруживается при иммунофенотипировании. Трудности для трактовки представляет описанный недавно случай поликлонового В-клеточного лимфоцитоза с комплексными хромосомными аберрациями — трисомией хромосом 3, 15 и 18, инверсией хромосомы 18, t(13;14) в отдельных клетках у длительно курящей женщины. Гематологическая картина остается стабильной на протяжении нескольких лет наблюдения, но отмечаются часто повторяющиеся инфекции верхних дыхательных путей. Необходимо длительное наблюдение для выяснения вопроса о том, не являются ли имеющиеся хромосомные аберрации отражением начала лимфопролиферативного заболевания.
При некоторых хронических инфекциях (туберкулез, сифилис), иногда при неинфекционных заболеваниях (тиреотоксикоз, болезнь Аддисона) наблюдается постоянный Т-клеточный лимфоцитоз, чаще всего при нормальном количестве лейкоцитов. Его также нетрудно дифференцировать от хронического лимфолейкоза (ХЛЛ) на основании данных иммунологического исследования.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021