Thirads2 что за диагноз
TI-RADS в диагностике рака щитовидной железы
TI-RADS (Thyroid Imaging, Reporting and Data System Lexicon Directory) ― это система оценки ультразвуковых признаков узлов щитовидной железы для отчета о вероятности злокачественности (рака) и показания тонкоигольной пункционной биопсии. Эта система обладает признаками классификации и помогает унифицировать вывод о вероятности рака щитовидной железы и выбора диагностической тактики для врачей разных специальностей. Существуют разные национальные системы TI-RADS, отличающиеся алгоритмом оценки и заключением.
Зачем нужна система TI-RADS?
Проще говоря, система TI-RADS создана для упрощения ультразвуковой диагностики рака узлов щитовидной железы. TI-RADS даёт возможность любому врачу УЗД и эндокринологу одинаково оценивать вероятность рака и своевременно проводить дополнительное исследование ― пункционную биопсию.
Система TI-RADS ― это алгоритм (или последовательность выводов) ведущий к заключению о риске злокачественности и выбору показания к пункции узла железы. Этот алгоритм уменьшает возможность врача ошибиться в диагностике признаков рака при УЗИ, но не исключает такую вероятность. Можно сказать, что система защиты от дурака, т.е. малоопытного или невнимательного врача.
История TI-RADS
Исследователи накапливали знания об ультразвуковых признаках рака узлов щитовидной железы. Поэтому требовалась их систематизации, удобная для практического применения.
Впервые такую систему предложил в 2009 году E.Horvath с соавт. Они создали TI-RADS по аналогии с уже существовавшей системой УЗИ рака молочных желез (BI-RADS). Предложенная E.Horvath с соавт. система TI-RADS оказалось громоздкой и сложной для использования, поскольку каждый вариант этой системы показывал совокупность признаков (паттерн), встречающихся в других вариантах.
Улучшить TI-RADS удалось в 2011 г. J.Y.Kwak и соавт. Эта система имела 6 вариантов TI-RADS, включая безузловое состояние щитовидной железы, а сами варианты и подварианты различались по количеству признаков рака. Эта более удобная система продержалась относительно долго. Почти до 2018 года включительно. Она использовалась в странах Западной Европы и России.
В 2017 году американскими, европейскими и корейскими специалистами отдельно были созданы свои национальные системы TI-RADS. Вместе с тем, отдельные системы TI-RADS создают и в некоторых других странах. В России врачи отдают предпочтение двум системам TI-RADS ― американской и европейской.
Европейская TI-RADS (EU TI-RADS; сентябрь 2017) стала лишь модернизацией системы TI-RADS J.Y.Kwak и соавт. (2011). Авторы EU TI-RADS ― 6 специалистов из Франции, Дании, Турции, Италии и Великобритании.
В связи с некоторыми особенностями EU TI-RADS, ведущая группа отечественных специалистов приняла её за основу для создания русской национальной системы EU TI-RADS. На VIII съезде РАСУДМ (2-6 октября 2019) в выступлениях представителей этой группы по созданию отечественной TI-RADS указывалось на обязательность применения такой оценки при УЗИ щитовидной железы.
Американская система TI-RADS (май, 2017) обладает рядом преимуществ, но, как и другие аналоги, не лишена недостатков и ограничений. Группа из 16 специалистов (они называют себя «комитет») из Американского радиологического колледжа (ACR) и других научно-медицинских организаций США предложила к 2017 г. лучший вариант TI-RADS. Он основан на разделении групп признаков рака (категории) и суммации баллов, присвоенных каждому признаку.
ACR TI-RADS имеет 5 уровней, определяющих процент вероятности рака и показание к пункционной биопсии в зависимости от величины узла. Система ACR TI-RADS оказалась удобной в практическом применении и во многом достоверной в диагностике. В частности, за счет разделения признаков рака узлов ЩЖ и присуждения каждому признаку такого количества баллов, которое соответствует вероятности злокачественности.
В нашей Клинике щитовидной железы доктора А.В. Ушакова в настоящее время в качестве отчетности в Протоколе УЗИ применяется ACR TI-RADS. Вместе с тем, специалисты Клиники компетентны в области других систем TI-RADS.
Система ACR TI-RADS
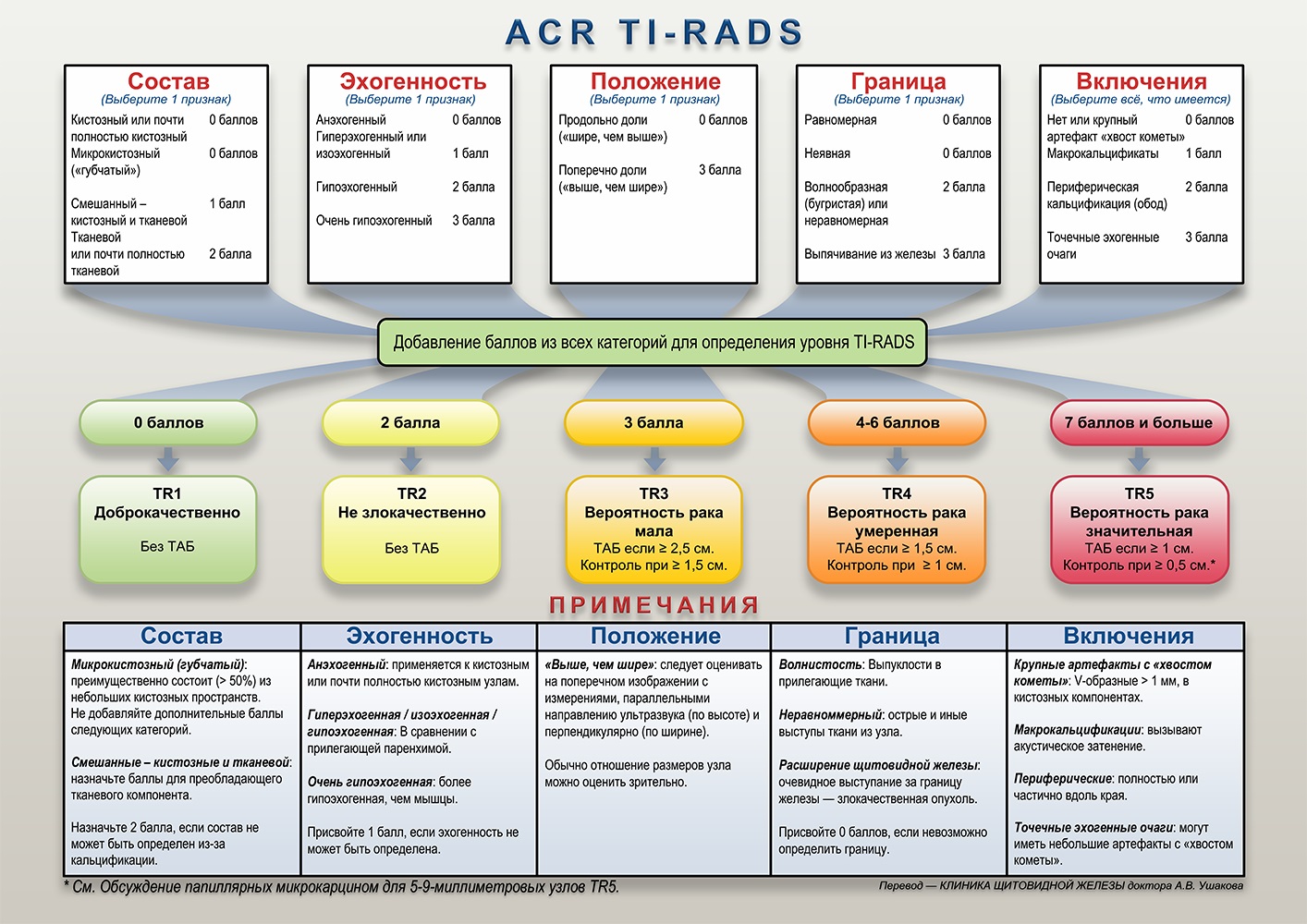
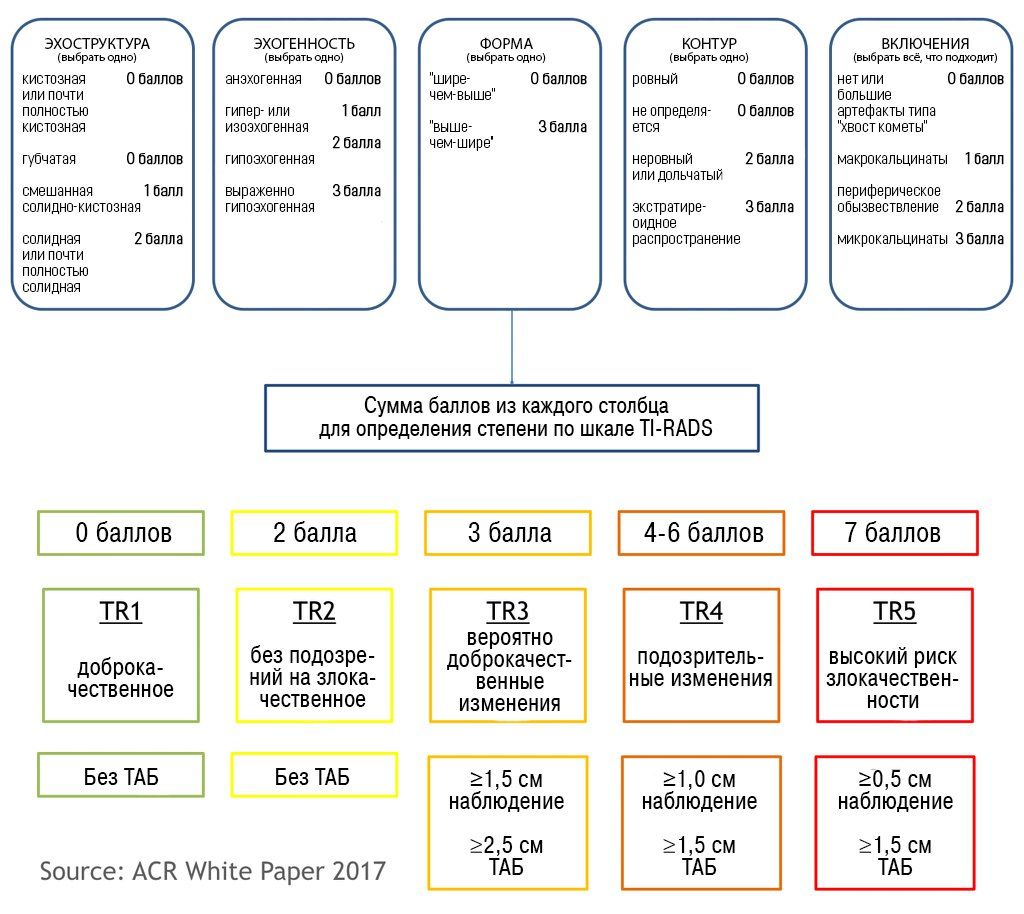
Система ACR TI-RADS определила 5 категорий (групп) признаков рака узлов щитовидной железы (рисунок 1). В ACR TI-RADS не оценивается железа без узлов. Только узлы.
Категории в ACR TI-RADS характеризуют состояние внутри узла, эхогенность ткани узла, расположение узла относительно доли, границу узла и включения внутри узла. Применяется обычная серая шкала (В-режим). Комитет ACR TI-RADS исключил оценку злокачественности по сосудистой сети (при ЭДК или ЦДК) и эластографии-эластометрии.
Рисунок 1 Схема ACR TI-RADS, перевод от Клиники щитовидной железы доктора А.В. Ушакова (по материаламTessler FN, Middleton WD, Grant EG, Hoang JK, Berland LL, Teefey SA, Cronan JJ, Beland MD, Desser TS, Frates MC, Hammers LW, Hamper UM, Langer JE, Reading CC, Scoutt LM, Stavros AT ACR Thyroid Imaging, Reporting and Data System (TI-RADS): White Paper of the ACR TI-RADS Committee. J Am Coll Radiol. 2017 May;14(5):587-595).
Существует 5 уровней AC TI-RADS:
1 уровень ― абсолютная доброкачественность узла,
2 уровень ― отсутствие злокачественности узла,
3 уровень ― малая вероятность злокачественности узла,
4 уровень ― средняя (умеренная) вероятность рака узла,
5 уровень ― значительная вероятность злокачественности узла.
Показание к пункционной биопсии узла
Вероятность злокачественности узла по ACR TI-RADS:
1 уровень ACR TI-RADS ― 0,3%*,
2 уровень ACR TI-RADS ― 1,5%*,
3 уровень ACR TI-RADS ― 4,8%*,
4 уровень ACR TI-RADS ― 9,1%*,
5 уровень ACR TI-RADS ― 35%*.
*по данным Middleton WD, Teefey SA, Reading CC et al. Multiinstitutional analysis of thyroid nodule risk stratification using the American College of Radiology Thyroid Imaging Reporting and Data System. AJR Am J Roentgenol 2017; 208 (6), р.1331-1341.
Обучение врачей ACR TI-RADS
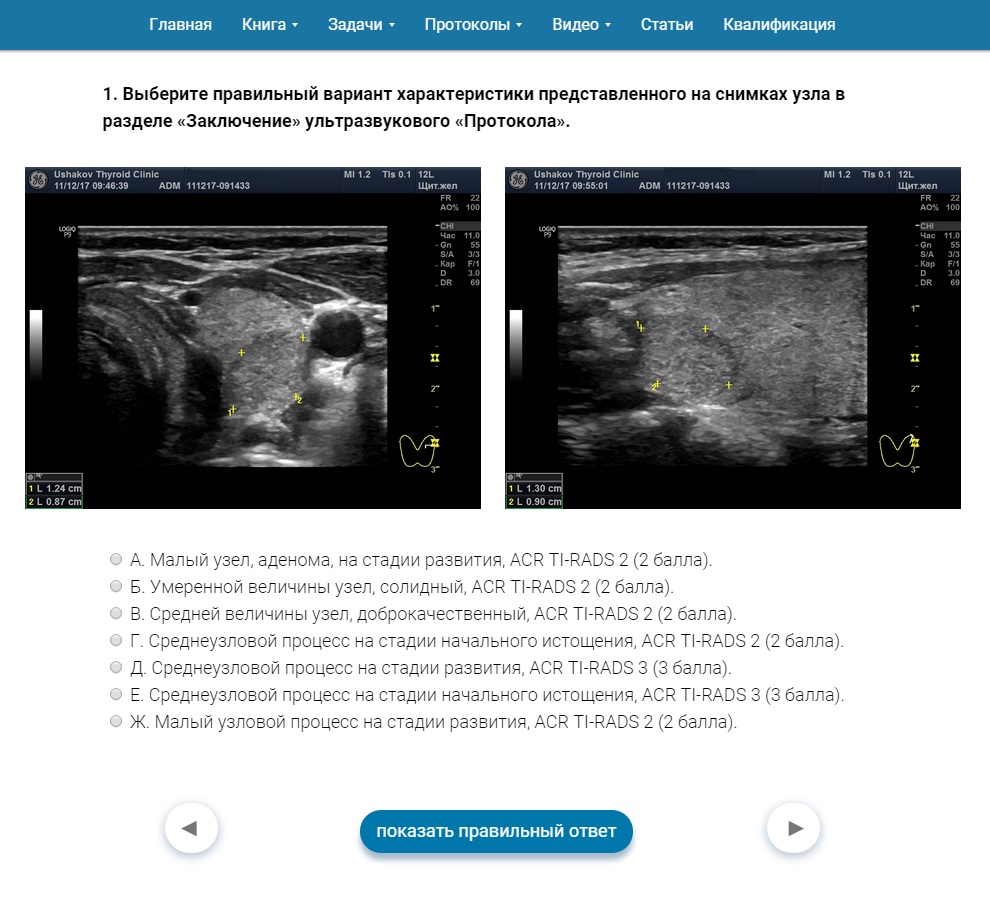
От нашей Клиники создана Научная школа УЗИ щитовидной железы, где подготовлен курс обучения ACR TI-RADS. Этот курс содержит тесты и примеры УЗИ узлов щитовидной железы по ACR TI-RADS (рисунок 2).
Рисунок 2 Более 80 теоретических и практических задач по ACR TI-RADS на сайте Научной школы УЗИ щитовидной железы от Клиники щитовидной железы доктора А.В. Ушакова.
Система EU TI-RADS
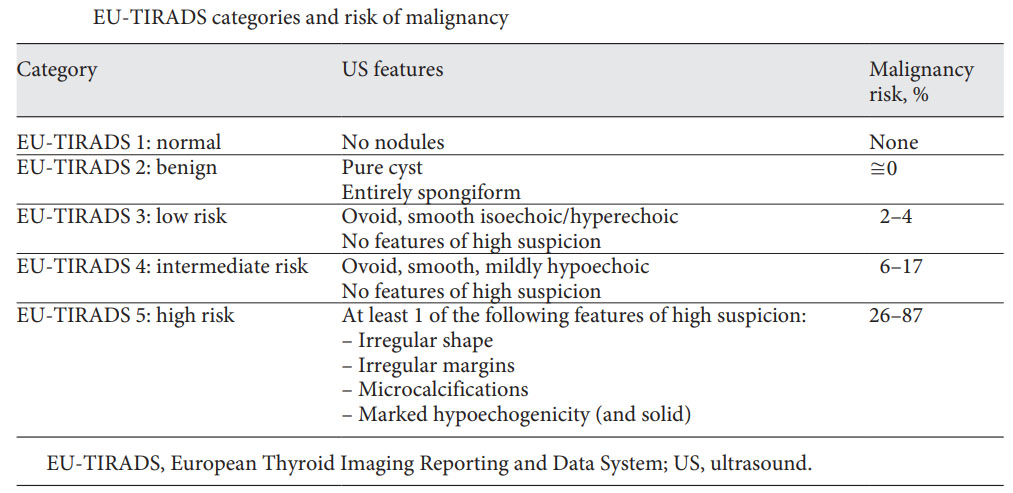
Европейская система TI-RADS, как и система TI-RADS J.Y.Kwak и соавт. (2011). включает 5 категорий, которые в ACR TI-RADS называются уровнями (рисунок 3).
Рисунок 3 Схема EU TI-RADS в таблице, с указанием вероятности злокачественности в процентах (По данным Eur Thyroid J. 2017 Sep;6(5):225-237. Russ G, Bonnema SJ, Erdogan MF, Durante C, Ngu R, Leenhardt L. European Thyroid Association Guidelines for Ultrasound Malignancy Risk Stratification of Thyroid Nodules in Adults: The EU-TIRADS).
К задачам EU TI-RADS авторы отнесли такие же принципы, как ACR TI-RADS:
1) оценка риска развития злокачественности в узлах ЩЖ,
2) единая ультразвуковая терминология,
3) критерии показаний к пункционной биопсии узла ЩЖ,
4) шаблон ультразвуковой отчетности,
5) практическое руководство для специалистов.
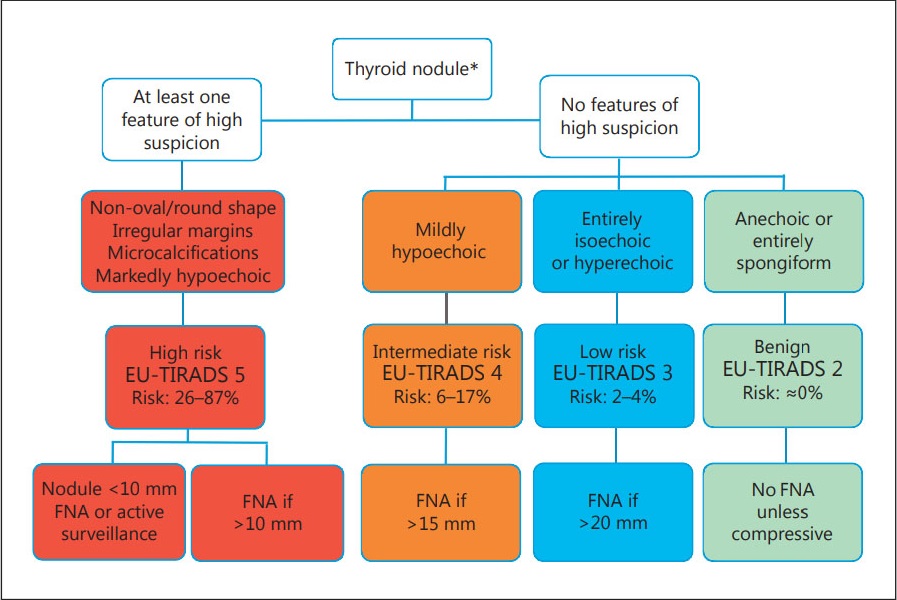
Также как и комитет ACR TI-RADS, авторы EU TI-RADS опирались на многочисленные исследования других специалистов по определению признаков рака и ультразвуковых терминов. В результате, EU TI-RADS создала 11 рекомендаций по применению этой системы анализа и вывода, предоставила пояснение терминам, алгоритм (блок-схему) и рисунок (чертеж), а также примеры ультразвуковой оценки (рисунок 4).
Рисунок 4 Алгоритм (блок-схема) EU TI-RADS (По материалам Eur Thyroid J. 2017 Sep;6(5):225-237. Russ G, Bonnema SJ, Erdogan MF, Durante C, Ngu R, Leenhardt L. European Thyroid Association Guidelines for Ultrasound Malignancy Risk Stratification of Thyroid Nodules in Adults: The EU-TIRADS).
1 категория EU TI-RADS соответствует щитовидной железе без узлов. По мнению нашей Клиники, это совершенно лишняя часть системы, которую исключил комитет ACR TI-RADS.
2 категория EU TI-RADS соответствует 1 уровню системы ACR TI-RADS и применяет абсолютно аналогичные признаки УЗИ в оценке узлов щитовидной железы. Пункционная биопсия не показана (за исключением лечебных целей).
3 категория EU TI-RADS соответствует 2 или 3 уровню системы ACR TI-RADS и применяет подобные сочетания признаков узлов при УЗИ щитовидной железы. Пункционная биопсия показана при наибольшем размере узла от 20 мм и более (По рекомендации экспертов ACR TI-RADS, показание к пункции в таком случае- размер узла более 25 мм).
4 категория EU TI-RADS соответствует 4 уровню системы ACR TI-RADS, поскольку он включает лишь 1 мало выраженный ультразвуковой признак рака узлов щитовидной железы – мало выраженную гипоэхогенность ткани. Пункционная биопсия показана при размере узла от 15 мм и более (Система ACR TI-RADS 4 уровня включает 1 или 2 признака рака, разной выраженности).
5 категория EU TI-RADS соответствует 4 или 5 уровню системы ACR TI-RADS, поскольку он включает 1 и более значительно выраженные ультразвуковые признаки рака узлов щитовидной железы. Пункционная биопсия в таком случае показана при размере узла от 10 мм и более (Система ACR TI-RADS 4 уровня рекомендует диагностическую пункцию узла от 15 мм, а 5 категория – 10 мм).
Авторы EU TI-RADS, как и комитет ACR TI-RADS, изучили результаты исследований по признакам рака узлов щитовидной железы. Поэтому дополнительно к основной системе EU TI-RADS (в рекомендациях и их комментариях) сориентировали в особенностях выбора ультразвуковых или иных проявлений для клинической диагностики злокачественности.
По их мнению, не следует применять допплеровскую оценку кровотока узла (ЦДК или ЭДК), а также контроль величины узлов для выявления рака. Эластография не может заменить обычное УЗИ щитовидной железы в сером режиме в оценке признаков рака, но может использоваться как дополнительный признак (вне системы EU TI-RADS). Также внесистемным признаком доброкачественности, по мнению авторов EU TI-RADS, являются теплые (горячие) узлы по данным сцинтиграфии щитовидной железы.
Советы пациентам по TI-RADS
1. При выявлении узла (узлов) в результате УЗИ, требуйте от врача УЗД обязательно указывать уровень/категорию TI-RADS в Протоколе УЗИ щитовидной железы. Это обязательная норма в России.
2. При указании номера TI-RADS уточняйте, по какой национальной системе проводилось определение (ACR, EU или иное). Всё это должно присутствовать в Протоколе УЗИ щитовидной железы.
3. В случае многоузлового процесса щитовидной железы, как минимум, 3 или 4 узла с признаками рака должны быть характеризованы по TI-RADS.
4. Помните, что оценка TI-RADS не является диагнозом или показанием к операции. Но уровень TI-RADS сообщает о показании к проведению пункционной биопсии узла. TI-RADS лишь ориентирует в величине вероятности рака, но не указывает на него однозначно.
5. Только врач-клиницист может принять решение о показании и величине операции щитовидной железы на основании данных УЗИ (не только TI-RADS), цитологического исследования (не только Bethesda) и клинических обстоятельств. Врач- хирург может лишь выбрать вариант хирургического вмешательства.
6. В случае выявления 4 или 5 уровней/категорий по TI-RADS обратитесь к врачу УЗД для пояснения конкретных признаков узла, которые были определены как злокачественные и повлияли на оценку по системе TI-RADS. Важно, чтобы врач УЗД показал эти ультразвуковые признаки на изображении и прокомментировал. Запомните и затем запишите эти пояснения.
7. В случае определения 4 или 5 уровней по ACR TI-RADS уточните у врача количество баллов. Величина баллов позволит точнее оценить выраженность признаков злокачественности.
8. Диагностика по системе TI-RADS является субъективной, т.к. зависит от специализации (в т.ч. знаний), опыта и внимания врача УЗД. При необходимости, в случае сомнений или иных условий можете провести контрольное УЗИ у другого специалиста, получив второе врачебное мнение. Готовьтесь к контрольному УЗИ, предварительно и внимательно изучив ультразвуковые признаки рака узлов щитовидной железы.
УЗ-признаки рака узлов щитовидной железы
Известные специалистам ультразвуковые признаки рака узлов щитовидной железы могут в большей или меньшей мере указывать на злокачественный процесс. Поэтому все признаки рака при УЗИ можно разделить на две группы.
Комитет ACR TI-RADS присудил каждому признаку разное количество баллов (от 0 до 3), в зависимости от частоты встречаемости при раке. По сумме таких баллов выносится суждение о вероятности рака и показании к пункционной биопсии. Авторы EU TI-RADS, зная о разной достоверности признаков и возможности бальной оценки, тем не менее, сохранили в своей системе TI-RADS прежний принцип определения величины вероятности рака.
Но все специалисты опирались на одни и те же признаки рака. Читайте об ультразвуковых признаках рака узлов в специальной статье сайта нашей Клиники. Пример ультразвуковых признаков показан на рисунке 5.
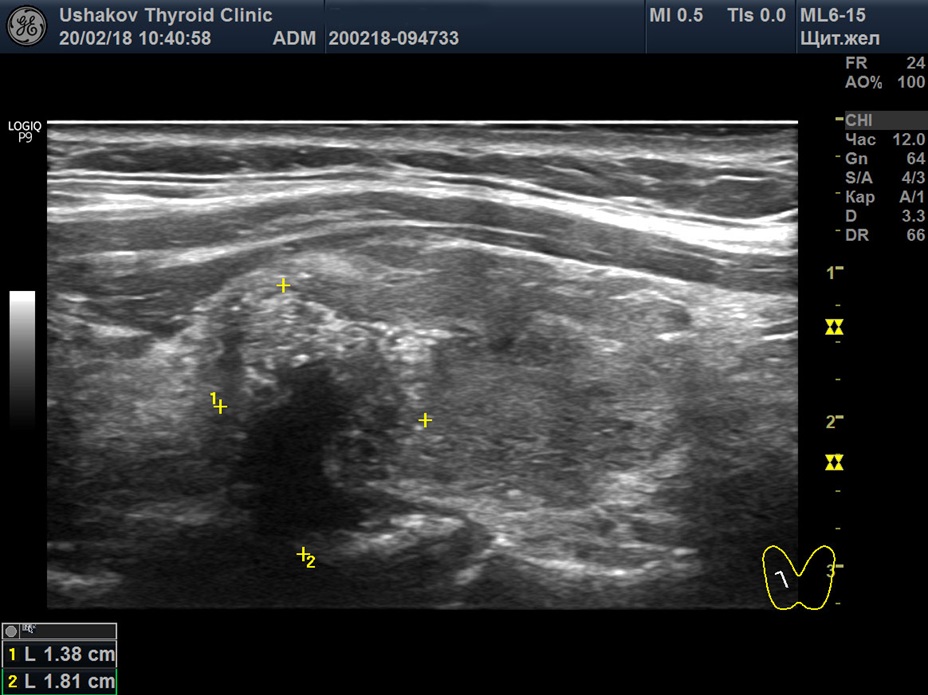
Рисунок 5 Узел верхней (краниальной) части правой доли щитовидной железы (ограничен желтыми метками). Признаки рака узла: 1) неправильная форма, 2) неравномерный край узла, местами прерывистая граница, 3) значительно гипоэхогенная (темная) зона внутри узла, постепенно переходящая в остальную ткань, 4) микрокальцинаты. 5 уровень по ACR TI-RADS (10 баллов) или 5 категория по EU TI-RADS.
Обновлённые критерии TI-RADS — диагностика узловых поражений щитовидной железы
Узловые поражения щитовидной железы широко распространены: у примерно 1/3 взрослого населения на УЗИ обнаруживаются узловые поражения щитовидной железы. Однако менее 10% из них являются злокачественными. УЗИ высокого разрешения является методом первой линии для выявления и оценки узловых поражений щитовидной железы. Всё возрастающее число проводимых УЗИ-исследований и важность их результатов в дальнейшей тактике ведения больного обусловили потребность в наличии единой терминологии, которая позволила бы УЗИ-специалистам и клиницистам лучше понимать друг друга, а также единой системы классификации найденных узловых поражений, на основе которой можно было бы оценить вероятность злокачественности находок и тактику их дальнейшего ведения.
В 2009 году Eleonora Horvath с соавторами опубликовали результаты 8-летнего проспективного трехэтапного исследования, целью которого было создание такой единой УЗИ-классификации. Авторы проанализировали УЗИ-картины в общей сложности 1959 пациентов с узловыми поражениями щитовидной железы. Всем пациентам была проведена тонкоигольная аспирационная биопсия, а затем проанализирована корреляция результатов цитологического и гистологического исследования и найденных УЗИ-критериев.
На основе этих данных была создана классификация TI-RADS (Thyroid Imaging Reporting and Data System). В 2011 году Jin Young Kwak с соавторами предложили более простую в использовании модель, основанную на подсчете количества подозрительных ультразвуковых признаков. Эта модель была названа К-TIRADS (Korean Thyroid Imaging Reporting and Data System).В настоящий момент в клинической практике применяются несколько модификаций TI-RADS: чилийская, украинская, корейская и французская. Эти модификации не имеют принципиальных отличий.
По результатам проведенного Xi Wei (Head Neck, июнь 2016) метаанализа TI-RADS, чувствительность и специфичность этого диагностического инструмента составили 0,79 и 0,71 соответственно; это указывает на то, что категории TI-RADS являются перспективным инструментом для оценки доброкачественных и злокачественных узлов щитовидной железы и для принятия решения о дальнейшей биопсии. Стоит заметить, что TI-RADS не является единственной классификацией узловых поражений ЩЖ. Специалисты УЗИ используют также шкалы, разработанные Американской (American Thyroid Association (АTA), Statement on Preoperative Imaging for Thyroid Cancer Surgery, 2014) и Британской (British Thyroid Association (BTA), Ultrasound assessment of thyroid nodules, 2014) Тиреоидными Ассоциациями. Однако, на сегодняшний день TI-RADS и её различные модификации являются самыми популярными.
В марте 2017 года Journal of American College of Radiology опубликовал новую версию TI-RADS (ACR TI-RADS) и рекомендации к ее использованию. Еще более упрощенная, новая схема подразумевает, что каждому приведенному признаку будет присвоено определенное количество баллов, а затем по результатам подсчета найденное образование можно будет отнести к одной из существующих категорий. Для разработки новых рекомендаций были использованы данные литературы, результаты программы SEER (Surveillance, Epidemiology, and End Results) Национального Института Рака США и оценка существующих классификационных систем.
По заявлению Комитета TI-RADS, новые критерии должны:
снизить количество проводимых биопсий узловых образований ЩЖ с низким риском злокачественности;
давать возможность оценить все возможные узловые образования;
базироваться на уже разработанном лексиконе;
быть простыми в применении специалистами УЗИ-диагностики.
ACR TI-RADS согласуется с большинством других рекомендаций, предписывающих биопсию для образований высокого риска размером 1 см и более. Однако, порог для образований среднего и умеренного риска (2,5 и 1,5 см соответственно) выше, чем рекомендованые ATA и Korean Society of Thyroid Radiology. Последние ссылаются на исследование Machens с соавт., которое показало, что совокупный риск отдаленных метастазов от сосочкового и фолликулярного рака щитовидной железы существенно возрастал при размере образования 2 и более см. По утверждению авторов TI-RADS, они опирались на собственную интерпретацию данных этого исследования и отметили постепенное нарастание рисков, которое начиналось с большего размера узла. Немаловажно также и то, что Machens и др. основывали свой анализ на размере опухоли при патологоанатомическом исследовании, а не на параметрах, измеренных при УЗИ — а эти данные могут значительно отличаться. Исключение может быть сделано для узловых образований категории TR5 размерами 5‒9 мм.
Авторы рекомендуют определять эхоструктуру образования как губчатую только в том случае, если оно более чем на 50% состоит из небольших кистозных включений. В новой классификации понятия преимущественно солидного и преимущественно кистозного образования объединены в графу смешанного образования, так как само появление солидного компонента оказалось более прогностически важным, чем соотношение. Кроме того, хотя определение кровотока во включении с помощью доплеровского картирования не вошло в критерии новой классификации, авторы рекомендуют использовать его, чтобы отличить истинно солидный компонент от включений и кровоизлияния.
Наличие или отсутствие гидрофильной границы (HALO) также было опущено в новой версии TI-RADS. Зато появился термин «границы плохо определяются». Это нововведение позволит классифицировать большее количество образований. Термин «неровный дольчатый край» включает в себя зубчатые края, с или без протрузии в окружающую паренхиму. Могут возникнуть трудности с распознанием данного критерия, если контур не определяется, если эхогенность окружающей узел ткани ЩЖ гетерогенна или если узловых образований много и они «упираются» краями друг в друга. Выход контура образования за пределы железы обычно классифицируют при описании как обширный или минимальный. Обширное экстратиреоидное расширение, которое характеризуется выраженным прорастанием в смежные мягкие ткани и/или сосудистые структуры, является очень надёжным признаком злокачественности и неблагоприятным прогностическим фактором. Минимальное экстратиреоидное распространение может быть заподозрено по выпучиванию контура железы или снижению его эхогенности в месте образования, однако прогностическая ценность этого критерия дискутабельна. Авторы рекомендуют с осторожностью определять минимальное экстратиреоидное распространение, особенно если образование доброкачественно по другим критериям.
В случае если не удаётся оценить внутреннюю структуру образования из-за кальцификатов, дающих сильные акустические тени, авторы рекомендуют считать их солидными. Примечательно, что небольшие эхогенные включения, обнаруживаемые в губчатых узлах, чаще всего представляют собой задние стенки мелких кист. Такие включения не должны учитываться при подсчете баллов. В протоколе исследования следует особо указывать на локализацию образования в критических местах — если узел расположен близко к трахее или к борозде возвратного нерва. Важной частью протокола УЗИ является сонографическая оценка шейных лимфоузлов. Если пациенту ранее проводились оперативные вмешательства и/или биопсии ЩЖ, это также должно быть указано в протоколе.
Что касается сроков наблюдения, комитет TI-RADS рекомендует для категории TR5 обследования каждый год последующие 5 лет. Для TR4 сканирование должно проводиться через 1, 2, 3 и 5 лет. Для TR3 последующая визуализация может быть выполнена на 1-й, 3-й, и 5-й год. Наблюдение можно прекращать через 5 лет, если УЗИ-картина остается без изменений. Следует помнить, что данные критерии носят рекомендательный характер, и решение о дальнейшей биопсии и/или оперативном вмешательстве выносит клиницист после обсуждения тактики с пациентом, при этом учитывая многие другие факторы риска для каждого конкретного пациента, включая его семейный анамнез, возраст, пол, сопутствующую патологию и т.д.
Источники
Xu T. et al. Thyroid nodule sizes influence the diagnostic performance of TIRADS and ultrasound patterns of 2015 ATA guidelines: a multicenter retrospective study //Scientific reports. – 2017. – Т. 7. – С. 43183.
Tessler F. N. et al. ACR thyroid imaging, reporting and data system (TI-RADS): white paper of the ACR TI-RADS committee //Journal of the American College of Radiology. – 2017. – Т. 14. – №. 5. – С. 587-595.
О необходимости внедрения классификации TI-RADS в России
Полный текст:
Аннотация
В мировых профессиональных медицинских сообществах продолжается активное обсуждение модификаций системы стратификации признаков злокачественности узлов щитовидной железы TI-RADS (англ. Thyroid Imaging Reporting And Diagnostic System). Система предназначена в первую очередь для отбора узлов для выполнения пункционной биопсии. Классификация должна быть единой для всех медицинских учреждений нашей страны, простой в использовании и понятной для врачей различных специальностей. В статье представлена модификация TI-RADS, подготовленная для обсуждения в профессиональных сообществах России. Выделены “большие” эхопризнаки (специфичность ≥95%), наиболее характерные для рака щитовидной железы, и “малые” признаки (специфичность ≥90%), дополнительные, позволяющие перевести узел из категории TI-RADS 3 в категорию TI-RADS 4 для выполнения пункции. При сравнении показателей диагностической информативности данного варианта TI-RADS с европейским (EU-TIRADS) отмечено, что оба варианта имели одинаковую специфичность – 93%. Отечественный вариант несколько превышал европейский по показателям чувствительности, соответственно 94,2 и 91,0%, что можно объяснить учетом дополнительных “малых” признаков злокачественности, что позволяет рекомендовать к обсуждению в России предложенный отечественными экспертами вариант TI-RADS.
Ключевые слова
Для цитирования:
Фисенко Е.П., Сенча А.Н., Катрич А.Н., Сыч Ю.П., Цветкова Н.В., Борсуков А.В., Костромина Е.В. О необходимости внедрения классификации TI-RADS в России. Клиническая и экспериментальная тиреоидология. 2019;15(2):55-63. https://doi.org/10.14341/ket10115
For citation:
Fisenko E.P., Sencha A.N., Katrich A.N., Sych Yu.P., Tsvetkova N.V., Borsukov A.V., Kostromina E.V. Оn the need to introduce the TI-RADS classification in Russia. Clinical and experimental thyroidology. 2019;15(2):55-63. (In Russ.) https://doi.org/10.14341/ket10115
Система стратификации признаков злокачественности узлов ЩЖ TI-RADS должна быть проста в применении и понятна не только специалистам, выполняющим пункционную биопсию узлов ЩЖ, но и тем врачам первичного звена (в первую очередь специалистам ультразвуковой диагностики), которые чаще первыми дифференцируют очаговые изменения ЩЖ и должны решить вопрос о передаче пациента в службы (специалистам-клиницистам), непосредственно занимающиеся морфологической оценкой и определением дальнейшей тактики ведения пациента. На это в очередной раз обращено внимание в последних предложенных вариантах TI-RADS американскими и европейскими коллегами [1, 2].
Система TI-RADS также предполагает стандартизацию обмена медицинской информацией между врачами-клиницистами (эндокринологами, хирургами) и специалистами ультразвуковой диагностики, что требует более быстрой валидации данной системы в РФ с закреплением этого в клинических рекомендациях для двух специальностей: эндокринологии и ультразвуковой диагностики.
Дифференцировка узлов ЩЖ часто проводится не столько по наличию основных признаков злокачественности (раки), сколько по их отсутствию (доброкачественные образования) [3, 4]. Однако хорошо известно, что рак щитовидной железы (РЩЖ) имеет много “масок” (клинических, ультразвуковых, цитологических) и часто имитирует доброкачественную природу узла.
Набор эхопризнаков, наиболее часто встречающихся при РЩЖ при мультипараметрическом УЗИ, практически совпадает в большинстве литературных источников [5–10], что представлено и в Российских клинических рекомендациях по диагностике и лечению высокодифференцированного РЩЖ у взрослых (2017) [11]:
– снижение эхогенности узла;
– вертикальная пространственная (или непараллельная) ориентация узла или “размеры выше больше, чем шире”;
– наличие микрокальцинатов в узле;
– неровные (мелкодольчатые, звездчатые, лучистые) и нечеткие контуры.
Эти признаки являются высокоспецифичными (таблица), что подтверждается многочисленными исследованиями, в том числе метаанализом [5, 9, 10, 12–20].
Таблица. Показатели специфичности эхографических признаков злокачественности в узлах щитовидной железы по данным различных авторов
Автор
УЗ-признак
Неровный контур
Вертикальная ориентация
Снижение эхогенности
Микрокальцинаты
В работах последних лет обращено внимание, что признак “понижение эхогенности” узлов ЩЖ следует подразделять на “умеренное” и “значительно сниженное” [1, 2]. При этом специфичность признака “выраженное снижение эхогенности” значительно превышает “умеренное снижение эхогенности” узла в диагностике РЩЖ [19, 20].
Наибольшие разногласия возникают при обсуждении термина “нечеткие границы” узла, что связано с субъективной оценкой врача-оператора. Известно, что доброкачественные гиперпластические процессы, представленные узловыми образованиями, часто не имеют капсулы, в связи с чем четкость их контуров тем хуже определяется, чем меньше размер очага [14, 20, 21], что приводит к гипердиагностике инвазивных процессов. Использование высокочастотных датчиков (12–18 МГц) позволяет определить микродольчатость, лучистость/игольчатость/звездчатость инфильтрирующих краев опухоли, что более важно для проведения дифференциально-диагностического процесса [1, 20].
Основные противоречия представленных в литературе модификаций TI-RADS сводятся к распределению узлов в категориях Т3 и Т4, Т5. В первой группе более ранних вариантов TI-RADS в категорию Т3 предложено определять узлы без перечисленных выше признаков злокачественности, соответственно начиная с Т4 – с признаками злокачественности [5–9]. Пункцию предложено выполнять и в категории Т3 (однако не представлены критерии отбора узлов для пункции в данной категории), и в категориях Т4, Т5. Распределение узлов в Т4 и Т5 определяется количеством выявленных признаков злокачественности. При этом Т4 подразделяется на подкатегории (2 или 3).
Во второй группе вариантов TI-RADS предложено отказаться от подразделения Т4 на подкатегории, что значительно облегчает работу. Разделение на категории преимущественно идет по характеру их эхогенности [1, 2].
В нашей стране также продолжается обсуждение классификации TI-RADS. Выделены ультразвуковые признаки, по которым происходит отбор узлов из категории Т3 (изо- или гиперэхогенных) в Т4 для пункции (согласно логике системы BI-RADS, а именно она взята в основу TI-RADS [22], узел, требующий выполнения биопсии, из Т3 (категория для динамического наблюдения узлов) должен быть перенесен в категорию Т4). Основными критериями в этом случае для узлов ЩЖ являются следующие “малые” ультразвуковые признаки злокачественности, полученные в В-режиме [19, 23, 24]:
– умеренное снижение эхогенности или неравномерная эхогенность узла (наличие гипоэхогенных включений);
– округлая форма узла;
– неравномерной толщины хало вокруг узла;
– наличие макрокальцинатов в узле.
Таким образом, появление этих признаков в гипер- или изоэхогенных узлах указывает на необходимость их морфологической оценки, т.е. перевода в категорию Т4 для выполнения пункционной биопсии.
К “малым” признакам отнесены также патологический интранодулярный сосудистый рисунок (по результатам применения цветокодированных режимов) и высокая жесткость узла (по результатам применения количественных и качественных параметров ультразвуковой эластографии). Эти методики широко внедряются в мировой ультразвуковой диагностике, однако на настоящий момент для оценки узлов ЩЖ являются дополнительными [23, 25]. При наличии соответствующей аппаратуры эти признаки могут быть определены как на этапе первичного диагностического поиска, так и на этапе непосредственного решения вопроса о выполнении биопсии при использовании оборудования высокого или экспертного класса.
Суммируя вышесказанное, мы предлагаем на страницах журнала обсудить возможный вариант TI-RADS, приемлемый для всех служб в нашей стране, и, возможно, сформировать общие рекомендации.
Проект TI-RADS
TI-RADS 1. Нет очаговых изменений в паренхиме ЩЖ.
TI-RADS 2. Очаговые образования, не требующие морфологической оценки (макрофолликулы; губчатые или кистозные узлы), представленные на рис. 1.
TI-RADS 3. Очаговые структуры, требующие динамического наблюдения без выполнения биопсии (гипер- или изоэхогенные образования с ровными контурами, в том числе на фоне аутоиммунного тиреоидита; кальцинированные узлы по типу “яичной скорлупы”) (рис. 2).
Пункция в категории TI-RADS 3 возможна по настоянию пациента или при наличии клинической необходимости по рекомендации лечащего врача.
При отрицательной динамике в процессе выполнения динамического мониторинга предполагается перевод в категорию TI-RADS 4 узлов, которые за 6–12 мес наблюдения значительно изменили свои характеристики в В-режиме:
– увеличились размеры узла (объем увеличился более чем на 30%);
– узлы приобрели шаровидную форму, появились кальцинаты, деформация капсулы узла (и/или капсулы ЩЖ);
– появились патологически измененные лимфатические узлы шеи, не выявляемые ранее.
Все гипоэхогенные узлы предлагается отнести в категории 4 и 5.
Рис. 1. Категория TI-RADS 2: а – кистозно расширенный или макрофолликул; б – губчатый узел (стрелки).
Рис. 2. Категория TI-RADS 3: а – изоэхогенный очаг (стрелки), окруженный тонким хало (узловой зоб); б – гиперэхогенный очаг округлой формы, с четкими контурами, тонким гипоэхогенным ободком на фоне аутоиммунного тиреоидита; в – кальцинированный узел по типу “яичной скорлупы”.
TI-RADS 4. Узлы более 1,0 см в диаметре с “малыми” признаками злокачественности для выполнения ПУНКЦИИ (рис. 3):
– неравномерно утолщенное хало;
Рис. 3. TI-RADS 4: а – узел шаровидной формы, с ровными и четкими контурами, умеренно пониженной эхогенности, с участками более низкого эхо, с макрокальцинатом. Узел окружен тонким хало (фолликулярная неоплазия); б, в, г (поперечное и продольное сканирование левой доли ЩЖ) – изоэхогенные узлы с гипоэхогенными включениями, с четкими контурами, с тонким хало (фолликулярная аденома); д – изоэхогенный узел с гипоэхогенными включениями, с неравномерно утолщенным хало (фолликулярный рак).
TI-RADS 5. Солидные узлы с “большими” признаками злокачественности для выполнения ПУНКЦИИ:
– значительно сниженная эхогенность;
– вертикальная пространственная ориентация образования;
– неровный контур образования: бугристый, микродольчатый, лучистый;
– наличие в опухоли микрокальцинатов;
Рис. 4. TI-RADS 5. Узлы ЩЖ размером >1,0 см (папиллярные раки): а, б – узлы значительно пониженной эхогенности с микрокальцинатами, с неровными микродольчатыми контурами; в – узел вертикальной пространственной ориентации, с нечеткими, неровными контурами, значительно сниженной эхогенности, с множественными микрокальцинатами; г – узел с микродольчатыми нечеткими контурами, неравномерно пониженной эхогенности, с микрокальцинатами; д – узел значительно пониженной эхогенности, вертикальной пространственной ориентации, с нечеткими, неровными (лучистыми) контурами; е – узел с нечеткими контурами, с множественными микрокальцинатами.
При наличии измененных лимфатических узлов (шаровидная форма, исчезновение дифференцировки внутренних структур, кистозные изменения, кальцинаты) к указанию категории ТI-RADS целесообразно в заключении добавлять “ЛИМФАДЕНОПАТИЯ”. На основании заключения ультразвукового исследования и клинико-лабораторных данных врач-эндокринолог принимает окончательное решение о необходимости выполнения пункционной биопсии узла ЩЖ и измененных лимфатических узлов шеи.
Представленный вариант модификации TI-RADS наиболее близок к европейскому варианту [1]. Для работы в условиях нашей страны менее приемлемыми представляются варианты TI-RADS, предлагающие присвоение баллов каждому ультразвуковому признаку, с дальнейшим распределением узлов по категориям TI-RADS в зависимости от суммы баллов [2, 9].
Группой авторов проведено пилотное исследование по оценке воспроизводимости европейского варианта системы ТI-RADS и варианта, предложенного группой отечественных авторов, при помощи критерия Кохрейна [26]. Доля совпадений результатов (когда разные исследователи относили один и тот же узел к одинаковой категории) составила 79%, коэффициент Кохрейна составил 03–05 (p < 0,001), что свидетельствует о хорошей воспроизводимости данного метода оценки злокачественного потенциала узлов ЩЖ разными операторами.
Оба варианта TI-RADS имели одинаковую специфичность – 93%. Отечественный вариант несколько превышал европейский по показателям чувствительности: 94,2 против 91,0% соответственно, что можно объяснить учетом большего количества “малых” признаков злокачественности. Нам представляется важным обратить внимание на эти признаки. В ряде работ показано, что в 13,4% случаев в раковых узлах ЩЖ не удается выявить ни одного “большого” признака злокачественности; в 10,1% случаев выявляется только один “большой” признак рака; в 25,6% случаев определяется сочетание одного “большого” признака с несколькими “малыми”; в 13% случаев удается дифференцировать только “малые” признаки злокачественности [21, 27].
“Малые” признаки чаще возникают в узлах, приближающихся к 2,0 см в диаметре [21]. В настоящее время мы оперируем размерами узлов до 1,0 см и свыше 1,0 см, согласно ряду российских клинических рекомендаций [11, 28]. В последних западных вариантах TI-RADS размеры узлов разделяют от 0,5; 1,0; 1,5; 2,0 см и более [1, 2]. Возможно, нам также следует рассмотреть данные модификации.
Заключение
Мы предлагаем провести широкое обсуждение предложенного варианта классификации TI-RADS для его дальнейшей оптимизации и приемлемой стандартизации в обозримом будущем. Наш подход обусловлен желанием сблизить позиции отечественных специалистов ультразвуковой диагностики и российских эндокринологов. Переход на единую информационную диагностическую площадку этих двух специальностей, надеемся, будет положительно влиять на конечные показатели результатов ведения пациентов с узловыми новообразованиями ЩЖ.
Дополнительная информация
Источник финансирования. Работа выполнена без привлечения внешних источников финансирования на личные средства авторов.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Участие авторов: Фисенко Е.П. – концепция и инициатива создания публикации, анализ материалов, написание текста; Сыч Ю.П. – сбор и обработка материалов, анализ материалов, написание текста; Сенча А.Н. – сбор и анализ материалов, редактирование текста; Катрич А.Н. – сбор и анализ материалов, редактирование текста; Цветкова Н.В. – сбор и анализ материалов, редактирование текста; Борсуков А.В. – сбор и анализ материалов, редактирование текста; Костромина Е.В. – сбор и анализ материалов, редактирование текста. Все авторы внесли существенный вклад в проведение поисково-аналитической работы и подготовку статьи, прочли и одобрили итоговую версию до публикации.
Благодарности. Коллектив авторов выражает искреннюю благодарность коллегам, принявшим активное участие в обсуждении и подготовке материалов статьи: профессору кафедры ультразвуковой диагностики ФГБОУ ДПО РМАНПО Заболоцкой Наталье Владленовне, заведующей отделением ультразвуковой диагностики ФГБУ “НМИЦ эндокринологии” Минздрава России Солдатовой Татьяне Васильевне, заведующей отделением ультразвуковой диагностики НИИ клинической и экспериментальной радиологии ФГБУ “НМИЦ онкологии им. Н.Н. Блохина” Минздрава России, профессору Синюковой Галине Тимофеевне, старшему научному сотруднику НИИ клинической и экспериментальной радиологии ФГБУ “НМИЦ онкологии им. Н.Н. Блохина” Минздрава России Данзановой Татьяне Юрьевне, врачу отделения лучевой диагностики ФБУ здравоохранения “Центральная медико-санитарная часть № 141” ФМБА России, г. Удомля Тверской области, Пищугиной Алене Владимировне.