угарный газ это какой оксид
Угарный газ это какой оксид
Физические свойства: бесцветный ядовитый газ без вкуса и запаха, горит голубоватым пламенем, легче воздуха, плохо растворим в воде. Концентрация угарного газа в воздухе 12,5—74 % взрывоопасна.
Формальная степень окисления углерода +2 не отражает строение молекулы СО, в которой помимо двойной связи, образованной обобществлением электронов С и О, имеется дополнительная, образованная по донорно-акцепторному механизму за счет неподеленной пары электронов кислорода:
В связи с этим молекула СО очень прочна и способна вступать в реакции окисления-восстановления только при высоких температурах. При обычных условиях СО не взаимодействует с водой, щелочами или кислотами.
Основным антропогенным источником угарного газа CO в настоящее время служат выхлопные газы двигателей внутреннего сгорания. Угарный газ образуется при сгорании топлива в двигателях внутреннего сгорания при недостаточных температурах или плохой настройке системы подачи воздуха (подается недостаточное количество кислорода для окисления угарного газа CO в углекислый газ CO2). В естественных условиях, на поверхности Земли, угарный газ CO образуется при неполном анаэробном разложении органических соединений и при сгорании биомассы, в основном в ходе лесных и степных пожаров.
1) Получение в промышленности (в газогенераторах):
CO2 + C = 2CO – 175 кДж
В газогенераторах иногда через раскалённый уголь продувают водяной пар:
При обычных условиях CO инертен; при нагревании – восстановитель ;
1) Взаимодействие с кислородом:
2 C +2 O + O 2 t ˚ C → 2 C +4 O 2 ↑
C +2 O + CuO t ˚ C → Сu + C +4 O2↑
3) Взаимодействие с хлором (на свету)
CO + Cl2 свет → COCl2 (фосген – ядовитый газ)
4) Взаимодействие с расплавами щелочей (под давлением)
CO + NaOH P асплав → HCOONa (формиат натрия)
Влияние угарного газа на живые организмы:
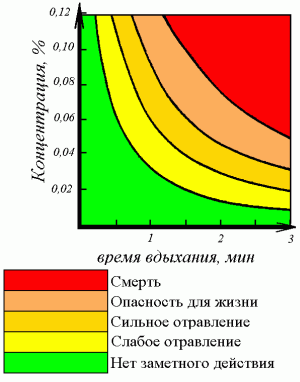
Угарный газ опасен, потому что он лишает возможности кровь нести кислород к жизненно важным органам, таким как сердце и мозг. Угарный газ объединяется с гемоглобином, который переносит кислород к клеткам организма, в следствии чего тот становится непригодным для транспортировки кислорода. В зависимости от вдыхаемого количества, угарный газ ухудшает координацию, обостряет сердечно-сосудистые заболевания и вызывает усталость, головную боль, слабость, Влияние угарного газа на здоровье человека зависит от его концентрации и времени воздействия на организм. Концентрация угарного газа в воздухе более 0,1% приводит к смерти в течение одного часа, а концентрация более 1,2% в течении трех минут.
Применение оксида углерода :
Главным образом угарный газ применяют, как горючий газ в смеси с азотом, так называемый генераторный или воздушный газ, или же в смеси с водородом водяной газ. В металлургии для восстановления металлов из их руд. Для получения металлов высокой чистоты при разложении карбонилов.
Оксид углерода (IV) СO2 – углекислый газ
Все четыре связи ковалентые полярные.
Получение углекислого газа:
1. В промышленности: Термическим разложением солей угольной кислоты (карбонатов). Обжиг известняка.
2. В лаборатории. Действием сильных кислот на карбонаты и гидрокарбонаты –
3. Сгорание углеродсодержащих веществ:
4. При медленном окислении в биохимических процессах (дыхание, гниение, брожение)
1) Взаимодействие с водой с образованием непрочной угольной кислоты:
Качественная реакция на углекислый газ: п омутнение известковой воды Ca ( OH )2 за счёт образования белого осадка – нерастворимой соли CaCO 3 :
Угарный газ
Угарный газ
| Монооксид углерода | |
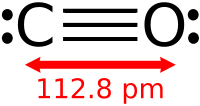 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Монооксид углерода |
| Химическая формула | CO |
| Отн. молек. масса | 28.0101 а. е. м. |
| Молярная масса | 28.0101 г/моль |
| Физические свойства | |
| Плотность вещества | 0,00125 (при 0°C) г/см³ |
| Состояние (ст. усл.) | бесцветный газ |
| Термические свойства | |
| Температура плавления | −205 °C |
| Температура кипения | −191,5 °C |
| Энтальпия (ст. усл.) | −110,52 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 0.0026 г/100 мл |
| Классификация | |
| номер CAS | [630-08-0] |
Монооксид углерода (лат. Carbon monoxide ; другие названия — уга́рный газ, окись углерода, моноокись углерода, оксид углерода (II)) — бесцветный газ без вкуса и запаха. Химическая формула CO.
Содержание
Строение молекулы
Молекула CO, так же, как и изоэлектронная ей молекула азота, имеет тройную связь. Так как эти молекулы сходны по строению, то и свойства их также схожи — очень низкие температуры плавления и кипения, близкие значения стандартных энтропий и т. п.
В рамках метода валентных связей строение молекулы CO можно описать формулой :C≡O:, причём третья связь образована по донорно-акцепторному механизму, где углерод является акцептором электронной пары, а кислород — донором.
Согласно методу молекулярных орбиталей электронная конфигурация невозбуждённой молекулы CO σ 2 Oσ 2 zπ 4 x, yσ 2 C. Тройная связь образована σ—связью, образованной за счёт σz электронной пары, а электроны дважды вырожденного уровня πx, y соответствуют двум σ—связям. Электроны на несвязывающих σC—орбитали и σO—орбитали соответствуют двум электронным парам, одна из которых локализована у атома углерода, другая — у атома кислорода.
Благодаря наличию тройной связи молекула CO весьма прочна (энергия диссоциации 1069 кДж/моль, или 256 ккал/моль, что больше, чем у любых других двухатомных молекул) и имеет малое межъядерное расстояние (dC≡O=0,1128 нм или 1,13Å).
История открытия
Монооксид углерода был впервые получен французским химиком Жаком де Лассоном в 1776 при нагревании оксида цинка с углём, но первоначально его ошибочно приняли за водород, так как он сгорал синим пламенем. То, что в состав этого газа входит углерод и кислород, выяснил в 1800 английский химик Вильям Крукшэнк. Моноксид углерода вне атмосферы Земли впервые был обнаружен бельгийским ученым М. Мижотом (M. Migeotte) в 1949 году по наличию основной колебательно-вращательной полосы в ИК спектре Солнца.
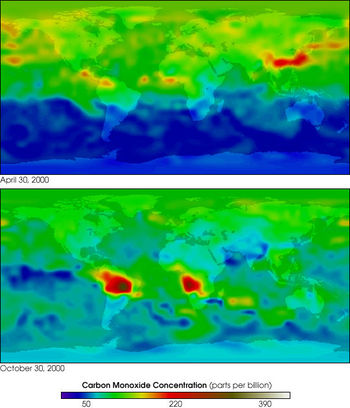
Монооксид углерода в атмосфере Земли
Различают природные и антропогенные источники поступления в атмосферу Земли. В естественных условиях, на поверхности Земли, CO образуется при неполном анаэробном разложении органических соединений и при сгорании биомассы, в основном в ходе лесных и степных пожаров. Монооксид углерода образуется в почве как биологическим путём (выделение живыми организмами), так и небиологическим. Экспериментально доказано выделение монооксида углерода за счёт обычных в почвах фенольных соединений, содержащих группы OCH3 или OH в орто- или пара-положениях по отношению к первой гидроксильной группе.
Общий баланс продуцирования небиологического CO и его окисления микроорганизмами зависит от конкретных экологических условий, в первую очередь от влажности и значения pH. Например, из аридных почв монооксид углерода выделяется непосредственно в атмосферу, создавая таким образом локальные максимумы концентрации этого газа.
В атмосфере СО является продуктом цепочек реакций с участием метана и других углеводородов (в первую очередь, изопрена).
Основным антропогенным источником CO в настоящее время служат выхлопные газы двигателей внутреннего сгорания. Оксид углерода образуется при сгорании углеводородного топлива в двигателях внутреннего сгорания при недостаточных температурах или плохой настройке системы подачи воздуха (подается недостаточное количество кислорода для окисления CO в CO2). В прошлом значительную долю антропогенного поступления CO в атмосферу обеспечивал светильный газ, использовавшийся для освещения помещений в XIX веке. По составу он примерно соответствовал водяному газу, то есть содержал до 45 % монооксида углерода. В настоящее время в коммунальной сфере этот газ вытеснен гораздо менее токсичным природным газом (низшие представители гомологического ряда алканов — пропан и др.)
Поступление CO от природных и антропогенных источников примерно одинаково.
Монооксид углерода в атмосфере находится в быстром круговороте: среднее время его пребывания составляет около 0,1 года, окисляясь гидроксилом до диоксида углерода.
Получение
Промышленный способ
1. Образуется при горении углерода или соединений на его основе (например, бензина) в условиях недостатка кислорода:
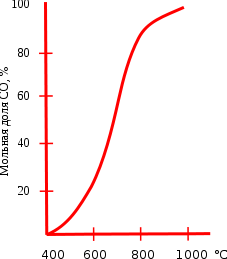
2. или при восстановлении диоксида углерода раскалённым углём:
Реакция восстановления диоксида углерода обратимая, влияние температуры на состояние равновесия этой реакции приведено на графике. Протекание реакции вправо обеспечивает энтропийный фактор, а влево — энтальпийный. При температуре ниже 400°C равновесие практически полностью сдвинуто влево, а при температуре выше 1000°C вправо (в сторону образования CO). При низких температурах скорость этой реакции очень мала, поэтому монооксид углерода при нормальных условиях вполне устойчив. Это равновесие носит специальное название равновесие Будуара.
3. Смеси монооксида углерода с другими веществами получают при пропускании воздуха, водяного пара и т. п. сквозь слой раскалённого кокса, каменного или бурого угля и т. п. (см. генераторный газ, водяной газ, смешанный газ, синтез-газ).
Лабораторный способ
1. Разложение жидкой муравьиной кислоты под действием горячей концентрированной серной кислоты, либо пропуская муравьиную кислоту над оксидом фосфора P2O5. Схема реакции:
Можно также обработать муравьиную кислоту хлорсульфоновой. Эта реакция идёт уже при обычной температуре по схеме:
2. Нагревание смеси щавелевой и концентрированной серной кислот. Реакция идёт по уравнению:
Выделяющийся совместно с CO диоксид углерода можно удалить, пропустив смесь через баритовую воду.
3. Нагревание смеси гексацианоферрата (II) калия с концентрированной серной кислотой. Реакция идёт по уравнению:
Физиологическое действие, токсичность
Опытами на молодых крысах выяснено, что 0,02-процентная концентрация CO в воздухе замедляет их рост и снижает активность по сравнению с контрольной группой. Интересно то, что крысы, живущие в атмосфере с повышенным содержанием CO, предпочитали воде и раствору глюкозы спиртовой раствор в качестве питья (в отличие от контрольной группы, особи в которой предпочитали воду).
Помощь при отравлении монооксидом углерода: пострадавшего следует вынести на свежий воздух, полезно также кратковременное вдыхание паров нашатырного спирта.
TLV (предельная пороговая концентрация, США): 25 ПДКр.з. по Гигиеническим нормативам ГН 2.2.5.1313—03 составляет 20 мг/м³
Защита от монооксида углерода
Свойства
Монооксид углерода представляет собой бесцветный газ без вкуса и запаха. Так называемый «запах угарного газа» на самом деле представляет собой запах органических примесей.
| Стандартная энергия Гиббса образования ΔG | −137,14 кДж/моль (г) (при 298 К) |
| Стандартная энтропия образования S | 197,54 Дж/моль·K (г) (при 298 К) |
| Стандартная мольная теплоёмкость Cp | 29,11 Дж/моль·K (г) (при 298 К) |
| Энтальпия плавления ΔHпл | 0,838 кДж/моль |
| Энтальпия кипения ΔHкип | 6,04 кДж/моль |
| Критическая температура tкрит | −140,23°C |
| Критическое давление Pкрит | 3,499 МПа |
| Критическая плотность ρкрит | 0,301 г/см 3 |
Основными типами химических реакций, в которых участвует монооксид углерода, являются реакции присоединения и окислительно-восстановительные реакции, в которых он проявляет восстановительные свойства.
При комнатных температурах CO малоактивен, его химическая активность значительно повышается при нагревании и в растворах (так, в растворах он восстанавливает соли Au, Pt, Pd и других до металлов уже при комнатной температуре. При нагревании восстанавливает и другие металлы, например CO + CuO → Cu + CO2↑. Это широко используется в пирометаллургии. На реакции CO в растворе с хлоридом палладия основан способ качественного обнаружения CO, см. ниже).
Окисление СО в растворе часто идёт с заметной скоростью лишь в присутствии катализатора. При подборе последнего основную роль играет природа окислителя. Так, KMnO4 быстрее всего окисляет СО в присутствии мелкораздробленного серебра, K2Cr2O7 — в присутствии солей ртути, KClO3 — в присутствии OsO4. В общем, по своим восстановительным свойствам СО похож на молекулярный водород.
Ниже 830°C более сильным восстановителем является CO, — выше — водород. Поэтому равновесие реакции:
до 830°С смещено вправо, выше 830°C влево.
Интересно, что существуют бактерии, способные за счёт окисления СО получать необходимую им для жизни энергию.
Монооксид углерода горит синим пламенем (температура начала реакции 700°C) на воздухе:
Температура горения CO может достигать 2100°C, она является цепной, причём инициаторами служат небольшие количества водородсодержащих соединений (вода, аммиак, сероводород и др.)
Благодаря такой хорошей теплотворной способности, CO является компонентом разных технических газовых смесей (см., например генераторный газ), используемых, в том числе, для отопления.
Монооксид углерода реагирует с галогенами. Наибольшее практическое применение получила реакция с хлором:
Реакция экзотермическая, её тепловой эффект 113 кДж, в присутствии катализатора (активированный уголь) она идёт уже при комнатной температуре. В результате реакции образуется фосген — вещество, получившее широкое распространение в разных отраслях химии (а также как боевое отравляющее вещество). По аналогичным реакцииям могут быть получены COF2 (карбонилфторид) и COBr2 (карбонилбромид). Карбонилиодид не получен. Экзотермичность реакций быстро снижается от F к I (для реакций с F2 тепловой эффект 481 кДж, с Br2 — 4 кДж). Можно также получать и смешанные производные, например COFCl (подробнее см. галогенпроизводные угольной кислоты).
Реакцией CO с F2, кроме карбонилфторида можно получить перекисное соединение (FCO)2O2. Его характеристики: температура плавления −42°C, кипения +16°C, обладает характерным запахом (похожим на запах озона), при нагревании выше 200°C разлагается со взрывом (продукты реакции CO2, O2 и COF2), в кислой среде реагирует с иодидом калия по уравнению:
Монооксид углерода реагирует с халькогенами. С серой образует сероксид углерода COS, реакция идёт при нагревании, по уравнению:
Получены также аналогичные селеноксид COSe и теллуроксид COTe.
C переходными металлами образует очень летучие, горючие и ядовитые соединения — карбонилы, такие как Cr(CO)6, Ni(CO)4, Mn2CO10, Co2(CO)9 и др.
Как указано выше, монооксид углерода незначительно растворяется в воде, однако не реагирует с ней. Также он не вступает в реакции с растворами щелочей и кислот. Однако с расплавами щелочей вступает в реакцию:
Интересна реакция монооксида углерода с металлическим калием в аммиачном растворе. При этом образуется взрывчатое соединение диоксодикарбонат калия:
Реакцией с аммиаком при высоких температурах можно получить важное для промышленности соединение — циановодород HCN. Реакция идёт в присутствии катализатора (оксид тория ThO2) по уравнению:
Определение монооксида углерода
Качественно можно определить наличие CO по потемнению растворов хлорида палладия (или пропитанной этим раствором бумаги). Потеменение связано с выделением мелкодисперсного металлического палладия по схеме:
Эта реакция очень чувствительная. Стандартный раствор 1 грамма хлорида палладия на литр воды.
Количественное определение монооксида углерода основано на иодометрической реакции:
Применение
См. также
Литература
Ссылки
Полезное
Смотреть что такое «Угарный газ» в других словарях:
УГАРНЫЙ ГАЗ — (монооксид углерода, СО), бесцветный, лишенный запаха ядовитый газ, который образуется при неполном сгорании ископаемых топлив; он присутствует, например, в составе угольного газа и выхлопных газов автомобилей. Ядовитое действие угарного газа… … Научно-технический энциклопедический словарь
Угарный газ — оксид углеродa, CO (a. carbon monoxide; н. Kohlenoxyd, Kohlenmonoxyd; ф. oxyde de carbone; и. oxido de carbono), хим. соединение углерода c кислородом из группы оксидов; природный газ без цвета и запаха. Bпервые выделен в лабораторных… … Геологическая энциклопедия
угарный газ — сущ., кол во синонимов: 2 • газ (55) • угар (22) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
УГАРНЫЙ ГАЗ — (монооксид углерода, оксид углерода, СО) продукт неполного окисления углерода и его соединений (в печи, двигателе и др.), чрезвычайно ядовитый газ (вызывает отравление организма угар (см. (1))) без цвета, запаха и вкуса, плохо растворим в воде.… … Большая политехническая энциклопедия
УГАРНЫЙ ГАЗ — УГАРНЫЙ ГАЗ, то же, что углерода оксид … Современная энциклопедия
УГАРНЫЙ ГАЗ — то же, что углерода оксид … Большой Энциклопедический словарь
УГАРНЫЙ ГАЗ — неполный окисел углерода, возникающий в условиях горения при недостатке кислорода воздуха. У. г. не имеет цвета, вкуса и запаха, ядовит; при содержании его в воздухе от 0,02% отравляет организм, а потому во всех цехах, в к рых может возникнуть… … Технический железнодорожный словарь
Угарный газ — см. Оксид углерода … Российская энциклопедия по охране труда
Угарный газ — УГАРНЫЙ ГАЗ, то же, что углерода оксид. … Иллюстрированный энциклопедический словарь
угарный газ — то же, что оксид углерода. * * * УГАРНЫЙ ГАЗ УГАРНЫЙ ГАЗ, то же, что углерода оксид (см. УГЛЕРОДА ОКСИД) … Энциклопедический словарь
УГАРНЫЙ ГАЗ
ОКСИД УГЛЕРОДА (УГАРНЫЙ ГАЗ). Углерода(II) оксид (угарный газ) СО, несолеообразующий оксид углерода. Это означает, что не существует кислоты, соответствующей этому оксиду. Оксид углерода(II) – газ без цвета и запаха, сжижающийся при атмосферном давлении при температуре –191,5о С и затвердевающий при –205о С. Молекула СО по своему строению аналогична молекуле N2: обе содержит равное число электронов (такие молекулы называются изоэлектронными), атомы в них соединены тройной связью (две связи в молекуле СО образованы за счет 2р-электронов атомов углерода и кислорода, а третья – по донорно-акцепторному механизму с участием неподеленной электронной пары кислорода и свободной 2р-орбитали углерода). В результате физические свойства СО и N2 (температуры плавления и кипения, растворимость в воде и т.д.) очень близки.
Оксид углерода(II) образуется при сгорании углеродсодержащих соединений при недостаточном доступе кислорода, а также при соприкосновении раскаленного угля с продуктом полного сгорания – углекислым газом: С + СО2 → 2СО. В лаборатории СО получают дегидратацией муравьиной кислоты действием концентрированной серной кислоты на жидкую муравьиную кислоту при нагревании, либо пропусканием паров муравьиной кислоты над Р2О5: НСООН → СО + Н2О. Получают СО и разложением щавелевой кислоты: Н2С2О4 → СО + СО2 + Н2О. От других газов СО легко отделить пропусканием через раствор щелочи.
При обычных условиях СО, как и азот, химически довольно инертен. Лишь при повышенных температурах проявляется склонность СО к реакциям окисления, присоединения и восстановления. Так, при повышенных температурах он реагирует со щелочами: CO + NaOH → HCOONa, CO + Ca(OH)2 → CaCO3 + H2. Эти реакции используются для удаления СО из технических газов.
Оксид углерода(II) – высококалорийное топливо: горение сопровождается выделением значительного количества теплоты (283 кДж на 1 моль СО). Смеси СО с воздухом взрываются при его содержании от 12 до 74%; к счастью, на практике такие смеси встречаются исключительно редко. В промышленности для получения СО проводят газификацию твердого топлива. Например, продувание водяного пара через слой раскаленного до 1000o С угля приводит к образованию водяного газа: С + Н2О → СО + Н2, обладающего очень высокой теплотворной способностью. Однако сжигание – далеко не самое выгодное использование водяного газа. Из него, например, можно получить (в присутствии различных катализаторов под давлением) смесь твердых, жидких и газообразных углеводородов – ценное сырье для химической промышленности (Реакция Фишера – Тропша). Из той же смеси, обогатив ее водородом и применив нужные катализаторы, можно получить спирты, альдегиды, кислоты. Особое значение имеет синтез метанола: СО + 2Н2 → СН3ОН – важнейшего сырья для органического синтеза, поэтому эту реакцию проводят в промышленности в больших масштабах.
Реакции, в которых СО является восстановителем, можно продемонстрировать на примере восстановления железа из руды в ходе доменного процесса: Fe3O4 + 4CO → 3Fe + 4CO2. Восстановление оксидов металлов оксидом углерода(II) имеет большое значение в металлургических процессах.
Для молекул СО характерны реакции присоединения к переходным металлам и их соединениям с образованием комплексных соединений – карбонилов. Примерами могут служить жидкие или твердые карбонилы металлов Fe(CO)4, Fe(CO)5, Fe2(CO)9, Ni(CO)4, Cr(CO)6 и др. Это очень ядовитые вещества, при нагревании вновь распадающиеся на металл и СО. Так можно получить порошкообразные металлы высокой чистоты. Иногда на конфорке газовой плиты видны «подтеки» металла, это – следствие образования и распада карбонила железа. В настоящее время синтезированы тысячи разнообразных карбонилов металлов, содержащих, помимо СО, неорганические и органические лиганды, например, PtCl2(CO), K3[W(CO)6(OH)3], Cr(C6H5Cl)(CO)3.
Для СО характерна также реакция соединения с хлором, которая на свету идет уже при комнатной температуре с образованием исключительно ядовитого фосгена: CO + Cl2 → COCl2. Реакция эта цепная, она идет по радикальному механизму с участием атомов хлора и свободных радикалов COCl. Несмотря на ядовитость, фосген широко применяется для синтеза многих органических соединений.
Обычно в атмосфере содержание СО не превышает 10–5%. Этот газ попадает в воздух в составе вулканических и болотных газов, с выделениями планктона и других микроорганизмов. Так, из поверхностных слоев океана в атмосферу ежегодно выделяется 220 млн тонн СО. Высока концентрация СО в угольных шахтах. Много угарного газа образуется при лесных пожарах. Выплавка каждого миллиона тонн стали сопровождается образованием 300 – 400 т СО. В сумме техногенное выделение СО в воздух достигает 600 млн тонн в год, из них более половины приходится на автотранспорт. При неотрегулированном карбюраторе в выхлопных газах может содержаться до 12% СО! Поэтому в большинстве стран введены жесткие нормы на содержание СО в выхлопе автомобилей.
Образование СО всегда происходит при сгорании углеродсодержащих соединений, в том числе древесины, при недостаточном доступе кислорода, а также при соприкосновении раскаленного угля с углекислым газом: С + СО2 → 2СО. Такие процессы происходят и деревенских печах. Поэтому преждевременное закрывание дымохода печи для сохранения тепла часто приводит к отравлению угарным газом. Не следует думать что горожане, которые не топят печи, застрахованы от отравления СО; им, например, легко отравиться в плохо проветриваемом гараже, где стоит автомобиль с работающим мотором. Содержится СО и в продуктах сгорания природного газа на кухне. Многие авиационные катастрофы в прошлом произошли из-за износа двигателей или плохой их регулировки: в кабину пилотов проникал СО и отравлял экипаж. Опасность усугубляется тем, что СО невозможно обнаружить по запаху; в этом отношении угарный газ опаснее хлора!