уничтожают бактерии какие клетки крови
 masterok
masterok
Мастерок.жж.рф
Хочу все знать
Фагоцитоз, процесс активного захватывания и поглощения живых и неживых частиц одноклеточными организмами или особыми клетками (фагоцитами) многоклеточных животных организмов. Явление Ф. было открыто И. И. Мечниковым, который проследил его эволюцию и выяснил роль этого процесса в защитных реакциях организма высших животных и человека, главным образом при воспалении и иммунитете. Большую роль фагоцитоз играет при заживлении ран.
Способность захватывать и переваривать частицы лежит в основе питания примитивных организмов. В процессе эволюции эта способность постепенно перешла к отдельным специализированным клеткам, вначале пищеварительным, а затем – к особым клеткам соединительной ткани. У человека и млекопитающих животных активными фагоцитами являются нейтрофилы (микрофаги, или специальные лейкоциты) крови и клетки ретикуло-эндотелиальной системы, способные превращаться в активных макрофагов. Нейтрофилы фагоцитируют мелкие частицы (бактерии и т.п.), макрофаги способны поглощать более крупные частицы (погибшие клетки, их ядра или фрагменты и т.п.). Макрофаги способны также накапливать отрицательно заряженные частицы красителей и коллоидных веществ. Поглощение мелких коллоидных частиц называют ультрафагоцитозом, или коллоидопексией.
Фагоцитоз требует затраты энергии и связан прежде всего с активностью клеточной мембраны и внутриклеточных органоидов – лизосом, содержащих большое количество гидролитических ферментов. В ходе Ф. различают несколько стадий. Вначале фагоцитируемая частица прикрепляется к клеточной мембране, которая затем обволакивает её и образует внутриклеточное тельце – фагосому. Из окружающих лизосом в фагосому попадают гидролитические ферменты, переваривающие фагоцитируемую частицу. В зависимости от физико-химических свойств последней переваривание может быть полным или неполным. В последнем случае образуется остаточное тельце, которое может оставаться в клетке длительное время.
А вспомните, как мы тут рассматривали деление клетки, а именно что такое МИОЗ , а вот Как вирус борется за то, чтобы заразить клетку и вот так ШАГАЕТ БЕЛОК
Уничтожают бактерии какие клетки крови
Получить результаты
Компания «Новые Медицинские Технологии»
Иммунный статус
Иммунные реакции здорового организма неусыпно защищают его, обеспечивая жизнеспособность, динамическое равновесие организма с внешней средой. Однако довольно часто по целому ряду причин иммунные реакции нарушаются. Тогда могут возникнуть различные заболевания. Что интересно, согласно данным Всемирной Организации Здравоохранения, практически все заболевания сопровождаются той или иной степенью несостоятельности иммунной системы. Например, повышения иммунных реакций вызывают аллергии, понижения же иммунных реакций приводят к иммунодефицитным состояниям.
При грубом снижении иммунитета защитные силы организма ослабевают настолько, что многие виды бактериальной и вирусной микрофлоры начинают активно функционировать, проявляется хроническими воспалительными процессами. Это особенно ярко видно по возбудителям герпеса, хламидиоза, вирусных гепатитов и многим другим. При длительном протекании перечисленных заболеваний иммунитет дополнительно снижается, что приводит к дополнительной опасности – риску появления онкологических изменений.
В иммунологии различают врожденные иммунодефициты, которые возникли по причине генетического дефекта одного или нескольких компонентов системы иммунитета. В настоящее время выявлено более 70 врожденных дефектов системы иммунитета, они отличаются глубиной и постоянством, но встречаются довольно редко. И только ранняя диагностика и лечение могут предотвратить развитие необратимых инфекционно-воспалительных поражений.
Намного чаще иммунитет нарушается в более позднем возрасте и носит приобретенный характер. Наиболее ярким примером приобретенной формы в иммунологии является СПИД. Снижения защитных сил могут вызвать и такие причины, как рентгеновское облучение, действие кортикостероидов, цитостатиков, травм и хирургических вмешательств, диабет, заболевания почек и печени, злокачественные новообразования и пр. Однако во многих случаях при устранении причины происходит восстановление функции системы иммунитета.
Оценить состояние иммунной системы возможно при помощи исследования иммунного статуса.
Иммунный статус – это показатели работы иммунной системы. Он включает исследование количественных показателей компонентов иммунной системы и определение их функциональной активности.
Показанием к назначению исследования иммунологического статуса может быть любое подозрение на неадекватную работу иммунной системы: тяжелое течение инфекционных болезней, наличие хронических или часто рецидивирующих инфекционных заболеваний, наличие очагов хронического воспаления, заболевания соединительной ткани, аутоиммунные процессы и др.
Среди нарушений работы иммунной системы в первую очередь следует выделить следующие:
Клетки иммунной системы
Лейкоциты. Их назначение – распознавать чужеродных веществ и микроорганизмов, бороться с ними, а также запоминать информацию о них.
Выделяют несколько видов лейкоцитов:
— лимфоциты:
— натуральные киллеры (НК) – это лимфоцитоподобные клетки, которые лишены признаков Т- и В-лимфоцитов. Они способны уничтожать опухолевые клетки и клетки, инфицированные вирусами;
— нейтрофильные лейкоциты (палочкоядерные: ядро имеет вид изогнутых палочек; сегментоядерные: ядра сегментированы, имеют перетяжки);
— эозинофильные лейкоциты;
— базофильные лейкоциты.
Нейтрофилы, эозинофилы и базофилы – это разновидности лейкоцитов, однако эти клетки не одинаково воспринимают красящие вещества, вследствие чего и различаются в названиях.
Эозинофилы участвуют в уничтожении паразитов (выделяют специальные ферменты, оказывающие на них повреждающее действие), а также в аллергических реакциях (выделяют вещества, уничтожающие гистамин, предотвращающие выход ферментов из гранул тучных клеток).
Нейтрофилы иногда называют «микрофагоцитами», указывая на их способность фагоцитировать микроорганизмы.
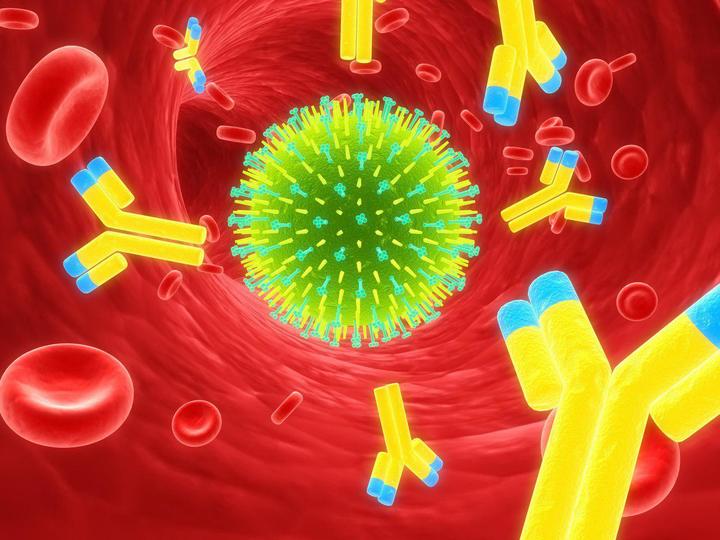
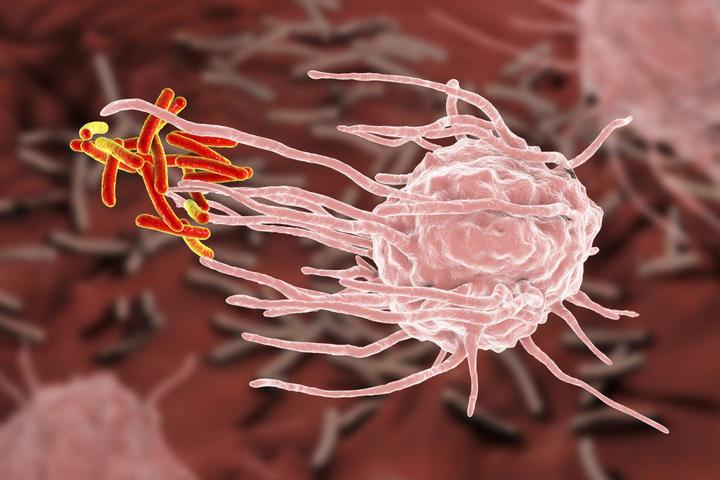
Макрофаги, или фагоциты «поедают» живых и мертвых микробов, комплексы антиген-антитело (образуются в процессе борьбы с вирусами, бактериями и их токсинами), погибшие клетки самого организма. Без этих клеток невозможна деятельность лимфоцитов, поскольку именно они «помогают» последним распознавать антигены, выделяют медиаторы (вещества, которые стимулируют или угнетают деятельность других клеток иммунной системы).
Среднее число микробов, поглощенных одной фагоцитирующей клеткой, называют фагоцитарным числом, а процент фагоцитирующих макрофагов – фагоцитарным показателем.
На поверхности клеток находятся антигены – своеобразные маркеры (метки), по которым одни клетки отличаются от других. Их называют кластерами дифференцировки (CD). То, какие метки находятся на поверхности клетки, зависит от ее вида (Т-лимфоцит, В-лимфоцит и т.д.) и ее зрелости (способности выполнять свои функции). Метки нумеруются по очереди, в соответствии с тем, когда они были открыты: чем раньше был открыт кластер, тем меньше у него номер.
В лабораториях кластеры дифференцировки выявляются с помощью моноклональных антител.
٭Клоном называют совокупность клеток, появившихся от одной общей клетки. Клетки клона идентичны на 100%. Одинаковые клетки синтезируют одинаковые антитела, которые и называют моноклональными.
Наиболее часто встречающиеся следующие виды кластеров:
Обследование на иммуноглобулины дает информацию о состоянии гуморального звена иммунитета. Это используется в диагностике первичных и вторичных иммунодефицитов, аутоиммунных, инфекционных, гематологических и других заболеваний.
Изменения иммунологических показателей могут быть проявлением нормальной реакции организма на воздействие физиологических или патологических факторов (с различной картиной сдвигов на разных стадиях заболевания), отражать чрезмерную активацию, истощение иммунной системы, характеризовать врожденный или приобретенный дефект отдельных звеньев иммунной системы.
Как устроен иммунитет: Объясняем по пунктам
Андрей Смирнов СПИД.ЦЕНТР
«Йогурт для укрепления иммунитета», «Иммуностимулирующие витамины», «Да простудился, наверное, иммунитет упал»… Мы слышим слово «иммунитет» так часто, что уже почти не задумываемся, как он устроен и работает. На уроках биологии нам рассказывали, что иммунитет защищает от микробов, но только ли этим ограничивается его функция и как именно он понимает, от кого нужно нас защищать? СПИД.ЦЕНТР объясняет, как устроена иммунная система.
Наш организм непрерывно меняется, но при этом очень «любит» постоянство и может нормально работать только при определенных параметрах своей внутренней среды. Например, нормальная температура тела колеблется между 36 и 37 градусами по Цельсию. Вспомните последнюю простуду и то, как плохо вы себя чувствовали, стоило температуре подняться всего на полградуса. Такая же ситуация и с другими показателями: артериальным давлением, рН крови, уровнем кислорода и глюкозы в крови и другими. Постоянство значений этих параметров называется гомеостазом, а поддержкой его стабильного уровня занимаются практически все органы и системы организма: сердце и сосуды поддерживают постоянное артериальное давление, легкие — уровень кислорода в крови, печень — уровень глюкозы и так далее.
Иммунная же система отвечает за генетический гомеостаз. Она помогает поддерживать постоянство генетического состава организма. То есть ее задача — уничтожать не только все чужеродные организмы и продукты их жизнедеятельности, проникающие извне (бактерии, вирусы, грибки, токсины и прочее), но также и клетки собственного организма, если «что-то пошло не так» и, например, они превратились в злокачественную опухоль, то есть стали генетически чужеродными.
Как клетки иммунной системы уничтожают «врагов»?
Чтобы разобраться с этим, сначала нужно понять, как иммунная система устроена и какие бывают виды иммунитета.
Иммунитет бывает врожденным (он же неспецифический) и приобретенным (он же адаптивный, или специфический). Врожденный иммунитет одинаков у всех людей и идентичным образом реагирует на любых «врагов». Реакция начинается немедленно после проникновения микроба в организм и не формирует иммунологическую память. То есть, если такой же микроб проникнет в организм снова, система неспецифического иммунитета его «не узнает» и будет реагировать «как обычно». Неспецифический иммунитет очень важен — он первым сигнализирует об опасности и немедленно начинает давать отпор проникшим микробам.
по теме
Мнение
«Иммунитет пациента с ВИЧ похож на иммунитет пожилого человека»
Однако эти реакции не могут защитить организм от серьезных инфекций, поэтому после неспецифического иммунитета в дело вступает приобретенный иммунитет. Здесь уже реакция организма индивидуальна для каждого «врага», поэтому «арсенал» специфического иммунитета у разных людей различается и зависит от того, с какими инфекциями человек сталкивался в жизни и какие прививки делал.
Специфическому иммунитету нужно время, чтобы изучить проникшую в организм инфекцию, поэтому реакции при первом контакте с инфекцией развиваются медленнее, зато работают гораздо эффективнее. Но самое главное, что, один раз уничтожив микроба, иммунная система «запоминает» его и в следующий раз при столкновении с таким же реагирует гораздо быстрее, часто уничтожая его еще до появления первых симптомов заболевания. Именно так работают прививки: когда в организм вводят ослабленных или убитых микробов, которые уже не могут вызвать заболевание, у иммунной системы есть время изучить их и запомнить, сформировать иммунологическую память. Поэтому, когда человек после вакцинации сталкивается с реальной инфекцией, иммунная система уже полностью готова дать отпор, и заболевание не начинается вообще или протекает гораздо легче.
Кто отвечает за работу различных видов иммунитета?
Таким образом, органы иммунной системы обеспечивают образование, созревание и место для жизни иммунных клеток. В нашем организме есть много их видов, вот основные из них.
Как клетки иммунной системы отличают «своих» от «чужих» и понимают, с кем нужно бороться?
В этом им помогает главный комплекс гистосовместимости первого типа (MHC-I). Это группа белков, которая располагается на поверхности каждой клетки нашего организма и уникальна для каждого человека. Это своего рода «паспорт» клетки, который позволяет иммунной системе понимать, что перед ней «свои». Если с клеткой организма происходит что-то нехорошее, например, она поражается вирусом или перерождается в опухолевую клетку, то конфигурация MHC-I меняется или же он исчезает вовсе. Натуральные киллеры и Т-киллеры умеют распознавать MHC-I рецептор, и как только они находят клетку с измененным или отсутствующим MHC-I, они ее убивают. Так работает клеточный иммунитет.
по теме
Эпидемия
Учёные выяснили, как вирусы обманывают иммунитет
Но у нас есть еще один вид иммунитета — гуморальный. Основными защитниками в этом случае являются антитела — специальные белки, синтезируемые B-лимфоцитами, которые связываются с чужеродными объектами (антигенами), будь то бактерия, вирусная частица или токсин, и нейтрализуют их. Для каждого вида антигена наш организм умеет синтезировать специальные, подходящие именно для этого антигена антитела. Молекулу каждого антитела, также их называют иммуноглобулинами, можно условно разделить на две части: Fc-участок, который одинаков у всех иммуноглобулинов, и Fab-участок, который уникален для каждого вида антител. Именно с помощью Fab-участка антитело «прилипает» к антигену, поэтому строение этого участка молекулы зависит от строения антигена.
Как наша иммунная система понимает устройство антигена и подбирает подходящее для него антитело?
Рассмотрим этот процесс на примере развития бактериальной инфекции. Например, вы поцарапали палец. При повреждении кожи в рану чаще всего попадают бактерии. При повреждении любой ткани организма сразу же запускается воспалительная реакция. Поврежденные клетки выделяют большое количество разных веществ — цитокинов, к которым очень чувствительны нейтрофилы и макрофаги. Реагируя на цитокины, они проникают через стенки капилляров, «приплывают» к месту повреждения и начинают поглощать и переваривать попавших в рану бактерий — так запускается неспецифический иммунитет, но до синтеза антител дело пока еще не дошло.
Расправляясь с бактериями, макрофаги выводят на свою поверхность разные их кусочки, чтобы познакомить Т-хелперов и B-лимфоцитов со строением этих бактерий. Этот процесс называется презентацией антигена. Т-хелпер и B-лимфоцит изучают кусочки переваренной бактерии и подбирают соответствующую структуру антитела так, чтобы потом оно хорошо «прилипало» к таким же бактериям. Так запускается специфический гуморальный иммунитет. Это довольно длительный процесс, поэтому при первом контакте с инфекцией организму может понадобиться до двух недель, чтобы подобрать структуру и начать синтезировать нужные антитела.
После этого успешно справившийся с задачей B-лимфоцит превращается в плазматическую клетку и начинает в большом количестве синтезировать антитела. Они поступают в кровь, разносятся по всему организму и связываются со всеми проникшими бактериями, вызывая их гибель. Кроме того, бактерии с прилипшими антителами гораздо быстрее поглощаются макрофагами, что также способствует уничтожению инфекции.
Есть ли еще какие-то механизмы?
Специфический иммунитет не был бы столь эффективен, если бы каждый раз при встрече с инфекцией организм в течение двух недель синтезировал необходимое антитело. Но здесь нас выручает другой механизм: часть активированных Т-хелпером В-лимфоцитов превращается в так называемые клетки памяти. Эти клетки не синтезируют антитела, но несут в себе информацию о структуре проникшей в организм бактерии. Клетки памяти мигрируют в лимфатические узлы и могут сохраняться там десятилетиями. При повторной встрече с этим же видом бактерий благодаря клеткам памяти организм намного быстрее начинает синтезировать нужные антитела и иммунный ответ запускается раньше.
Таким образом, наша иммунная система имеет целый арсенал различных клеток, органов и механизмов, чтобы отличать клетки собственного организма от генетически чужеродных объектов, уничтожая последние и выполняя свою главную функцию — поддержание генетического гомеостаза.
Данная страница не существует!
Услуги инфекционной клиники
Диагностика, профилактика и лечение
Фиброэластометрия и УЗ-диагностика молочных желез, щитовидной железы, мошонки, брюшной полости
Биохимия. Анализ крови: общий, клинический. Анализы на витамины, микроэлементы и электролиты. Анализ на ВИЧ-инфекцию, вирусные гепатиты, бактерии, грибки и паразиты
Максимально точное определение выраженности фиброза печени неинвазивным методом при помощи аппарата FibroScan 502 TOUCH
Гинеколог в H-Сlinic решает широчайший спектр задач в области женского здоровья. Это специалист, которому вы можете полностью доверять
Дерматовенерология в H-Сlinic — это самые современные и эффективные алгоритмы диагностики и лечения заболеваний, передающихся половым путем, грибковых и вирусных поражений, а также удаление доброкачественных невусов, бородавок, кондилом и папиллом
Возможности вакцинопрофилактики гораздо шире Национального календаря прививок. H-Clinic предлагает разработку плана вакцинации и современные высококачественные вакцины в наличии
Терапевт в H-Сlinic эффективно решает задачи по лечению заболеваний, которые зачастую могут становиться большой проблемой при наличии хронического инфекционного заболевания
Врач-кардиолог H-Сlinic проведет комплексную диагностику сердечно-сосудистой системы и при необходимости назначит эффективное терапию. Сердечно-сосудистые проблемы при инфекционных заболеваниях, требуют специфичных подходов, которые мы в состоянии обеспечить
Наша цель — новое качество вашей жизни. Мы используем современные диагностические алгоритмы и строго следуем наиболее эффективным протоколам лечения.
Общая терапия, Инфекционные заболевания, Гастроэнтерология, Дерматовенерология, Гинекология, Вакцинация, УЗИ и фиброэластометрия, Кардиология, Неврология
Биохимия, Общий/клинический анализ крови, Витамины и микроэлементы/электролиты крови, ВИЧ-инфекция, Вирусные гепатиты, Другие инфекции, бактерии, грибки и паразиты, Комплексы и пакеты анализов со скидкой
В наличии и под заказ качественные бюджетные решения и препараты лидеров рынка лечения инфекционных болезней. Аптека H-Clinic готова гибко реагировать на запросы наших клиентов. Мы поможем с оперативным поиском препаратов, которые обычно отсутствуют в сетях.
Иммунитет: борьба с чужими и… своими
Автор
Редакторы
Рецензент
Около 5% населения Земли страдают аутоиммунными заболеваниями — состоянием, при котором собственные клетки иммунной системы организма вместо того, чтобы бороться с патогенами, уничтожают нормальные клетки органов и тканей. В этой статье, предваряющей спецпроект по аутоиммунным заболеваниям, мы рассмотрим основные принципы работы иммунной системы и покажем, почему возможна такая диверсия с ее стороны.
Аутоиммунные заболевания
Этой статьей мы начинаем цикл по аутоиммунным заболеваниям — болезням, при которых организм начинает бороться сам с собой, вырабатывая аутоантитела и/или аутоагрессивные клоны лимфоцитов. Мы расскажем о том, как работает иммунитет и почему иногда он начинает «стрелять по своим». Некоторым самым распространенным заболеваниям будут посвящены отдельные публикации. Для соблюдения объективности мы пригласили стать куратором спецпроекта доктора биологических наук, чл.-корр. РАН, профессора кафедры иммунологии МГУ Дмитрия Владимировича Купраша. К тому же у каждой статьи есть свой рецензент, более детально вникающий во все нюансы. Рецензентом этой — вводной — статьи стал Евгений Сергеевич Шилов, кандидат биологических наук, научный сотрудник этой же кафедры.
Партнеры проекта — Михаил Батин и Алексей Маракулин (Open Longevity / «Объединенные Консультанты Финправо»).
Иммунитет — система реакций, призванная защитить организм от вторжения бактерий, вирусов, грибов, простейших и других вредоносных агентов — так называемых патогенов. Если представить, что наше тело — это страна, то иммунную систему можно сравнить с ее вооруженными силами. Чем более слаженным и адекватным будет их ответ на интервенцию патогенов, тем надежнее окажется защита организма.
В мире существует великое множество патогенов, и для того чтобы эффективно бороться со всеми ними, в результате длительной эволюции сформировалась замысловатая система из иммунных клеток, каждая из которых имеет свою стратегию борьбы. Клетки иммунной системы взаимно дополняют друг друга: применяют разные способы уничтожения патогена, могут усиливать или ослаблять действие других клеток, а также привлекать всё новых бойцов на поле битвы, если сами не справляются.
Нападая на организм, патогены оставляют молекулярные «улики», которые «подбирают» иммунные клетки. Такие улики называются антигенами.
Антигены — любые вещества, которые организм воспринимает как чужеродные и, соответственно, отвечает на их появление активацией иммунитета. Самыми важными для иммунной системы антигенами являются кусочки молекул, расположенных на внешней поверхности патогена. По этим кусочкам можно определить, какой именно агрессор напал на организм, и обеспечить борьбу с ним.
Цитокины — азбука Морзе организма
Для того чтобы иммунные клетки могли скоординировать свои действия в борьбе с врагом, им необходима система сигналов, сообщающих, кому и когда вступать в бой, или заканчивать битву, или, наоборот, возобновлять ее, и многое-многое другое. Для этих целей клетками вырабатываются небольшие белковые молекулы — цитокины, например, различные интерлейкины (IL-1, 2, 3 и т.д.) [1]. Многим цитокинам сложно приписать однозначную функцию, однако с некоторой степенью условности их можно разделить на пять групп: хемокины, факторы роста, провоспалительные, противовоспалительные и иммунорегуляторные цитокины.
Упомянутая выше условность классификации означает, что цитокин, входящий в одну из перечисленных групп, при определенных условиях в организме может сыграть диаметрально противоположную роль — например, из провоспалительного превратиться в противовоспалительный.
Без налаженной связи между видами войск любая хитроумная военная операция обречена на провал, поэтому клеткам иммунной системы очень важно, принимая и отдавая приказы в виде цитокинов, правильно их интерпретировать и слаженно действовать. Если цитокиновые сигналы начинают вырабатываться в очень большом количестве, то в клеточных рядах наступает паника, что может привести к повреждению собственного организма. Это называется цитокиновым штормом: в ответ на поступающие цитокиновые сигналы клетки иммунной системы начинают продуцировать всё больше и больше собственных цитокинов, которые, в свою очередь, действуют на клетки и усиливают секрецию самих себя. Формируется замкнутый круг, который приводит к разрушению окружающих клеток, а позже и соседних тканей.
По порядку рассчитайсь! Иммунные клетки
Как в вооруженных силах существуют разные рода войск, так и клетки иммунной системы можно разделить на две большие ветви — врожденного и приобретенного иммунитета, за изучение которых в 2011 году была вручена Нобелевская премия [3], [4], [5]. Врожденный иммунитет — та часть иммунной системы, что готова защищать организм немедленно, как только совершилось нападение патогена. Приобретенный же (или адаптивный) иммунный ответ при первом контакте с врагом разворачивается дольше, так как требует хитроумной подготовки, но зато после может осуществлять более сложный сценарий защиты организма. Врожденный иммунитет очень эффективен в борьбе с единичными диверсантами: он обезвреживает их, не беспокоя специализированные элитные воинские подразделения — адаптивный иммунитет. Если же угроза оказалась более существенной и есть риск проникновения патогена всё глубже в организм, клетки врожденного иммунитета немедленно сигнализируют об этом, и в бой вступают клетки иммунитета приобретенного.
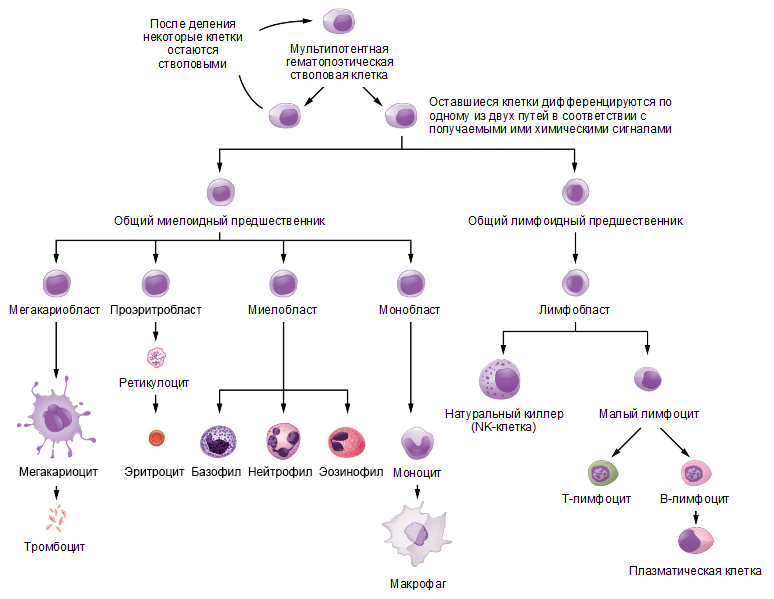
Все иммунные клетки организма образуются в костном мозге от кроветворной стволовой клетки, которая дает начало двум клеткам — общему миелоидному и общему лимфоидному предшественникам [2], [6]. Клетки приобретенного иммунитета происходят от общего лимфоидного предшественника и, соответственно, называются лимфоцитами, тогда как клетки врожденного иммунитета могут брать начало от обоих предшественников. Схема дифференцировки клеток иммунной системы изображена на рисунке 1.
Рисунок 1. Схема дифференцировки клеток иммунной системы. Кроветворная стволовая клетка дает начало клеткам — предшественницам миелоидной и лимфоидной линий дифференцировки, из которых дальше образуются все типы клеток крови.
Сайт opentextbc.ca, рисунок адаптирован.
Врожденный иммунитет — регулярная армия
Клетки врожденного иммунитета распознают патоген по специфичным для него молекулярным маркерам — так называемым образам патогенности [7]. Эти маркеры не позволяют точно определить принадлежность патогена к тому или иному виду, а лишь сигнализируют о том, что иммунитет столкнулся с чужаками. Для нашего организма подобными маркерами могут служить фрагменты клеточной стенки и жгутиков бактерий, двухцепочечная РНК и одноцепочечная ДНК вирусов, и т.д. При помощи специальных рецепторов врожденного иммунитета, таких как TLR (Toll-like receptors, Толл-подобные рецепторы) и NLR (Nod-like receptors, Nod-подобные рецепторы), клетки взаимодействуют с образами патогенности и приступают к реализации своей защитной стратегии.
Теперь подробнее рассмотрим некоторые клетки врожденного иммунитета.
Макрофаги и дендритные клетки поглощают (фагоцитируют) патоген, и уже внутри себя при помощи содержимого вакуолей растворяют его. Такой способ уничтожения врага очень удобен: осуществившая его клетка не только может и дальше активно функционировать, но и получает возможность сохранить в себе фрагменты патогена — антигены, которые при необходимости послужат сигналом активации для клеток адаптивного иммунитета. Лучше всего с этим справляются дендритные клетки — именно они работают связистами между двумя ветвями иммунной системы, что необходимо для успешного подавления инфекции.
Видео 1. Нейтрофилы (обозначены зеленым) приходят в очаг повреждения ткани. Видео снято при помощи прижизненной двухфотонной микроскопии.
Эозинофилы, базофилы и тучные клетки выделяют в окружающую ткань содержимое своих гранул — химическую защиту против крупных патогенов, например, паразитических червей. Однако, как это часто бывает, химикатами может отравиться и мирное население, и эти клетки широко известны не столько своей прямой физиологической ролью, сколько вовлеченностью в развитие аллергической реакции.
Помимо вышеупомянутых миелоидных клеток, во врожденном иммунитете работают и клетки лимфоидного ряда, которые так и называются — лимфоидные клетки врожденного иммунитета. Они продуцируют цитокины и, соответственно, регулируют поведение других клеток организма.
Один из типов этих клеток — так называемые натуральные киллеры (natural killers, или NK-клетки). Они — пехота в вооруженных силах организма: борются с зараженными клетками один на один, вступая с ними в рукопашный бой. NK-клетки выделяют белки перфорин и гранзим В. Первый, как следует из названия, перфорирует клеточную мембрану мишени, встраиваясь в нее, а второй, подобно картечи, проникает через эти бреши и запускает гибель клетки, расщепляя белки, ее образующие.
Удивительно, но на разных стадиях своего развития некоторые клетки иммунной системы могут выполнять функции, противоположные друг другу. Так, выделяют гетерогенную группу предшественников различных иммунных клеток врожденного иммунитета, которые в таком незрелом виде подавляют иммунный ответ. Их так и назвали: миелоидные супрессорные клетки. Их количество увеличивается в организме в ответ на появление хронической инфекции или рака. Роль таких клеток очень важна, ведь они не позволяют другим бойцам армии иммунитета слишком сильно бороться с врагом, повреждая тем самым мирное население — ни в чем не повинные клетки, находящиеся поблизости.
Адаптивный иммунитет — спецподразделения вооруженных сил организма
Для того чтобы понять, как работает Т-клеточный рецептор, надо вначале немного обсудить еще одно важное семейство белков — главный комплекс гистосовместимости (MHC, major histocompatibility complex) [9]. Эти белки — молекулярные «пароли» организма, позволяющие клеткам иммунной системы отличать своих соотечественников от неприятеля. В любой клетке постоянно идет процесс деградации белков. Специальная молекулярная машина — иммунопротеасома — расщепляет белки на короткие пептиды, которые могут быть встроены в MHC и, как яблочко на тарелочке, преподнесены Т-лимфоциту. Тот при помощи TCR «видит» пептид и распознает, принадлежит ли он собственным белкам организма или является чужеродным. Одновременно TCR проверяет, знакома ли ему молекула MHC, — это позволяет отличать собственные клетки от «соседских», то есть клеток того же вида, но другой особи. Именно совпадение молекул MHC необходимо для приживления пересаженных тканей и органов, отсюда и такое мудреное название: histos по-гречески означает «ткань». У человека молекулы MHC также называются HLA (human leukocyte antigen — человеческий лейкоцитарный антиген).
Видео 2. Кратковременные взаимодействия Т-клеток с дендритной клеткой (обозначена зеленым). Видео снято при помощи прижизненной двухфотонной микроскопии.
T-лимфоциты
Для активации Т-лимфоцита нужно, чтобы он получил три сигнала. Первый из них — взаимодействие TCR с MHC, то есть распознавание антигена. Второй — так называемый костимуляторный сигнал, передающийся антигенпрезентирующей клеткой через молекулы CD80/86 на СD28, находящуюся на лимфоците. Третий же сигнал — продукция коктейля из множества провоспалительных цитокинов. Если какой-то из этих сигналов ломается, это чревато серьезными последствиями для организма, например, реакцией аутоиммунитета.
Существует два типа молекул главного комплекса гистосовместимости: MHC-I и MHC-II. Первый присутствует на всех клетках организма и несет на себе пептиды клеточных белков или же белков заразившего ее вируса. Специальный подтип Т-клеток — Т-киллеры (их еще называют CD8+ Т-лимфоциты) — своим рецептором взаимодействует с комплексом «MHC-I—пептид». Если это взаимодействие достаточно сильное, значит, пептид, который видит Т-клетка, не характерен для организма и, соответственно, может принадлежать внедрившемуся в клетку врагу — вирусу. Необходимо срочно обезвредить нарушителя границ, и Т-киллер отлично справляется с этой задачей. Он, подобно NK-клетке, выделяет белки перфорин и гранзим, что приводит к лизису клетки-мишени.
Т-клеточный рецептор другого подтипа Т-лимфоцитов — Т-хелперов (Th-клетки, CD4+ T-лимфоциты) — взаимодействует с комплексом «MHC-II—пептид». Это комплекс есть не на всех клетках организма, а в основном на иммунных, и пептиды, которые могут презентироваться молекулой MHC-II, являются фрагментами патогенов, захваченных из внеклеточного пространства. Если Т-клеточный рецептор взаимодействует с комплексом «MHC-II—пептид», то Т-клетка начинает продуцировать хемокины и цитокины, помогающие другим клеткам эффективно осуществлять свою функцию — борьбу с врагом. Потому-то эти лимфоциты и называются хелперами — от английского helper (помощник). Среди них выделяют множество подтипов, которые различаются спектром вырабатываемых цитокинов и, следовательно, ролью в иммунном процессе. Например, существуют Th1-лимфоциты, эффективные в борьбе с внутриклеточными бактериями и простейшими, Th2-лимфоциты, помогающие В-клеткам в работе и потому важные для противостояния внеклеточным бактериям (о чём мы скоро поговорим), Th17-клетки и многие другие.
Видео 3. Движение Т-хелперов (красные) и Т-киллеров (зеленые) в лимфоузле. Видео снято при помощи прижизненной двухфотонной микроскопии.
Среди CD4+ T-клеток существует особый подтип клеток — регуляторные Т-лимфоциты. Их можно сравнить с военной прокуратурой, сдерживающей фанатизм рвущихся в бой солдат и не дающей им причинить вред мирному населению. Эти клетки продуцируют цитокины, подавляющие иммунный ответ, и таким образом ослабляют иммунную реакцию, когда враг повержен.
То, что Т-лимфоцит распознает только чужеродные антигены, а не молекулы собственного организма, является следствием хитроумного процесса, называемого селекцией. Она происходит в специально созданном для этого органе — тимусе, где завершают свое развитие Т-клетки. Суть селекции такова: клетки, окружающие юный, или наивный, лимфоцит, показывают (презентируют) ему пептиды собственных белков. Тот лимфоцит, который слишком хорошо или слишком плохо узнает эти белковые фрагменты, уничтожается. Выжившие же клетки (а это менее 1% всех предшественников Т-лимфоцитов, пришедших в тимус) обладают промежуточным сродством к антигену, следовательно, они, как правило, не считают собственные клетки мишенями для атаки, но имеют возможность среагировать на подходящий чужеродный пептид. Селекция в тимусе — механизм так называемой центральной иммунологической толерантности.
Всё вышесказанное относится к αβ-Т-лимфоцитам, однако существует еще один тип Т-клеток — γδ-T-лимфоциты (название определяет состав белковых молекул, образующих TCR) [11]. Они относительно малочисленны и в основном заселяют слизистую оболочку кишечника и другие барьерные ткани, играя важнейшую роль в регуляции состава обитающих там микробов. У γδ-T-клеток механизм распознавания антигенов отличается от αβ-Т-лимфоцитарного и не зависит от TCR [12].
B-лимфоциты
В-лимфоциты несут на своей поверхности В-клеточный рецептор [13]. При контакте с антигеном эти клетки активируются и превращаются в особый клеточный подтип — плазматические клетки, обладающие уникальной способностью секретировать свой B-клеточный рецептор в окружающую среду — именно эти молекулы мы называем антителами. Таким образом, как BCR, так и антитело имеет сродство к распознаваемому им антигену, как бы «прилипает» к нему. Это дает возможность антителам обволакивать (опсонизировать) клетки и вирусные частицы, покрытые молекулами антигена, привлекая макрофаги и другие иммунные клетки для уничтожения патогена. Антитела также умеют активировать специальный каскад иммунологических реакций, называемый системой комплемента, который приводит к перфорации клеточной мембраны патогена и его гибели.
Для эффективной встречи клеток адаптивного иммунитета с дендритными клетками, несущими в составе MHC чужеродные антигены и поэтому работающими «связными», в организме существуют специальные иммунные органы — лимфоузлы. Распределение их по организму неоднородно и зависит от того, насколько уязвимой является та или иная граница. Бόльшая их часть находится вблизи пищеварительного и дыхательного трактов, ведь проникновение патогена с пищей или вдыхаемым воздухом — наиболее вероятный способ заражения.
Видео 4. Перемещение Т-клеток (обозначены красным) по лимфоузлу. Клетки, образующие структурную основу лимфоузла и стенки сосудов, помечены зеленым флуоресцентным белком. Видео снято при помощи прижизненной двухфотонной микроскопии.
Развитие адаптивного иммунного ответа требует достаточно много времени (от нескольких дней до двух недель), и для того чтобы организм мог защищаться от уже знакомой инфекции быстрее, из Т- и В-клеток, участвовавших в прошлых битвах, формируются так называемые клетки памяти. Они, подобно ветеранам, в небольшом количестве присутствуют в организме, и если появляется знакомый им патоген, вновь активируются, быстро делятся и целой армией выходят на защиту границ.
Логика иммунного ответа
Когда организм атакуют патогены, в бой в первую очередь вступают клетки врожденного иммунитета — нейтрофилы, базофилы и эозинофилы. Они выделяют вовне содержимое своих гранул, способное повредить клеточную стенку бактерий, а также, например, усилить кровоток, чтобы как можно больше клеток поспешило в очаг инфекции.
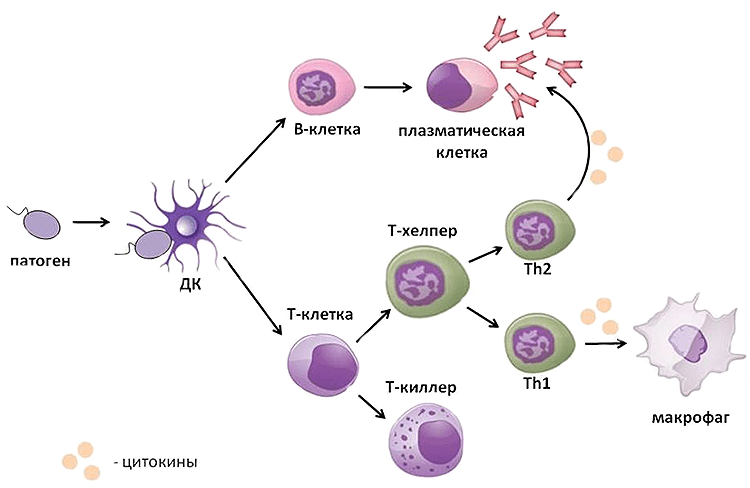
Одновременно с этим дендритная клетка, поглотившая патоген, спешит в ближайший лимфоузел, где передает информацию о нём находящимся там Т- и В-лимфоцитам. Те активируются и путешествуют до местонахождения патогена (рис. 2). Битва разгорается: Т-киллеры при контакте с зараженной клеткой убивают ее, Т-хелперы помогают макрофагам и В-лимфоцитам осуществлять их механизмы защиты. В итоге патоген гибнет, а победившие клетки отправляются на покой. Бόльшая их часть погибает, но некоторые становятся клетками памяти, которые поселяются в костном мозге и ждут, когда их помощь снова понадобится организму.
Рисунок 2. Схема иммунного ответа. Проникший в организм патоген обнаруживается дендритной клеткой, которая движется в лимфоузел и там передает информацию о враге Т- и В-клеткам. Те активируются и выходят в ткани, где реализуют свою защитную функцию: В-лимфоциты продуцируют антитела, Т-киллеры при помощи перфорина и гранзима В осуществляют контактный киллинг патогена, а Т-хелперы продуцируют цитокины, помогающие другим клеткам иммунной системы в борьбе с ним.
Схема составлена автором статьи.
Так выглядит схема любого иммунного ответа, однако она может заметно видоизменяться в зависимости от того, какой именно патоген проник в организм. Если мы имеем дело с внеклеточными бактериями, грибами или, скажем, глистами, то основными вооруженными силами в этом случае будут эозинофилы, В-клетки, продуцирующие антитела, и Th2-лимфоциты, помогающие им в этом. Если же в организме поселились внутриклеточные бактерии, то на помощь в первую очередь спешат макрофаги, которые могут поглотить инфицированную клетку, и Th1-лимфоциты, помогающие им в этом. Ну а в случае вирусной инфекции в бой вступают NK-клетки и Т-киллеры, которые уничтожают зараженные клетки методом контактного киллинга.
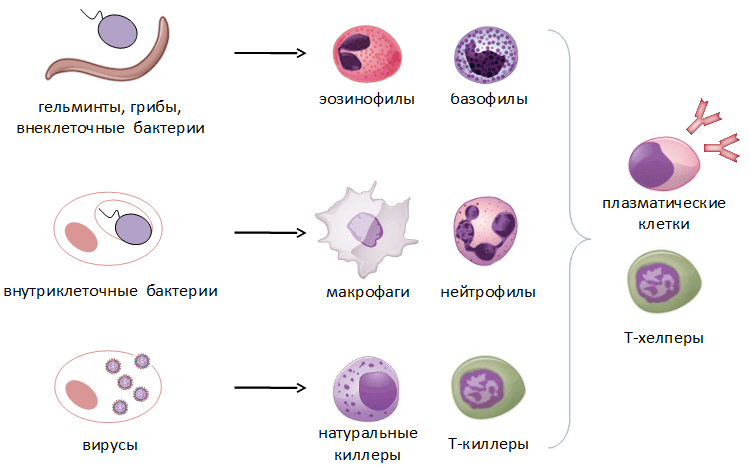
Как мы видим, многообразие типов иммунный клеток и механизмов их действия неслучайно: на каждую разновидность патогена у организма припасен свой эффективный способ борьбы (рис. 3).
Рисунок 3. Основные типы патогенов и клетки, принимающие участие в их уничтожении.
Схема составлена автором статьи.
А теперь все вышеописанные иммунные перипетии — в коротком видео.
Видео 5. Механизм иммунного ответа.
Громыхает гражданская война.
К сожалению, ни одна война не обходится без потерь среди гражданского населения. Долгая и интенсивная защита может дорого стоить организму, если агрессивные высокоспециализированные войска выйдут из-под контроля. Повреждение собственных органов и тканей организма иммунной системой называется аутоиммунным процессом [3]. Заболеваниями этого типа страдает около 5% человечества.
Селекция Т-лимфоцитов в тимусе, а также удаление аутореактивных клеток на периферии (центральная и периферическая иммунологическая толерантность), о которых мы говорили ранее, не могут полностью избавить организм от аутореактивных Т-лимфоцитов. Что же касается В-лимфоцитов, вопрос о том, насколько строго осуществляется их селекция, до сих пор остается открытым. Поэтому в организме каждого человека обязательно присутствует множество аутореактивных лимфоцитов, которые в случае развития аутоиммунной реакции могут повреждать собственные органы и ткани в соответствии со своей специфичностью.
За аутоиммунные поражения организма могут быть ответственны как Т-, так и В-клетки. Первые осуществляют непосредственное убийство безвинных клеток, несущих на себе соответствующий антиген, а также помогают аутореактивным В-клеткам в продукции антител. Т-клеточный аутоиммунитет хорошо изучен при ревматоидном артрите, сахарном диабете первого типа, рассеянном склерозе и многих других болезнях.
В-лимфоциты действуют куда более изощренно. Во-первых, аутоантитела могут вызывать гибель клеток, активируя на их поверхности систему комплемента или же привлекая макрофаги. Во-вторых, мишенями для антител могут стать рецепторы на поверхности клетки. При связывании такого антитела с рецептором тот может или блокироваться, или же активироваться без реального гормонального сигнала. Так происходит при болезни Грейвса: В-лимфоциты производят антитела против рецептора к ТТГ (тиреотропному гормону), мимикрируя действие гормона и, соответственно, усиливая продукцию тиреоидных гормонов [14]. При миастении гравис антитела против рецептора к ацетилхолину блокируют его действие, что приводит к нарушению нейромышечной проводимости. В-третьих, аутоантитела вместе с растворимыми антигенами могут образовывать иммунные комплексы, которые оседают в различных органах и тканях (например, в почечных клубочках, суставах, на эндотелии сосудов), нарушая их работу и вызывая воспалительные процессы.
Как правило, аутоиммунное заболевание возникает внезапно, и невозможно точно определить, что стало его причиной. Считается, что триггером для запуска может послужить практически любая стрессовая ситуация, будь то перенесенная инфекция, травма или переохлаждение. Значительный вклад в вероятность возникновения аутоиммунного заболевания вносит как образ жизни человека, так и генетическая предрасположенность — наличие определенного варианта какого-либо гена.
Предрасположенность к тому или иному аутоиммунному заболеванию часто ассоциирована с определенными аллелями генов MHC, о которых мы уже много говорили. Так, наличие аллеля HLA-B27 может служить маркером предрасположенности к развитию болезни Бехтерева, ювенильного ревматоидного артрита, псориатического артрита и других заболеваний. Интересно, что присутствие в геноме того же самого HLA-B27 коррелирует с эффективной защитой от вирусов: например, носители этого аллеля имеют пониженные шансы заразиться ВИЧ или гепатитом С [15], [16]. Это еще одно напоминание о том, что чем агрессивнее воюет армия, тем вероятнее потери среди гражданского населения.
Кроме того, на развитие болезни может влиять уровень экспрессии аутоантигена в тимусе. Например, продукция инсулина и, соответственно, частота презентации его антигенов Т-клеткам различается от человека к человеку. Чем она выше, тем ниже риск развития сахарного диабета первого типа, так как это позволяет удалить специфичные к инсулину Т-лимфоциты.
Все аутоиммунные заболевания можно разделить на органоспецифические и системные. При органоспецифических болезнях поражаются отдельные органы или ткани. Например, при рассеянном склерозе — миелиновая оболочка нейронов, при ревматоидном артрите — суставы, а при сахарном диабете первого типа — островки Лангерганса в поджелудочной железе. Системные аутоиммунные заболевания характеризуются поражением многих органов и тканей. К таким болезням относятся, например, системная красная волчанка и первичный синдром Шегрена, поражающие соединительную ткань. Более подробно об этих заболеваниях будет рассказано в других статьях спецпроекта.
Заключение
Как мы уже убедились, иммунитет — это сложнейшая сеть взаимодействий как на клеточном, так и на молекулярном уровнях. Создать идеальную систему, надежно защищающую организм от атак патогенов и одновременно ни при каких условиях не повреждающую собственные органы, не смогла даже природа. Аутоиммунные заболевания — побочный эффект высокой специфичности работы системы адаптивного иммунитета, те издержки, которыми нам приходится платить за возможность успешно существовать в мире, кишащем бактериями, вирусами и другими патогенами.
Медицина — творение рук человека — не может в полной мере исправить то, что было создано природой, поэтому на сегодняшний день ни одно из аутоиммунных заболеваний полностью не излечивается. Поэтому цели, которых стремится достичь современная медицина, — это своевременная диагностика заболевания и эффективное купирование его симптомов, от которого напрямую зависит качество жизни пациентов. Однако для того чтобы это было возможно, необходимо повысить информированность населения об аутоиммунных заболеваниях и способах их лечения. «Предупрежден — значит вооружен!» — вот девиз общественных организаций, созданных для этого по всему миру.
 masterok
masterok