В чем заключается коррекция сфинктера одди
В чем заключается коррекция сфинктера одди
Полный текст статьи:
Чаще всего данная патология выявляется у людей перенесших холецистэктомию, но с сохраняющимся типичным приступами билиарной боли. Одной из гипотез развития, а точнее проявления этого патологического состояния именно после холецистэктомии является потеря резервуарной функции (позволявшей компенсировать повышения давления в желчных протоках) выполнявшейся желчным пузырем [8]. Так же существует мнение о роли пересечения нервных волокон идущих от желчного пузыря к сфинктеру по пузырному протоку [7]. Вопрос о существовании клинически самостоятельной ДСО до операции является дискутабельным. ДСО встречается у 1-2 % пациентов после холецистэктомии [8]. Типичный пациент с данной патологией это женщина 40-60 лет с перенесенной в последние 5 лет холецистэктомией. Выделяют 3 группы билиарной ДСО, каждая из которых обладает определенными клинико-лабораторными критериями [5].
Следует отметить, что в клинической практике преобладают пациенты 3-й группы.
Клинически может проявляться рецидивирующим хроническим панкреатитом. Для этой формы ДСО так же выделены 3 ее типа [11].
Считается, что «золотым стандартом» диагностики ДСО является манометрия сфинктера Одди [13]. Выполняется манометрия во время РХПГ с помощью специального баллона. Определяется базовый тонус сфинктера и его фазовые сокращения. Патологическим считается давление выше 40 мм водного столба. К другим патологическим признакам относят повышенную частоту волновых сокращений, увеличения числа ретроградных перистальтических волн [12]. Отсутствие снижения давления сфинктера при введении гладкомышечных релаксантов (нитраты, блокаторы кальцевых каналов) так же имеет диагностическое значение. Однако повышенное давление в сфинктере Одди выявляется при билиарной форме в 86 % случаев в 1й группе, примерно в 55 % случаев во второй группе и у 28 % больных третьей группы (билиарный тип) и при панкреатической форме ДСО в 92 %, 58 %, 35 % больных соответственно [4]. Таким образом приходиться признать, что хотя бы у части больных с характерной клиникой постоянного гипертонуса сфинктера не наблюдается. К сожалению метод манометрии в нашей стране малодоступен, дорог и кроме того, ее выполнение связанно с определенным риском развития панкреатита. Что мы можем использовать в реальной клинической практике?
УЗИ. Выполнение УЗИ после назначения пациенту завтрака с высоким содержанием жира (что стимулирует выделение желчи) у пациентов с ДСО приводит к дилатации холедоха в результате повышения в нем давления из-за нарушения оттока. Диагностическим считается увеличение диаметра более чем на 2 мм при измерении его через 45 минут после завтрака. Метод легко доступен практически в любом лечебном учреждении. Его специфичность достигает 97 %, однако чувствительность только 21 % (сравнение проводилось с манометрией) [10]. Кстати, вместо завтрака можно использовать стимуляцию холецистокинином, а для исследования панкреатического протока серетином.
Существуют сообщения об успешном использовании синцитографии для диагностики ДСО. Однако методика достаточно сложна, да и специфичность с чувствительностью составляют 78 % и 49 % соответственно [10].
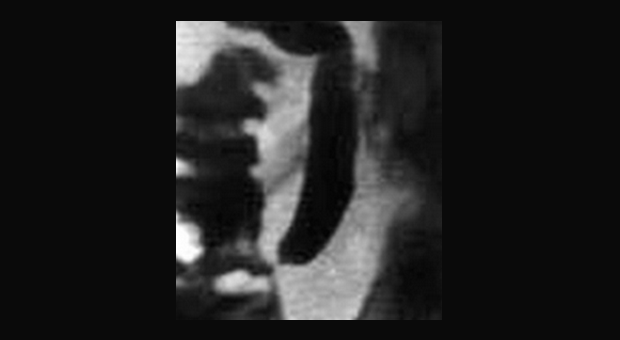
В нашей практике мы в основном используем УЗИ. Кроме того, при выполнении таким больным РХПГ и выявленной стриктуре терминального отдела холедоха или просто замедлении опорожнения желчных путей пациенту даются нитраты. Начало (или ускорение) их опорожнения после введения нитратов по нашему мнению с определенной степенью уверенности позволяет говорить о наличии у больного ДСО. Этот тест в определенной степени помогает дифференцировать анатомические и функциональные изменения сфинктера. В ряде случаев, казалось бы, явные стриктуры терминального отдела холедоха полностью исчезали поле применения нитратов, рубцовые сужения на введение препаратов не реагировали. На рисунках показана типичная для пациентов ДСО картина РХПГ (сужение в терминальном отделе общего желчного протока).
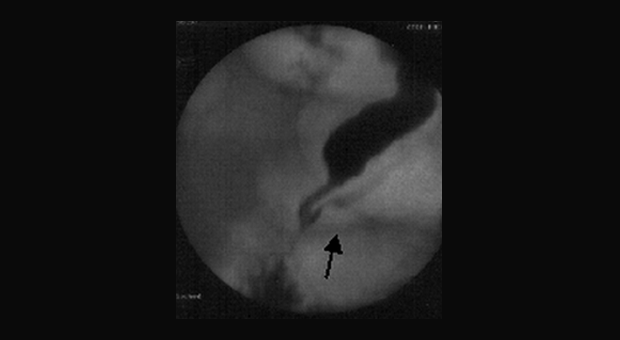
Выявленный на РХПГ билиарно-панкреатический рефлюкс так же позволяет заподозрит эту патологию, особенно при наличии у пациента клиники идиопатического рецидивирующего панкреатита. Картина рефлюкса представлена на следующем рисунке.
Лечение
Хирургическую сфинктеротомию, сфинктеропласику и иссечение сфинктера, описанные в качестве лечения ДСО мы в своей практике не применяли. В любом случае, только манометрические данные, точно верифицирующие ДСО и неэффективность всех вышеописанных методов могут оправдывать такие высоко инвазивные вмешательства.
Заключение
Конечно, проблема ДСО весьма сложна и далека от своего решения. Необходимо разработать неинвазивные, простые, дешевые и достоверные методы диагностики, эффективное медикаментозное лечение. Здесь были изложены как общемировые подходы к диагностике и лечению данной патологии, так и наши собственные мысли по решению данной проблемы (о правильности последних судить Вам).
Дисфункция сфинктера Одди (постхолецистэктомический синдром)
Выделяют 3 группы патологических состояний органов пищеварительной системы у больных после холецистэктомии:
I. Функциональные расстройства сфинктера Одди (вследствие потери функционирующего желчного пузыря). II. Билиарная гипертензия с наличием органического препятствия току желчи:
Сопутствующие заболевания пищеварительного тракта, имеющиеся до холецистэктомии или развившиеся после нее:
Согласно Римскому консенсусу по функциональным расстройствам органов пищеварения, вместо терминов «постхолецистэктомический синдром (ПХЭС)», «билиарная дискинезия» в качестве диагноза рекомендуется использовать термин «дисфункция сфинктера Одди (ДСО)».
Определение. Под термином ПХЭС (ДСО) понимают развившуюся после оперативного лечения дисфункцию сфинктера Одди, обусловленную нарушением сократительной функции сфинктера общего желчного протока, тонуса панкреатического протока или общего сфинктеРа, что препятствует нормальному оттоку желчи и панкреатического секрета в двенадцатиперстную кишку при отсутствии в нем органических препятствий
Распространенность. ПХЭС (ДСО) встречается у 1030 % пациентов после удаления желчного пузыря и характеризуется болью, сходной с билиарной, у больных после перенесенной холецистэктомии.
Что провоцирует / Причины Дисфункции сфинктера Одди (постхолецистэктомического синдрома):
Существует несколько причин ДСО. изменение состава желчи, нарушение ее пассажа, дискинезия сфинктера печеночноподжелудочной ампулы; избыточный бактериальный рост в кишечнике, качество оперативного вмешательства и др. Нарушения функции сфинктера могут быть связаны с наличием дискинезий (преимущественно спазм) или сочетаться со структурными нарушениями, в частности со стенозом.
Патогенез (что происходит?) во время Дисфункции сфинктера Одди (постхолецистэктомического синдрома):
Анализируя характер функциональных нарушений, необходимо остановиться на особенностях анатомического строения сфинктера Одди. Он включает:
Симптомы Дисфункции сфинктера Одди (постхолецистэктомического синдрома):
О дисфункции сфинктера Одди у больных, перенесших холецистэктомию, можно предположить при наличии болевого синдрома в эпигастрии в случаях, если не выявляются другие причины, способные объяснить их происхождение (сопутствующие заболевания, структурные изменения билиарных и панкреатических протоков); при наличии идиопатического рецидивирующего панкреатита, рецидивирующих билиарных коликах у больных с наличием неизмененного желчного пузыря и холедоха.
У ряда лиц после холецистэктомии возникают симптомы, свидетельствующие о нарушении процесса пищеварения и моторных расстройствах тонкой или толстой кишки.
Ведущие патогенетические факторы формирования клинических симптомов у больных после холецистэктомии, основными из которых являются:
Диагностика Дисфункции сфинктера Одди (постхолецистэктомического синдрома):
Особенности диагностики. Для исключения органической патологии оилиарной системы используют ряд скрининговых и уточняющих методов. К непрямым методам, позволяющим предположить дисфункцию сфинктера Одди, относят исследование в крови содержания билирубина, активности щелочной фосфатазы, аминотрансфераз, амилазы и липазы, проводимое во время или не позже 6 ч после окончания болевого приступа, а также в динамике. Дисфункция сфинктера подтверждается транзиторным их повышением в 2 раза и более или не менее чем при двух последовательных болевых приступах. Большое значение в диагностике дисфункции имеет провокационный морфинопростигминовый тест. Расширение холедоха и главного панкреатического протока, свидетельствующее о нарушении тока желчи и панкреатического сока на уровне сфинктера Одди, определяется при проведений УЗИ органов брюшной полости. Вместе с тем необходимо погнить, что у 34 % лиц, перенесших холецистэктомию, при отсутствии клинической симптоматики имеется расширение общего желчного протока. В диагностике дисфункции сфинктера Одди используется динамическое УЗИ диаметра общего желчного протока с применением жирных завтраков, стимулирующих выработку эндогенного холецистокинина и увеличивающих холерез. При этом после пробного завтрака измерение холедоха проводится в течение 1 ч каждые 15 мин. Увеличение его диаметра на 2 мм и более может свидетельствовать о наличии неполной обтурации холедоха в результате дисфункции сфинктера Одди или органической патологии билиарной системы.
Изменение диаметра панкреатических протоков определяется при проведении пробы с секретином. У здорового человека после введения 1 мг/кг секретина при УЗИ в течение 30 мин отмечается расширение панкреатического протока с последующим его уменьшением до исходного уровня. Расширение протока в течение более чем 30 мин указывает на нарушение его проходимости. Важным в диагностике дисфункции сфинктера является компьютерная томография гепатодуоденального отдела ЖКТ. К инвазивным непрямым методам оценки функции сфинктера Одди относится эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ). Косвенными признаками повышения его тонуса являются увеличение диаметра холедоха более 12 мм и задержка контраста в холедохе свыше 45 мин. На дисфункцию сфинктера главного панкреатического протока указывает его расширение более 5 мм, а также замедление эвакуации контраста из протока.
Прямым методом, подтверждающим дисфункцию сфинктера, является манометрия. При проведении манометрии возможно раздельное канюлирование холедоха и вирсунгова протока с манометрией их сфинктеров. Это дает возможность выделить соответствующий тип расстройств, установить причину рецидивирующих панкреатитов после холецистэктомии и папиллотомии.
В то же время манометрическое исследование сфинктера Одди доступно не всем медицинским учреждениям, где проводится ЭРХПГ. Это стимулирует интерес к использованию неинвазивных методов исследования функции сфинктера Одди.
Для исключения органической патологии сфинктера Одди используется проба с гладкомышечным релаксантом. На наличие функциональных расстройств указывает снижение базального давления после введения релаксантов. В то же время манометрия сфинктера не всегда является информативной, что послужило поводом для разработки критериев, учитывающихся при выборе тактики лечения данного состояния.
Признаки дисфункции сфинктера Одди
Выделяют несколько вариантов дисфункции сфинктера Одди, что необходимо учитывать при выборе тактики ведения указанной категории больных.
При панкреатическом типе большое значение отводится двукратному повышению в сыворотке крови активности панкреатических ферментов в период двух последовательных приступов болей, а также расширению панкреатического протока более 5 мм.
Больным с первым вариантом дисфункции сфинктера Одди и высокой вероятностью развития стеноза (более 70 %) показана эндоскопическая сфинктеротомия без предварительного манометрического исследования, что способствует уменьшению частоты осложнений.
Больным со вторым вариантом показана медикаментозная терапия. При отсутствии эффекта необходимо проведение манометрического исследования.
У лиц с признаками дисфункции сфинктера Одди при третьем варианте причины болевого синдрома чаще обусловлены его дискинезией Манометрическое исследование сфинктера в данном случае не показано.
В диагностике патологии кишечника используются рентгенологическое исследование желудка, двенадцатиперстной и тонкой кишки, эндоскопическое исследование ЖКТ со взятием биоисийного материала слизистых.
Для подтверждения избыточного бактериального роста в кишечнике используются аспирация и посев содержимого кишечника, кала, исследование концентрации ионов водорода в выделяемом натощак воздухе, проведение дыхательных тестов с лактулозой или глюкозой. Наиболее простым и информативным тестом служит улучшение состояния больного после антибактериальной терапии.
Лечение Дисфункции сфинктера Одди (постхолецистэктомического синдрома):
Лечение ДСО. Терапия больных с дисфункцией сфинктера Одди направлена на нормализацию поступления желчи и панкреатического секрета из желчных и панкреатических протоков в двенадцатиперстную кишку путем коррекции химического состава желчи, проходимости сфинктера Одди, микроэкологии кишечника, моторики тонкой кишки и процессов пищеварения.
Лечение включает в себя:
Существенное место в лечении занимает диетотерапия. Основным принципом диеты является питание с частыми приемами небольших порций пищи (4х разовое питание) с последним приемом непосредственно перед сном, что способствует регулярному опорожнению желчных путей, устранению застоя желчи. Необходимы ограничение (но не полное исключение) продуктов, содержащих холестерин (жиры животного происхождения), жирные кислоты (жиры, прошедшие термическую обработку свыше 100 °С, жареные продукты), медленное снижение массы тела, добавление в пищевой рацион пищевых волокон в виде продуктов растительного происхождения или пищевых добавок (отруби). Овощи и фрукты лучше использовать после термической обработки. Необходимо стремиться к обеспечению ежедневного эффективного стула.
Для снятия спазма сфинктера Одди используются препараты, обладающие спазмолитическим эффектом. Препаратом выбора является дюспаталин по 200 мг 2 раза в день утром и вечером в течение 24 нед. Его антиспастическое действие обусловлено снижением проницаемости клеток гладкой мускулатуры для катионов натрия и замедлением процесса деполяризации, уменьшением оттока катионов калия, что предотвращает развитие гипотонии. У больных с ДСО монотерапия данным препаратом нормализует работу сфинктера Одди, приводит к снижению интенсивности или исчезновению болей, а также уменьшению явлений диспепсии.
Для лиц после холецистэктомии, с целью нормализации оттока желчи, наряду с проходимостью сфинктера Одди, важное значение имеет уровень давления в двенадцатиперстной кишке. В случае, если уровень давления превышает секреторное давление желчи и панкреатического сока, последние будут депонироваться в желчных и панкреатических протоках с соответствующими последствиями. Основным механизмом развития дуоденальной гипертензии является избыточное содержание жидкости и газа в результате бродильногнилостных процессов, обусловленных микробной контаминацией в просвете двенадцатиперстной кишки.
С целью деконтаминации двенадцатиперстной кишки проводятся один или два курса антибактериальной терапии со сменой препаратов. Антибактериальные препараты подбирают, как правило, эмпирически.
Препаратами выбора являются:
При наличии запоров принимают дюфалак по 12 ст. л. 1 раз в день для нормализации стула. В пребиотической дозе препарат оказывает избирательное действие на рост бифидо и лактобактерий.
Известно, что удаление желчного пузыря по поводу ЖКБ не избавляет больного от обменных нарушений, в том числе от печеночноклеточной дисхолии, определяющей литогенность желчи, в связи с чем целесообразно использование препаратов урсо и хенодезоксихолевой кислот на ночь.
При вовлечении в патологический процесс печени показаны гептрал, гепатофальк, LIV52 и др.
Отсутствие эффективности проводимых терапевтических мероприятий служит показанием к повторному оперативному вмешательству. Абсолютными показаниями к оперативному лечению являются:
Прогноз постхолецистэктомического синдрома благоприятен. При соблюдении правильной диеты, режима, проведения соответствующей медикаментозной терапии клинические проявления исчезают.
К каким докторам следует обращаться если у Вас Дисфункция сфинктера Одди (постхолецистэктомический синдром):
Место тримебутина в консервативной терапии дисфункции сфинктера Одди
Дисфункция сфинктера Одди может иметь как структурную (органическую), так и функциональную, связанную с нарушением двигательной активности сфинктера, природу. Согласно IV Римскому консенсусу по функциональным расстройствам органов пищеварения от 2016 года
Oddi’s sphincter dysfunction may have the nature both structural (organic), and functional connected with mobile activity disorders of the sphincter. According to IV Roman Consensus on functional disorders of digestive system 2016, the term «Oddi’s sphincter dysfunction» is recommended for use instead of the terms «postcholecystectomy syndrome», «biliary dyskinesia», etc. The approaches to treatment of Oddi’s sphincter disorders, without its anatomic changes, were considered.
Сфинктер Одди — это фиброзно-мышечный футляр, окружающий конечные участки общего желчного и панкреатического протоков и общий канал в месте их прохождения через стенку двенадцатиперстной кишки (ДПК). Гладкомышечные волокна сфинктера располагаются как продольно, так и циркулярно. Хотя сфинктер холедоха впервые описал Francis Glisson в 1681 г., он был назван по имени Ruggero Oddi, который опубликовал свои морфологические наблюдения о структуре сфинктера в 1887 г., будучи студентом университета Перуджи в Италии.
Сфинктер Одди состоит из трех сегментов (рис.):
Манометрические исследования показывают, что длина физиологической части сфинктера составляет примерно 8–10 мм и может быть меньше, чем его истинная анатомическая длина. СО выполняет три основные функции: 1) регулирует ток желчи (и панкреатического сока) в ДПК; 2) предотвращает рефлюкс содержимого ДПК в холедох и панкреатический проток; 3) обеспечивает накопление в желчном пузыре печеночной желчи. Эти функции обусловливают способность сфинктера регулировать градиент давления между системой протоков и ДПК. Координированная сократительная активность желчного пузыря и СО обеспечивает наполнение желчного пузыря в период между приемами пищи [3].
Основная функция СО — контроль за беспрепятственным поступлением желчи и панкреатического сока соответственно из холедоха и вирсунгова протока в ДПК во время нахождения в ней химуса, а также препятствие рефлюксу дуоденального содержимого в общий желчный и главный панкреатический протоки для предотвращения развития ферментативного холецистита и панкреатита [4].
Физиология СО изучалась как у животных, так и у людей. У людей базальное давление СО составляет 10 мм рт. ст. Антероградные фазовые сокращения возникают в месте соединения общего желчного протока (ОЖП) и СО при выходе в ДПК и происходят в ответ на физиологические и экзогенные раздражители, что приводит к эвакуации содержимого из СО в ДПК. Во время сжатия дополнительный поток от ОЖП в СО не происходит. Затем СО расслабляется, позволяя пассивно заполнять желчью проксимальный сегмент СО. После заполнения начинается другая волна фазовых сокращений [5, 6]. Когда базальное давление увеличивается, сопротивление потоку усиливается, что приводит к заполнению желчного пузыря и предотвращает попадание желчи в ДПК. Когда базальное давление становится ниже, чем в ОЖП, происходит расслабление СО, желчь и панкреатический секрет изливаются в ДПК. В межпищеварительный период активность СО имеет циклический характер, вызывая периодический выброс желчи и секрета поджелудочной железы в ДПК [7]. Активность СО в течение пищеварительного периода определяется как нервными, так и гормональными факторами. В этот период сокращения желчного пузыря, стимуляция секреции поджелудочной железы и релаксация СО приводят к высоким темпам выделения желчи и секрета поджелудочной железы в ДПК. Следует отметить, что в течение пищеварительного периода существуют разные пищевые фазы, каждая из которых обеспечивает стимуляцию СО. Например, до 30–40% опорожнения желчного пузыря и 25% секреции поджелудочной железы происходит во время основной дуоденальной фазы, в то время как 10–20% секреции происходит во время желудочной фазы пищеварения. Однако желчный пузырь «выбрасывает» большую часть содержимого и поджелудочная железа до 50% ее секрета во время кишечной фазы, вызванной высвобождением холецистокинина (ХЦК) и секретина из ДПК и проксимальных отделов тощей кишки. Дуоденальный ХЦК вызывает сокращение желчного пузыря, расслабляет СО и вызывает секрецию экзокринных пищеварительных ферментов поджелудочной железы посредством прямого воздействия на ХЦК-рецепторы и косвенно через холинергические нейроны. Это подтверждается при введении атропина, который блокирует сокращение желчного пузыря и подавляет панкреатическую секрецию, вызванные физиологическими концентрациями ХЦК и приемом жирной еды [8, 9].
Наиболее важным гормоном, определяющим функцию СО, является ХЦК. ХЦК продуцируется энтероэндокринными клетками в ответ на еду, оказывает прямое гормональное действие, а также косвенные эффекты, взаимодействуя с нейронными путями, что приводит к сокращению желчного пузыря и секреции поджелудочной железы. ХЦК уменьшает базовое давление СО и ингибирует фазовые сокращения, тем самым стимулируя антероградную перистальтику [10]. Вазоактивный кишечный полипептид и оксид азота присутствуют в собственных нейронах СО, участвуют в релаксационном ответе на ХЦК, а также в релаксации, наблюдаемой в основной фазе пищеварения [11].
Мотилин, соматостатин и октреотид оказывают гормональное влияние на функцию СО. Мотилин, секретируемый М-клетками в двенадцатиперстной и тощей кишке, вызывает сокращение гладкой мускулатуры желчного пузыря и стимулирует секрецию желчи [12]. Соматостатин, присутствующий в эндокринных клетках по всему желудочно-кишечному тракту, может оказывать ингибирующее действие как на сокращение желчного пузыря, так и на релаксацию СО [13], что подтверждается наблюдением, в котором 50 мкг внутривенного октреотида, аналога соматостатина, вызывает значительное увеличение базального давления и частоту фазовых сокращений СО [14].
Дисфункция сфинктера Одди — это клинический синдром, вызванный нарушением дискинезии (функциональной) или анатомической (механической) обструкции, связанный с абдоминальной болью и «уклонением в кровь» ферментов печени или поджелудочной железы, расширением ОЖП или панкреатического протока или формированием панкреатита [15]. Следует отметить, что термин «дискинезия» более конкретно обозначает нарушения моторики СО, тогда как ДСО включает как механическую обструкцию, так и дискинезию СО. В этом контексте термин «желчная дискинезия» исторически использовался в качестве общего термина, который включал как дискинезию СО, так и дискинезию желчного пузыря [16]. Поскольку сегодня доступны сцинтиграфия и магнитно-резонансная холангиопанкреатография (МРХПГ), функциональное расстройство желчного пузыря (то есть дискинезия/дисфункция желчного пузыря) теперь признается дискретной сущностью и его следует отличать от дискинезии СО [17–19]. Различные формы первичной ДСО рассматриваются как функциональные расстройства желудочно-кишечного тракта и могут возникать у взрослых и детей любого возраста, но чаще ДСО встречается у женщин в возрасте 20–50 лет [20–22]. ДСО часто начинается в среднем через 4–5 лет после холецистэктомии, которая обычно проводится по поводу желчнокаменной болезни [23]. Распространенность ДСО составляет 1,5% от общей популяции, но может быть столь же высокой, как, например, у 72% пациентов с идиопатическим рецидивирующим панкреатитом, выявленных в небольших когортных исследованиях [24–26]. Однако его истинную распространенность трудно определить из-за отсутствия достоверных биомаркеров или диагностических критериев, а также множества вторичных причин ДСО, таких как фиброз сфинктерного канала (папиллярный стеноз и склерозирующий папиллит) или обструктивная карцинома.
Клинически ДСО может протекать по билиарному, панкреатическому или смешанному вариантам [27]. Билиарный тип ДСО обычно представляет собой рецидивирующую билиарную боль, характеризующуюся локализацией в эпигастрии или правом верхнем квадранте живота, длительностью от 30 минут до нескольких часов, с повышением печеночных ферментов или без их уклонения. Боль может иррадиировать в спину, плечо или лопатку, может сопровождаться тошнотой и рвотой, т. е. имитировать желчную колику. Боль не является постпрандиальной и не облегчается постуральными изменениями, приемом антацидов или после дефекации [28].
Предполагается, что поджелудочная ДСО ответственна у части пациентов с рецидивирующими эпизодами острого панкреатита. Пациенты жалуются на боль в животе, в проекции поджелудочной железы, иррадиирующую в спину, которая сопровождается повышением уровня амилазы и липазы в сыворотке крови. Симптомы, связанные с панкреатической ДСО, часто усугубляются приемом пищи. У этих пациентов обычно нет других этиологических факторов панкреатита, и им часто выставляется диагноз идиопатического острого рецидивирующего панкреатита (ИОРП) [29, 30]. J. Toouli и его коллеги сравнили манометрическое давление в СО у 28 пациентов с ИОРП с 10 здоровыми людьми и обнаружили, что более 57% пациентов с ИОРП имеют повышенное давление в СО [31]. Однако истинная частота панкреатита, вызванного ДСО, неизвестна. Когда в патологический процесс вовлекаются как поджелудочная часть, так и желчная часть сфинктера, боль в животе будет более диффузной и может произойти как повышение уровня печеночных ферментов, так и ферментов поджелудочной железы в сыворотке крови.
Диагноз ДСО является сложной задачей, важны физикальный осмотр, соответствующие лабораторные и инструментальные данные. Иногда ДСО является структурной аномалией, в других случаях — это функциональное расстройство. Система классификации ДСО как структурной аномалии была разработана в 1988 г. Изначально известная как классификация ДСО Hogan-Geenan, позднее модифицированная как классификация Milwaukee, она подразделяет ДСО на 1-й, 2-й и 3-й типы на основе клинических проявлений, а также лабораторных и/или визуализационных отклонений [16, 19]. IV Римские критерии рассматривают ДСО как функциональное расстройство и подразделяют ее на функциональное расстройство билиарного сфинктера Одди (Е1b) и функциональное расстройство панкреатического сфинктера Одди (Е2) [32]. Эти критерии предназначены для того, чтобы сделать диагностическую оценку более применимой к клинической практике и, по возможности, избегать инвазивных процедур. Ряд исследований продемонстрировал более высокие показатели депрессии, обсессивно-компульсивные расстройства и тревогу у пациентов с ДСО по сравнению со здоровыми людьми [33].
К неинвазивному тестированию для диагностики ДСО относятся количественная гепатобилиарная сцинтиграфия с целью оценки динамического состояния билиарного тракта [34], эндоУЗИ и МРХПГ с секретином [35]. Однако эти тесты не чувствительны и не специфичны для ДСО. Манометрия СО считается «золотым стандартом» для диагностики ДСО, но это утверждение до сих пор остается спорным [36, 37]. Кроме того, изолированное базальное давление не может дифференцировать функциональные нарушения СО и анатомический стеноз [38].
Ряд пациентов, например, перенесшие холецистэктомию [22], предрасположены к ДСО [21]. У людей с нормальным желчным пузырем ХЦК ингибирует активность СО-фазной волны, но даже через 6 месяцев после холецистэктомии ХЦК не может ингибировать эту активность [39]. S. Sherman сообщил, что у 10–20% пациентов после холецистэктомии наблюдается желчная колика, а 9–51% этих пациентов с болевым синдромом соответствуют диагностическим критериям ДСО после холецистэктомии [21]. W. Luman и коллеги продемонстрировали, что у пациентов с постхолецистэктомическим синдромом повышено базальное давление СО, а также увеличено ретроградное сокращение фазических волн и частота фазовых волн (таходдия) [40].
Дисфункция сфинктера Одди также связана с гипо- и акинезией желчного пузыря [41], предоперационным холелитиазом [15], литотрипсией желчного пузыря [42], трансплантацией печени [43] и алкоголизмом [44]. Нарушение опорожнения желчного пузыря, связанное с гипотиреозом, предполагает другой фактор риска для ДСО [45]. Кроме того, пациенты с гипотиреозом имеют повышенный риск развития желчных камней, что является вторичным по отношению к отсутствию расслабляющего эффекта тироксина на СО [46].
Пациенты с синдромом раздраженного кишечника (СРК) имеют повышенный риск формирования ДСО. P. R. Evans и его коллеги сообщили, что пациенты с СРК после холецистэктомии более склонны демонстрировать сниженный ответ на расслабляющие сфинктерные свойства ХЦК по сравнению с пациентами после холецистэктомии без СРК [47]. Распространенность и заболеваемость ДСО среди пациентов с СРК неясны из-за трудности диагностики ДСО у пациентов с СРК из-за совпадения симптомов [48].
Экзогенные агенты играют аддитивную роль у пациентов, подверженных риску развития ДСО. Например, лоперамид ингибирует нормальный сократительный ответ желчного пузыря на ХЦК [49], а у пациентов с синдромом короткой кишки уменьшает панкреатический и желчный выброс [50].
Наиболее часто используемым немедикаментозным лечением ДСО является эндоскопическая сфинктеротомия для пациентов с ДСО 1-го и 2-го панкреатического типа по Milwaukee. Уменьшение боли было достигнуто у 90% пациентов с ДСО 1-го типа и 70% пациентов со 2-м типом. Однако она не эффективна и может даже ухудшать качество жизни у пациентов с 3-м типом — функциональным спазмом. Это было многоцентровое, контролируемое рандомизированное исследование у пациентов с болью после холецистэктомии, без аномалий при визуализации или лабораторных исследованиях. Участникам исследования была выполнена сфинктеротомия или фиктивная сфинктеротомия при боли в животе. Исследователи пришли к выводу, что выполнение сфинктеротомии у пациентов с ДСО 3-го типа неэффективно [51]. В результате эндоскописты воздерживаются от выполнения сфинктеротомии у этих пациентов.
Имеются ограниченные исследования, оценивающие роль стентирования панкреатического протока и сфинктеротомии у пациентов с ДСО поджелудочного типа. L. Jacob и его коллеги обнаружили значительное снижение частоты рецидивирующего острого панкреатита у стентированных пациентов [52]. Coté и соавт. оценили роль эндоскопической двойной (билиарной и поджелудочной) сфинктеротомии против билиарной сфинктеротомии только у пациентов с ИОРП и обнаружили, что оба типа сфинктеротомий имели сходные эффекты в предотвращении рецидивов острого панкреатита [53]. В другом исследовании не было обнаружено различий в предотвращении рецидивирующего панкреатита, когда двойная сфинктеротомия сравнивалась с панкреатической или билиарной сфинктеротомией [54].
Ряд препаратов расслабляют СО, уменьшая его давление и сопротивление. Это — блокаторы кальциевых каналов [55, 56], трициклические антидепрессанты [57], ботокс, глицерилтринитрат (ГТН) и соматостатин. S. Santhosh и соавт. показали, что нифедипин снимал спазм СО [58], вызванный опиатами, и уменьшал боль, связанную с ДСО, в краткосрочном исследовании. Инъекция ботокса в СО снижала давление сфинктера на 50% в течение 4 месяцев и сопровождалась 50%-м улучшением оттока желчи у пациентов с болью после холецистэктомии и повышенным давлением в СО [59]. ГТН использовался для облегчения удаления камней из холедоха без эндоскопической папиллярной дилатации или эндоскопической папиллотомии и уменьшал как основное давление в СО, так и амплитуду и частоту сокращений СО-фазы в нерандомизированном контролируемом клиническом исследовании [60]. G. Brandstätter и соавт. показали, что внутривенное введение соматостатина снижает среднее давление в СО [61] у пациентов с острым алкогольным панкреатитом.
Большой интерес терапевтического воздействия на СО представляет тримебутин. Модулирующее влияние тримебутина на моторику желудочно-кишечного тракта (ЖКТ) и его обезболивающий эффект предполагают его использование при различных функциональных нарушениях ЖКТ, в том числе на СО как при терапевтической, так и хирургической патологии. Тримебутин (Дебридат, Модулон) много лет, начиная с 1969 г., применяется во многих странах для лечения функциональных расстройств кишечника, в основном при СРК [62]. Тримебутин является агонистом периферических опиатных рецепторов — µ, κ и δ. В ЖКТ найдены все три типа опиатных рецепторов, при этом они расположены как на гладкомышечных клетках ЖКТ, так и в энтеральной нервной системе (ЭНС). В гладкомышечной ткани опиатные рецепторы присутствуют в циркулярном слое гладких мышц [63]. В ЭНС опиатные рецепторы расположены на ганглионарных клетках миоэнтерального и подслизистого сплетений тонкой кишки и на интрамуральных нервных волокнах [64, 65]. Тримебутин также обладает антисеротониновой активностью, особенно в отношении µ-рецепторов, способствует высвобождению мотилина и других гастроинтестинальных пептидов — вазоактивного интестинального пептида, гастрина и глюкагона [66].
Авторы IV Римских критериев с учетом высокого риска осложнений инвазивных вмешательств при функциональном билиарном расстройстве сфинктера Одди большое значение определили консервативным лечебным мероприятиям. Среди препаратов, снижающих давление в СО, представлен и тримебутин, как доказавший свою эффективность при данной патологии в ряде исследований. Достоверно показано, что лечение тримебутином позволило избежать сфинктеротомии у 77% пациентов [67].
Очень показательным стало исследование Barthet и соавт., в котором оценивалось влияние тримебутина (внутривенная инъекция 50 мг) у 15 пациентов после холецистэктомии на подвижность сфинктера Oдди с помощью эндоскопической манометрии. Инъекции тримебутина привели к значительному увеличению фазовой скорости антеградных сокращений СО (p = 0,02), уменьшилось основное давление в СО (32,5 против 27,5 мм рт. ст.). Эффекты тримебутина различались в зависимости от основных аномалий подвижности СО, но латентный период был сходным (среднее значение 89 с, диапазон 30–240 с). Основными терапевтическими целями были — увеличение базального давления SO > 40 мм рт. ст. у трех пациентов, таходдия (частота фазовых сокращений (ФС) > 10/мин) у шести пациентов, длительность ФС (> 10 с) у двух пациентов и отсутствие ФС у одного пациента. На фоне лечения тримебутином базовое давление СО уменьшилось у трех пациентов с гиперчувствительностью СО, а в одном случае полностью нормализовалось. Частота ФС снизилась до нормы у трех из шести пациентов с таходдией. Продолжительность ФС нормализовалась у двух пациентов с длительными ФС, тогда как их частота увеличивалась. Таким образом, данное исследование продемонстрировало, что тримебутин модулирует двигательную активность СО различными способами в зависимости от аномалии базальной подвижности СО, наблюдаемой после холецистэктомии [68].
В исследовании V. Vitton и соавт. [69] показали, что прием тримебутина может значительно уменьшить боль у пациентов, страдающих ДСО, и уменьшает потребность в эндоскопической сфинктеротомии (ЭС). Цель другого исследования этих авторов состояла в том, чтобы определить эффективность консервативной терапии в снятии симптомов ДСО по сравнению с ЭС после продолжительного периода наблюдения. Это исследование подтвердило, что консервативное лечение может быть альтернативой ЭС, потому что после промежуточного периода наблюдения оба медицинских пособия показывают одинаковые показатели успеха [70].
ФГБОУ ВО КемГМУ МЗ РФ, Кемерово
Место тримебутина в консервативной терапии дисфункции сфинктера Одди/ Е. Ю. Плотникова, Т. Ю. Грачева
Для цитирования: Лечащий врач № 2/2018; Номера страниц в выпуске: 47-52
Теги: кишечник, перистальтика, нарушение проходимости протоков желчи
.gif)