Аберрантная поджелудочная железа что делать
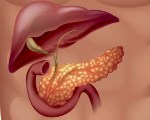
Аберрантная поджелудочная железа — это гетеротопия панкреатической железистой ткани в стенке желудка, кишечника или других органах брюшной полости. Аномалия характеризуется скудными клиническими проявлениями с преобладанием диспепсических расстройств. Осложненные формы патологии манифестируют симптомокомплексом «острого живота», желудочно-кишечными геморрагиями. Диагностика основана на инструментальных методах: УЗИ, рентгенографии с пероральным контрастированием, ЭФГДС. Диагноз подтверждают патоморфологическим исследованием биоматериала. Бессимптомные аномалии лечения не требуют, при осложнениях в основном прибегают к хирургическим вмешательствам.
МКБ-10
Общие сведения
В медицинской литературе аномалия имеет ряд синонимов: добавочная поджелудочная железа, хористома, эктопия ПЖ. Заболевание является самым частым пороком развития поджелудочной железы и выявляется у 0,2% пациентов в ходе оперативных вмешательств на органах брюшной полости. По данным аутопсий, гетеротопия встречается у 1,3% людей в популяции. Аномалия в 2 раза чаще наблюдается у мужчин. Преимущественно она обнаруживается случайно в возрасте 40-70 лет при инструментальном обследовании пищеварительной системы.
Причины
В современной гастроэнтерологии не существует единого мнения по поводу этиологических факторов. Большинство ученых утверждают, что патология возникает во внутриутробном периоде при сочетанном влиянии нескольких причин. К наиболее вероятным из них относят спонтанные генетические мутации, инфекции, перенесенные матерью во время беременности. Реже определяется связь аберрантной поджелудочной железы с приемом лекарств, обладающих тератогенным эффектом.
К факторам риска развития хористомы относят курение, употребление алкоголя и наркотических веществ беременной женщиной. Вероятность появления болезни увеличивается при проживании в экологически неблагоприятных регионах, воздействии ионизирующего излучения на ребенка в эмбриональном периоде внутриутробного развития. Риск формирования аберрантной ткани повышается при генетической предрасположенности — наличии различных аномалий у ближайших родственников.
Патогенез
Точный механизм образования аномалии до сих пор остается неясным. Наиболее вероятно, что аберрантная ткань — проявление атавизма в онтогенезе. Нарушение закладки и дифференцировки поджелудочной железы при антенатальном развитии приводит к аномальному расположению части органа. Сформированная добавочная железа имеет изолированное кровоснабжение и иннервацию, функционирует независимо от основной массы железистых клеток.
Классификация
Хористомы различаются по анатомической локализации. Аберрантная ткань железы может располагаться в различных органах:
Среди желудочных аберрантных ПЖ большинство (58,2%) располагается в привратнике. По макроскопическим признакам выделяют 4 формы: узловатую, полипозную, диффузную и смешанную.
Симптомы
Подавляющее большинство гетеротопий протекает бессимптомно и выявляется случайно при гастроэнтерологической диагностике, проведении операций в полости живота. Симптоматика обычно возникает при осложненном течении заболевания и определяется локализацией аберрантной поджелудочной железы. Начальными признаками являются неспецифические диспепсические расстройства: тяжесть в животе после приема пищи, тошнота, неустойчивость стула.
Клиническое проявление крупной аберрантной железы возможно уже в раннем детском возрасте. Беспокоит срыгивание после еды, периодически бывает обильная рвота створоженным молоком или частично переваренной пищей. Дети плохо едят, медленно набирают вес, отстают в физическом развитии. Во взрослом возрасте аномалия, как правило, протекает под маской хронического гастрита, панкреатита, холецистита.
Типичный симптом осложненных форм патологии — сильные боли в животе различной локализации. Часто встречается рвота с примесями слизи и желчи. При поражении желчевыводящих протоков выделяется обесцвеченный кал. Редко аберрантная поджелудочная железа манифестирует желудочно-кишечным кровотечением, которое проявляется кровавой рвотой или меленой.
Осложнения
Зачастую при хористоме наблюдается стеноз пилорического отдела желудка, что затрудняет продвижение пищи в тонкий кишечник. В компенсированной стадии питание и энергетический обмен практически не нарушены. На этапе декомпенсации характерны истощение больных, анемия и признаки авитаминозов. При расположении аберрантной ткани в тонком кишечнике существует вероятность развития острой кишечной непроходимости, требующей неотложной хирургической помощи.
Добавочные поджелудочные железы часто подвергаются воспалению и некрозу. Начинается асептическое либо гнойное поражение аберрантной ткани, которое чревато прободением стенки пораженного органа. При расплавлении сосудистых стенок может открыться профузное кровотечение. Наличие гетеротопии повышает риск возникновения язвенной болезни, механической желтухи. Наиболее опасное последствие вовремя не диагностированной хористомы — малигнизация.
Диагностика
Выявление аберрантной железистой ткани стандартными методами исследования затруднительно, поскольку внешне аномальные образования напоминают доброкачественную опухоль. Для верификации диагноза врач-гастроэнтеролог назначает инвазивные методики с последующим гистологическим подтверждением. При подозрении на гетеротопию поджелудочной железы диагностический поиск включает следующие исследования:
Лечение аберрантной поджелудочной железы
Консервативная терапия
В гастроэнтерологии есть успешный опыт применения аналогов гормона соматостатина. Эти препараты тормозят пролиферацию железистых клеток, препятствуют трансформации доброкачественной гетеротопии в опухолевый процесс. При недостаточной экзокринной функции поджелудочной ткани назначают заместительную ферментную терапию. Для устранения неприятных симптомов используют анальгетики, желчегонные препараты, прокинетики.
Хирургическое лечение
В абдоминальной хирургии целесообразность оперативного вмешательства при аберрантной поджелудочной железе остается предметом научных дискуссий. При бессимптомном течении и нормальном функционировании органа с железистой геторотопией больным требуется наблюдение. Возможность проведения операции решается индивидуально для пациентов со сниженной функциональной активностью основной ПЖ.
Абсолютными показаниями к выполнению радикального лечения считают осложненные варианты аберрантной аномалии. Рекомендована максимально экономная резекция в пределах здоровых тканей. При формировании стеноза привратника или кишечника обеспечивается хирургическая коррекция, при необходимости накладывается анастомоз. Обязательному удалению подлежат хористомы с высоким риском малигнизации.
Прогноз и профилактика
Бессимптомные формы аберрантной ПЖ не представляют риска для здоровья и жизни человека, в таком случае прогноз считается благоприятным. Прогностически неблагоприятно расценивается появление осложнений со стороны желудка, кишечника, билиарной системы, быстрое увеличение размеров добавочной железы. Учитывая неясный этиопатогенез, специфические меры первичной профилактики не разработаны.
Острая тонкокишечная непроходимость, вызванная эктопированным участком поджелудочной железы. Клинический случай
Полный текст:
Аннотация
Введение. Эктопия поджелудочной железы — это аномалия, связанная с необычным расположением панкреатической ткани с собственным кровоснабжением и протоками. Она не имеет анатомического, сосудистого и нервного контакта с нормально расположенной поджелудочной железой. Добавочная поджелудочная железа (ПЖ), самый частый порок развития железы, который заключен в гетеротопии ее ткани в стенку желудка, кишечника, желчного пузыря, дивертикул Меккеля, печень, селезенку и, значительно реже, в другие органы без связи с основной поджелудочной железой. В настоящее время частота встречаемости гетеротопии поджелудочной железы значительно увеличилась и составляет в среднем до 0,2 % при оперативных вмешательствах на органах брюшной полости и 0,5–13 % случаев при аутопсиях. Наиболее часто аберрантная ПЖ локализована в гастродуоденальной зоне (63–70 % от всех случаев гетеротопии ПЖ) с преимущественным расположением в антральном и пилорическом отделах желудка (85–95 % от всех случаев гетеротопии ПЖ в желудке).
Материалы и методы. В статье представлен клинический пример успешного лечения 39-летнего мужчины с острой тонкокишечной непроходимостью, вызванной эктопированной тканью поджелудочной железы в стенку тонкой кишки. Пациенту была выполнена диагностическая лапароскопия, произведена средне-срединная лапаротомия с клиновидной резекцией тонкой кишки.
Результаты. Послеоперационный период гладкий, больной выписан на девятые сутки после хирургического вмешательства после снятия кожных швов. По результатам гистологического исследования: фрагмент тонкой кишки и полиповидное образование, представленное гетеротопированными участками поджелудочной железы, состоящими из ацинусов и проток, располагающихся между мышечными тяжами, с обширными кровоизлияниями и некрозами.
Заключение. Диагностика эктопированной ткани поджелудочной железы в тонкую кишку является крайне сложной проблемой в абдоминальной хирургии и выявляется в большинстве случаев при развитии осложнений. Для окончательной диагностики данного заболевания имеет огромное значение патоморфологическая верификация, которая позволяет правильно пределить причину и механизм развития острого хирургического заболевания
Ключевые слова
Для цитирования:
Хасанов А.Г., Суфияров И.Ф., Бакиров Э.Р., Нуртдинов М.А., Ибраев А.В., Евдокимов Е.В. Острая тонкокишечная непроходимость, вызванная эктопированным участком поджелудочной железы. Клинический случай. Креативная хирургия и онкология. 2019;9(1):75-79. https://doi.org/10.24060/2076-3093-2019-9-1-75-79
For citation:
Khasanov A.G., Sufiyarov I.F., Bakirov E.R., Nurtdinov M.A., Ibraev A.V., Evdokimov E.V. Acute Small Intestinal Obstruction Caused by Ectopic Pancreas. A Clinical Case Report. Creative surgery and oncology. 2019;9(1):75-79. (In Russ.) https://doi.org/10.24060/2076-3093-2019-9-1-75-79
Введение
Эктопия поджелудочной железы — это аномалия, связанная с необычным расположением панкреатической ткани с собственным кровоснабжением и протоками. Она не имеет анатомического, сосудистого и нервного контакта с нормально расположенной поджелудочной железой [1]. Добавочная (аберрантная) поджелудочная железа (ПЖ) — самый частый порок развития железы, который заключен в гетеротопии ее ткани в стенку желудка, кишечника, желчного пузыря, дивертикул Мек- келя, печень, селезенку и, значительно реже, в другие органы без связи с основной поджелудочной железой [2, 3]. Аберрантная ПЖ по своим проявлениям неспецифична, в значительной степени клиническая картина зависит от локализации и размера гетеротопии и чаще всего появляется при развитии осложнений, к которым относят воспаление, некроз, перфорацию желудочной или кишечной стенки, кровотечение, кишечную непроходимость — которую мы хотим представить в виде клинического примера.
Рисунок 1. Обзорная рентгенография органов брюшной полости — картина острой тонкокишечной непроходимости
Figure 1. Plain abdominal X-ray presenting acute small intestinal obstruction
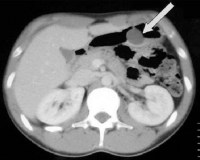
Рисунок 2. Ультразвуковая картина инвагинации кишечника
Figure 2. Intestinal intussusception, ultrasound imaging
Клинический случай
Описан случай острой тонкокишечной непроходимости, вызванной эктопированной тканью поджелудочной железы в стенку тонкой кишки.
Больной Б., 39 лет, доставлен скорой помощью в приемное отделение хирургии ГКБ № 13 г. Уфы с жалобами на приступообразные боли в животе, тошноту, однократную рвоту, вздутие живота, слабость. Заболел около 4-х часов назад, когда появился сначала дискомфорт в животе, в области эпигастрия. В динамике боли в животе усилились, начали носить приступообразный характер. Принимал лекарственные препараты из группы нестероидных противовоспалительных средств. До госпитализации обращался в частную клинику, где периодически обследовался и находился на амбулаторном лечении в течение 4-х месяцев, и был направлен на скорой помощи в ГКБ № 13 с направительным диагнозом «Перфоративная язва двенадцатиперстной кишки», так как в анамнезе у больного отмечалась язвенная болезнь двенадцатиперстной кишки.
При осмотре — состояние средней тяжести. Кожные покровы, видимые слизистые чистые, бледноватой окраски. Язык суховат, обложен серым налетом. Живот умеренно вздут, при пальпации мягкий, болезненный преимущественно в нижних отделах живота. Симптомов раздражения брюшины нет. Перистальтика кишечника усилена. Печень у края реберной дуги. Печеночная тупость сохранена. Стул самостоятельный жидкий, накануне, естественной окраски. Газы не отходили. Мочеиспускание не нарушено. Per rectum: сфинктер в тонусе. Ампула прямой кишки пустая. Патологических образований на высоте пальца не определяется. На перчатке следы кала естественной окраски.
Больной обследован в приемном отделении: ОАК: эр. 4,2х10 12 /л, Hb 128 г/л, Ht 37,3 %, тр. 221,0х10 9 /л, Л 8,3х10 9 /л; биохимический анализ крови: общий белок 57,0 г/л, мочевина 2,8 ммоль/л, креатинин 69,3 ммоль/л, билирубин общий 8,0 мкмоль/л, глюкоза 10,5 ммоль/л, АЛТ 8,6 Е/л, АСТ 16,8 Е/л.
Обзорная рентгенография органов брюшной полости показала чаши Клойбера, арки, преимущественное расположение — левые отделы брюшной полости (рис. 1). На УЗИ ОБП — картина инвагинации кишечника на фоне выраженного пневматоза и гиперперистальтики, на левой половине правого рисунка — поперечная проекция инвагинации, так называемый «бутон розы» (рис. 2).
Принято решение о диагностической лапароскопии.
На лапароскопии — в брюшной полости серозный выпот до 40 мл, вздутые петли тонкой кишки, при ревизии обнаружен тонко-тонкокишечный инвагинат (рис. 3). Учитывая опасность повреждения стенки тонкой кишки, выполнена конверсия.
Рисунок 3. Диагностическая лапароскопия. Тонкокишечный инвагинат
Figure 3. Diagnostic laparoscopy, small intestine intussusceptum
Рисунок 4. Фрагмент тонкой кишки и полиповидное образование, представленное гетеротопиро- ванными участками поджелудочной железы, состоящими из ацинусов и протоков, располагающихся между мышечными тяжами, с обширными кровоизлияниями и некрозами. Слева ацинусы и протоки поджелудочной железы, справа — эпителий тонкой кишки. Окраска по Ван-Гизону
Figure 4. Small intestinal fragment with the polyp-like neoplasm: heterotypic pancreatic foci (with acini and ducts) located between muscular bands, with extensive areas of haemorrhaging and necrosis. On the left — pancreatic acini and ducts, on the right — small intestine epithelium
Произведена средне-срединная лапаротомия, в тонкой кишке на расстоянии 240 см от связки Трейтца определяется инвагинат. С техническими трудностями произведена дезинвагинация. При ревизии тонкой кишки, вовлеченной в инвагинацию, перистальтика и пульсация прослеживаются, кишка признана жизнеспособной. В просвете данного участка тонкой кишки пальпируется округлой формы образование размерами 6,0х1,5х1,5 см, которое внешне напоминает дивертикул Меккеля, инвагинированный в просвет кишки.
Произведена клиновидная резекция тонкой кишки с данным образованием, с ушиванием просвета кишки двухрядным узловым швом. Данное образование и вызвало непроходимость тонкой кишки, явившееся этаким «грузилом», запустившим механизм инвагинации.
Результаты
Послеоперационный период гладкий, больной выписан на девятые сутки после хирургического вмешательства после снятия кожных швов.
Нас удивил результат патоморфологического исследования материала. В материале — фрагмент тонкой кишки и полиповидное образование, представленное гете- ротопированными участками поджелудочной железы, состоящими из ацинусов и протоков, располагающихся между мышечными тяжами, с обширными кровоизлияниями и некрозами.
Таким образом, можно говорить о развитии панкреатита добавочной поджелудочной железы в течение нескольких месяцев, обструкция выводных протоков которой вызвала отек и воспаление, что, в свою очередь, запустило механизм инвагинации тонкой кишки.
При контрольном осмотре через два месяца — жалоб не предъявляет, самочувствие у больного хорошее, дискомфорт, периодические боли в животе, беспокоившие его несколько месяцев до поступления в стационар, купировались. Послеоперационный рубец в удовлетворительном состоянии. На УЗИ органов брюшной полости без значимой патологии. Уровень глюкозы крови в пределах нормы.
Ближайшие результаты проведенного лечения оцениваются как хорошие.
Обсуждение
Впервые описание дополнительной поджелудочной железы предоставил Шульц (1727), который обнаружил ее в дивертикуле Меккеля.
Существуют описания ассоциации аберрантной ПЖ, локализующейся в дивертикуле Меккеля, в сочетании с болезнью Крона, при этом эктопированная железа не проявлялась какими-либо самостоятельными симптомами. Вероятно, данную связь следует признать случайной, по крайней мере в настоящее время. При воспалении аберрантной ПЖ, локализующейся в дивертикуле Меккеля [4, 5], клиническая картина может имитировать острый аппендицит [6].
Первое гистологическое описание гетеротопии поджелудочной железы принадлежит J. Klob в 1859 г. К 1927 г. было описано 60 случаев добавочной поджелудочной железы. В последующие 20 лет — еще 415. В отечественной и зарубежной литературе к 1960 г. было описано 724 случая хористом.
Учитывая морфологическую картину, различают четыре варианта эктопии ПЖ:
В настоящее время частота встречаемости гетеротопии поджелудочной железы значительно увеличилась и составляет в среднем до 0,2 % при оперативных вмешательствах на органах брюшной полости и 0,5-13 % случаев при аутопсиях.
Такой существенный разброс статистических данных объясняют особенностями исследования секционного материала в разных прозектурах. Аберрантную ПЖ примерно вдвое чаще встречают у мужчин, чем у женщин. Наиболее часто аберрантная ПЖ локализована в гастродуоденальной зоне (63-70 % от всех случаев гете- ротопии ПЖ) с преимущественным расположением в антральном и пилорическом отделах желудка (85-95 % всех случаев гетеротопии ПЖ в желудке) [7, 8]. В желудке аберрантная ПЖ чаще находится в подслизистом слое, ограничиваемая мышечной оболочкой, реже располагается субсерозно). В двенадцатиперстной и тощей кишке аберрантную железу встречают сравнительно реже: 9-36 % и 0,5-27 % случаев соответственно [9, 10]. Остальные локализации эктопии ПЖ: в стенку желчного пузыря, печень и внепеченочные желчные протоки, селезенку, дивертикул Меккеля обнаруживают не часто [11]. Достаточно редкой локализацией аберрантной ПЖ считают субсерозное расположение в тонкой кишке [12, 13], в стенке кисты ДПК, пищеводе. В исключительных случаях встречают гетеротопию ПЖ в легочную ткань, пупок и корень языка [14, 15].
Следует отметить, что при локализации в тонкой кишке бессимптомно протекает менее половины случаев, поскольку осложнения возникают несколько чаще [1].
Заключение
Диагностика эктопированной ткани поджелудочной железы в тонкую кишку является крайне сложной проблемой в абдоминальной хирургии и выявляется в большинстве случаев при развитии осложнений. Для окончательной диагностики данного заболевания имеет огромное значение патоморфологическая верификация, которая позволяет правильно определить причину и механизм развития острого хирургического заболевания. В нашем случае можно предположить, что своевременное хирургическое вмешательство у данного больного предупредило развитие возможных последующих осложнений эктопированной ткани поджелудочной железы в стенку тонкой кишки, таких как малигнизация, кишечное кровотечение, перфорация стенки кишки и перитонит.
Список литературы
1. Marques J., Castro J., Oliveira H. Ectopic pancreas: a less common presentation. Rev Portug Cir. 2015;(34):43.
2. Jang K.M., Kim S.H., Park H.J., Lim S., Kang T.W., Lee S.J., et al. Ectopic pancreas in upper gastrointestinal tract: MRI findings with emphasis on differentiation from submucosal tumor. Acta Radiol. 2013;54(10):1107–16. DOI: 10.1177/0284185113491251
3. Litchinko A., Cherbanyk F., Rosskopfova P., Blant S.A., Macedo O. Jejunal mucinous cystadenoma in ectopic pancreatic tissue: a first observation. J Gastrointest Liver Dis. 2017;26(3):223. DOI: 10.15403/jgld.2014.1121.263.ltk
4. Juricic M., Djagbare D.Y., Carmassi M., Panait N., Faure A., NDour O., et al. Heterotopic pancreas without Meckel’s diverticulum in children as unique cause of gastrointestinal bleeding: think about it! Surg Radiol Anat. 2018;40(8):963–5. DOI: 10.1007/s00276-018-2042-0
5. Kim S.W., Kim H.C., Yang D.M., Kim G.Y., Choi S.I. MDCT findings of a Meckel’s diverticulum with ectopic pancreatic tissue. Clin Imaging. 2014;38(1):70–2. DOI: 10.1016/j.clinimag.2013.09.004
6. Shiratori H., Nishikawa T., Shintani Y., Murono K., Sasaki K., Yasuda K., et al. Perforation of jejunal diverticulum with ectopic pancreas. Clin J Gastroenterol. 2017;10(2):137–41. DOI: 10.1007/s12328-017-0712-9
7. Li W.W., van Boven W.J., Jurhill R.R., Bonta P.I., Annema J.T., de Mol B.A. Ectopic pancreas in a giant mediastinal cyst. Clin Respir J. 2016;10(1):125–8. DOI: 10.1111/crj.12176
8. Vitiello G.A., Cavnar M.J., Hajdu C., Khaykis I., Newman E., Melis M., et al. Minimally invasive management of ectopic pancreas. J Laparoendoscop Adv Surg Tech A. 2017;27(3):277–82. DOI: 10.1089/lap.2016.0562
9. Hashimoto R., Matsuda T. Jejunal ectopic pancreas. Clin Gastroenterol Hepatol. 2018. PII: S1542-3565(18)30366-5. DOI: 10.1016/j.cgh.2018.04.010
10. Giordano A., Alemanno G., Bergamini C., Prosperi P., Bruscino A., Valeri A. The Role of laparoscopy in the management of a diagnostic dilemma: jejunal ectopic pancreas developing into jejunojejunal intussusception. Case Rep Surg. 2017;2017:8452947. DOI: 10.1155/2017/8452947
11. Stauffer J.A., Asbun H.J. Minimally invasive pancreatic surgery. Semin Oncol. 2015;42(1):123–33. DOI: 10.1053/j.seminoncol.2014.12.011
12. Montalvo D., Hernandez P., Larrazabal A. Unexpected ectopic pancreatic tissue during laparoscopic bariatric surgery. Case report and literature review. Surg Obes Relat Dis. 2016;12(10):e87–8. DOI: 10.1016/j.soard.2016.09.019
13. Serrano J.S., Stauffer J.A. Ectopic pancreas in the wall of the small intestine. J Gastrointest Surg. 2016;20(7):1407–8. DOI: 10.1007/s11605-016-3104-4
14. Yogi N., Kaiho T., Yanagisawa S., Kataoka M., Nishimura M., Kobayashi S., et al. A case of jejunal ectopic pancreatic cancer with small bowel obstruction. Gan To Kagaku Ryoho. 2017;44(12):1829–31. PMID: 29394790.
15. Nasser H.A., Sleiman Y.A., Hassoun Z.A., Elzaatari M., Berjawi T., Hamdan W., et al. Bowel obstruction secondary to an ectopic pancreas in the small bowels: About 2 cases. Int J Surg Case Rep. 2017;31:72–4. DOI: 10.1016/j.ijscr.2017.01.019
Об авторах
Хасанов Анвар Гиниятович — доктор медицинских наук, профессор, зав. кафедрой хирургических болезней
450008, Уфа, ул. Ленина, 3
Суфияров Ильдар Фанусович — доктор медицинских наук, профессор кафедры хирургических болезней
450008, Уфа, ул. Ленина, 3
Бакиров Эльдар Рифович — врач-хирург хирургического отделения
450112, Уфа, ул. Нежинская, 28
Нуртдинов Марат Акдасович — доктор медицинских наук, профессор кафедры хирургических болезней
450008, Уфа, ул. Ленина, 3
Ибраев Айрат Вагизович — зав. хирургическим отделением
450112, Уфа, ул. Нежинская, 28
Евдокимов Евгений Викторович — зав. центральным патологоанатомическим отделением
450112, Уфа, ул. Нежинская, 28
Для цитирования:
Хасанов А.Г., Суфияров И.Ф., Бакиров Э.Р., Нуртдинов М.А., Ибраев А.В., Евдокимов Е.В. Острая тонкокишечная непроходимость, вызванная эктопированным участком поджелудочной железы. Клинический случай. Креативная хирургия и онкология. 2019;9(1):75-79. https://doi.org/10.24060/2076-3093-2019-9-1-75-79
For citation:
Khasanov A.G., Sufiyarov I.F., Bakirov E.R., Nurtdinov M.A., Ibraev A.V., Evdokimov E.V. Acute Small Intestinal Obstruction Caused by Ectopic Pancreas. A Clinical Case Report. Creative surgery and oncology. 2019;9(1):75-79. (In Russ.) https://doi.org/10.24060/2076-3093-2019-9-1-75-79