Аденовекторная вакцина что это
Ученый из МФТИ раскрыл процесс создания вакцины от коронавируса
Как создают вакцину от коронавируса?
Об эксперте: Павел Волчков — кандидат биологических наук, вирусолог, генетик, заведующий Лабораторией геномной инженерии Московского физико-технического института (МФТИ).
Существует много разных подходов к созданию вакцины от COVID-19. Она может быть вирусной, инактивированной, векторной, на основе нуклеиновых кислот. Какая из них окажется самой эффективной — пока никто точно не знает. Если вы разработчик, то можете выбрать любую и принять участие в большой мировой гонке по созданию долгожданной прививки. А можете, как ученые из МФТИ, сознательно отказаться от возможных бенефитов и неспешно заняться разработкой экспериментальной вакцины нового типа.
Одни из самых популярных на сегодняшний день — это рекомбинантные или векторные вакцины. Они изготавливаются на основе вирусов-носителей или вирусных векторов. Как это работает? Вы берете какие-то вирусные частицы, «вычищаете» из них все патогенные составляющие и на их место вставляете нужные вам элементы — генетический материал вируса, против которого изготавливается вакцина. По такому принципу была создана прививка от вирусного гепатита B или ротавирусной инфекции. И по такому же принципу сегодня многие разработчики создают вакцину от COVID-19. В частности, в России векторную вакцину от коронавируса разработали в НИИ эпидемиологии и микробиологии имени Н.Ф. Гамалеи.
Павел Волчков:
«Чем хорош вирусный вектор? Он способен инфицировать клетки только один раз и не может размножаться в организме человека дальше. Такая особенность делает рекомбинантные вакцины довольно безопасными. При этом в качестве вирусного вектора можно использовать буквально любой вирус из библиотеки человеческих патогенов. Выбор зависит от того, для какого заболевания вы изготавливаете вакцину. Потому что одни вирусы лучше заражают мышцы, другие — легкие, третьи — центральную нервную систему. Например, та же вакцина Центра Гамалеи выполнена на аденовирусном векторе».
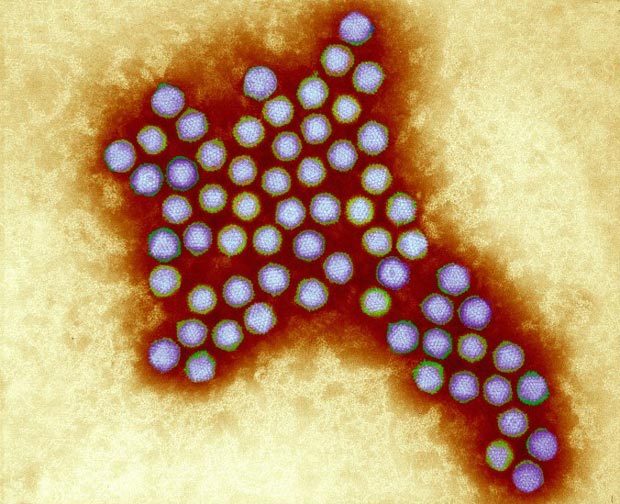
Аденовирусы — ДНК-вирусы. Относятся к группе острых респираторных вирусных инфекций (ОРВИ) и характеризуются поражением слизистых оболочек верхних дыхательных путей, конъюнктив, лимфоидной ткани. Большинство аденовирусных инфекций представляют собой легкую форму инфицирования. Существует семь видов аденовирусов человека (от А до G) и 57 серотипов. Подразделение на серотипы связано с различными способами заражения.
В качестве векторов для вакцин, аденовирусы применяются довольно давно. Эти вирусы хорошо изучены. Согласно данным сайта ClinicalTrials.gov, клинические испытания на людях успешно прошли или проходят более сотни различных вакцин на основе аденовирусных векторов.
Среди главных преимуществ этих вирусов — их естественный механизм взаимодействия с клетками человека. Они способны обеспечивать довольно длительную экспрессию антигена, а это успешно активирует врожденный иммунный ответ.
Антигены — это любые вещества, содержащиеся в микроорганизмах и других клетках (или выделяемые ими), которые несут в себе признаки генетически чужеродной информации, и которые потенциально могут быть распознаны иммунной системой организма.
Павел Волчков:
«При всех плюсах, у аденовирусов есть и ряд минусов. Первое — они обладают провоспалительным эффектом. То есть могут чрезмерно драйвить иммунную систему. Проще говоря — вызывать сильный иммунный ответ. Это один из возможных побочных эффектов вообще всех аденовирусных вакцин. Но есть еще один нюанс. Большинство аденовирусов — это естественные патогены человека. Многие из нас сталкивались в течение жизни с аденовирусными инфекциями. А что это значит? Что в крови у таких людей уже есть нейтрализирующие антитела к этому вирусу. Они могут связываться с компонентами вакцины и блокировать ее действие. Поэтому для некоторых из нас такая вакцина будет совершенно неэффективна».
Вакцина МФТИ: в чем инновация?
Поскольку у аденовирусных векторов есть существенные недостатки, ученые из МФТИ выбрали другие вирусы в качестве вектора — аденоассоциированные вирусы. Что любопытно, раньше никто в мире не использовал их в таком качестве.
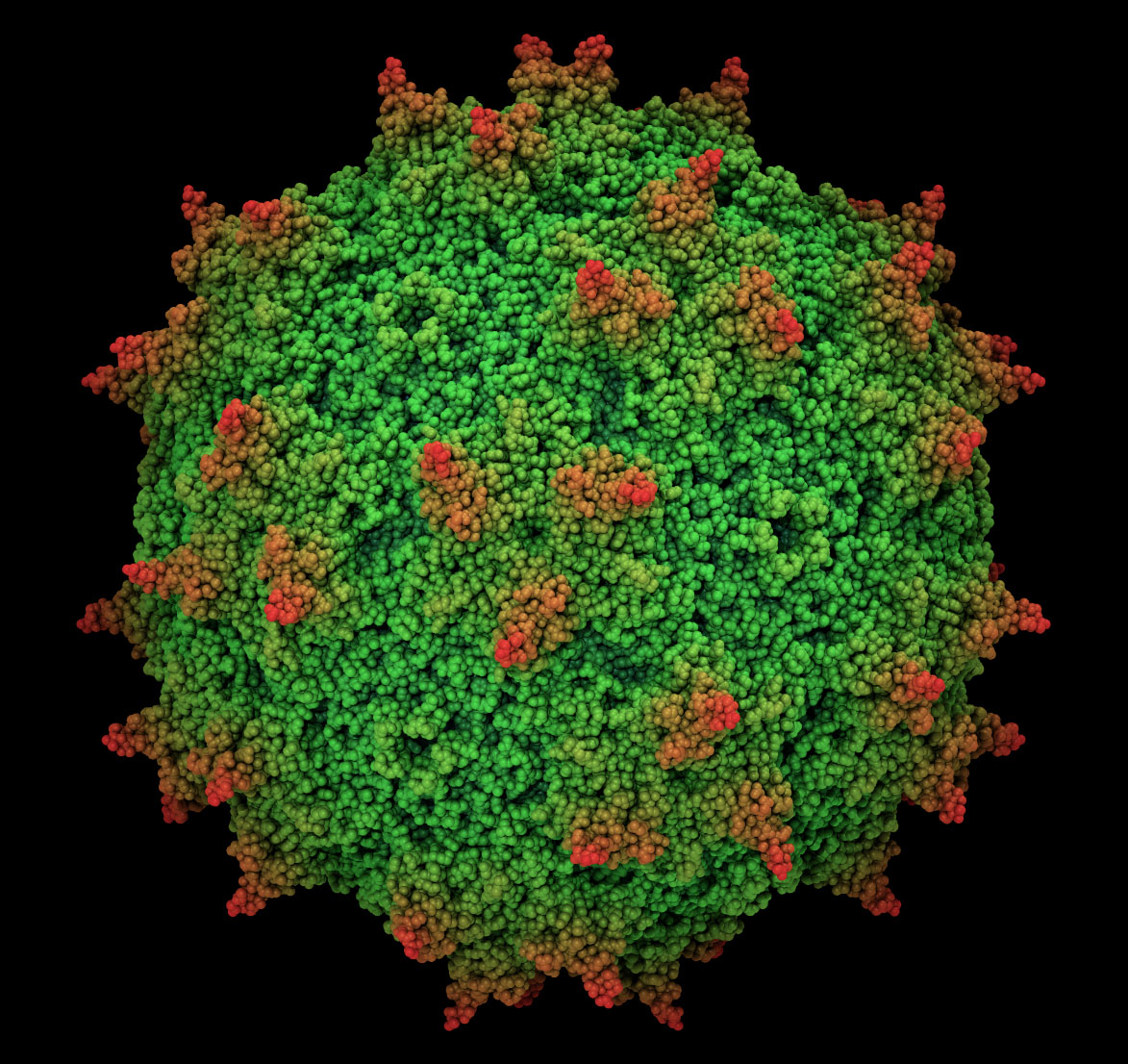
Аденоассоциированные вирусы — мелкие ДНК-содержащие вирусы. Размер частиц 22-24 нм. Размножаются только в присутствии аденовирусов. Способны инфицировать клетки человека и некоторых других приматов. Аденоассоциированный вирус, по-видимому, не вызывает заболеваний у человека, поэтому провоцирует слабый иммунный ответ.
Один из плюсов аденоассоциированных вирусов — они давно и успешно используются в генной терапии. Сегодня зарегистрировано несколько лекарственных средств на их основе. Одно из самых нашумевших — Luxturna. Это первое генное лекарство, созданное для лечения наследственной слепоты, вызванной мутацией гена RPE65.
По аденоассоциированным вирусам также накоплена внушительная клиническая база. На сайте ClinicalTrials.gov можно увидеть, в каком количестве клинических экспериментов аденоассоциированные вирусы уже приняли участие. Это несколько сотен доклинических исследований и порядка 50 клинических экспериментов. Носитель хорошо охарактеризован и, что еще важнее, показана его безопасность. Все это делает аденоассоциированные вирусы весьма привлекательным кандидатом для создания вирусных векторов не только для генной терапии, но и для вакцин, уверены в Лаборатории геномной инженерии МФТИ.
Еще одной веской причиной создать вакцину на аденоассоциированном векторе стало то, что ученые из МФТИ уже давно придумывают, модифицируют и создают аденоассоциированные вирусы. На сегодняшний день в библиотеке МФТИ их более миллиона. Все они имеют разную специфичность и разные свойства. Что важно, к этим вирусам у человека не может быть иммунного ответа, который бы снизил эффективность вакцины. Поскольку все они созданы искусственно.
Павел Волчков:
«Мы с самого начала понимали, что сможем не только разработать вакцину, но и масштабировать ее производство. То есть произвести столько доз, сколько потребуется или столько, сколько захотим. В мире существует огромное количество аутсорсинговых компаний, которые по GMP сделают вам любое количество доз препарата.
Good Manufacturing Practice (GMP) — правила, которые устанавливают требования к организации производства и контроля качества лекарственных средств для медицинского и ветеринарного применения.
Поэтому с самого начала у нас было четкое понимание, что проблем с производством не будет. Как и проблем с лицензией на вирусный носитель. Это качественно отличает нашу лабораторию от многих других разработчиков вакцин в Российской Федерации. В современном мире все технологии так или иначе кому-то принадлежат, и аденовирусы, и прочие системы векторной доставки, аденоассоциированные в том числе. Живя по правилам свободного рынка, вы не можете просто взять и сделать вакцину на основе любого понравившегося вектора. Вы должны иметь разрешение от компании, которая обладает правами на технологию, либо владеет непосредственно интеллектуальной собственностью в области этого вектора. И тут у нас все хорошо — мы как раз владеем патентом по разработке аденоассоциированных вирусов. Нам не нужно просить ни у кого лицензию на производство данной вакцины, поскольку мы используем собственные же аденоассоциированные вирусы».
Вакцина МФТИ будет эффективна против разных штаммов SARS-CoV-2
Изначально ученые хотели разработать вакцину, которая бы вырабатывала иммунитет практически ко всем поверхностным белкам вируса SARS-CoV-2. А не только к S-белку, как это делают большинство разработчиков вакцин по всему миру (включая НИИ им. Гамалеи). Но в итоге разработчики остановились на конечном числе компонентов. Ими стали S-белок, Е-белок и М-белок.
Павел Волчков:
«По сути мы воплощаем идею совершенно нового типа вакцин — так называемых поливалентных вакцин. Это когда в одном препарате сразу несколько вирусных компонентов. Такой подход кажется нам крайне эффективным применительно к SARS-CoV-2. Ведь на самом деле это не один какой-то конкретный вирус, который распространился по планете. Если мы начнем секвенировать разные изоляты коронавируса, то они все будут отличаться друг от друга. Либо на одну аминокислотную замену, либо на несколько. Поливалентная вакцина как раз направлена на то, чтобы вырабатывать иммунный ответ не к одному поверхностному белку вируса, а сразу к нескольким. В том числе к консервативным поверхностным белкам, которые меньше остальных подвержены мутациям. Так наша вакцина поможет сформировать иммунитет к разным штаммам вируса SARS-CoV-2».
Если текущая разработка покажет свою эффективность и безопасность, ученые планируют пойти еще дальше и разработать вакцину, которая будет содержать не только различные компоненты SARS-CoV-2, но еще и вируса гриппа или других сезонных респираторных вирусов. То есть объединить в одной вакцине генетический материал от самых разных сезонных патогенов. По мнению ученых из МФТИ, такие ассемблированные, поливалентные вакцины могли бы готовить людей каждый сезон к новому остро-респираторному вирусному нашествию.
Что касается текущей разработки (вакцины от COVID-19), то на данный момент ее разработка завершена. Впереди подготовка к доклиническим испытаниям на китайских хомяках и приматах. Если они пройдут успешно, вакцину ожидают испытаниях на людях. Но торопиться и участвовать в текущей «вакцинной» гонке разработчики из МФТИ не собираются.
Павел Волчков:
«Дело в том, что в нашей вакцине слишком много новых компонентов. Несмотря на то, что аденоассоциированные вирусы используются в генной терапии, для создания вакцин их еще никто не применял. Спешка или сокращение сроков проведения доклинических и клинических исследований может обернуться ошибкой и поставить крест на такой многообещающей и перспективной платформе. Но это не значит, что сейчас мы создаем вакцину, что называется «в стол». Во-первых, когда она будет испытана, мы сможем ее продавать другим нуждающимся странам. Во-вторых, наша основная цель — получить опыт по созданию быстрых вакцин, который мы планируем применять в будущем. Как научная лаборатория мы можем проводить такие эксперименты — создавать платформу для вакцин совершенно нового типа. И если у нас все получится, то в следующий раз, когда в мире появится новость о новой вспышке заболевания, мы будем готовы пройти весь путь создания препарата гораздо быстрее, чем мы проходим его сейчас».
Массовая вакцинация от COVID-19 может не понадобиться?
Павел Волчков уверен, что сама по себе гонка по созданию вакцин от короновируса уже не имеет смысла. Он уверен, что к тому моменту, когда российские вакцины будут испытаны и наработаны для массовой вакцинации населения, потребность в них может отпасть. Ученый считает, что уже к осени мы все, так или иначе, переболеем COVID-19 и получим естественный иммунитет.
У этой оптимистичной гипотезы есть основания. Не так давно шведские ученые провели исследование и померяли иммунитет в шведской популяции. Измерялся и гуморальный иммунитет (то есть антитела в крови), и клеточный иммунитет. А именно Т-лимфоциты — так называемые клетки иммунной памяти, которые при повторной встрече с инфекцией «просыпаются» и активизируют иммунный ответ.
Исследование показало, что лишь у небольшой части шведов в крови присутствовали антитела, но примерно треть граждан имела ту самую клеточную память. Это говорит о том, что существенная часть популяции шведов в той или иной форме переболела COVID-19 или имела непродолжительный контакт с вирусом. В последнем случае большой продукции антител не происходит, но благодаря Т-лимфоцитам формируется иммунологическая память к COVID-19.
Павел Волчков:
«Согласно московской статистике, антитела к коронавирусу были определены в крови примерно у 20% жителей столицы. А это около 2 млн человек. Следуя логике шведского исследования, которому у меня лично нет причин не доверять, то скорее всего еще у 20% (а может и у 40% или даже 50-60%) людей уже есть клеточный иммунитет к COVID-19. Эти люди контактировали с небольшими дозами вируса, их иммунная система его детектировала и сформировала клетки памяти. Фактически, половина населения столицы естественным образом получила живую вакцину от COVID-19. Что примечательно, иммунитет, полученный в результате натуральной инфекции, оказывается более стойким, чем от гипотетической вакцины. Потому что в таком случае, иммунная система знакомится с полноценным вирусом (со всеми поверхностными белками), а не с его редуцированной версией, как это происходит при вакцинации. Я думаю, что такая ситуация с клеточным иммунитетом к COVID-19 обстоит не только в Москве, а во многих российских городах. То есть огромное количестве людей по всей России на самом деле уже имеет иммунитет к коронавирусной инфекции».
Аденовирусные вакцины
Аденовирусные вакцины
Аденовирусные векторы считаются абсолютно безопасными, а также наиболее подходящими для генетической модификации. Вектор – это вирус, лишенный гена размножения, поэтому он не представляет опасности заражения для организма. Ученые используют векторы для транспортировки генетического материала из другого вируса, против которого делается вакцина, в клетку.
Аденовирусы, извлекаемые из аденоидов и в обычном состоянии вызывающие острые респираторные вирусные инфекции (ОРВИ), стали наиболее часто используемыми вирусами для создания векторов. В мире существует более 350 научных исследований в различных источниках на тему создания и безопасности аденовирусных векторов.
АДЕНОВИРУСЫ ЧЕЛОВЕКА – ЭТО ХОРОШО ИЗУЧЕННАЯ ПЛАТФОРМА С ПОДТВЕРЖДЕННОЙ ДОЛГОСРОЧНОЙ БЕЗОПАСНОСТЬЮ
В клинических испытаниях препаратов на основе аденовирусных векторов приняли участие более 20 тысяч человек по всему миру.
Препараты на основе аденовируса человека массово применяются уже более 50 лет.
Одобренный для гражданского оборота в Китае препарат для лечения раковых опухолей был принят уже более 30 000 пациентами.
УСПЕШНЫЙ ОПЫТ ЦЕНТРА ИМЕНИ Н.Ф. ГАМАЛЕИ
Ученые из Центра имени Н.Ф. Гамалеи работали с вакцинами на основе аденовирусных векторов с 1980-х годов и стали мировыми лидерами в разработке такого рода вакцин.
Вакцина на основе аденовирусных векторов против ближневосточного респираторного синдрома проходит последние клинические испытания. Многие вакцины-кандидаты против COVID-19 также основаны на аденовирусных векторах, но пока ни одна не использует двухвекторную систему вакцинации, созданную в Центре имени Н.Ф. Гамалеи.
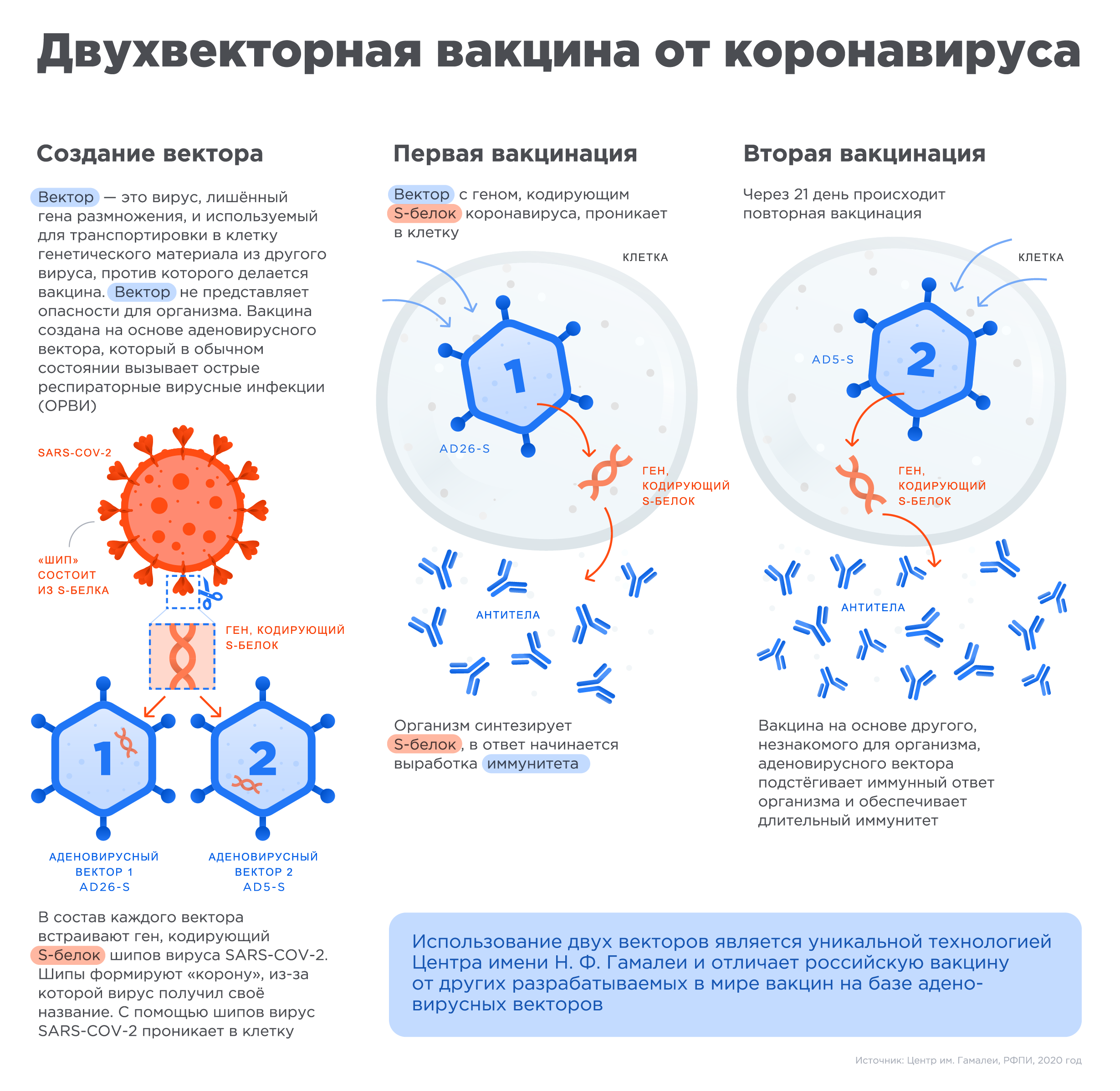
В процессе создания вакцины ген, кодирующий S-белок шипа коронавируса встраивается в аденовирусный вектор. Вставленный элемент является безопасным для организма, но он заставляет иммунную систему реагировать и вырабатывать антитела, которые защищают нас от инфекции.
Используя векторы на основе аденовируса, ученые Центра имени Н.Ф. Гамалеи успешно создали и получили регистрационное удостоверение Министерства Здравоохранения РФ на вакцину против лихорадки Эбола на основе аденовирусных векторов.
Ниже представлены ссылки на подтверждающие официальные документы и научные публикации по вакцинам Центра имени Н.Ф. Гамалеи против лихорадки Эбола и ближневосточного респираторного синдрома (MERS).
Вакцина против лихорадки Эбола
Регистрационные удостоверения Министерства здравоохранения
О Спутник V
О Спутник V
«Спутник V» — первая в мире зарегистрированная вакцина на основе хорошо изученной платформы вектора аденовируса человека. Она одобрена в 71 стране с общим населением 4 млрд человек.
Вакцина названа в честь первого советского космического спутника. Запуск «Спутника-1» в 1957 году дал новый импульс космическим исследованиям во всем мире, создав так называемый «момент Спутника» для мирового сообщества.
Эффективность вакцины составляет 97,6% по результатам анализа данных о заболеваемости коронавирусом среди россиян, привитых обоими компонентами препарата в период с 5 декабря 2020 года по 31 марта 2021 года.
Фаза 1 и 2 клинических испытаний вакцины были завершены 1 августа 2020 года. Итоги третьей фазы клинических испытаний в России опубликованы в журнале Lancet 2 февраля 2021 года. Клинические испытания третьей фазы «Спутник V» также успешно проходят в ОАЭ, Индии, Венесуэле и Беларуси.
Вакцина «Спутник V» создана на проверенной и хорошо изученной платформе аденовирусных векторов человека, которые вызывают обычную простуду и с которыми человечество сталкивалось на протяжении тысячелетий.
В вакцине «Спутник V» впервые среди вакцин против коронавируса был применен подход гетерогенного бустирования, в основе которого лежит применение двух разных векторов для двух уколов в процессе вакцинации. Такой подход формирует более стойкий иммунитет по сравнению с вакцинами, которые используют одинаковый механизм доставки для обоих уколов.
Безопасность, эффективность и отсутствие долгосрочных негативных последствий у аденовирусных вакцин доказаны в более чем 250 клинических исследованиях на протяжении двух десятилетий.
«Спутник V» не вызывает сильной аллергии.
Температура хранения на уровне +2+8 градусов Цельсия позволяет хранить вакцину в обычном холодильнике без необходимости инвестиций в дополнительную инфраструктуру холодовой цепи.
Как работают вакцины на основе аденовирусного вектора
«Векторы» являются носителями, которые могут доставить генетический материал из другого вируса в клетку. При этом генетический материал аденовируса, который вызывает инфекцию, удаляется и вставляется материал с кодом белка от другого вируса, в данном случае от шипа коронавируса. Этот новый элемент безопасен для организма, но он помогает иммунной системе реагировать и вырабатывать антитела, которые защищают от инфекции.
Технологическая платформа векторов на основе аденовирусов упрощает и ускоряет создание новых вакцин путем модификации исходного вектора-носителя генетическим материалом из новых появляющихся вирусов, что позволяет получать новые вакцины в сжатые сроки. Такие вакцины вызывают сильный ответ со стороны иммунной системы человека.
Человеческие аденовирусы считаются одними из самых простых для модификации, поэтому они стали очень популярными в качестве векторов.
Преимущества прайм-буст иммунизации

Безопасность и эффективность
После начала пандемии российские исследователи извлекли фрагмент генетического материала нового коронавируса SARS-COV-2, кодирующий информацию о структуре S белка шипа вируса (белок формирующего «корону» вируса и отвечающий за его связывание с клетками человека), и вставили его в уже знакомый им аденовирусный вектор для доставки в человеческую клетку, создав, таким образом, первую в мире вакцину против коронавируса SARS-COV-2.
Чтобы обеспечить длительный иммунитет, российские ученые предложили использовать два разных типа аденовирусных векторов для первой и второй вакцинации, усиливая действие вакцины.
Использование аденовирусов человека в качестве векторов безопасно, так как данные вирусы, вызывающие ОРВИ, не являются новыми и существуют уже тысячи лет.
Эффективность против новых штаммов
Вакцинация препаратом вырабатывает защитные нейтрализующие титры антител против новых штаммов, включая Alpha B.1.1.7 (впервые выявлен в Великобритании), Beta B.1.351 (впервые выявлен в ЮАР), Gamma P.1 (впервые выявлен в Бразилии), Delta B.1.617.2 и B.1.617.3 (впервые выявлены в Индии) и выявленных в Москве вариантов B.1.1.141 и B.1.1.317 с мутациями в рецептор-связывающем домене (RBD).Методология исследования основана на оценке вируснейтрализующей активности (ВНА) с применением живого вируса, что позволяет получить наиболее достоверные данные и является «золотым» стандартом. В ходе исследования сравнивалась ВНА сыворотки крови людей после вакцинации препаратом «Спутник V» на образцах штаммов, имеющих международное распространение, с ВНА против исходного штамма B.1.1.1. Сыворотка крови была собрана у лиц, иммунизированных обоими компонентами «Спутника V».
Полученные данные демонстрируют, что «Спутник V» сохраняет защитные свойства против новых штаммов. Снижение уровня вируснейтрализующей активности у препарата «Спутник V» к ряду штаммов оказалось значительно меньшим по сравнению с данными, опубликованными производителями других вакцин, которые ранее подтвердили эффективность своих препаратов против новых мутаций коронавирусной инфекции.
Научно-
образовательный
портал IQ
«Новая платформа, совершенно не изученная и никогда не использовавшаяся»: мРНК от Pfizer против вирусных векторов «Спутник-V»
Одним из самых громких событий последних дней стало сообщение американской компании Pfizer и немецкой BioNTech о том, что разрабатываемая ими вакцина BNT162b2 против СOVID-19 показала 90% эффективность в III фазе клинических испытаний. Во всем мире новость встретили с большим воодушевлением, но, между тем, вакцина Pfizer и BioNTech сделана на новой, малоисследованной платформе. По протоколу её испытания закончатся только в 2022 году. О том, чем отличается американо-немецкая вакцина от российской «Спутник-V», и каковы шансы победить СOVID-19 c помощью массовой иммунизации в ближайшие месяцы IQ поговорил с директором Института экономики здравоохранения НИУ ВШЭ Ларисой Попович.
Лариса Попович,
директор Института экономики
здравоохранения НИУ ВШЭ,
кандидат биологических наук
— Один из вопросов, который сейчас волнует всех в отношении новой вакцины от СOVID-19 — возможность её массового и эффективного применения в связи с тем, что температура хранения вакцины должна быть не менее минус 70 градусов по Цельсию, а это сильно осложняет возможность транспортировки. Что Вы можете сказать по этому поводу?
— Вряд ли это тема для обсуждения. У любой вакцины достаточно жёсткие условия хранения и транспортировки. Это нужно для сохранения жизнеспособности препарата.
— То есть, озвучиваемая сейчас температура хранения вакцины в минус 70 градусов — это нормально?
— Наличие холодовой цепочки — это нормальная практика для хранения многих вакцин. Температура может быть разной, и чем ниже она должна быть, тем сложнее использовать вакцину. Если говорить о сравнении вакцин, то очевидно, что создать условия с температурой минус 70 градусов куда сложнее, чем минус 18, как необходимо для нашей вакцины «Спутник-V». В любом случае, условия хранения и транспортировки пока лимитируют возможность широкой региональной распространенности вакцинации, что отмечают в первую очередь как недостаток технологий. И будущее развитие должно идти в сторону повышения стабильности препаратов при температурах, приближенных к естественным.
— Вокруг вакцины Pfizer и BioNTech сейчас очень много разговоров. А какие перспективы появления альтернатив в ближайшее время? Ведь многие страны одновременно начали разработки. Что происходит в этом направлении сейчас?
— Давайте расскажу подробнее. На данный момент 47 вакцин прошли, как минимум, две фазы испытаний, в том числе и несколько российских. Третью фазу заканчивают восемь вакцин, включая «Спутник-V». Ещё 144 кандидата пока проходят доклинические испытания.
— И это меньше, чем за год. А как обычно проходит процесс испытаний вакцин?
— Любая вакцина, как и любой биологически активный препарат должны проходить несколько стадий исследования. Сначала с помощью компьютерных программ, химических экспериментов ищут самые интересные варианты, которые имеют шансы стать перспективными кандидатами на лекарства или вакцины. Таких вариантов может быть несколько тысяч. После этого начинаются доклинические испытания — сначала на мелких животных, затем на крупных. Доклинические испытания лекарств и вакцин в нормальных условиях занимают около двух лет. И в итоге остаются несколько (в лучшем случае) кандидатов.
Дальше начинается первая фаза клинических испытаний, когда анализируется профиль безопасности для человека. Для этого находят порядка десятка здоровых добровольцев, которые получают препарат. Далее, во втором этапе испытаний участвует несколько десятков или даже сотен человек, в том числе больных определенным заболеванием. Группы делятся на тех, кто получает кандидата на лекарство, и тех, кто получает плацебо (пустышку). потом результаты сравниваются. На данной стадии исследуется эффективность в отношении терапии этой болезни.
Что касается именно вакцин, то здесь очень часто совмещают второй этап с третьим, когда набирается не 100 человек, а около 10 000 и им вводят уже точно безопасную вакцину, чтобы понять заражаются они или нет при столкновении с инфекцией.
Всё это очень тонкие вещи, которые проходят обязательную оценку этического компонента. Понятно, что при исследовании вакцин не предполагается специально заражать людей (хотя в некоторых вариантах такой подход иногда мог использоваться), но точно не в случае с COVID-19. Поэтому необходим длительный период наблюдения, потому что люди могут столкнуться с инфекцией далеко не завтра и не послезавтра. Когда это произойдет — неизвестно. Клинические испытания обычно проводят на тех группах, которые с большей вероятностью могут столкнуться с патогеном и оказаться зараженными — например, медиках.
— На какой стадии испытаний сейчас находится отечественная вакцина?
— До конца декабря отечественная вакцина «Спутник-V» пока на клинических испытаниях — в III фазе. В этих испытаниях по протоколу участвует 40 000 человек в разных республиках, областях и даже странах.
— Можете ли Вы рассказать, чем отличаются вакцина Pfizer и BioNTech от отечественной вакцины «Спутник-V»?
— Это вакцины, сделанные на совершенно разных платформах. Чтобы это понять, необходимо разбираться в том, какие вакцинные платформы существуют.
— И как много этих платформ? Каковы их принципиальные отличия?
— Всего есть около шести основных типов платформ или баз для вакцин. Во-первых, это живой, но ослабленный вирус. Такого рода вариант известен, например, в случае полиомиелита, и считается, что живой вирус вызывает более стойкий иммунитет. Но среди вакцинных кандидатов от СOVID-19, вошедших в стадию клинических испытаний, платформ с живым ослабленным вирусом пока нет.
Есть вакцины на основе инактивированного, то есть убитого вируса. Вакцину на такой платформе делают, например, в Китае, причем сразу несколько разработчиков — компания Sinovac, институты в Ухане и Пекине. В целом у китайцев сейчас в клинических испытаниях второго и третьего этапов находятся шесть вакцин, в том числе и на иных платформах.
— То есть, ни наша вакцина, ни вакцина Pfizer и BioNTech не основана ни на одной из этих первых трёх платформ?
— НИЦЭМ им. Н.Ф. Гамалеи также использует вирусной вектор в качестве основы. Но вакцина «Спутник-V» в этом плане уникальна — у неё двойная платформа. Если англичане и китайцы используют аденовирус 5 серотипа, то в нашу вакцину дополнительно включен аденовирус 26 серотипа. Такой двухвекторный вариант вызывает более сильный иммунный ответ, чем одновекторный.
— В чем специфика более сильного иммунного ответа, и за счёт чего он образуется в организме?
— Иммунный ответ может определяться формированием антител — фрагментов белка, которые опознают и «подсвечивают» вирус, как фонарики, и он становится виден для иммунной системы. А далее приходят большие клетки и съедают этот вирус. Антитела формируются организмом каждый раз индивидуально, из «подручных материалов».
Поэтому когда человек сталкивается с новой инфекцией, из имеющихся антител формируются новые. Из-за этого антитела быстро распадаются — обычно через три-пять месяцев после столкновения с инфекцией.
Но есть так называемый клеточный иммунный ответ — формирование пула клеток иммунной системы — специализированных лимфоцитов, развивающихся в тимусе (вилочковой железе). Именно такой ответ, как отмечают эксперты, напрямую стимулируется аденовирусом 26 серотипа, который используется в отечественной вакцине. И это существенно ускоряет формирование приобретенного иммунитета к коронавирусной инфекции и усиливает его.
В результате формируется устойчивый и гарантированный не только антительный, но и клеточный иммунитет. И этот иммунитет может сохраняться достаточно долго. Возможно, — несколько лет, хотя реальную продолжительность покажут дальнейшие исследования. Вот этим российская вакцина отличается в лучшую сторону от английской и китайской, которые сделаны на платформе только аденовируса 5 серотипа.
Если говорить о платформах далее, то есть в исследовании и одновекторная вакцина на базе аденовируса 26 серотипа. Такую вакцину делает, например, дочерняя компания фармакологического гиганта Johnson & Johnson, под названием Janssen Pharmaceutica. Они тоже недавно вышли на третью фазу испытаний.
— В чём особенности остальных трех типов платформ, и на какой из них основана нашумевшая вакцина Pfizer и BioNTech?
— Четвертый тип платформы — это белковый кусочек вируса. Вакцина с такой платформой есть у китайцев, и она также на третьей стадии испытаний.
Пятый тип платформы основан на вживлении в кольцевую молекулу ДНК безобидного вируса (в плазмиду) кусочка генетического материала коронавируса, в которой записаны «инструкции» по созданию вирусного белка. Такую платформу делают во многих странах, но пока все они находятся на стадии доклинических или в лучшем случае втором этапе клинических испытаний. В материалах ВОЗ о такой платформе сообщают исследователи из Японии, Китая, Индии и Израиля.
И вот мы наконец подошли к шестой платформе, на которой сделана вакцина Pfizer и BioNTech. Это новая платформа, совершенно не изученная и ранее никогда не использовавшаяся. Она основана на матричной РНК — кусочке генетического материала вируса, который вживляется в организм. Такую платформу используют не только Pfizer и BioNTech, но также ещё одна компания из США, компании из Китая и Казахстана. Но у последних исследования пока находятся на более ранних стадиях.
— Если из этих шести платформ сравнивать аденовирусную, на которой сделана российская вакцина и платформу на мРНК, на которой сделала вакцина Pfizer и BioNTech, какие тогда принципиальные различия у этих вакцин с точки зрения перспектив применения?
— В первую очередь, стоит обратить внимание на то, что НИЦЭМ им. Н.Ф. Гамалеи, который делает вакцину «Спутник-V» — очень известный институт с колоссальным опытом разработки вакцин. В создании вакцины от коронавируса этот институт пошёл самым простым путём, использовав платформу, с которой работал несколько десятилетий. Вакцины на основе аденовирусов изучались, начиная с 1953 года. До этого на их основе учёные из института делали вакцину против вируса Зика, против Эболы и очень хорошо знают, как ведёт себя аденовирус.
В институте Гамалеи начали работать над новой вакциной сразу с февраля, как только получили генетический материал коронавируса. То есть, под российской вакциной есть основательная теоретическая и практическая база, наработанная в течение многих лет. Однозначно нельзя говорить, что отечественная вакцина сделана «на коленке», как это иногда пытаются представить в СМИ.
Аденовирусная платформа используется не только нашими, но и многими западными разработчиками, именно потому, что она очень хорошо изучена. И это большое достижение, что именно наш институт так быстро сделал вакцину на данной платформе, объединив при этом ещё и два аденовируса.
Теперь, если посмотреть на Pfizer и BioNTech — они, в отличие от России, только подали заявление на временное одобрение вакцины (Emergency Use Authorization, EUA). Но по протоколу третья фаза испытаний у них заканчивается лишь в 2022 году — ровно потому, что абсолютно никто не знает, что будет происходить в отдалённой перспективе после использования РНК-вакцины. Самая большая проблема вакцины, основанной на технологии мРНК, в том, что она ранее никогда не использовалась в утвержденных вакцинах. Так что отличием BNT162b2 от «Спутник-V» является фактор неизвестности. Мы не знаем, какой эффект может проявиться в долгосрочной перспективе.
— Перспективы массовой иммунизации в России и мире в 2021 году реальны?
— Можно предполагать. Несмотря на более сложные условия хранения и массу проблем из-за неизвестности, какие будут отдаленные последствия, технология производства вакцины Pfizer и BioNTech, как отмечается, позволяет быстро наработать большие объёмы препарата. Так что, если страны решатся рисковать здоровьем своего населения при использовании совершенно незнакомого продукта, то они могут получить вакцину уже довольно скоро.
Испытания отечественной вакцины должны закончиться по протоколу уже к концу года — в силу того, что мы используем хорошо известную платформу. Все шансы есть, что в России, благодаря наличию вакцины, проблема с COVID-19 будет во многом решена уже весной.
— В последние дни появились сообщения о заражении нескольких медиков, которые участвовали в качестве добровольцев в испытаниях «Спутник-V». О чём это может говорить?
— Нужно проанализировать, что именно получали эти врачи — плацебо (пустышку) или вакцину? Нужно понять, получили ли они полный объём препаратов или часть? Нужно выяснить особенности протекания у них болезни — в какой форме они перенесли заболевание? Никакая вакцина не может на 100% защитить все 100% вакцинированных. Всегда есть люди с ослабленным иммунитетом, которые всё равно заболеют, но благодаря вакцине, перенесут болезнь легче. И сравнение числа тех, кто заболел без вакцины, с числом тех, кто заболел после вакцинации, даёт параметр эффективности вакцины. У исследователей Pfizer и BioNTech эффективность 90% получается потому, что среди вакцинированных заболевших было в 10 раз меньше, чем среди невакцинированных. У нас, насколько мне известно, это соотношение лучше. Но посмотрим после завершения всех процедур испытаний, сравним все вакцины. Тогда и можно будет говорить, у кого какие профили эффективности и безопасности.
— Как думаете, россияне смогут выбрать, каким типом вакцины прививаться и от какого производителя — западного или отечественного?
— Что касается вакцины Pfizer и BioNTech, то здесь всё непросто, она у нас не исследовалась. Согласно нашему законодательству, регистрация проводится только в отношении тех препаратов, которые прошли клинические многоцентровые испытания, в том числе в России. Если эта вакцина не будет исследована в России, то она и не будет зарегистрирована. Но напомню — у нас в России проходят испытания ещё и китайские вакцины, и вакцины центра «Вектор», да и ещё несколько научных центров выходят на клинические испытания. Так что выбор вакцин с точки зрения разных платформ точно будет.
IQ