Аденовирус человека что это такое
Аденовирус человека что это такое
Аденовирусная инфекция — группа острых вирусных заболеваний, проявляющихся поражением слизистых оболочек дыхательных путей, глаз, кишечника и лимфоидной ткани преимущественно у детей и лиц молодого возраста.
Дети чаще болеют аденовирусной инфекцией, чем взрослые. Большинство детей переболеют, по крайней мере, одним типом аденовирусной инфекции к тому времени, когда им исполнится 10 лет.
Возбудители инфекции — аденовирусы.
Источник инфекции — больной человек или вирусоноситель.
Инфекция передается воздушно-капельным, пищевым, контактно-бытовым путями. Возможно внутриутробное инфицирование плода.
Вирусы распространены в местах с организованными группами детей (детские сады, школы и летние лагеря).
Инфекция распространяется при кашле или чихании. Капли, содержащие вирус, разлетаются по воздуху и приземляются на поверхности.
Аденовирусы чрезвычайно устойчивы в окружающей среде. При комнатной температуре сохраняют жизнеспособность до 2 недель, на предметах обихода в высушенном виде – более 8 дней. К низким температурам высокоустойчивы, однако, при 60 0 С инактивируются в течение 2 минут.
Аденовирусная инфекция быстро распространяется среди детей, дети часто касаются руками лица, берут пальцы в рот, игрушки.
Аденовирусная инфекция обычно протекает без осложнений, симптомы проходят через несколько дней. Но клиническая картина может быть более серьезной у людей со слабой иммунной системой, особенно у детей.
Аденовирусная инфекция характеризуется многообразием клинических проявлений.
лихорадка длительностью от 2-3 дней до 2 недель
Аденовирус (Аденовирусная инфекция)
Аденовирусная инфекция — патологический процесс, возникающий на фоне попадания в организм человека аденовируса (Adenoviridae). Заболевание сопровождается поражением органов дыхания, глаз, желудочно-кишечного тракта и лимфатической системы. Инфицированные пациенты страдают от интоксикации, лихорадки, потери голоса, кашля, кишечных расстройств. Постановка диагноза осуществляется на основании клинической картины заболевания и результатов лабораторных исследований. В процессе лечения взрослые и дети получают противовирусные препараты, иммуномодуляторы и средства, снимающие острые симптомы инфекции.
Общие сведения о патологии
Аденовирус относится к группе респираторно-вирусных инфекций. Течение заболевания осложняется конъюнктивитом, ринофарингитом, лимфаденопатией, диспепсическим синдромом. Доля аденовирусных инфекций в общей структуре ОРВИ достигает 20%.
В группу риска входят пациенты в возрасте от полугода до трех лет. Почти все дети дошкольного возраста были инфицированы аденовирусом хотя бы один раз. Патология не обладает выраженной сезонностью: уровень заболеваемости остается стабильным на протяжении всего года. Лечение заболевания осуществляется под надзором педиатра и отоларинголога.
Причины развития патологии
Вирусологи выявили три десятка патогенов, относящихся к семейству Adenoviridae. Возбудители инфекции приспособлены к длительному выживанию в неблагоприятных условиях, хорошо переносят отрицательные температуры и низкую влажность окружающей среды. ДНК патогенов разрушается под воздействием ультрафиолетового излучения и химических соединений на основе хлора.
Пациент, перенесший аденовирусную инфекцию, обладает иммунитетом к определенному типу вируса. Ребенок или взрослый может повторно заболеть, столкнувшись с носителем другого серотипа Adenoviridae. Подобный механизм передачи аденовируса от человека к человеку характерен для внутрибольничных инфекций.
 Механизм инфицирования
Механизм инфицирования
Первые проявления аденовируса начинают беспокоить пациента после попадания патогенов на слизистые оболочки дыхательных путей и кишечника или конъюнктиву глаза. Вирусы репродуцируются в клетках эпителия, лимфатических узлах и лимфоидных образованиях кишечника. После завершения инкубационного периода пораженные клетки гибнут — вирусы попадают в кровеносную систему человека.
В местах первичного поражения слизистых формируются отёки. Типичная локализация очага воспаления — задняя стенка глотки. Воспалительный процесс протекает на фоне обильного отделения экссудата. При отсутствии лечения пациент может столкнуться с поражением бронхов, почек, печени и селезенки.
Симптоматика патологии
Симптомы попадания аденовируса в организм человека специфичны и зависят от формы, которую приняла инфекция. При поражении дыхательных путей могут развиться фарингиты, тонзиллофарингиты и бронхиты. В случае проникновения инфекции к тканям конъюнктивы пациенты страдают от фарингоконъюнктивной лихорадки и острого конъюнктивита. Попадание вирусов семейства Adenoviridae на слизистые оболочки кишечника провоцирует развитие диарейного синдрома.
Пациенты могут столкнуться с легким, средним и тяжелым течением заболевания. В некоторых случаях патология осложняется присоединением вторичной инфекции. Инкубационный период длится от пяти до семи дней. По его завершении пациент ощущает резкое повышение температуры тела (до 38–39 градусов). Позднее проявляются типичные признаки аденовирусной инфекции:
Перечисленные симптомы аденовируса развиваются у детей и взрослых в течение нескольких часов после повышения температуры. При отсутствии лечения состояние пациентов быстро ухудшается.
Поражение органов дыхания
Распространение инфекции в дыхательных путях провоцирует появление гнойно-слизистого отделяемого из носа. Дыхание человека учащается. При осмотре пациента отоларинголог обнаружит белый налет на миндалинах и выраженный отек слизистой оболочки глотки. Подчелюстные и шейные лимфатические узлы значительно увеличиваются в размерах. Голос ребенка или взрослого обретает характерную осиплость. В некоторых случаях врачи диагностируют у пациентов сухой кашель и одышку.
Поражение конъюнктивы
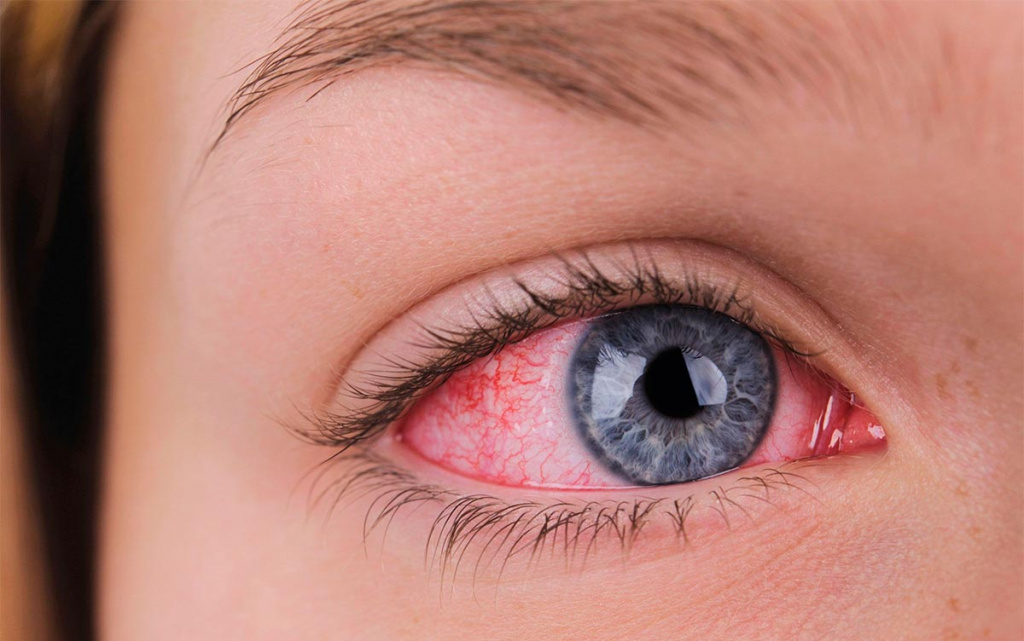
Репродуцирование вирусов в тканях конъюнктивы приводит к развитию конъюнктивитов различных форм: катаральной, фолликулярной и пленчатой. Патологический процесс начинает развиваться в одном глазу, но постепенно затрагивает и второй. Пациенты жалуются на рези, жжение, ощущение инородного тела. Офтальмологический осмотр позволяет выявить покраснение и отечность кожи век. В некоторых случаях врачи фиксируют образование плотной белесой пленки на конъюнктиве. Запущенная аденовирусная инфекция осложняется кератитом.
Поражение желудочно-кишечного тракта
Проникновение Adenoviridae в кишечник человека провоцирует развитие острого болевого синдрома в околопупочной области. Пациент страдает от диареи, систематических приступов тошноты и рвоты. Частично клиническая картина заболевания совпадает с острым аппендицитом.
Возможные осложнения
Тяжелое течение аденовирусной инфекции может привести к развитию менингоэнцефалита. Младенцы страдают от аденовирусной пневмонии и дыхательной недостаточности. Взрослые часто сталкиваются со вторичными инфекциями, на фоне которых развиваются синуситы, отиты и бактериальные пневмонии.
 Диагностические мероприятия
Диагностические мероприятия
Диагностика выполняется терапевтом или отоларингологом — врач проводит осмотр пациента с признаками инфицирования аденовирусом. В анамнез ребенка или взрослого вносятся объективные данные о симптомах: лихорадке, конъюнктивите, дыхательной недостаточности, кишечных расстройствах. Подтверждение первичного диагноза выполняется в ходе лабораторных исследований биоматериалов пациента — крови, мазков из носоглотки, соскобов с конъюнктивы, каловых масс.
Дифференциальная диагностика позволяет исключить из анамнеза человека грипп, инфекционный мононуклеоз, дифтерию глотки, микоплазменную инфекцию. При неясных результатах лабораторных анализов терапевт может направить пациента на офтальмологический осмотр.
 Лечение патологии
Лечение патологии
Медикаментозный курс, назначаемый врачами на фоне подтвержденного диагноза, основан на противовирусных препаратах. Стационарное или амбулаторное лечение лиц, страдающих от аденовируса, предполагает назначение глазных капель, мазей (накладываются на веко), жаропонижающих и противокашлевых средств. При поражении органов дыхания пациенту потребуются регулярные ингаляции и отхаркивающие препараты. Лечение осложненного аденовируса у детей и взрослых может потребовать применения антибиотиков.
Прогноз и профилактические меры
При неосложненном течении заболевания пациенты добиваются полного выздоровления за пять–семь дней. Осложненная форма аденовирусной инфекции может потребовать госпитализации ребенка или взрослого. В этом случае сроки выздоровления увеличиваются в 1,5–2 раза.
При резком росте инфицирования аденовирусом в детских садах или школах врачи рекомендуют проводить специфическую профилактику. Носителей вируса необходимо направить на амбулаторной или стационарное лечение. Все помещения образовательных учреждений следует обработать антисептическими растворами.
Диагностика и лечение аденовирусной инфекции в Москве
АО «Медицина» (клиника академика Ройтберга) обладает всем необходимым оборудованием для диагностики и лечения аденовирусной инфекции у детей и взрослых. Прием пациентов осуществляется в современном диагностическом комплексе, построенном с учетом последних достижений медицины.
Вопросы и ответы
Какой врач лечит аденовирусную инфекцию?
Лечение детей осуществляется под надзором педиатра. Взрослые могут обратиться к терапевту. При наличии показаний врач направит пациента на консультацию с офтальмологом или отоларингологом.
Существуют ли вакцины, стимулирующие выработку антител к возбудителям аденовирусной инфекции?
Нет, поскольку патогены группы Adenoviridae отличаются значительным разнообразием.
Аденовирусная инфекция
Аденовирусы человека впервые выделил У. Роу (1953) из миндалин и аденоидов детей, а затем у больных ОРВИ и атипичной пневмонией с явлениями конъюнктивита (Huebner R., Hilleman M., Trentin J. и др., 1954). В опытах на животных доказана онкогенная активность аденовирусов (Trentin J. и др., Huebner R. и др., 1962).
Что провоцирует / Причины Аденовирусной инфекции:
По способности агглютинировать эритроциты аденовирусы разделяют на 4 подгруппы (I-IV). Аденовирусы устойчивы во внешней среде, сохраняются до 2 нед при комнатной температуре, но погибают от воздействия ультрафиолетовых лучей и хлорсодержащих препаратов. Хорошо переносят замораживание. В воде при 4 °С сохраняют жизнедеятельность 2 года.
Естественная восприимчивость людей высокая. Перенесённое заболевание оставляет типоспецифический иммунитет, возможны повторные заболевания.
Основные эпидемиологические признаки. Аденовирусная инфекция распространена повсеместно, составляет 5-10 % всех вирусных болезней. Заболеваемость регистрируют в течение всего года с подъёмом в холодное время. Аденовирусные заболевания наблюдают как в виде спорадических случаев, так и в виде эпидемических вспышек. Эпидемические типы вирусов (особенно 14 и 21) обусловливают большие вспышки заболеваний среди взрослых и детей. Аденовирусный геморрагический конъюнктивит чаще возникает при инфицировании вирусом 3, 4 и 7 типов. Развитие случаев конъюнктивита связано с перенесённой респираторной аденовирусной инфекцией или же является результатом заражения вирусом через воду в плавательных бассейнах или открытых водоёмах. Чаще болеют дети раннего возраста и военнослужащие. Особенно высока заболеваемость во вновь сформированных коллективах детей и взрослых (в первые 2-3 мес); болезнь протекает по типу ОРВИ. В отдельных случаях возможно внутрибольничное инфицирование при проведении различных лечебных манипуляций. Заболевание у новорождённых и детей раннего возраста протекает по типу кератоконъюнктивита или поражения нижних отделов дыхательных путей. К редким аденовирусным поражениям относят менингоэнцефалиты и геморрагические циститы, чаще выявляемые у детей старшего возраста.
Патогенез (что происходит?) во время Аденовирусной инфекции:
При аэрозольном заражении возбудитель проникает в организм человека через слизистые оболочки верхних дыхательных путей и распространяется по бронхам в их нижние отделы. Входными воротами инфекции могут быть слизистые оболочки глаз, а также кишечника, куда вирус попадает при заглатывании слизи из верхних дыхательных путей. Вирус локализуется в клетках эпителия дыхательных путей и тонкой кишки, где происходит его размножение. В очагах поражения развивается воспалительная реакция, сопровождаемая расширением капилляров слизистой оболочки, гиперплазией подслизистои ткани с инфильтрацией мононуклеарными лейкоцитами и иногда кровоизлияниями в ней, что клинически проявляется ангиной, фарингитом, конъюнктивитом (часто плёнчатого характера), диареей. Иногда развивается кератоконъюнктивит с помутнением роговицы и нарушением зрения. Лимфогенным путём возбудитель проникает в регионарные лимфатические узлы, где происходят гиперплазия лимфоидной ткани и накопление вируса в течение инкубационного периода заболевания. В клинической картине эти механизмы обусловливают развитие периферической лимфаденопатии и мезаденита.
В результате подавления активности макрофагов и повышения проницаемости тканей в дальнейшем развивается вирусемия с диссеминацией возбудителя по различным органам и системам. В этот период вирус проникает в клетки эндотелия сосудов, повреждая их. При этом часто наблюдают синдром интоксикации. Фиксация вируса макрофагами в печени и селезёнке сопровождается развитием изменений в этих органах с увеличением их размеров (гепатолиенальный синдром). Вирусемия и репродукция возбудителя в клетках эпителия и лимфоидной ткани могут быть длительными.
Симптомы Аденовирусной инфекции:
Длительность инкубационного периода варьирует от 1 дня до 2 нед, чаще составляя 5-8 сут. Заболевание начинается остро с развития слабых или умеренных явлений интоксикации: озноба или познабливания, несильной и непостоянной головной боли, миалгий и артралгий, вялости, адинамии, снижения аппетита. Со 2-3-го дня болезни начинает повышаться температура тела, чаще она остаётся субфебрильной в течение 5-7 дней, лишь иногда достигая 38-39 °С. В редких случаях возможны боли в эпигастральной области и диарея.
При осмотре больных можно отметить гиперемию лица, инъекцию склер, иногда папулёзную сыпь на коже. Часто развивается конъюнктивит с гиперемией конъюнктивы и слизистым, но не гнойным отделяемым. У детей первых лет жизни и изредка у взрослых больных на конъюнктиве могут появиться плёнчатые образования, нарастает отёк век. Возможно поражение роговицы с образованием инфильтратов; при сочетании с катаральным, гнойным или плёнчатым конъюнктивитом обычно процесс сначала носит односторонний характер. Инфильтраты на роговице рассасываются медленно, в течение 1-2 мес.
Конъюнктивит может сочетаться с проявлениями фарингита (фарингоконъюнктивальная лихорадка).
Слизистая оболочка мягкого нёба и задней стенки глотки незначительно воспалена, может быть зернистой и отёчной. Фолликулы задней стенки глотки гипертрофированы. Миндалины увеличены, разрыхлены, иногда покрыты легко снимающимися рыхлыми беловатыми налётами разнообразной формы и размеров. Отмечают увеличение и болезненность при пальпации подчелюстных, нередко шейных и даже подмышечных лимфатических узлов.
Если воспалительный процесс дыхательных путей принимает нисходящий характер, возможно развитие ларингита и бронхита. Ларингит у больных аденовирусной инфекцией наблюдают редко. Он проявляется резким «лающим» кашлем, усилением болей в горле, охриплостью голоса. В случаях бронхита кашель становится более стойким, в лёгких выслушивают жёсткое дыхание и рассеянные сухие хрипы в разных отделах.
Период катаральных явлений иногда может осложниться развитием аденовирусной пневмонии. Она возникает через 3-5 дней от начала заболевания, у детей до 2-3 лет может начаться внезапно. При этом нарастает температура тела, лихорадка принимает неправильный характер и продолжается длительно (2-3 нед). Кашель становится сильнее, прогрессирует общая слабость, возникает одышка. Губы принимают цианотичный оттенок. При ходьбе одышка нарастает, появляется испарина на лбу, усиливается цианоз губ. По рентгенологическим признакам пневмония может быть мелкоочаговой или сливной.
У детей раннего возраста в тяжёлых случаях вирусной пневмонии возможны пятнисто-папулёзная сыпь, энцефалит, очаги некроза в лёгких, коже и головном мозге.
Патологические изменения со стороны сердечно-сосудистой системы развиваются лишь при редких тяжёлых формах заболевания. Характерны приглушение тонов сердца и мягкий систолический шум на его верхушке.
Поражения различных отделов дыхательных путей могут сочетаться с нарушениями со стороны ЖКТ. Возникают боли в животе и дисфункция кишечника (диарея особенно характерна для детей младшего возраста). Увеличиваются печень и селезёнка.
Аденовирусная инфекция чаще поражает детей и лиц среднего возраста. Заболевание в среднем продолжается от нескольких дней до 1 нед, но при длительной задержке вируса в организме возможно рецидивирующее течение, при этом инфекция затягивается на 2-3 нед.
По преобладанию тех или иных симптомов и их сочетанию выделяют несколько форм болезни:
• ОРВИ;
• ринофарингит;
• ринофаринготонзиллит;
• ринофарингобронхит;
• фарингоконъюнктивит (фарингоконъюнктивальная лихорадка);
• конъюнктивит и кератоконъюнктивит;
• пневмония и др.
Осложнения аденовирусной инфекции
Наиболее типичны отиты и гнойные синуситы, обструкция евстахиевой трубы у детей вследствие длительной гипертрофии лимфоидной ткани в глотке, ларингоспазм (ложный круп), вторичные бактериальные пневмонии, поражения почек. Прогноз заболевания обычно благоприятный.
Диагностика Аденовирусной инфекции:
В зависимости от клинической формы аденовирусной инфекции проводят дифференциальную диагностику с гриппом, группой ОРВИ, конъюнктивитами и кератоконъюнктивитами различной этиологии (в том числе дифтерийной), пневмониями, туберкулёзом.
Для аденовирусной инфекции характерны слабая или умеренная интоксикация и полиморфизм клинических проявлений в динамике заболевания: симптомы поражения дыхательных путей (фарингит, ларингит, бронхит), глаз (конъюнктивит, ирит), регионарная или распространённая лимфаденопатия, иногда экзантема, нарушения со стороны ЖКТ, гепатолиенальный синдром.
Лабораторная диагностика аденовирусной инфекции
Гемограмма при аденовирусных инфекциях не имеет существенных изменений, за исключением некоторого повышения СОЭ. Вирусологические исследования, основанные на выделении вируса из носоглоточных смывов, отделяемого глаз при конъюнктивитах (реже из испражнений), сложны и длительны, в широкой практике их не применяют. Обнаружение сывороточных антител проводят с помощью группоспецифичной РСК и типоспецифичных РТГА и РН. При постановке этих реакций с парными сыворотками, взятыми в острый период заболевания и период реконвалесценции, диагностически значимым считают нарастание титров антител не менее чем в 4 раза. Также применяют ИФА с групповым антигеном. Для ориентировочной экспресс-диагностики можно использовать РИФ и метод иммунной электронной микроскопии.
Лечение Аденовирусной инфекции:
При неосложнённом течении заболевания обычно ограничиваются проведением местных мероприятий: назначают глазные капли (0,05% раствор дезоксирибонуклеазы или 20-30% раствор сульфацила натрия). При гнойном или плёнчатом конъюнктивите и кератоконъюнктивите (исключая случаи с изъязвлениями роговицы!) за веко закладывают 1% гидрокортизоновую или преднизолоновую мазь. Рекомендованы витамины, антигистаминные препараты, симптоматические средства.
Тяжело протекающая аденовирусная инфекция требует усиления дезинтоксикационной терапии с внутривенным введением полиионных кристаллоидных и коллоидных растворов. Этиотропные препараты (антибиотики широкого спектра действия) назначают при осложнениях, вызванных вторичной бактериальной флорой, а также лицам преклонного возраста, страдающим хроническими заболеваниями дыхательной системы, и больным с проявлениями иммуносупрессии.
Профилактика Аденовирусной инфекции:
К каким докторам следует обращаться если у Вас Аденовирусная инфекция:
Крохотные курьеры: как аденоассоциированные вирусы спасают жизни
Крохотные курьеры: как аденоассоциированные вирусы спасают жизни
Авторы
Редакторы
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Вирусы и микроорганизмы» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Введение
Эта история началась в середине 1960-х, когда в препаратах аденовируса обезьян случайно было обнаружено загрязнение из маленьких неизвестных частиц [1]. Эти частицы были впоследствии названы аденоассоциированным вирусом (сокращенно ААВ, англ. adeno-associated virus, AAV). Тогда мало кто мог предположить, что именно эти крошечные вирусы дадут надежду многим неизлечимым больным. И лишь несколько исследовательских групп, движимых чисто научным любопытством, отправились изучать базовую биологию ААВ.
Прошло несколько десятков лет, и стало понятно, что ААВ обладает множеством уникальных свойств. Эти особенности позволяют использовать его в поистине революционном направлении — генной терапии. По разным оценкам, около 5% новорожденных детей страдает от различных генетических заболеваний [2]. Долгие годы такие болезни считались неизлечимыми, и для многих подобный диагноз приравнивался к приговору. К счастью, времена изменились. Мы находимся на пороге эры лекарств принципиально нового типа [3], и немаловажную роль в этом сыграл аденоассоциированный вирус [4].
Биология вируса
Какими же уникальными особенностями обладает ААВ? Чтобы ответить на этот вопрос, нужно подробнее поговорить про его жизненный цикл и строение.
Аденоассоциированный вирус принадлежит к роду Dependoparvovirus семейства Parvoviridae. Название рода отражает его необычный жизненный цикл, когда для размножения необходимо наличие вспомогательного вируса (от лат. Dependo — «зависеть»). В качестве такого вируса-помощника, как правило, выступает аденовирус (что явно следует из названия) или представители семейства герпесвирусов [5].
ААВ настолько безобиден, что помимо неспособности самостоятельно размножаться, он не вызывает никаких заболеваний человека и животных. Более того, согласно некоторым исследованиям, большинство людей (>70%) в течение жизни были заражены одним или несколькими серотипами ААВ [6]. (Серотип — вариант вируса, который отличается от других антигенами на своей белковой оболочке).
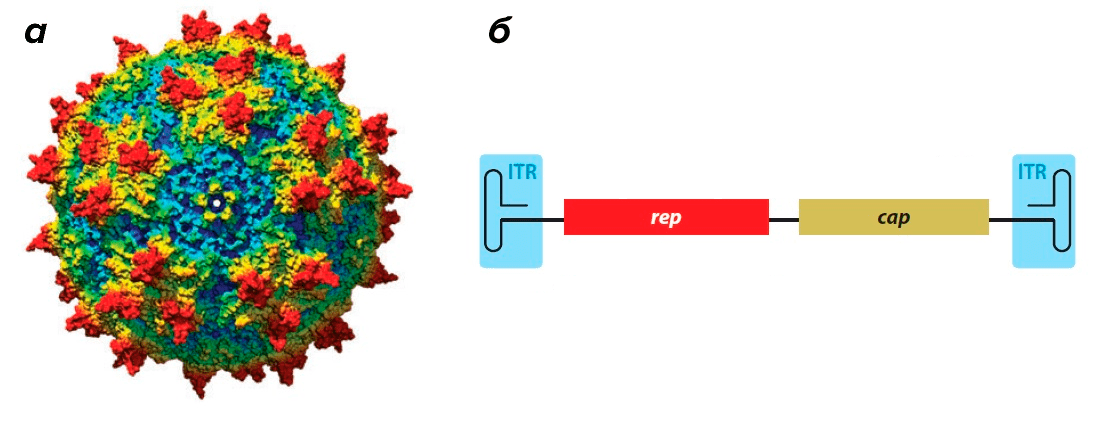
Вирус довольно мал — его икосаэдрическая белковая оболочка (капсид) в диаметре составляет всего около 25 нм (риc. 1а). Капсид необычайно стабилен: устойчив к кратковременному воздействию тепла, кислой среде и протеазам [7]. Геном, представленный одноцепочечной ДНК, по размерам также весьма скромен — всего 4,7 тысяч нуклеотидов [7].
Этот небольшой геном содержит минимальное количество генов. Ген rep (от слова replication) кодирует белки, необходимые для размножения вируса и его дальнейшей сборки внутри клетки (рис. 1б). Ген cap (от слова capsid) кодирует белки капсида (рис. 1б).
Геном ААВ обрамлен двумя Т-образными шпильками — инвертированными концевыми повторами (inverted terminal repeats, ITR) (рис. 1б).
Рисунок 1. Аденоассоциированный вирус. а — Модель капсида ААВ. б — Геном аденоассоциированного вируса. ITR (inverted terminal repeats) — инвертированные концевые повторы, образующие Т-образные шпильки; rep — ген, кодирующий белки, отвечающие за репликацию; cap — ген, кодирующий белки капсида.
Судьба вируса в клетке
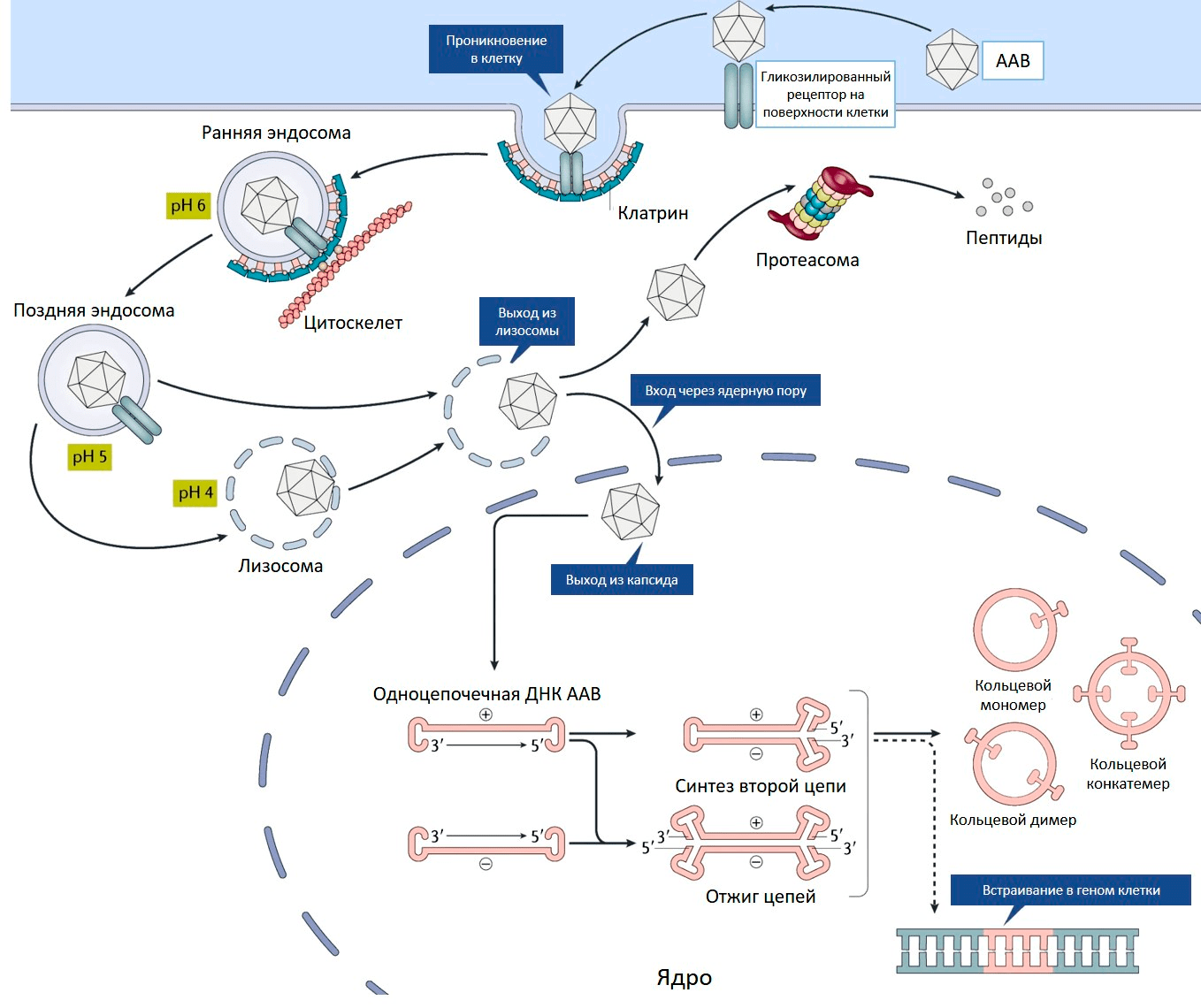
Ценное свойство ААВ — его способность проникать как в делящиеся, так и неделящиеся клетки [8]. На первом этапе аденоассоциированный вирус связывается с рецептором на поверхности клетки (рис. 2) [9]. Разные серотипы ААВ предпочтительно связываются со своими рецепторами, характерными для определенных типов клеток [10].
Рисунок 2. Проникновение ААВ внутрь клетки. Пояснения в тексте.
[9], рисунок с изменениями
И это важное свойство — определенный серотип преимущественно проникает лишь в конкретную ткань или орган, то есть обладает своим уникальным тропизмом.
Связывание вируса с рецептором запускает процесс проникновения внутрь клетки. Эндосома (мембранный пузырек, содержащий вирусную частицу) передвигается в цитоплазме по цитоскелету. Постепенно среда в эндосоме закисляется, что приводит к изменениям капсида, необходимым для дальнейшего успешного заражения клетки. После выхода из эндосомы у вируса два пути. Либо он попадает в клеточную машину по уничтожению белков (протеасому) и разрушается, либо переносится в ядро, где вирусный геном высвобождается из капсида (рис. 2) [10].
С одноцепочечного вирусного генома еще не могут нарабатываться белки, для этого необходимо достроить вторую цепь ДНК. Она синтезируется с помощью ДНК-полимеразы клетки-хозяина, используя шпильку ITR в качестве затравки для построения второй цепи.
Вирусные ITR помогают не только строить вторую цепь ДНК, но способствуют межмолекулярной и внутримолекулярной рекомбинации геномов вируса. В результате в ядре клетки образуются кольцевые молекулы ДНК — эписомы (рис. 2). В такой форме геномы ААВ могут в течение многих лет присутствовать в ядре [10].
Кроме того, геном ААВ может с низкой частотой встраиваться в определенный локус на 19 хромосоме человека [11]. Этот феномен обусловлен сходством последовательностей ДНК данного локуса и ITR вируса. У ААВ, лишенного гена rep, способность к встраиванию своего генома сильно снижена. Такие вирусные геномы присутствуют в клетках в виде эписом.
Модификация ААВ для применения в генной терапии
Если в гене человека произошла мутация, которая привела к развитию заболевания, то болезнь можно победить или облегчить, если доставить в клетки организма рабочую копию поломанного гена. Вот тут и выходит на сцену аденоассоциированный вирус.
Что же нужно было в нем изменить, чтобы он стал курьером для доставки таких терапевтических генов? Как это часто бывает в биологии, ученые просто воспользовались успешными решениями, уже созданными природой. Раз капсид ААВ сам по себе является ключом к входу в клетку и ядро, то можно смело этим воспользоваться. Остается только заменить гены самого вируса на гены, интересующие исследователя, и вирусный курьер готов!
Модификация генома ААВ
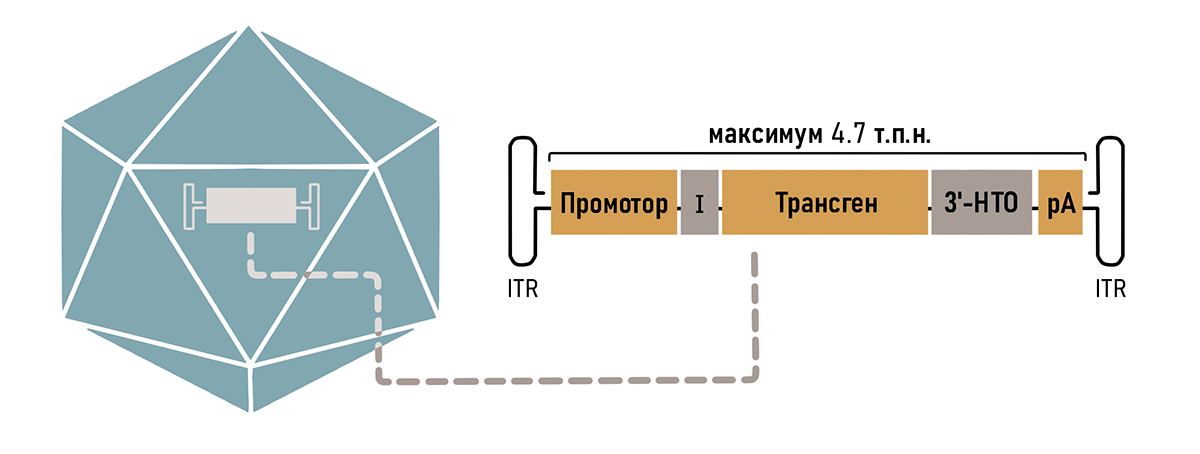
Оказалось, что от всего генома ААВ необходимо было оставить только концевые шпильки ITR, необходимые для сборки самого вируса и сохранения его генома в ядре (рис. 3) [12]. Таким образом, можно без последствий удалить до 96% генома ААВ, используя полученное пространство для кодирования нужных генов.
Так как ААВ вмещает в себя всего около 5000 пар нуклеотидов, то нужно очень тщательно продумать остальной состав кассеты. В первую очередь туда необходимо поместить рабочую копию гена (трансген), в зависимости от того генетического заболевания, на которое направлено лечение. Также обязательно наличие регуляторных последовательностей, таких как промотор и сигнал полиаденилирования (рис. 3). Разберем элементы кассеты подробнее.
Рисунок 3. Компоненты типичной кассеты ААВ вектора. Оранжевые блоки (промотор, трансген и сигнал полиаденилирования — рА) являются обязательными компонентами. Для повышения эффективности экспрессии могут быть включены необязательные регуляторные элементы, такие как интрон (I) и другие компоненты 3′-нетранслируемой области (НТО). Кассета обрамлена инвертированными терминальными повторами (ITR).
рисунок авторов статьи
Из-за ограниченной емкости вируса могут возникнуть трудности с доставкой больших терапевтических генов. Очевидное решение проблемы — разработка сокращенной версии гена, который кодирует усеченный, но функциональный белок. Создание таких укороченных генов требует глубокого понимания биологии терапевтического белка, взаимосвязи его структуры и функции. Такой подход уже успешно применяется в нескольких клинических испытаниях по лечению миодистрофии Дюшенна [13] (ссылки на клинические испытания: NCT03368742, NCT04281485, NCT03769116), в доклинических исследованиях по лечению дисферлинопатии, амавроза Лебера и многих других заболеваний.
Другим потенциально перспективным подходом для доставки слишком больших трансгенов может быть разделение гена между двумя ААВ-векторами [14]. Два этих векторных генома, попадая в одно и то же ядро клетки, могут подвергаться межмолекулярной рекомбинации с последующим восстановлением полноразмерного гена. Такой двухвекторный подход пока применяется лишь в редких клинических испытаниях (пример — NCT02710500). Низкая эффективность восстановления полноразмерного гена ограничивает более широкое применение этого приема.
Правильно выбранный промотор — во многом залог успешной генной терапии. Идеальный промотор должен запускать стабильную высокую экспрессию трансгена в пораженных органах в течение длительного периода, при этом быть неактивным в других тканях. Малая емкость ААВ также требует уменьшения размера промотора [15].
К кассету можно добавить необязательные элементы, способные улучшить экспрессию трансгена (рис. 3). Так, например, присутствие интрона повышает стабильность РНК в ядре [16], а также способствует эффективному транспорту мРНК из ядра в цитоплазму [17].
К обеспечению тканеспецифичности можно подойти с другой стороны — не только стимулируя экспрессию в целевых тканях, но и подавляя ее в нежелательных органах с помощью механизмов РНК-интерференции [18]. Для этого в 3′-НТО-кассеты добавляют сайты связывания микроРНК, присутствующих строго в нецелевых органах (рис. 3) [19]. Если трансген оказывается в нежелательном органе, то микроРНК связывается с комплементарными ей сайтами в транскрипте и запускает его деградацию.
Модификация капсида ААВ
Хотя капсид ААВ — сам по себе уже удачное изобретение природы, человечество не остановилось в своем научном поиске. Новые серотипы ААВ могут обладать рядом преимуществ:
Благодаря развитию новых методов анализа выделяют несколько основных направлений для создания или выявления новых серотипов.
К сожалению, всегда существует вероятность, что хорошо работающий in vitro модифицированный капсид в экспериментах на лабораторных животных продемонстрирует низкую эффективность или даже токсичность. Всестороннее изучение свойств разрабатываемых препаратов и строгий контроль качества призваны минимизировать риск неблагоприятного исхода исследований [23].
Применение ААВ в клинике
Целевые органы, на которые направлена терапия
К 14 декабря 2020 года 227 препаратов на основе ААВ проходят клинические испытания (по данным сайта ClinicalTrials.gov). Сегодня уже существует несколько препаратов на основе ААВ, которые получили одобрение от регулирующих органов для коммерческого использования у пациентов (подробнее про эти препараты можно почитать в [4]):
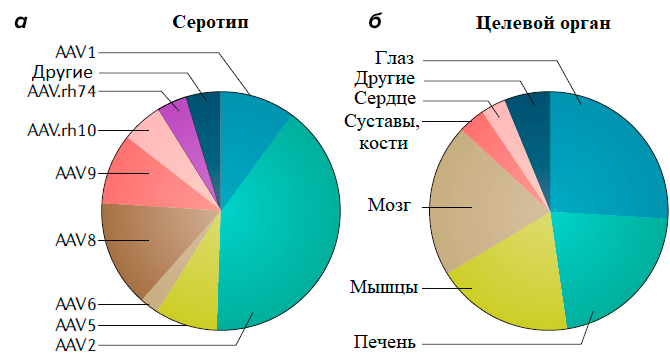
Большинство серотипов ААВ «предпочитают» проникать в такие органы, как печень, поперечно-полосатые мышцы и ЦНС, что и определило направление большинства программ генной терапии (рис. 4).
Рисунок 4. Данные с сайта ClinicalTrials.gov: на 13 ноября 2018 г. было зарегистрировано 145 клинических испытаний с использованием ААВ. а — Классифицикация клинических испытаний на основе примененного серотипа ААВ (AAV). б — Целевой орган, на который направлена терапия в указанных клинических испытаниях. Можно заметить, что спустя два года количество клинических испытаний с применением ААВ почти удвоилось (227 на сегодняшний день против 145 испытаний два года назад).
Почти все природные серотипы ААВ эффективно заражают печень после внутривенного введения. Благодаря данному свойству вируса в клинических испытаниях находятся препараты для лечения гемофилии A и B (NCT03392974, NCT03587116), семейной гиперхолестеринемии (NCT02651675), дефицита орнитинтранскарбамилазы (NCT02991144), мукополисахаридоза-IIIA (NCT03612869) и синдрома Криглера—Найяра (NCT03223194) [25].
Серотипы ААВ8 и ААВ9 могут эффективно заражать разные типы мышц по всему телу. Такое свойство делает их идеальными векторами для генной терапии множества мышечных заболеваний [26]. Так, активно исследуются в клинике препараты для лечения миодистрофии Дюшенна (NCT03375164), дисферлинопатии (NCT02710500), миотубулярной миопатии (NCT03199469), болезни Помпе (NCT03533673). Примечательно, что зараженная мышца может также служить биофабрикой для производства секретирующихся терапевтических белков для лечения немышечных заболеваний. Хотя большинство сердечных заболеваний полигенны и подвержены влиянию окружающей среды, ведется разработка препаратов генной терапии для лечения сердечной недостаточности [26].
Большой процент разрабатываемых препаратов на основе ААВ направлен на лечение неврологических и глазных болезней (рис. 4) [27], [28]. Глаз — весьма обособленный орган, обладающий уникальной иммунологической толерантностью, и легко доступный для прямого введения препарата. Нетрудно понять, почему один из первых одобренных препаратов, «Люкстурна», был направлен именно на лечение наследственной слепоты. Мозг, напротив, намного более крупный и сложно организованный орган. Прямая доставка препарата в мозг или спинномозговую жидкость позволяет локализовать вирус и снизить дозу препарата, но это инвазивная процедура, сопряженная со многими рисками. К счастью, такие серотипы, как ААВ9 или ААВrh.10, могут пересекать гематоэнцефалический барьер, что позволяет использовать рутинное внутривенное введение. В настоящий момент в клинических испытаниях уже находятся препараты для лечения болезни Паркинсона (NCT02418598), метахроматической лейкодистрофии (NCT01801709), болезни Баттена (NCT01414985), мукополисахаридоза 3 типа (NCT03300453).
Основные стратегии генной терапии на основе рААВ
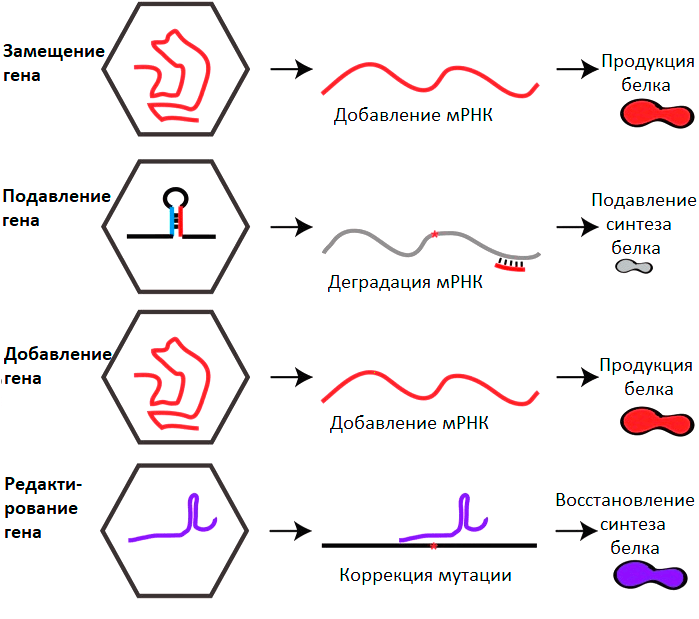
Можно выделить 4 глобальных направления генной терапии с применением ААВ (рис. 5).
Рисунок 5. Основные стратегии генной терапии на основе ААВ. Пояснения в тексте.
[29], рисунок с изменениями
Производство ААВ
Когда речь идет о клинических испытаниях, требуется очень большое количество вирусного препарата высокого качества. Его производство — весьма нетривиальная задача.
Вирусы не могут самостоятельно себя воспроизводить, им необходима помощь клеточной машинерии. Для наработки ААВ стали использовать культуры клеток. Вариантов может быть много: использование культуры дрожжей (Saccharomyces cerevisiae) [33], клеток насекомых (культура клеток Sf9 бабочки Spodoptera frugiperda) [34], человека — HEK293, HeLa. Некоторые из этих подходов, — скорее, экзотика, но использование культур клеток млекопитающих (HEK293) или насекомых (Sf9) уже прочно закрепилось на производстве.
Итак, для начала необходимо определиться с методикой производства, ведь от этого зависит, в чем будет расти сама культура. Вариантов масса: для клеток, растущих, прикрепившись к субстрату, это могут быть большие чашки Петри, специальные сосуды с множеством перегородок для увеличения площади поверхности (рис. 6а). Для культур, хорошо чувствующих себя в виде суспензии и при постоянном перемешивании, — колбы, герметичные пакеты и многое другое. При увеличении масштабов производства можно переходить на специальные биореакторы (рис. 6б). С их помощью можно следить за целой панелью важных для процесса параметров. Они делают производство более технологичным и позволяют увеличить объемы продукции до нескольких сотен литров вирус-содержащей суспензии за один цикл работы.
Рисунок 6. Производство ААВ: на культуральных чашках (а) и в биореакторе iCellis Nano (Pall corporation) (б)
фотографии авторов статьи
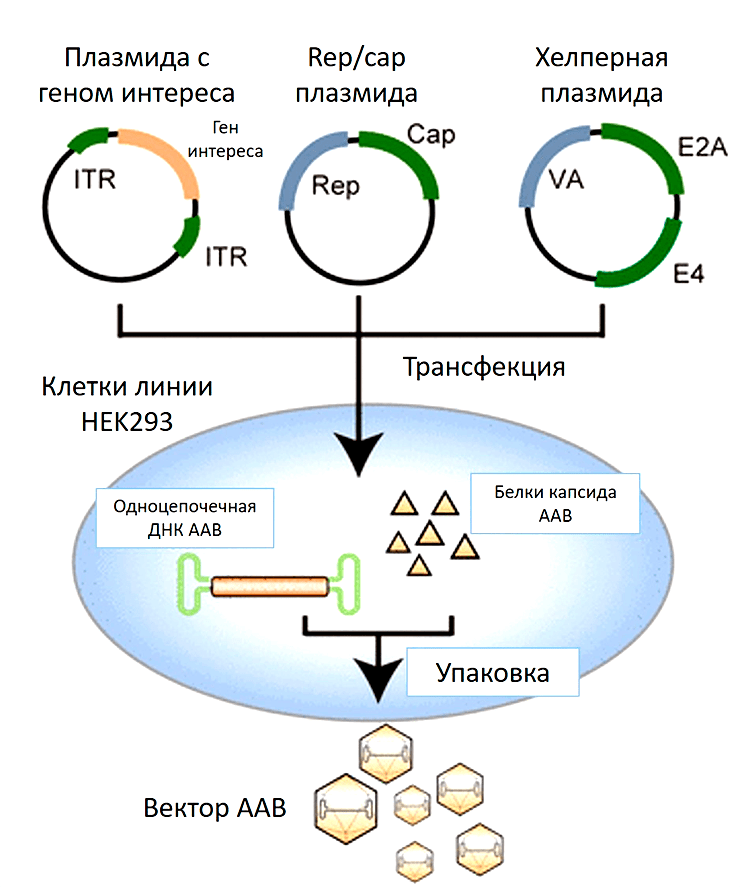
Что нужно сделать с культурой клеток, чтобы она стала биофабрикой по производству вирусных частиц? В такие клетки-производители вносят плазмидную ДНК, кодирующую необходимую для сборки вирусов информацию. Наиболее популярный протокол предполагает одновременное заражение клеток тремя плазмидами (рис. 7):
Кстати, вместо третьей плазмиды может быть добавлен сам вирус-помощник (аденовирус или герпесвирус), как это было в более ранних протоколах по производству частиц ААВ [35].
Рисунок 7. Производство ААВ, использующее в качестве клеток-производителей культуру клеток человека HEK293. Смесь трех плазмид доставляют внутрь клетки (плазмиду с терапевтическим геном, плазмиду, кодирующая гены rep/cap, и плазмиду с генами вируса помощника). Начинается наработка необходимых белков для сборки вирусных частиц. ДНК, содержащая терапевтический ген, упаковывается в готовый капсид ААВ.
Клетки начинают производить вирусные частицы, после чего их надо собрать и очистить.
Это критически важный этап, которому стоит уделить особое внимание [22], [23]. Любые примеси, которые будут содержаться в препарате, могут вызвать нежелательный иммунный ответ.
Вначале собирают сырой материал: это может быть клеточная среда, если вирусы выделяются клетками преимущественно в жидкость вокруг, а могут быть и сами клетки, если большинство вирусных частиц накапливается внутри. Как правило, это зависит от конкретного серотипа ААВ. Чтобы разрушить клеточные мембраны и высвободить вирус, клетки подвергают многочисленным циклам замораживания-оттаивания, ультразвуковой обработке или воздействию детергентов.
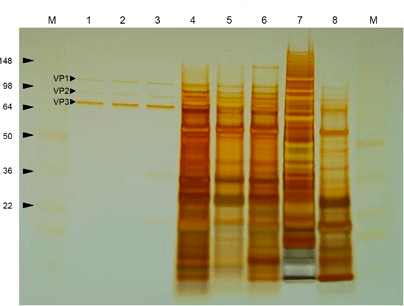
Теперь основная задача — очистить вирусные частицы от многочисленных примесей, находящихся в суспензии (рис. 8). В сыром материале находятся внутриклеточные свободные ДНК и РНК, белки и ферменты, крупные обломки клеточных мембран и многое другое. Способов очистки существует множество, и постоянно появляются как улучшенные версии уже применяемых методик, так и принципиально новые подходы. Все они различаются по уровням специфичности, эффективности и, разумеется, стоимости. Условно способы очистки можно разделить на серотип-специфичные и универсальные. К первой категории относится, например, аффинная хроматография [37], основанная на специфическом узнавании капсидов антителами. Ко второй — ультрацентрифугирование в градиентах плотности растворов йодиксанола или хлорида цезия, преципитация полиэтиленгликолем или сульфатом аммония, ионообменная хроматография и многие другие методы, основанные на общих физических свойствах вирусных частиц [38].
Рисунок 8. Окрашивание серебром очищенного (лунки 1–3) и загрязненного другими белками (лунки 4–8) препарата ААВ после гель-электрофореза [38].
Одна из неочевидных нежелательных примесей — так называемые пустые капсиды — вирусные частицы, не несущие в себе терапевтический ген, или содержащие внутри себя постороннюю ДНК. Дело в том, что изначально в клетке формируется пул пустых капсидов. Лишь потом ДНК связывается с пустым капсидом при помощи специальных сигналов на ITR и компактно упаковывается, формируя полноценную вирусную частицу. Но иногда пустой капсид может так и остаться пустым при нехватке вирусной ДНК или ее неэффективной упаковке. В пустой капсид может также упаковаться обрывок свободной ДНК, находящейся в клетке и содержащей последовательность, схожую с сигналом упаковки. Такие частицы (совсем пустые или несущие неправильную последовательность) не функциональны и подлежат удалению из очищаемого препарата. С определенной эффективностью их можно отделить от функциональных капсидов, используя градиенты плотности или методы хроматографии.
Основные проблемы
Наработка большого количества плазмид высокой степени очистки, поддержание культур клеток, дорогостоящие реактивы, сложный процесс очистки вирусных частиц и разработка аналитических методик для характеризации препаратов ведут к таким космическим ценам при масштабировании производства. На стоимость также влияет серьезный контроль качества вирусного препарата. Чтобы препарат вышел на рынок, проводятся исследования его токсичности, безопасности, биораспределения, эффективности. Оценивается содержание белковых примесей, бактериальных эндотоксинов, количество пустых капсидов, стерильность препарата, концентрация вирусных частиц в растворе и множество других характеристик [23]. В настоящий момент гиганты производств ААВ по всему миру работают над удешевлением препаратов, разрабатывая более эффективные протоколы сборки и очистки ААВ.
Иммунный ответ также представляет собой серьезную проблему. Потенциально иммунные реакции могут возникать на вирусный капсид, его геном, а также на белковый продукт трансгена. Препаратам на основе ААВ могут помешать нейтрализующие антитела к его капсиду [39]. Связываясь с вирусами в кровотоке, антитела препятствуют проникновению вирусных частиц в клетки, что ведет к низкой эффективности препарата. В настоящий момент обязательно проводится скрининг пациентов на наличие антител к применяемому серотипу ААВ [40]. В случае их обнаружения такой пациент исключается из клинических испытаний. Ведется разработка новых капсидов, которые не будут узнаваться нейтрализующими антителами [41]. После доставки терапевтических доз ААВ быстро развивается гуморальный иммунный ответ, который впоследствии помешает повторному введению препарата [42]. Именно поэтому большинство генотерапевтических препаратов на основе ААВ рассчитано на однократное введение. Для подавления Т-клеточного иммунного ответа у пациентов применяется фармакологическая супрессия стероидами [40].
Заключение
Генная терапия на основе ААВ — бурно развивающееся направление, и мы в данном обзоре затронули лишь небольшой кусочек этой удивительной области. Текущий экспоненциальный рост клинических испытаний с использованием ААВ предполагает, что мы находимся в самом начале эры новых генотерапевтических препаратов. Еще очень много задач предстоит решить, и для этого требуются мультидисциплинарные усилия. Дальнейшее развитие молекулярной биологии, биоинформатики, эпидемиологии, структурной биологии, иммунологии, геномики и других дисциплин, безусловно, будет способствовать совершенствованию технологии. Уже пройден длинный путь в попытке человечества победить генетические заболевания. Мы надеемся, что именно генная терапия приведет к окончательной победе!


 Механизм инфицирования
Механизм инфицирования Диагностические мероприятия
Диагностические мероприятия Лечение патологии
Лечение патологии