Анизоцитоз это признак чего
Анизоцитоз это признак чего
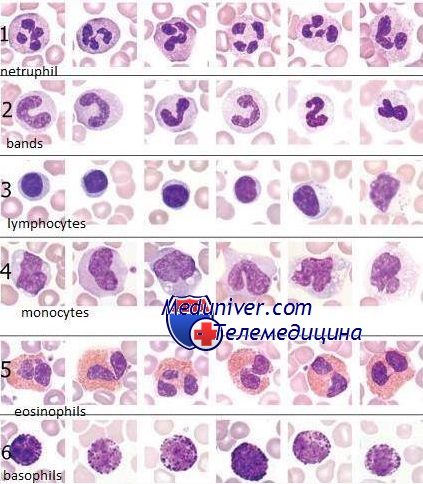
Морфологическое исследование эритроцитов, лейкоцитов, тромбоцитов и подсчет лейкоцитарной формулы производят в окрашенных мазках крови.
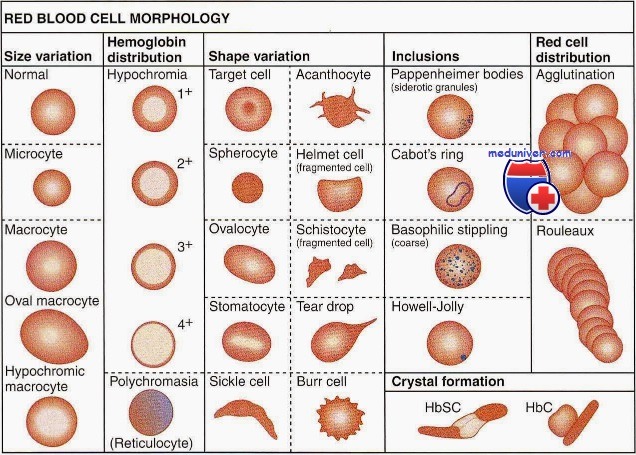
Качественная оценка эритроцитов имеет большое диагностическое и прогностическое значение. Обязательным является определение размеров и формы эритроцитов, их окраски, наличия и степени анизоцитоза и пойкилоцитоза, наличия патологических форм эритроцитов и включений в них.
При отсутствии автоматического анализатора для определения размеров эритроцитов измеряют их средний диаметр с построением эритроци-тометрической кривой Прайс-Джонса (гистограмма распределения эритроцитов по размеру). Диаметр нормальных эритроцитов в мазке равен 7-8 мкм, средний диаметр — 7,55 мкм.
Эритроциты размером более 8 мкм называются макроцитами (большие эритроциты с сохраненным просветлением в центре), более 12 мкм — мегалоциты или гигантоциты (гигантские эритроциты без просветления в центре). Эритроциты диаметром менее 6,5 мкм называются микроцитами, менее 2-3 мкм — шизоцитами. В норме в периферической крови выявляется 15,5% микроцитов и 16,5% макроцитов.
При использовании автоматического анализатора клеток крови проводится определение среднего объема эритроцитов (MCV), в зависимости от которого различают микроциты (MCV менее 75 мкм3), нормоциты (MCV в пределах 75-95 мкм3) и макроциты (MCV более 95 мкм3). На основании среднего объема эритроцитов строится эритроцитометрическая кривая.
Клиническое значение морфологического исследования клеток крови
При микроцитозе 30-50% от общего числа эритроцитов составляют микроциты. Микроцитоз наблюдается при ряде наследственных анемий (талассемии, гемоглобинопатии, микросфероцитоз, серповидноклеточная анемия, атрансферринемия, врожденная форма сидеробластной анемии).
Сдвиг эритроцитометрической кривой влево (увеличение количества эритроцитов малого диаметра) наблюдается при многих приобретенных анемиях (железодефицитные анемии, анемия хронических заболеваний, анемии при отравлении свинцом и др.).
При макроцитозе 50% и более от общего числа эритроцитов составляют макроциты. Макроцитоз чаще всего наблюдается при В12- и фолиеводефицитной анемиях.
Увеличение количества эритроцитов разного размера в мазке крови называется анизоцитозом. Это ранний признак анемии, наблюдающийся при ее легкой степени. Выделяют три степени анизоцитоза, которые обозначаются цифрами 1, 2 и 3.
Степень анизоцитоза эритроцитов (RDW — the Red cell Destribution Width) в современных гематологических анализаторах определяется автоматически. У здоровых людей большая часть эритроцитов (68%) представлена нормоцитами; микроциты составляют около 15%, макроциты — 17%. В норме RDW колеблется от 9,9 до 14,5%. При увеличении количества эритроцитов разного размера RDW нарастает.
В мазке крови большинство эритроцитов имеет округлую форму и только малая часть (до 10%) отличается по своей форме. Увеличение количества эритроцитов разной формы называется пойкилоцитозом. При этом эритроциты могут становиться овальными, грушевидными, звездчатыми, зазубренными и др.
Пойкилоцитоз является результатом продукции патологических клеток костным мозгом либо развивается вследствие повреждения нормальных клеток после выхода их из костного мозга в кровяное русло. Присутствие некоторых специфических форм эритроцитов (микросфероцитоз, эллиптоцитоз, стоматоцитоз) в большем количестве по сравнению с нормой имеет важное диагностическое значение.
Выделяют три степени пойкилоцитоза, которые также обозначаются цифрами 1, 2 и 3. Как и анизоцитоз, пойкилоцитоз является неспецифическим признаком любой анемии и отражает ее степень. Однако, в отличие от анизоцитоза, пойкилоцитоз появляется только при выраженной анемии и имеет более неблагоприятное прогностическое значение.
Эритроциты здоровых людей являются нормохромными, т. е. имеют равномерную окраску и небольшое (не более 1/3 диаметра клетки) просветление в центре. Гипохромия — увеличение центральной неокрашенной части эритроцита больше нормы. В зависимости от размеров просветления выделяют три степени гипохромии (1, 2, 3).
Усиленная окраска эритроцитов называется гиперхромией. Гиперхромия обусловлена увеличением объема эритроцитов и обычно сочетается с макроцитозом и мегалоцитозом. Более интенсивно окрашиваются микросфероциты.
В норме эритроциты окрашиваются кислыми красками, но молодые эритроциты с остатками ядерной субстанции (ретикулоциты) могут окрашиваться основными, приобретая различные оттенки серовато-сиреневого, серовато-фиолетового или серовато-голубого цвета. Эти клетки называются полихроматофилами. Полихроматофилия (полихромазия) — показатель усиленной регенерации костного мозга (наблюдается при гемолитических и постгеморрагических анемиях). В зависимости от числа полихроматофилов в поле зрения различают три степени полихромазии (1, 2, 3).
При различных состояниях в мазке крови могут обнаруживаться патологические формы эритроцитов (ядросодержащие — нормоциты), а также внутриэритроцитарные включения ядерного и цитоплазматического происхождения. Ядросодержащие эритроциты (синонимы: эритрокариоциты, нормоциты) в значительном количестве встречаются при гемолитических анемиях (прежде всего — гемолитическом кризе) и остром эритромиелозе (М6 по FAB-классификации).
Умеренный нормоцитоз наблюдается при постгеморрагических анемиях, сублейкемическом миелозе и метастазах злокачественных опухолей в костном мозге. Единичные нормоциты могут встречаться при В12-дефицитной анемии, миелодиспластических синдромах, хроническом миелолейкозе.
Среди внутриэритроцитарных включений ядерного происхождения различают тельца Жолли (круглые включения сине-фиолетового или вишнево-красного цвета диаметром 1-2 мкм), кольца Кебота (остатки ядерной оболочки в форме тонких нитеобразных колец, «восьмерки» или эллипса, окрашенные в красный цвет) и пылинки Вейденрейха (мелкая азурофильная, иногда голубая зернистость, чаще обнаруживается в мегалоцитах). Ядерные включения свидетельствуют о неэффективном эритропоэзе и встречаются при В12-дефицитных и гемолитических анемиях.
Кроме того, эритроциты с тельцами Жолли появляются после спленэктомии и при функциональной гипосплении и асплении у больных хроническими миелопролиферативными заболеваниями.
К внутриэритроцитарным включениям цитоплазматического происхождения относится базофильная пунктация (зернистость), которая представляет собой патологическую преципитацию вещества рибосом, перерожденных митохондрий и сидеросом и выглядит как точечная зернистость темно-синего цвета различной величины. Эритроциты с базофильной пунктацией встречаются при токсическом повреждении костного мозга (отравления свинцом, цинком, ртутью и др.), ряде анемий (талассемии, мегалобластные анемии), миелодиспластических синдромах и являются неблагоприятным прогностическим признаком.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Еще раз об анемии… Точная дифференциальная диагностика – залог успешного лечения
Куриляк О.А., к.б.н.
Анемией обозначается состояние, которое характеризуется снижением содержания в крови гемоглобина ( 3 4,5-11,0*10 9 /л
Дети до 2 лет: 0,4-1,0 мг/л (7 – 18,0 мкмоль/л)
Итак, на первом этапе в лаборатории следует повести анализ образца на гематологическом анализаторе. При выявлении снижения гемоглобина необходимо прежде всего определить характер анемии: гипо-, нормо- или гиперхромный. Критерием является величина МСН, отражающая, как известно, среднее содержание гемоглобина в эритроците.
Гипохромные анемии характеризуются низким значением МСН ( 95 фл). Значение MCHC тоже не выходит за пределы нормы, а снижение гемоглобина обычно обусловлено резким снижением количества эритроцитов с преобладанием фракции клеток с большим объемом (макроцитов). К данному типу анемий относят В12-дефицитную, фолиеводефицитную и аутоиммунную гемолитическую анемии.
Нормохромные анемии в большинстве случаев являются и нормоцитарными, т.е. все эритроцитарные индексы находятся в пределах нормы (см. Табл. 1). Причиной снижения гемоглобина в этих случаях является снижение общего количества эритроцитов. В группу нормохромно-нормоцитарных анемий входят анемии при острой кровопотере, а также разнообразные гемолитические анемии и анемии при костномозговой недостаточности.
МСН является аналогом цветового показателя (ЦП),который вычисляют в тех случаях, когда в лаборатории нет гематологического анализатора и подсчет эритроцитов осуществляется в камере Горяева. Нормальные значения ЦП находятся в пределах 0,85 – 1,0. Однако, в случае ошибочного подсчета числа эритроцитов, в частности занижения их количества (что при ручном подсчете случается достаточно часто!), цветовой показатель может оказаться близким к единице. Это может служить источником серьезной ошибки на начальном этапе диагностического поиска, которая повлечет за собой назначение необоснованных исследований, и, как следствие, существенно усложнит дифференциальную диагностику.
Алгоритм диагностического поиска при анемии
Гипохромно-микроцитарные анемии
Как было упомянуто выше, при выявлении у пациента гипохромного характера анемии в первую очередь следует заподозрить ЖДА (все ЖДА являются гипохромными!). Однако факт наличия гипохромной анемии сам по себе не исключает других патогенетических вариантов анемии, поскольку не все гипохромные анемии являются железодефицитными. Например, гипохромная анемия может возникать при нарушении синтеза гемоглобина в результате нарушения включения в его молекулу железа при нормальном или даже повышенном уровне железа в сыворотке крови (см. нарушение синтеза порфиринов). Поэтому для дифференциальной диагностики этих состояний следует в первую очередь провести исследование содержания железа в сыворотке. Причем, этот анализ надо выполнять обязательно до назначения больным лекарственных препаратов железа или проведения трансфузий эритроцитов.
Если уровень железа в сыворотке крови находится в пределах нормы или повышен, следует заподозрить у пациента анемию, связанную с нарушением синтеза порфиринов или талассемию и на следующем этапе диагностики целесообразно определить концентрацию ретикулоцитов. Выявление пониженного уровня железа в сыворотке крови однозначно указывает на необходимость определения других показателей обмена железа (ОЖСС и уровень ферритина).
При ЖДА этот показатель снижается (менее 15%), а при перегрузке железом значительно повышается (более 50%).
Еще одним высоко специфичным диагностическим признаком ЖДА является концентрация ферритина в сыворотке крови. Уровень ферритина отражает величину запасов железа в организме. Поскольку истощение запасов железа является обязательным этапом формирования ЖДА, то снижение содержания ферритина (менее 15 мкг/л) – характерный признак не только ЖДА, но и латентного дефицита железа. Однако этот показатель следует оценивать с осторожностью при сопутствующих острых воспалительных процессах, болезнях печени и некоторых опухолях. Дело в том, что ферритин принадлежит к классу острофазных белков и при перечисленных выше состояниях его синтез увеличивается, что при ЖДА может маскировать гипоферритинемию.
снижение содержания ферритина в сыворотке.
Клинический пример №1: У 34-летней женщины выявлена гипохромная микроцитарная анемия с очень низкими MCV (49,0 фл) и МCH (15.0 пг), а также существенно увеличенным значением RDW ( 21.3%).
Т. о., биохимические исследования подтвердили диагноз ЖДА.
После 10-дневного курса терапии пероральными препаратами железа отмечено увеличение RDW, а также появление на гистограмме распределения эритроцитов по объему второго пика в области нормоцитов (отмечен стрелкой).
Полученная кривая свидетельствует об адекватности назначенного лечения.
Таким образом, по данным гемограммы анемия отсутствует. Однако, в картине крови преобладают микроциты с низким содержанием гемоглобина. Наиболее вероятен диагноз – латентный дефицит железа.
2. Анемии при хронических заболеваниях (АХЗ) = железораспределитель-ные анемии
Среди микроцитарно-гипохромных анемий второе место по частоте после ЖДА занимают анемии при различных воспалительных заболеваниях как инфекционного, так и неинфекционного происхождения.
При всем многообразии патогенетических механизмов анемий в данных ситуациях одним из основных при АХЗ считается перераспределение железа в клетки макрофагальной системы, активирующейся при различных воспалительных или опухолевых процессах. Поступающее в организм и высвобождающееся из разрушающихся эритроцитов железо переходит, главным образом, в депо, где и накапливается в макрофагальных клетках в виде железосодержащего белка ферритина. В то же время, перенос железа из клеточного ферритина к трансферрину нарушен, что влечет за собой снижение уровня сывороточного железа. Развивается перераспределительный, или функциональный, дефицит железа вследствие накопления и блокады освобождения железа в тканевых макрофагах, что приводит к снижению доставки железа к эритрокариоцитам костного мозга, нарушению эритропоэза и развитию анемии. Поскольку истинного дефицита железа при этих АХЗ не наблюдается, более оправданно говорить не о железодефицитных, а о железоперераспределительных анемиях. Выделение железоперераспределительных анемий в отдельный патогенетический вариант имеет важное значение, так как при сходстве данного варианта с ЖДА терапевтические подходы при этих анемиях абсолютно различны.
Критерии железоперераспределительных анемий:
3. Анемии, связанные с нарушением синтеза порфиринов = сидероахрести-ческие анемии
Картина гемограммы при данном типе анемий аналогична таковой при ЖДА, поэтому для уточнения диагноза следует обращать пристальное внимание на биохимические показатели обмена железа (Табл.3).
Критериями сидероахрестических анемий являются:
Пациентку лечили препаратами железа. Эффекта не было. После проведения дополнительных исследований получены следующие результаты:
Поскольку при мегалобластном типе кроветворения соотношение лейкопоэз/эритропэз сдвигается в сторону эритропоэза, при анализе гемограммы обычно отмечается лейкопения и тромбоцитопения, которые носят умеренно выраженный характер. Нарушение процессов созревания гранулоцитарного ростка приводит к появлению в крови гигантских гиперсегментированных нейтрофилов.
На этапе синдромной диагностики основным методом является исследование костного мозга, при котором выявляется мегалобластический тип кроветворения с высоким уровнем неэффективного эритропоэза. Данное исследование должно проводиться до назначения витамина В12, т.к. иньекция В12 в течение 1-2 суток изменяет тип кроветворения в костном мозге. Мегалобласты уменьшаются в размерах, меняется структура ядра, клетки становятся макронормобластами. Только по присутствию гиганских форм нейтрофилов можно предположить, что имело место мегалобластическое кроветворение. При невозможности выполнить диагностическое исследование костного мозга допустимо пробное назначение витамина В12 с последующим обязательным исследованием количества ретикулоцитов через 3–5 дней (не позже), приобретающим диагностическое значение. Если анемия связана с дефицитом витамина В12, то под влиянием нескольких инъекций препарата происходит трансформация мегалобластического кроветворения в нормобластическое, что приводит к значительному увеличению в периферической крови количества ретикулоцитов по сравнению с исходным (ретикулоцитарный криз).
Окончательная верификация В12-дефицитного характера анемии может быть осуществлена с помощью исследования концентрации в крови витамина В12 (норма для взрослых: 148-616 пмоль/л, старше 60-ти лет: 81-568 пмоль/л).
Макроцитоз в комбинации с гиперсегментацией нейтрофилов и дефицитом витамина В12 подтверждают диагноз В12-дефицитной анемии.
Фолиево-дефицитные анемии
Фолиево-дефицитные анемии по своим гематологическим признакам (макроцитоз, мегалобластический эритропоэз) аналогичны В12-дефицитным анемиям. Отличительной особенностью является снижение в сыворотке крови уровня фолата (норма 6-20 нг/мл), а также снижение его концентрации в эритроцитах (норма 160-640 нг/мл).
Нормохромно-нормоцитарные анемии
1. Гемолитические анемии ГА
Основным патогенетическим механизмом развития гемолитической анемии (ГА) является укорочение продолжительности жизни эритроцитов (в норме в среднем 120 дней) и их преждевременный распад под воздействием различных причин.
Критерии ГА:
Большинство ГА являются нормохромными, за исключением ГА, связанной с нарушением синтеза глобина (талассемия), которая, как было отмечено выше, является гипохромной. Основным лабораторным признаком, позволяющим заподозрить ГА, является повышение в крови количества ретикулоцитов, в связи с чем данный анализ следует считать обязательным при всех неясных анемиях. Фактически ретикулоцитоз встречается в двух ситуациях, при которых активируется нормальный эритропоэз – при гемолизе и острых кровопотерях. Наряду с ретикулоцитозом при интенсивном гемолизе в крови обнаруживаются ядросодержащие эритроидные клетки (эритрокариоциты), обнаруживаемые в норме только в костном мозге. Наличие или отсутствие гипербилирубинемии определяется, с одной стороны, интенсивностью гемолиза, а с другой – функциональной способностью печени связывать билирубин с глюкуроновой кислотой и экскретировать его в желчь. Поэтому нормальные показатели содержания билирубина в крови не исключают гемолиза. При некоторых ГА, сопровождающихся внутрисосудистым гемолизом (болезнь Маркиафавы, аутоиммунные ГА), в крови увеличивается содержание свободного гемоглобина, выделяющегося с мочой в виде гемосидерина. Последний может быть обнаружен в моче с помощью бензидиновой пробы (аналогичной исследованию скрытой крови в кале) или при окраске осадка мочи на выявление гемосидерина. Эти информативные тесты должны чаще использоваться в лабораторной практике при подозрении на внутрисосудистый гемолиз.
Наследственные ГА связаны с различными генетическими дефектами, в частности с дефектом мембраны эритроцитов (наследственный микросфероцитоз, овалоцитоз), дефицитом некоторых ферментов в эритроцитах (глюкозо-6-фосфат-дегидрогеназа, пируваткиназа и др.), нарушением синтеза цепей глобина (талассемия), наличием нестабильных гемоглобинов.
Среди приобретенных ГА наиболее распространенными являются аутоиммунные ГА (симптоматические и идиопатические). Симптоматические аутоиммунные ГА возникают на фоне лимфопролиферативных заболеваний (хронический лимфолейкоз, лимфогранулематоз и др.), системных васкулитов (системная красная волчанка, ревматоидный артрит), хронического активного гепатита, некоторых инфекций, в частности, вирусных, при приеме ряда медикаментов (альфа-метилдопа). Если причина аутоиммунного гемолиза не выявляется, то говорят об идиопатических ГА. К приобретенным ГА относятся болезнь Маркиафавы (перманентный внутрисосудистый гемолиз), микроангиопатические ГА (гемолиз вследствие ДВС-синдрома на фоне различных заболеваний), механический гемолиз при протезированных сосудах и клапанах сердца, маршевой гемоглобинурии, ГА при воздействии различных токсических веществ (уксусная кислота, мышьяк и др.).
При наличии соответствующих подозрений уточнению причины ГА, т.е. нозологической диагностике, могут способствовать следующие исследования:
2. Анемии при костномозговой недостаточности
В основе данного патогенетического варианта анемий лежит нарушение нормальной продукции эритроидных клеток в костном мозге. При этом часто одновременно с угнетением эритропоэза имеется нарушение продукции клеток гранулоцитарного и тромбоцитарного ростков, что отражается на составе периферической крови (панцитопения) и служит ориентиром в распознавании возможного механизма развития анемии.
Критерии анемии при костномозговой недостаточности:
Ключевой особенностью, позволяющей предположить данный патогенетический вариант анемий, является нарушение со стороны других ростков костного мозга (гранулоцитопения, тромбоцитопения), что может проявляться соответствующей клинической симптоматикой в виде инфекционных осложнений (часто отмечается только лихорадка) или геморрагического синдрома (зависит от выраженности тромбоцитопении). Уместно напомнить, что при В12-дефицитной анемии также может наблюдаться лейко- и тромбоцитопения, однако цитопении при этом выражены умеренно и обычно не сопровождаются описанными симптомами.
Анемия при костномозговой недостаточности может возникать при следующих заболеваниях и патологических процессах: острые и хронические лейкозы; метастазы злокачественных опухолей в костный мозг; замещение костного мозга фиброзной тканью (миелофиброз) вследствие различных причин; замещение костного мозга жировой тканью (апластическая анемия) вследствие различных причин; изолированное угнетение продукции эритроидных клеток костного мозга, чаще иммунной природы (парциальная красноклеточная анемия); миелодиспластический синдром (гетерогенная группа гематологических нарушений, одними из которых являются так называемые рефрактерные анемии).
Фактически с помощью исследования костного мозга (цитологического, гистологического) при данном патогенетическом варианте осуществляется нозологическая диагностика, хотя часто требуется уточнение формы и причины выявленных изменений.
В основе развития анемии может лежать так называемый миелодиспластический синдром (МДС), который является результатом приобретенного дефекта стволовой клетки-предшественницы миелопоэза, что приводит к нарушению нормальной дифференцировки клеток различных ростков костного мозга (эритроидного, гранулоцитарного, тромбоцитарного). В результате этого гемопоэз оказывается неэффективным, что в конечном счете проявляется цитопениями в различных сочетаниях. Неэффективность эритропоэза позволяет трактовать анемию при МДС как следствие костномозговой недостаточности. Основным признаком, позволяющим заподозрить МДС, является бедность клетками периферической крови в сочетании с высокой клеточностью костного мозга и признаками дисплазии всех ростков кроветворения. МДС встречается почти исключительно у больных пожилого и старческого возраста, характеризуется анемией, рефрактерной к лечению препаратами железа, витамином В12, фолиевой кислотой, повышением в костном мозге эритроидных клеток, содержащих железо (рефрактерная анемия с сидеробластами).
3. Анемия при уменьшении массы циркулирующих эритроцитов
Данный патогенетический вариант анемии отличается от остальных и характеризуется уменьшением количества эритроцитов и гемоглобина за счет уменьшения массы циркулирующей крови. Основной причиной развития данного варианта анемий являются острые кровопотери различной локализации.
Основные признаки анемии при уменьшении массы эритроцитов:
Железодефицитная анемия у детей
Почему при ЖДА необходимы препараты железа? В чем преимущества препаратов последнего поколения? Почему прием препаратов железа должен быть длительным? Картина крови при хронической железодефицитной анемии. Выраженные гипохромия эритроци
Почему при ЖДА необходимы препараты железа?
В чем преимущества препаратов последнего поколения?
Почему прием препаратов железа должен быть длительным?
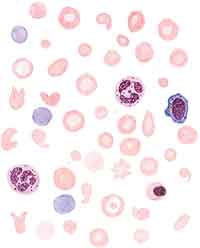 |
| Картина крови при хронической железодефицитной анемии. Выраженные гипохромия эритроцитов, анизоцитоз, пойкилозитоз, шизоцилы, присутствие полихроматофилов |
Анемия — это патологическое состояние, характеризующееся снижением массы эритроцитов, часто в сочетании с уменьшением количества эритроцитов в единице объема крови. Причин возникновения анемий очень много; для детского же возраста наиболее типична железодефицитная анемия (ЖДА). ЖДА характеризуется наличием небольших гипохромных эритроцитов и истощением запасов железа в организме.
Распространенность дефицита железа у детей в раннем возрасте, по данным ВОЗ, составляет от 17,5 до 30%.
Можно выделить следующие причины развития дефицита железа у детей.
Важно отметить, что у детей раннего возраста причинами дефицита железа, как правило, являются недостаточное депо железа и нерациональное питание, а у детей старшего возраста — кровопотеря и резкое вытяжение.
Патофизиологические аспекты
Поскольку всасывание железа ограничено, у большинства людей его поступление с пищей едва покрывает текущую потребность организма, в результате заболеваний или неправильного питания довольно легко развивается дефицит железа. Этот процесс состоит из нескольких стадий.
Стадия 1. Потеря железа превышает его поступление. На фоне отрицательного баланса железа его запасы в костном мозге постепенно истощаются. Хотя уровень железа в сыворотке и количество гемоглобина остаются нормальными, содержание ферритина в сыворотке уменьшается (ниже 20 нг/мл). По мере истощения запасов железа происходит компенсаторное повышение концентрации трансферрина (о чем свидетельствует увеличение железосвязывающей способности).
Стадия 2. Истощенные запасы железа уже не обеспечивают эритропоэтическую функцию костного мозга. В то время как уровень трансферрина в плазме растет, содержание железа в сыворотке снижается, что приводит к его всевозрастающей нехватке при образовании эритроцитов. Эритропоэз нарушается, когда уровень железа ниже 50 мкг%, а насыщение трансферрина — ниже 16%. Возрастает концентрация рецепторов ферритина в сыворотке (более 8,5 мг/л).
Стадия 3. Анемия при внешне нормальных эритроцитах и эритроцитарных индексах.
Стадия 4. Развитие микроцитоза и затем гипохромии.
Стадия 5. Дефицит железа сопровождается симптомами тканевых нарушений.
Клинические проявления
Представление о клиническом статусе больного с анемией зависит от основного заболевания и формы анемии (острой или хронической). ЖДА — состояние хроническое. Проявление анемии per se объясняют с помощью патофизиологических механизмов. Большинство симптомов ЖДА являются отражением сердечно-сосудистых и газообменных изменений, компенсирующих уменьшение массы эритроцитов. Степень выраженности симптомов зависит от скорости развития анемии (при медленном развитии анемии, характерном для железодефицитных состояний, времени для полного развития компенсаторных механизмов достаточно) и ее длительности. Даже анемия средней тяжести нередко протекает бессимптомно. Ребенок может жаловаться на усталость, одышку и сердцебиение, особенно после физической нагрузки. При тяжелой анемии симптоматика сохраняется и в состоянии покоя, больной не может переносить физические нагрузки. Если уровень гемоглобина менее 75 г/л, то минутный сердечный выброс в покое заметно повышается по мере увеличения как частоты сердечных сокращений, так и ударного объема. Симптомы сердечной недостаточности развиваются, когда резерв миокарда исчерпан. Следовательно, тяжесть состояния больного определяется прежде всего степенью выраженности сердечно-сосудистых нарушений.
Симптоматика при анемии средней и тяжелой степени распространяется и на другие системы органов. Больной часто жалуется на головокружение и головные боли, шум в ушах, возможен даже обморок. Человек становится раздражительным, нарушается сон, снижается концентрация внимания. Поскольку кровоток в коже снижен, может развиваться гиперчувствительность к холоду. Возникает симптоматика и со стороны желудочно-кишечного тракта — резкое снижение аппетита, диспепсические расстройства (тошнота, изменение характера и частоты стула), прежде всего это происходит за счет шунтирования крови, минующей сосудистое русло внутренних органов. У девочек-подростков нарушается менструальный цикл, что проявляется в виде аменореи или обильного кровотечения.
Основной признак анемии — бледность кожных покровов. Однако его информативность ограничена другими факторами, определяющими цвет кожи.
Поэтому наиболее информативным признаком анемии является бледность видимых слизистых — слизистой оболочки полости рта, ногтевого ложа и конъюнктивы век. Информативным также считается цвет кожи на сгибах ладонной поверхности — если по цвету они не отличаются от окружающей кожи, то уровень гемоглобина у больного, как правило, менее 80 г/л.
Развитие бледности кожных покровов при анемии объясняется двумя факторами: первый — это, несомненно, уменьшение уровня гемоглобина в крови, второй — шунтирование крови в обход сосудов кожи и других периферических тканей, способствующее усиленному кровоснабжению жизненно важных органов. Перераспределение кровотока представляет собой один из важных механизмов компенсации анемии.
Из других клинических симптомов анемии следует отметить уже упоминавшиеся выше тахикардию, значительные колебания пульсового давления, систолический шум изгнания над предсердиями, снижение умственной и физической активности, дети становятся раздражительными, быстро утомляются, их сон беспокойный, аппетит снижен.
При ЖДА к обычным симптомам анемии присоединяются признаки, специфичные для недостаточности железа. При длительном дефиците железа появляются извращенные аппетит (поедание мела, грязи, красок) и обоняние (нравятся резкие запахи бензина, красок, лаков, поедание льда (пагофагия), развиваются глосситы, хейлит, койлонихия (истонченные, исчерченные, ломкие ногти). При дефиците железа падает активность иммунной системы за счет снижения синтеза ИЛ-2, Т-киллеров; дети чаще болеют ОРВИ, что, в свою очередь, усугубляет имеющийся дефицит железа.
Диагноз подтверждается лабораторными данными. Критерием диагностики ЖДА является анемия микроцитарная, гипохромная, норморегенераторная. Для ЖДА характерны анизоцитоз, тромбоцитоз, снижение уровня сывороточного железа (менее 13 ммоль/л), общая железосвязывающая способность сыворотки не изменена или повышена, уровень сывороточного ферритина менее 15 нг/мл, насыщение трансферрина меньше 16%, уровень протопорфирина эритроцитов повышен, уровень Hb A2 снижен, в костном мозге отмечается раздражение красного ростка (эритроциты : гранулоциты = 1:1 — 1:2), типично отсутствие в костном мозге запасов железа и кольцевидных сидеробластов.
В дифференциально-диагностический поиск включаются талассемия, отравление свинцом, анемия при хронических заболеваниях, врожденные нарушения обмена железа (дефицит трансферрина, нарушение утилизации железа, нарушение реутилизации железа), гемосидероз, в том числе синдром Гудпасчера, дефицит меди.
Принципы лечения ЖДА у детей
Диетотерапия при ЖДА у детей
В настоящее время общепризнано, что устранить дефицит железа в организме только с помощью диетотерапии невозможно. Это связано с тем, что всасывание железа из пищевых продуктов ограничено — 1,8-2 мг (не более 2,5 мг) железа в сутки — даже при рациональном питании, соответствующем возрасту, и при потреблении достаточного количества продуктов с высоким содержанием железа. (Для сравнения: здоровый ребенок в зависимости от возраста теряет за сутки от 0,15 до 0,6 мг железа, девочка во время месячных — 15-50 мг) При приеме современных препаратов железа оно усваивается в 20 раз лучше. Диетотерапия должна быть одной из составляющих терапии ЖДА у детей.
С другой стороны, очень важно ориентироваться не на содержание железа в продуктах питания, а на его форму. Именно форма железа определяет процент его всасывания и усвоения и, следовательно, эффективность терапии. Из различных форм железа легче всего усваивается гемовое железо — сложное органическое соединение, в котором железо находится в составе гемоглобина; неорганические соединения — соли железа — усваиваются организмом значительно хуже. Железо в составе гема активно захватывается клетками слизистой кишечника и всасывается в неизмененном виде. Процессы всасывания гема в кишечнике не зависят от кислотности среды и активности пищевых ферментов. Железо из злаков, овощей, фруктов всасывается значительно хуже из-за присутствия в них ингибиторов ферроабсорбции, таких, как оксалаты, фосфаты, танин и другие. Сравните: коэффициент усвояемости железа из говядины (гемовое железо) составляет 17-22%, из фруктов — не более 3%. Степень усвояемости железа из продуктов животного происхождения также зависит от формы железосодержащих соединений. Так, из печени, где соединения железа представлены в виде ферритина и трансферрина, железо усваивается в значительно меньшем количестве, чем из мясных продуктов, хотя общее содержание железа в печени в 3 раза больше, чем в мясе. Поэтому включение печени в рацион питания для устранения дефицита железа или с профилактической целью не имеет никакого смысла. Таким образом, рацион питания должен быть максимально богат продуктами, в которых железо содержится в виде гема (язык говяжий, мясо кролика, говядина).
Необходимо отметить также, что мясо, печень и рыба улучшают всасывание железа из фруктов и овощей при одновременном их употреблении.
Всасываемость железа из злаковых, бобовых, клубневых, овощей, фруктов значительно ниже, поскольку железо в них содержится в негемовой форме, и во многом зависит от содержания в рационе веществ, ингибирующих или потенцирующих всасывание железа. Усиливают всасывание негемового железа аскорбиновая кислота, продукты из мяса, птицы, рыбы, а также вещества, понижающие кислотность пищи (например, молочная кислота). Снижают усвоение негемового железа соевый протеин, полифенолы, входящие в состав чая, кофе, орехов и бобовых. Несмотря на высокое содержание железа в некоторых продуктах растительного происхождения, они не могут обеспечить высокую потребность в железе, характерную для растущего организма, поскольку железо из них всасывается значительно хуже, чем из продуктов животного происхождения. Рекомендации употреблять в больших количествах фруктовые соки, яблоки, гранаты, гречневую крупу и другие продукты в целях восполнения депо железа при ЖДА также нельзя считать обоснованными. Сбалансированная по основным ингредиентам диета позволяет «покрыть» только физиологическую потребность организма ребенка в железе, но никак не устраняет дефицита железа и должна использоваться в комплексе с препаратами железа при лечении ЖДА. Однако полноценная и сбалансированная диета занимает важное место в профилактике развития дефицита железа в организме ребенка во все периоды детства.
Медикаментозная терапия при ЖДА
Основной задачей терапии ЖДА является устранение дефицита железа в организме ребенка. Это достигается благодаря приему железосодержащих лекарственных препаратов. Основные требования, предъявляемые к препаратам железа, — это достаточное содержание в них элементарного железа и отсутствие побочных эффектов и осложнений. В настоящее время на фармацевтическом рынке России достаточный выбор препаратов железа, что расширяет возможности врача и позволяет учитывать индивидуальные особенности пациентов при назначении лечения (табл. 1). В частности, появились удобные формы для детей младшего возраста — капли и сироп (феррум лек, мальтофер, актиферрин, гемофер).
Все препараты зарегистрированы и разрешены к применению в Российской Федерации.
Современные препараты железа разделяют на две группы:
Усвояемость железа из лекарственного препарата зависит от содержания в нем элементарного (активного) железа. Наибольшее количество элементарного железа содержится в препаратах, в которых железо представлено в виде фумарата (ферретаб, ферронат) или сульфата двухвалентного железа (актиферрин, ферро-фольгамма, гемофер пролангатум, ферро-градумет). В настоящее время появились препараты железа нового поколения, к которым относятся лекарственные средства, представленные гидроксид-полимальтозным комплексом трехвалентного железа (мальтофер, феррум лек). Особенностью этих препаратов является то, что поступление железа из кишечника в кровь происходит путем активного всасывания в отличие от солевых соединений железа, всасывание которых происходит по градиенту концентрации. Это важно, поскольку исключается возможность передозировки препаратов железа, содержащих гидроксид-полимальтозный комплекс трехвалентного железа.
Солевые препараты железа в просвете кишечника взаимодействуют с компонентами пищи и с другими лекарствами, что затрудняет абсорбцию железа. Поэтому эта группа препаратов железа назначается за час до еды. Однако на фоне выраженного свободнорадикального стресса, возникающего при взаимодействии железа со слизистой кишечника во время его диффузии, усиливается повреждающее действие на слизистую кишечника соединений железа, что проявляется диспепсическими расстройствами, вплоть до некроза слизистой. При плохой переносимости солевых препаратов железа их можно принимать и во время еды, что уменьшит побочные проявления, но и всасывание железа в свою очередь будет ухудшаться. Солевые препараты железа нельзя запивать чаем, молоком и сочетать их с приемом некоторых медикаментов (тетрациклинов, левомицетина, препаратов кальция, антацидов, пеницилламина), поскольку при этом снижается усвояемость железа.
Препараты неионного железа, как показывают проведенные исследования, не взаимодействуют с компонентами пищи и лекарствами, что позволяет использовать эти препараты, не нарушая режима питания детей (препараты можно добавлять в пищу, соки) и схемы терапии сопутствующей патологии (если есть необходимость в проведении такого лечения).
Суточная терапевтическая доза препаратов железа должна быть достаточной для нормализации уровня гемоглобина и восполнения запасов железа в костном мозге, что составляет для солевых препаратов железа 3-6 мг/кг/сут элементарного железа в два-три приема. Гидроксид-полимальтозный комплекс железа (феррум лек) назначается в дозе 3-6 мг/кг/сут в один или несколько (по желанию пациента) приемов.
Побочные реакции при приеме препаратов железа
Наиболее часто при лечении ферропрепаратами наблюдаются следующие побочные явления (табл. 2): металлический привкус во рту, потемнение эмали зубов, аллергические высыпания на коже, диспепсические нарушения в результате раздражающего действия на слизистую пищеварительного тракта, прежде всего кишечника (жидкий стул, тошнота, рвота). Поэтому начальные дозы препаратов должны составлять 1/2-1/3 терапевтической с последующим увеличением их до полной дозы в течение нескольких дней во избежание возникновения выраженных побочных действий. При непереносимости солевого препарата его можно заменить гидроксид-полимальтозным комплексом железа, в результате применения которого не возникает вышеописанных эффектов. Гидроксид-полимальтозный комплекс железа можно сразу применять в полной дозе. Неионные препараты железа не вызывают перечисленных выше побочных эффектов, чувство переполнения желудка также отмечается редко.
Парентеральное введение препаратов железа
Парентеральное введение препаратов железа проводится только по строгим показаниям из-за развития выраженных местных и системных побочных эффектов. Показания таковы: патология пищеварительного тракта (синдром нарушенного кишечного всасывания, неспецифический язвенный колит, хронический энтероколит, желудочно-кишечное кровотечение) и непереносимость железосодержащих препаратов при пероральном приеме.
Противопоказаниями к назначению препаратов железа являются анемии, не обусловленные дефицитом железа (гемолитические, апластические), гемосидероз, гемохроматоз.
Продолжительность курса лечения
Клинический и терапевтический эффекты при пероральной ферротерапии развиваются постепенно. Через некоторое время появляется клиническое улучшение: уменьшается слабость, исчезает головокружение, ребенок становится более активным, повышается аппетит, постепенно розовеют кожные покровы и видимые слизистые. На 8-10-й день терапии отмечается ретикулоцитарный криз — до 5%, что подтверждает эффективность лечения. Позже наблюдается повышение уровня гемоглобина, чаще всего нормализация гемоглобина происходит на 3-6-й неделе от начала терапии и зависит от степени тяжести анемии. В среднем уровень Hb повышается на 10 г/л за 10 дней. Однако нормализация уровня гемоглобина не является признаком устранения дефицита железа. Для полного восполнения депо железа в организме курс ферротерапии должен составлять не менее 3 месяцев.
Причины неэффективности ферротерапии
Неэффективность терапии на фоне приема препаратов железа при их хорошей переносимости может быть обусловлена следующими факторами:
ЖДА — это заболевание, при правильной терапии которого наступает полное выздоровление!