Антигистаминные препараты при кашле у детей для чего
ТОП лекарств от кашля
Кашель – защитная рефлекторная реакция организма, направленная на очищение закупоренных или раздраженных дыхательных путей. Половая принадлежность, возраст и генетика в данном случае значения не имеют. Лающий, мучительный, с мокротой или без нее, возникающий в течение всего дня, только в определенное время суток или при употреблении определенных продуктов – существуют совершенно разные типы кашля. Он может быть разделен, во-первых, по продолжительности (острый и хронический кашель), а во-вторых, по отношению к выделяемому секрету (сухой, продуктивный и кровохарканье).
Чтобы подобрать лучшее средство от кашля, следует обратиться к врачу. Только специалист, после проведения обследования и постановки диагноза, может назначить эффективный препарат, который не только устраняет симптом, но и борется с причиной его возникновения.
Какие виды кашля бывают
Сухой (раздражающий)
Называется непродуктивным или кашлем без мокроты. Вызван раздражением дыхательных путей. Острый сухой кашель может возникать, например, в начале бронхита, при небольших легочных эмболиях (закупорка легочного кровеносного сосуда), плеврите, а также при вдыхании раздражающих газов, пыли и других инородных тел.
Хронический сухой кашель может быть вызван, например, хроническим насморком или хронической синусовой инфекцией, рефлюксной болезнью и астмой. Кроме того, хронический сухой кашель также может быть побочным эффектом ингибиторов АПФ (сердечно-сосудистых средств).
Продуктивный (кашель с мокротой)
Сопровождается большим количеством слизистого образования. Слизь в основном прозрачная. Желтоватая мокрота, отходящая из нижних дыхательных путей, связана с воспалительными клетками. Зеленоватый бронхиальный секрет указывает на бактериальную инфекцию.
Острый продуктивный кашель может возникать, например, в рамках пневмонии, а также на более поздней стадии острого бронхита. Хронический продуктивный кашель может быть признаком хронического бронхита или ХОБЛ (хронической обструктивной болезни легких).
Кровохарканье
Причины возникновения кашля
Существует много провоцирующих факторов. Перед назначением лекарственной терапии назначается комплексное обследование для уточнения причины. Самолечение в данном случае недопустимо, т. к. может привести к развитию необратимых последствий для здоровья.
Простуда
Поражение верхних дыхательных путей вирусами. Обычно сопровождается кашлем, насморком, заложенностью носа и общим ухудшением самочувствия. Если не начать лечить кашель на данном этапе, то происходит прогрессирование патологического процесса и развитие поражения верхних дыхательных путей или легких.
Грипп
Респираторная вирусная инфекция протекает тяжелее простой простуды. Болезнь начинается очень внезапно с высокой температурой, головной и мышечной болью. Также присоединяется боль в горле с затруднением глотания. При гриппе чаще всего возникает сухой кашель. Иногда пациенты также страдают от тошноты.
Хронический синусит
Сопровождается в основном сухим кашлем, который усиливается в положении лежа. Воспалительный процесс часто распространяется и на слизистую оболочку носовой полости, поэтому сопровождается хроническим насморком.
Бронхит
Воспаление респираторного тракта, которое часто сопровождается мучительным кашлем. При остром бронхите сначала возникает сухой, позже продуктивный кашель. Кроме того, у больных отмечается насморк и боль в горле. Диагноз хронический бронхит ставится тем, у кого был ежедневный кашель и мокрота в течение как минимум 3 месяцев подряд по 2-3 эпизода в год. Часто курение является причиной хронического бронхита.
Пневмония
Плеврит
Острое воспаление легких. Возможные причины включают инфекции, рак и легочную эмболию. Сухая форма плеврита сопровождается раздражающим кашлем, сильной, односторонней и болью в груди при вдохе.
Воздействие раздражающих факторов
При попадании жидкости или пищи в трахею, а не в пищевод, возникает сухой раздражающий кашель – организм пытается снова транспортировать инородные тела вверх к полости рта. То же самое происходит при вдыхании или проглатывании инородных тел.
Аллергия
Кашель, связанный с аллергией, может возникать, например, при аллергии на плесень, пищевой аллергии и аллергии на пылевые клещи. Люди с аллергией на пыльцу (сенная лихорадка) позже часто дополнительно заболевают астмой, для чего кашель и одышка являются первыми признаками.
Бронхиальная астма
Астма является широко распространенным хроническим заболеванием с воспалением и сужением дыхательных путей. Пациенты страдают преимущественно сухим кашлем (даже ночью) и судорожной одышкой.
Хроническая обструктивная болезнь легких (ХОБЛ)
Дыхательные пути в легких хронически воспалены и сужены. Возникающий дискомфорт – это в первую очередь хронический кашель с мокротой, а также одышка при нагрузке. Основной причиной ХОБЛ является курение.
Коллапс легких (пневмоторакс)
Приводит к болезненному накоплению воздуха между внутренней и внешней легочной оболочкой. Причиной этого является, например, разрыв легочных пузырьков или травма легких. При коллапсе внезапно появляется боль в области груди, которая может иррадиировать в спину. Также усиливается нехватка воздуха.
Легочная эмболия
Рак легких
Подразумевает наличие различных злокачественных наростов. Упорный кашель является относительно ранним симптомом карцином, но также может указывать на многие другие заболевания. У некоторых пациентов также возникает кровохарканье. Основной причиной рака легких является курение.
Редкие причины
Некоторые лекарства могут вызвать хронический сухой кашель в качестве побочного эффекта, который часто возникает приступами. Речь идет о ингибиторах АПФ и бета-блокаторах. Обе группы лекарственных средств служат сердечно-сосудистыми препаратами и назначаются при сердечной недостаточности и гипертонии. Кроме того, прием противовоспалительного кортизона также может вызвать кашель.
У детей хронический кашель часто возникает из-за повышенной чувствительности дыхательных путей после вирусной инфекции и при рефлюксе кислотного содержимого желудка в пищевод. Причиной может стать отток слизи из носовых ходов в горло. Редкими причинами кашля у детей являются вдыхание инородных тел и кистозный фиброз.
Классификация препаратов от кашля
Лекарства дают при кашле только в том случае, если это абсолютно необходимо, или дискомфорт сильно влияет на состояние пациента. Поскольку кашель – это не болезнь, а симптом, перед его лечением обязательно следует диагностировать основное заболевание. Особенно длительный кашель может быть симптомом серьезного нарушения в организме. По этой причине перед составлением диагноза обязательно следует избегать препаратов, угнетающих кашель.
Таблица – Классификация препаратов от кашля
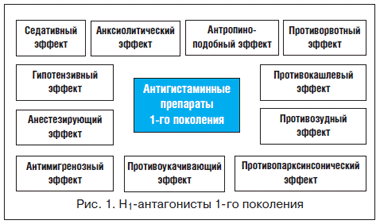
Механизмы эффективности антигистаминных препаратов первого поколения при ОРВИ
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
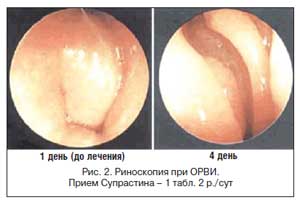
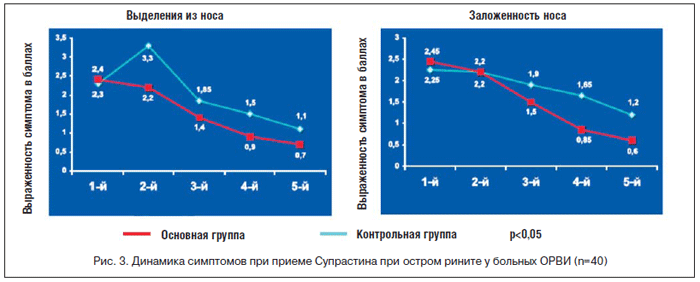
Использование антигистаминных препаратов при «простуде» (острых респираторных вирусных инфекциях – ОРВИ) базируется на данных об их эффективности как в естественных, так и экспериментальных условиях. В ряде публикаций показано, что антигистаминные препараты I поколения способны уменьшать ринорею, отек слизистой носа и чихание при ОРВИ, а также общую тяжесть заболевания. Эти свойства обнаружены у таких антигистаминных препаратов I поколения, как бромфенирамин, хлорфенирамин и хлоропирамин (Супрастин). Так, эффективность Супрастина при ОРВИ изучена в клинике ЛОР–болезней ММА имени И.М. Сеченова проф. С.В. Морозовой. В исследовании приняли участие 20 больных с острым неосложненным ринитом в возрасте 20–55 лет. Эффективность терапии оценивали по выраженности чихания и ринореи, а также инфильтрации и гиперемии слизистой носа (по данным риноскопии). Монотерапия Супрастином способствовала сокращению продолжительности заболевания до 2–3 дней. Тяжесть симптомов также уменьшалась, больные обходились без применения сосудосуживающих капель. У ряда больных отмечалась сонливость. Осложнений ринита не возникло ни в одном случае.
Несмотря на известную эффективность антигистаминных препаратов I поколения при ОРВИ, механизмы их действия оставались малоизученными.
Отдельные симптомы ОРВИ вызываются множественными, иногда специфичными для различных симптомов, механизмами воспаления. Чихание обычно объясняли выбросом гистамина из назальных тучных клеток и базофилов, который происходит при активации этих клеток во время ОРВИ. В качестве доказательства приводили факт, что интраназальное введение здоровым людям гистамина (но не других медиаторов) вызывает чихание. Известно также, что лечение антигистаминными препаратами I поколения высокоэффективно уменьшает чихание при ОРВИ и в обычных, и в экспериментальных условиях. Тем не менее, в отличие от аллергического ринита, при ОРВИ уровень гистамина в назальном секрете не повышен, хотя чувствительность слизистой оболочки носа к гистамину при ОРВИ возрастает.
Антигистаминные препараты как I, так и II поколения являются конкурентными антагонистами гистамина на уровне H1–рецепторов. Кроме этого, в отличие от препаратов II поколения, антигистаминные препараты I поколения проявляют конкурентный антагонизм в отношении ацетилхолина на уровне нейрональных и нейромышечных мускариновых рецепторов, а также проникают через гематоэнцефалический барьер. В ограниченных исследованиях было показано, что антигистаминные препараты II поколения не способны уменьшать чихание при ОРВИ.
Эти данные поставили перед исследователями вопрос о том, благодаря каким механизмам антигистаминные препараты I поколения (Супрастин и др.) способны уменьшать ринорею, отек слизистой носа и чихание при ОРВИ, и почему этот эффект не свойствен препаратам II поколения. Исследования ОРВИ в естественных условиях связаны с определенными техническими трудностями. Так, сложно набрать пациентов с начальными стадиями заболевания, когда можно наиболее точно оценить эффективность лечения. Поэтому следовало бы подтвердить результаты исследований антигистаминных препаратов при ОРВИ, проведенных в естественных условиях, с помощью экспериментальной риновирусной инфекции, позволяющей точно оценить чихание. Такое исследование было проведено P.S. Muether и J.M. Gwaltney, которые изучали эффекты лоратадина – антигистаминного препарата II поколения при экспериментальной риновирусной инфекции.
Материалы и методы
В исследование было включено 66 взрослых добровольцев, у которых титры антител к риновирусу 16 типа не превышали 2 единиц, и не переносивших ОРВИ или другое заболевание с лихорадкой за последнюю неделю. Кроме того, исключались пациенты с любыми серьезными сопутствующими заболеваниями, бронхиальной астмой, аллергическим ринитом; принимавшие в последнее время (в соответствии с особенностями их фармакокинетики) антигистаминные препараты, средства от простуды и другие препараты, которые могут оказать влияние на результаты исследования.
Риновирусную инфекцию вызывали путем двукратного (с перерывом в 20 мин) интраназального введения стандартизированной культуры риновируса 16 типа. Смывы из полости носа для последующей идентификации вируса получали за 8 дней и непосредственно перед инфицированием (для исключения случайного инфицирования «диким» штаммом риновируса), а также каждое утро перед приемом препарата. Нейтрализующие типоспецифические антитела определяли в анализах крови за 7 дней до инокуляции и через 2–3 недели после нее.
Симптомы болезни (чихание, выделения из носа, заложенность носа, боль в горле, кашель, головная боль, слабость, озноб) за предшествующие сутки пациенты оценивали по 5–балльной шкале: 0 – отсутствие симптома, 1 – слабый, 2 – умеренный, 3 – выраженный, 4 – очень выраженный. Общая тяжесть симптомов вычислялась, как сумма оценок всех симптомов. Оценка тяжести болезни также включала ежедневные измерения назальной секреции. Каждый пациент записывал в дневник частоту чихания и кашля. Наличие и тяжесть побочных действий оценивали ежедневно.
Пациентов двойным слепым методом рандомизировали в группы лоратадина или плацебо. Лоратадин или плацебо назначали с 1–го по 13–й день исследования, инокуляцию вируса производили на 8–й день.
Из 66 включенных в исследование пациентов 34 получали лоратадин, а 32 – плацебо. Четыре человека из группы лоратадина и один из группы плацебо заразились «диким» штаммом риновируса в начале исследования, поэтому их данные не оценивались. Один человек из группы плацебо прекратил его прием из–за появления мигрени на 10 день. Таким образом, оценивались данные 60 человек.
После инокуляции вирус определялся в назальном секрете у 28 (93%) человек из группы лоратадина и у 24 (80%) в группе плацебо; прирост типоспецифических антител отмечен у 40% и 37%, соответственно. Общая частота инфицирования составила 97% и 80% (различия недостоверны).
Средние титры вирусов не отличались между группами. Согласно критерию Джексона, заболевание развилось у 23 (79%) из 29 инфицированных в группе лоратадина и у 14 (58%) из 24 инфицированных в группе плацебо (различия недостоверны).
Выраженность чихания не отличалась между группами в первые 3 дня и была несколько меньше в группе плацебо в 4–й день. Выраженность заложенности носа, боли в горле, кашля и общая тяжесть симптомов также не отличались между группами. Головная боль и недомогание были меньше при приеме лоратадина в заключительные дни исследования. Ринорея была меньше в группе плацебо на 2–3 день, но больше – на 4–5 день. При объективном измерении объема назальной секреции наблюдалась тенденция к большему ее объему в группе лоратадина (различия недостоверны).
Побочные эффекты отмечены в группе плацебо: 2 случая рвоты и 1 случай мигрени.
Таким образом, не было обнаружено различий между группами лоратадина и плацебо по частоте инфицирования риновирусом и развития болезни, а также по выраженности симптомов.
Результаты показали также отсутствие терапевтического эффекта лоратадина в отношении чихания. Это подтверждает публикации, в которых показано, что антигистаминные препараты II поколения не способны уменьшать чихание при ОРВИ. Почему же антигистаминные препараты I поколения эффективны в отношении чихания, а препараты II поколения – нет?
Антигистаминные препараты I поколения блокируют не только Н1–рецепторы, но и мускариновые рецепторы, а также проникают через гематоэнцефалический барьер. Последние два свойства не присущи антигистаминным препаратам II поколения.
Информация о неврологических механизмах рефлекса чихания получена в основном из опытов на животных. Дуга рефлекса включает периферические нервы и продолговатый мозг, в ней участвуют гистаминовые Н1–рецепторы, мускариновые и никотиновые рецепторы. При ОРВИ рефлекс запускается инфекционным поражением клеток слизистой оболочки. Вовлечения тучных клеток и базофилов с последующим выбросом гистамина при ОРВИ не отмечается, но происходит стимуляция свободных нервных окончаний этмоидальной ветви тройничного нерва воспалительными медиаторами, такими как брадикинин. Затем нервный импульс по афферентным волокнам проходит в чувствительное ядро тройничного нерва и прилегающий центр чихания. Через синапс импульс достигает верхнего слюнного ядра лицевого нерва и, пройдя еще один синапс, по преганглионарным веточкам поступает в клиновидно–небный ганглий. Затем по постганглионарным волокнам возбуждение передается мускариновыми синапсами на слизистые железы и кровеносные сосуды. В результате секреция и экссудация стимулируют окончания тройничного нерва и импульс вновь направляется в центр чихания в продолговатом мозге. При достаточной силе сигнала возбуждение передается респираторным нейронам ретикулярной формации, а от них по волокнам блуждающего, диафрагмального и межреберных нервов через никотиновые синапсы – дыхательным мышцам, участвующим в акте чихания.
Гистамин потенциально может вовлекаться в процесс чихания в нескольких участках рефлекторной дуги, которые, следовательно, могут быть точками приложения для антигистаминных препаратов. Первый из них – слизистая оболочка носа, где Н1–рецепторы присутствуют на свободных нервных окончаниях тройничного нерва. Против того, что эффект антигистаминных препаратов при ОРВИ реализуется на уровне слизистой оболочки, говорят нормальные уровни гистамина в назальном секрете при ОРВИ, а также отсутствие эффекта от антигистаминных препаратов II поколения, которые достигают слизистой оболочки и блокируют в ней Н1–рецепторы. Но поскольку чувствительность слизистой оболочки носа к гистамину при ОРВИ возрастает, полностью исключить эту точку приложения антигистаминных препаратов при ОРВИ нельзя.
Следующая точка приложения для антигистаминных препаратов I поколения – продолговатый мозг, где происходит ряд синаптических переключений рефлекса чихания. В этих зонах обнаружены Н1– и мускариновые рецепторы. Эти никотиновые рецепторы могут быть мишенями для антигистаминных препаратов I поколения, проникающих через гематоэнцефалический барьер. Следует учитывать, что медиаторы синапсов продолговатого мозга, вовлеченных в рефлекс чихания, пока не идентифицированы. Неэффективность антигистаминных препаратов II поколения при ОРВИ подтверждает возможную важную роль названных нервных центров.
Парасимпатическая стимуляция секреции желез и вазодилатации опосредована исключительно мускариновыми рецепторами. На этом уровне вполне вероятно приложение антихолинергической активности, присущей антигистаминным препаратам I поколения. Действительно, они уменьшают объем назальной секреции при ОРВИ. Второй афферентный импульс в продолговатый мозг также обусловлен стимуляцией окончаний тройничного нерва. Экссудация из сосудов вызывает запуск кининовой системы. Образовавшиеся кинины стимулируют нервные окончания как сами по себе, так и приводя к выбросу гистамина из тучных клеток, что являет собой новую мишень для антигистаминных препаратов. Когда возбуждение достигает продолговатого мозга, оно может быть подавлено антигистаминными препаратами I поколения (как описано выше). Далее передача импульса зависит от никотиновых рецепторов и не чувствительна к антигистаминным препаратам.
Можно заключить, что терапевтический эффект антигистаминных препаратов I поколения при чихании в значительной мере может быть обусловлен блокадой Н1– и мускариновых рецепторов в продолговатом мозге. Н1–рецепторы присутствуют в большом количестве и в гипоталамусе, где гистамин, как нейротрансмиттер, участвует в поддержании бодрствования и в ряде других функций. С этим фактом может быть связана сонливость, вызываемая антигистаминными препаратами I поколения.
Антигистаминные препараты I поколения, как и скополамин (антихолинергический препарат, проникающий через гематоэнцефалический барьер), способны уменьшать тошноту при болезнях движения (укачивании). Это еще раз наталкивает на мысль о важной роли мускариновых рецепторов в центральной нервной системе.
Лечение ОРВИ антигистаминными препаратами I поколения (Супрастин и др.), в отличие от препаратов II поколения, высокоэффективно уменьшает такие симптомы, как ринорея, отек слизистой носа и чихание. Хотя информации о тонких нейротрансмиттерных механизмах этого явления пока и недостаточно, можно считать, что это происходит благодаря активности антигистаминных препаратов I поколения в отношении Н1–гистаминовых и мускариновых рецепторов, а также их способности проникать через гематоэнцефалический барьер.
Современные аспекты применения антигистаминных препаратов у детей
Опубликовано в журнале:
«РМЖ »№ 14, 2015 К.б.н. С.С. Сологова, к.ф.н. В.В. Тарасов
ГБОУ ВПО «Первый МГМУ имени И.М. Сеченова» Минздрава России
Антигистаминные средства – это лекарственные средства, полностью или частично угнетающие действие гистамина. Гистамин является одним из важнейших медиаторов различных физиологических и патологических процессов в организме, в т. ч. аллергических реакций. Освобождение гистамина из гранул тучных клеток происходит под действием различных физических и химических раздражителей, но наиболее активно – при взаимодействии аллергена с антителами на поверхности тучных клеток. Гистамин, высвобождаемый тучными клетками в ходе аллергических реакций, взаимодействует преимущественно с Н1-рецепто-рами. Повышение его концентрации вызывает спазм гладких мышц и бронхов, расширение кровеносных сосудов, увеличение проницаемости сосудистой стенки, выход плазмы из сосудистого русла, отек тканей, снижение артериального давления и т. д. [1, 2].
В течение последних лет увеличивается число больных с бронхиальной астмой (БА), аллергическими ринитами, атопическим дерматитом (АД). Эти состояния, как правило, не являются жизнеугрожающими, однако требуют активного терапевтического вмешательства, которое должно быть эффективным, безопасным и хорошо переносимым пациентами.
Целесообразность применения антигистаминных препаратов при различных аллергических заболеваниях (крапивнице, АД, аллергическом рините, конъюнктивите и др.) обусловлена широким спектром эффектов гистамина [2, 3].
Блокаторы Н1-рецепторов предупреждают развитие и облегчают течение аллергических реакций. Данная группа лекарственных препаратов предотвращает или устраняет избыточные физиологические эффекты эндогенного гистамина в организме путем снижения его концентрации в тканях, а также с помощью блокады гистаминовых рецепторов. Большинство используемых антигистаминных средств обладают рядом специфических фармакологических свойств, таких как противоаллергическое, противозудное, противоэкссудативное, антиспастическое, антихолинергическое, седативно-снотворное и др., а также уменьшают проницаемость капилляров, предупреждают развитие отека тканей, снимают спазмы гладкой мускулатуры [2, 3].
История создания и применения антигистаминных препаратов начинается с 1930х г г. и тесно связана со временем, когда в 1907 г. был осуществлен синтез гистамина из имидазолпропионовой кислоты [Windaus А., Vogt W.]. В 1910 г. гистамин был извлечен из спорыньи [4]. Тогда же был показан путь образования гистамина из гистидина под влиянием фермента декарбоксилазы [Ackermann D.].
В этом же году было установлено фармакологическое действие гистамина на животных, что позволило рассматривать его как важный физиологический медиатор. Серия исследований, выполненных в 1920-е гг., позволила сформулировать представление о том, что гистамин является важнейшим посредником таких аллергических проявлений, как анафилактический шок, риниты, БА, крапивница [5].
C этого момента стало очевидным, что средства, обладающие противогистаминным действием, должны со временем стать широко используемыми противоаллергическими лекарственными препаратами. В 1937 г. после синтеза D. Bovet и А. Staub первых антагонистов гистамина появилось понятие «гистаминовый рецептор». При взаимодействии с такими рецепторами гистамин реализует свою биологическую активность [6]. Изучаемые D. Bovet и А. Staub вещества хотя и обладали антигистаминными свойствами, но не могли быть еще использованы в клинической практике из-за их высокой токсичности. В 1942 г. В.N. Halpern получены первые антигистаминные вещества, применимые у человека: фенбензамин и пириламин малеат [7–9].
Вслед за этим стали появляться новые противогистаминные препараты, доступные для использования в клинике. Позже очень большая группа этих средств получила название противогистаминных препаратов 1-го поколения (или классических антигистаминных препаратов). В 1966 г. получены доказательства гетерогенности клеточных рецепторов гистамина, а затем сформулировано понятие о гистаминовых рецепторах 1-го и 2-го типов (Н1- и Н2-рецепторы) и показано, что стимуляция последних ответственна за желудочную секрецию соляной кислоты. Позже были описаны Н3- и Н4-рецепторы. Н3-рецепторы выполняют функцию чувствительных к гистамину пресинаптических рецепторов, представленных в основном в головном мозге на гистаминергических нервах, и являются ауторецепторами, регулирующими синтез и высвобождение гистамина из пресинаптических нервных окончаний. Есть также данные о том, что эти рецепторы могут участвовать и в гетерорецепторной пресинаптической модуляции высвобождения других медиаторов (норадреналина, допамина, ацетилхолина, 5-гидрокситриптамина).
Недавно идентифицированный Н4-рецептор, родственный Н3-рецептору, представлен в костном мозге, тимусе, на моноцитах и гранулоцитах периферической крови, в селезенке, легких, печени, кишечнике. Хотя функция этого рецептора изучена пока недостаточно, можно с уверенностью считать, что он вовлекается в разные иммунологические реакции организма. Например, Н4-рецептор участвует в хемотаксисе и мобилизации ионов Са 2+ в тучных клетках, в контроле вызванной гистамином секреции интерлейкина-16 из CD16+ Т-клеток, в продукции лейкотриена В4 и опосредуемом тучными клетками скоплении нейтрофилов в плевральной полости, вызванном зимозаном в условиях in vivo у мышей [7].
В течение последних лет список данных средств постоянно пополняется, синтезируются новые соединения блокаторов Н1-гистаминовых рецепторов, которые, проявляя выраженный антигистаминный эффект, отличаются особенностями фармакокинетических и фармакодинамических свойств.
Несмотря на появление антигистаминных препаратов 2-го поколения, препараты 1-го поколения и впредь будут оставаться в арсенале средств для широкого применения в связи с:
– постоянным получением новых клинических данных на основании длительного опыта использования этих препаратов и возможности дифференцированного подхода к их назначению;
– наличием у Н1-антагонистов 1-го поколения некоторых фармакологических эффектов (таких как антисеротониновая активность, седативное действие, анти-холинергическое действие и др.)
Супрастин является классическим антигистамин-ным препаратом 1-го поколения, обладающим выраженным антигистаминным и М-холинолитическим эффектами. В последние годы появились новые данные о механизмах действия Супрастина, благодаря которым он нашел широкое применение в практике врачей.
Так, в 2003 г. в апрельском номере журнала J Allergy Clin Immunol был опубликован метаанализ сравнительных исследований по изучению седативного действия Н1-блокаторов 1-го и 2-го поколений. По мнению авторов данной публикации, разница по частоте седативного действия между антигистаминными препаратами 1-го и 2-го поколений не является столь существенной, как предполагалось ранее [10].
Данные 18 клинических исследований показали, что результаты исследований значительно варьировали, причем уровень седации в некоторых исследованиях у пациентов, принимавших препараты 1-го поколения, был ниже, чем у пациентов, принимавших плацебо или антигистаминные препараты 2-го поколения.
Появились новые данные о фармакокинетике антигистаминных препаратов 1-го поколения: в частности, стало известно, что этот показатель у хлорфенирами-на, бромфенирамина и гидроксизина у взрослых превышает 14–20 ч, поэтому их можно применять 1 или 2 р./сут без снижения эффективности и с уменьшением частоты побочных эффектов [11, 12].
Супрастин является представителем классических антигистаминных препаратов 1-го поколения и назначается при аллергических заболеваниях, таких как крапивница, сывороточная болезнь, ангионевротический отек, поллиноз (сенная лихорадка), аллергические ри-нопатии, аллергические конъюнктивиты, контактный дерматит, острая и хроническая экзема, лекарственные сыпи, зудящие дерматозы, зуд при укусах насекомых.
Появились публикации об эффективности Супрастина при других патологиях: например, у лиц, страдающих аллергией, или при таких состояниях, когда назначение этого препарата является патогенетически обоснованным.
ОРВИ
В настоящее время продолжается дискуссия о необходимости включения антигистаминных препаратов в комплекс терапии гриппа и острых респираторных вирусных инфекций (ОРВИ). В исследованиях, которые были проведены в 2001 г. в Питсбурге (США), было установлено, что гистамин играет значительную роль в возникновении и выраженности симптомов гриппа. Со 2-го дня от начала гриппа на пике симптомов заболевания отмечается достоверно высокий уровень гистамина в крови [13, 14].
Результаты проведенного в 2003 г. метаанализа по изучению клинической эффективности антигистаминных препаратов для лечения гриппа и ОРВИ, включающего 22 рандомизированных клинических исследования, в которых антигистаминные препараты выступали в качестве монотерапии, и 13 испытаний, при которых антигистаминные препараты комбинировали с деконгестантами (общее количество исследуемых – 8930 человек, включая детей разного возраста и взрослых), показали, что использование антигистаминных препаратов в комплексной терапии ОРВИ и гриппа имеет клиническую эффективность, проявляющуюся улучшением носового дыхания, уменьшением ринореи, чихания [14, 15].
Результаты проведенного в 2008 г. метаанализа по изучению эффективности антигистаминных препаратов для лечения длительного кашля у детей, включающего 793 ребенка, показали их клиническую эффективность, проявляющуюся в уменьшении продолжительности кашля [14, 16].
Результаты проведенного в 2005 г. метаанализа по изучению клинической эффективности антигистаминных препаратов для лечения кашля при гриппе и ОРВИ у детей показали, что использование антигистаминных препаратов 1-го поколения в комплексе с деконгестантами у детей старшего возраста имеет клиническую эффективность, проявляющуюся в сокращении продолжительности кашля, заложенности носа, ринореи.
Антигистаминные препараты 2-го, 3-го поколений неэффективны при кашле [14, 17]. В отличие от Н1-блокаторов 2-го поколения и препаратов 1-го поколения, не обладающих холинолити-ческой активностью (мебгидролин и хифенадин), механизм действия Супрастина связан как с его способностью блокировать Н1-гистаминовые рецепторы, так и с конкурентным антагонизмом по отношению к мускариновым рецепторам, которые опосредуют парасимпатическую стимуляцию секреции назальных желез и вазодилатацию. Кроме того, благодаря способности проникать через гематоэнцефалический барьер Супрастин оказывает влияние на рецепторные образования продолговатого мозга и гипоталамуса и воздействует на центр чихания, блокируя парасимпатический каскад в отношении назальных желез и сосудов. Клинически Супрастин при ОРВИ эффективно уменьшает такие симптомы ринита, как отек слизистой оболочки и заложенность носа, ринорею, зуд и чихание [12, 18].
Пациентам, уже использующим назальные деконгестанты, удается значительно снизить кратность их применения (на 40%) [12, 19].
Астма
Вопрос о возможном применении антигистаминных препаратов при БА возник вскоре после их внедрения в клиническую практику (1940–1950 гг.): их стали применять при любых аллергических процессах, включая БА. Однако вскоре появились работы, указывающие не только на отсутствие клинического эффекта антигистаминных препаратов при БА, но и на ухудшение состояния больных, затруднение отделения мокроты (1950–1955 гг.).
Исследования, проведенные в 1980–1990 г г. (Schulle и др.), показали, что клиническое значение антиастматического действия антигистаминных препаратов невелико, однако и информация о побочном действии не подтвердилась. Было высказано мнение, что антигистаминные препараты при БА назначаются в тех случаях, когда имеются симптомы других сопутствующих аллергических заболеваний.
Сегодня позиция Американской академии аллергии и иммунологии в отношении использования антигистаминных препаратов при лечении БА такова: не являясь препаратами первой линии, препараты тем не менее не противопоказаны больным с БА с сопутствующими аллергическими заболеваниями (например, с аллергическим ринитом). В последние годы стало известно, что многие антигистаминные препараты, в т. ч. оказывающие двойное (холинолитическое и антигистаминное) действие, при применении у больных БА дают положительный эффект в связи с их бронхолитическими свойствами [11, 12].
Кроме того, БА у детей до 5-летнего возраста сопровождается гиперсекрецией мокроты, связанной с физиологическими особенностями раннего возраста. В такой ситуации многие практикующие врачи рекомендуют использовать Супрастин для уменьшения выделения мокроты [12].
Профилактика острого подскладочного ларингита («ложный круп») у детей при острых респираторных инфекциях Супрастин как антигистаминный препарат назначается при ОРВИ, поскольку в механизме развития отека слизистой оболочки гортани, особенно при «ложном крупе», аллергический компонент играет важную роль. Кроме того, Супрастин обладает М-холинолитическим эффектом, за счет которого он также устраняет отек слизистой оболочки. Существенно для детской практики то, что Супрастин разрешен к использованию у детей начиная с 1-го мес. жизни [12].
АД и другие зудящие аллергодерматозы (экземы, хроническая рецидивирующая крапивница и др.)
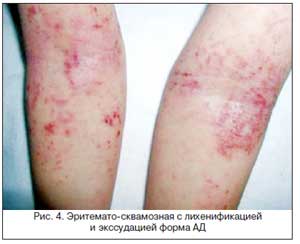
Зуд приводит к нарушению сна и развитию невротического состояния. В связи с этим кожный зуд в значительной степени влияет на качество жизни пациентов и определяет степень тяжести и течение АД [20, 21].
Наличие седативного эффекта делает антигистаминные препараты 1-го поколения незаменимыми в некоторых клинических ситуациях, например, при АД, сопровождающемся изнурительным кожным зудом, усиливающимся в ночное время и существенно нарушающим сон. Существование инъекционной формы этих препаратов позволяет включать их в дезинтоксикационные схемы у больных тяжелыми формами АД. Могут вводиться парентерально – в/м, в острых тяжелых случаях в/в (под контролем врача), что особенно важно в лечении детей, пациентов, страдающих тяжелыми и распространенными формами аллергодерматозов и имеющих сопутствующую патологию желудочно-кишечного тракта [20].
Ведущий американский дерматолог, профессор Гарвардского университета Т. Фицпатрик также рекомендует при выраженном зуде отдавать предпочтение антигистаминным препаратам с седативным действием [12, 22].
По мнению французского аллерголога А. Дидье, для лечения аллергии не только антигистаминное, но и антихолинергическое действие является необходимым. «Высвобождение ацетилхолина и субстанции Р из пресинаптических нервных окончаний может поддерживать реакцию аллергического воспаления на уровне холинергической нервной системы в поздней фазе анафилактической реакции. Антихолинергическое действие блокирует позднюю фазу анафилактической реакции (отсутствует у селективных антигистаминов) [12, 23].
ЛОР-заболевания
При остром среднем отите Супрастин уменьшает отечность слизистой оболочки барабанной полости и слуховой трубы. Благодаря холинолитическому эффекту препарат улучшает аэрацию барабанной полости, восстанавливая функцию слуховой трубы.
При синуситах Супрастин улучшает дренажную функцию естественных соустий, уменьшая отек слизистой оболочки полости носа и околоносовых пазух (за счет М-холинолитического механизма действия) и воспаление (за счет антигистаминного механизма действия) [12].
Острые аллергические реакции (крапивница, отек Квинке, анафилактический шок)
В последние годы отмечается увеличение числа аллергических заболеваний, в т. ч. острых аллергических реакций и состояний, нередко угрожающих жизни больного и требующих неотложной помощи [24, 25]. Наиболее тяжелым проявлением системных аллергических реакций является анафилактический шок [26, 27]. В случае, когда необходимо парентеральное введение антигистаминных лекарственных препаратов, наличие инъекционной формы Супрастина определяет его выбор в качестве препарата первого ряда. При анафилактическом шоке после введения адреналина Супрастин вводится в/в медленно (по 1–2 мл 2% раствора), обязательным условием является контроль уровня систолического артериального давления, которое не должно быть ниже 90 мм рт. ст. [12].
Супрастин предусматривает широкий диапазон используемых терапевтических доз, не накапливается в сыворотке крови, поэтому не вызывает передозировку при длительном применении. Для Супрастина характерны быстрое наступление эффекта и кратковременность (в т. ч. побочного) действия. При этом Супрастин может комбинироваться с неседативными Н1-блокаторами с целью увеличения продолжительности противоаллергического действия [20].
Заключение
Использование в клинической практике антигистаминных препаратов 1-го поколения не утратило своей актуальности. Многолетний положительный опыт широкого применения Супрастина у детей дает основание утверждать, что препарат имеет широкие показания для использования в различных областях практической медицины и остается надежным и испытанным средством для лечения аллергических и инфекционно-воспалительных заболеваний органов дыхательных путей у детей.