Аппарат ивл что это в медицине
Аппарат искусственной вентиляции лёгких
Из Википедии — свободной энциклопедии
Аппарат ИВЛ может использоваться как для инвазивной (через интубационную трубку, введенную в дыхательные пути пациента или через трахеостому), так и для неинвазивной искусственной вентиляции лёгких — через маску.
Аппарат ИВЛ может быть как ручным (мешок Амбу), так и механическим. Сжатый воздух и кислород для пневмопитания механического аппарата могут подаваться как из центральной системы газоснабжения медицинского учреждения или баллона сжатого воздуха (при транспортировке), так и от индивидуального миникомпрессора (реальность в странах экс-СССР) и кислородного концентратора. При этом смесь газов должна согреваться и увлажняться перед подачей пациенту.
Современные аппараты ИВЛ являются крайне высокотехнологичным медицинским оборудованием. Они обеспечивают респираторную поддержку пациента как по объёму, так и по давлению.
В настоящий момент наиболее совершенной технологией синхронизации аппарата ИВЛ с пациентом является технология нейро-контролируемой вентиляции лёгких, когда сигнал, идущий из дыхательного центра продолговатого мозга по диафрагмальному нерву к диафрагме, фиксируется специальными высокочувствительными датчиками, расположенными в области перехода пищевода в желудок (область кардии).
Аппарат высокочастотной струйной ИВЛ может обеспечивать как собственно высокочастотную струйную ИВЛ, так и сочетанную. При этом используется контроль по давлению для предотвращения баротравмы лёгких. Современный аппарат ВЧ струйной ИВЛ должен иметь встроенный роликовый увлажнитель и встроенную систему обогрева газовой смеси для предотвращения тяжёлых осложнений со стороны дыхательных путей. Обязательна возможность дозирования кислорода и контроль углекислого газа в выдыхаемом воздухе.
Аппарат ивл что это в медицине
Принципиальным физиологическим эффектом искусственной вентиляции легких, в отличие от акта самостоятельного дыхания, является положительное давление в дыхательных путях во время дыхательного цикла. Положительное давление имеет ряд преимуществ при газообмене, включая рекрутинг периферических альвеол, увеличение функциональной остаточной емкости, улучшение вентиляционно-перфузионного соотношения и снижение внутрилегочного шунтирования крови. Отрицательные же эффекты заключаются в возможности появления баротравмы и респираторного повреждения легких при использовании больших дыхательных объемов или давления на вдохе, а также потенциальном снижении сердечного выброса при увеличении среднего внутригрудного давления. В общем, некоторая степень позитивных и негативных эффектов искусственной вентиляции легких свойственна всем используемым режимам. Эта величина неодинакова у различных режимов, что обусловлено уровнем положительного давления на вдохе.
Принудительные (Control-mode, CV) и вспомогательные (assist/control-mode ventilation, ACV) режимы представляют собой циклические, объемные режимы, доставляющие фиксированный дыхательный объем с установленным минимальным числом вдохов и скоростью дыхательного потока. Дыхательные попытки пациента при первом варианте не являются триггерами для начала аппаратного вдоха. При CV, вентилятор не добавляет вдохов, несмотря на попытки пациента. Учитывая безопасность и комфорт вспомогательных режимов вентиляции, CV не должен применяться рутинно.
Режим ACV позволяет по запросу больного в виде дыхательных попыток, инициировать дополнительный аппаратный вдох. В зависимости от состояния пациента, а также чувствительности и типа (потоковый или по давлению) триггера вдоха, режим позволяет пациенту создавать свой ритм дыхания и дыхательный объем (с установлением минимального количества вдохов в качестве системы защиты). Использование ACV типично у больных с паралитическими состояниями (при использовании мышечных релаксантов или при паралитических нейромышечных заболеваниях), требующих большого количества седативных средств, а также при трудностях с синхронизацией или при невозможности инициировать вдох в PSV или IMV режимах. Путем повышения аппаратной ЧДД, приводящего к снижению количества спонтанных вдохов, с помощью ACV режима можно добиться уменьшения работы дыхания пациента. Чрезмерное увеличение количества инициированных вдохов значительно увеличивает цену дыхания. С другой стороны триггер вдоха должен быть достаточно чувствительным, чтобы не приводить к возникновению избыточных усилий при дыхательных попытках, что быстро истощает больного.
Режим вентиляции с контролем по объему (PRVC). При этом режиме возможно ограничение чрезмерно высокого пикового давления, приводящего к перерастяжению альвеол. При PCVR создается регулируемый, снижающийся поток на вдохе, который ограничивает пиковое давление, но доставляет установленный объем, в отличие от режима контроля вентиляции по давлению. Стоит отметить, что теоретические преимущества PCVR, не подтвердились рандомизированными исследованиями благоприятного эффекта при данном режиме, за исключением снижения пикового давления.
Перемежающая принудительная вентиляция (IMV). Режим IMV был разработан в 1970-х с целью сохранения спонтанного дыхания пациента в дополнение к аппаратному, с заранее заданной минимальной частотой и объемом вдохов. Вначале данный режим использовался для отлучения пациента от вентилятора, обеспечивая плавный переход по сравнению с классическим методом использования Т-переходников. Синхронизированный вариант режима (SIMV) создавался для предотвращения наложения аппаратных вдохов на пик или окончание спонтанного вдоха пациента.
SIMV продолжает широко использоваться как режим отлучения, и имеет преимущество, выражающееся в ступенчатом снижении частоты аппаратных вдохов и увеличении спонтанных. У пациентов со сниженным комплаенсом, IMV может не обеспечивать достаточный объем спонтанного вдоха из-за сильно ограниченных дыхательных возможностей. В данных условиях поддержка по давлению может быть использована в помощь к каждому вдоху IMV, значительно увеличивая объем спонтанного вдоха и снижая работу дыхания.
Вентиляция с поддержкой по давлению (PCV). Режим PSV был разработан в 1980-х как вспомогательный режим вентиляции. Каждый вдох в режиме PSV инициируется дышащим пациентом и поддерживается давлением, с максимальным потоком во время фазы вдоха. Окончание поддержки вдоха происходит в момент ослабления собственного потока вдоха пациента ниже установленного уровня, инициируя спонтанный выдох. В этом заключается отличие принципа переключения фаз вдох-выдох, регулируемого по потоку, от регуляции этого переключения по объему (рис. 60-3). Режим поддержки по давлению не подразумевает заранее установленной частоты аппаратных дыханий, так как каждый вдох должен быть инициирован пациентом. Это делает применение PSV невозможным у пациентов с нейромышечными заболеваниями, при применении мышечных релаксантов и глубокой седации.
PSV присущи некоторые преимущества, включая улучшение синхронизации пациента с аппаратом ИВЛ, так как ритм дыхания задает сам больной. PSV может обеспечивать минимальную поддержку дыхания перед моментом эксту-бации или значительную (20-40 мм водн. ст.), что означает полное протезирование дыхательной функции пациента и минимальную работу дыхания. Как режим отлучения, поддержка по давлению может использоваться совместно с IMV режимом, как описано выше, или как единственный режим, с постепенным снижением давления поддержки, позволяя пациенту брать на себя больше работы по обеспечению дыхания. У пациентов со сниженными дыхательными резервами, заниженные уровни поддержки давлением могут приводить к неадекватному минутному объему дыхания, что требует постоянного мониторинга частоты и объема дыхания.
Вентиляция с переключением фаз вдох-выдох
Вентиляция с переключением фаз вдох-выдох по объему в условиях тяжелого острого респираторного дистресс синдрома (ОРДС) и сниженного легочного комплаенса, может приводит к чрезмерному пиковому давлению или/и высокому объему вдоха в некоторых легочных сегментах, вызвав вторичное респиратор-ассоциированное легочное повреждение. Эти соображения привели к большему использованию режимов вентиляции с переключением фаз вдох-выдох по времени с регулированием по давлению. В этом режиме вентиляции дыхательный объем доставляется с постоянным потоком вплоть до достижения установленного давления. Время аппаратного вдоха устанавливается заранее и не зависит от потока, как в случае вентиляции с контролем по давлению. Контроль по давлению имеет преимущества в виде постоянного ограничения пикового давления, независимо от изменений податливости легких и грудной клетки или десинхронизации с аппаратом ИВЛ.
Учитывая вышесказанное, это наиболее распространенный и безопасный режим вентиляции в условиях поражения легких, сопровождающихся низкой податливостью, что типично для ОРДС. Как бы то ни было, PCV не очень хорошо переносится пациентами в сознании, что часто требует достаточного уровня седации.
Вентиляция с измененным соотношением фаз дыхания (IRV) может быть вариантом вентиляции с контролем по объему или по давлению, но наиболее часто используется при PCV. IRV является современной адаптацией практики прошлого, заключавшейся в удлинении фазы вдоха, результатом чего становилось увеличение остаточной функциональной емкости легких и улучшение газообмена у некоторых больных. Традиционная ИВЛ с использованием соотношения вдох-выдох 1:2 или 1:1,2 подразумевает относительно долгую экспираторную фазу, значительно снижая среднее давление в дыхательных путях. При IRV соотношение фаз обычно составляет от 1,1:1 до 2:1, что может быть достигнуто относительно быстрым инспираторным потоком и его снижением для поддержания достигнутого давления в фазу вдоха.
При применении IRV возникают два эффекта: а) удлинение времени вдоха ведет к увеличению среднего давления в дыхательных путях и открытию краевых альвеол, схожего результата достигают применением высокого ПДКВ; б) при более тяжелом поражении дыхательных путей, как результат перибронхиального сужения просвета терминальных отделов, с каждым вдохом происходит медленное выравнивание внутрилегочного давления, что приводит к неравномерной альвеолярной вентиляции. Эта неравномерность может стать причиной снижения перфузии альвеол с увеличением внутрилегочного шунтирования крови. При осторожном применении IRV, могут появляться воздушные ловушки, создающие внутреннее или аутоПДКВ, с селективным увеличинием интраальвеолярное давление в таких замкнутых полостях. Такой эффект может сочетаться с увеличением шунтирования и оксигенации. Внутреннее ПДКВ должно часто измеряться по причине возможного перерастяжения альвеол и вторичного респиратор-ассоциированного легочного повреждения.
Несмотря на привлекательность возможности создания селективного ПДКВ при IRV, остается вопрос, добавляет ли данный эффект что-нибудь новое, помимо простого эффекта повышения среднего давления в дыхательных путях. Исследования, подобные проведенному Lessard, свидетельствуют о том, что вентиляция с контролем по давлению может быть использована для ограничения пикового инспираторного давления и нет значительных преимуществ PCV или PCIRV в сравнении с традиционной объемной ИВЛ с добавлением ПДКВ у пациентов с острой дыхательной недостаточностью. Данная точка зрения в дальнейшем была развита Shanholtz и Brower, которые задались вопросом применения IRV при лечении ОРДС.
Вентиляция с освободждением давления (APRV)
В основе APRV лежит режим постоянно положительного давления в дыхательных путях (СРАР). Короткий период более низкого давления позволяет выводить из легких СО2. Пациент имеет возможность дышать самостоятельно во время всего цикла аппаратного дыхания. Теоретическими преимуществами APRV являются более низкое давление в дыхательных путях и минутная вентиляция, мобилизация спавшихся альвеол, более высокий уровень комфорта пациента при спонтанном дыхании и минимальные гемодинами-ческие эффекты. Поскольку пациент сохраняет способность к самостоятельному дыханию благодаря открытому экспираторному клапану, данный режим легко переносится пациентами, отлучаемыми от седации или имеющими положительную динамику после черепно-мозговой травмы. Раннее начало применения данного режима приводит к улучшению гемодинамики и к мобилизации альвеол. К тому же существуют научные данные, доказывающие, что сохранение самостоятельного дыхания при данном режиме вентиляции снижает потребность в седации.
Высокочастотная вентиляция легких
Интерес к высокочастотной вентиляции легких (HFOV) у взрослых с острой дыхательной недостаточностью возник вследствие того, что традиционные режимы вентиляции могут индуцировать дальнейшее повреждение легких повторяющимся циклом открытия и закрытия дыхательных путей. При HFOV поддерживается относительно высокое среднее давление в дыхательных путях при установленном малом дыхательном объеме, который доставляется с высокой частотой. Таким образом, целью является достижение и поддержание легких открытыми при отсутствии большого давления прилагаемого к альвеолам.
Большая часть опыта по применению данного метода описана в литературе по неонатальной и педиатрической практике. В только что опубликованном исследовании Mehta с соавт. 24 взрослых с ОРДС разной этиологии были вовлечены в проспективное исследование применения HFOV как «терапии спасения». Из этих пациентов 42% показали улучшение оксигенации и получили возможность вернуться к традиционным методам ИВЛ. Выжившие пациенты также провели меньшее количество дней на ИВЛ до перевода на HFOV, чем умершие. Требуются новые исследования, для того чтобы пролить свет на вопрос предполагаемой высокой эффективности данного режима у пациентов с ранними проявлениями ОРДС или ингаляционными поражениями.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Второе дыхание: Как работает аппарат ИВЛ и как он помогает в борьбе с коронавирусом
Искусственная вентиляция легких применяется в тяжелых случаях заболевания COVID-19, при котором поражаются нижние дыхательные пути. Таким больным требуется срочное подключение к аппарату ИВЛ. Спрос на подобные устройства в условиях пандемии сегодня сильно превышает предложение.
В начале пандемии даже были споры и очень острые, когда одни страны «перебивали цены» и буквально из-под носа «уводили» ИВЛ.
Разбираемся, как работают аппараты искусственной вентиляции легких и почему их так остро не хватает при пандемии коронавируса. Об этом мы сделали обзор ряда специализированных изданий.
История ИВЛ
Восстановление и поддержка дыхательных процессов волновали еще древних врачевателей и ученых. В классических трактатах содержатся теории дыхания и описания первых попыток искусственной вентиляции легких. Известно, что в XVI веке европейские реформаторы медицины Парацельс и Везалий применяли вентиляцию легких в своих практиках. С XVII века для поддержки дыхания использовались аппараты, устроенные на основе мехов для раздувания огня. К сожалению, такая вентиляция часто приводила к разрыву легких. Параллельно развиваются более щадящие мануальные методы вентиляции посредством наружного воздействия на грудную клетку.
Во второй половине XIX – начале XX века на волне научно-технического прогресса появляются новые методики и устройства для ИВЛ. В частности, в 1907 году был разработан мобильный респиратор Pulmotor «патефонного» типа, который применялся в горноспасательных работах. Однако ученые пришли к выводу, что экспираторные методы ИВЛ, основанные на активном вдувании воздуха в дыхательные пути, не физиологичны и могут приводить к негативным последствиям: изменению легочной механики, атрофии легочных мышц, недостаточному притоку крови к сердцу. Как следствие, появился новый тип устройств – камера с отрицательным давлением, в которую помещался пациент и из которой периодически откачивался воздух. Возникающий вакуум оказывал присасывающее воздействие на грудную клетку, создавая отрицательное давление в дыхательных путях и таким образом обеспечивая дыхание.
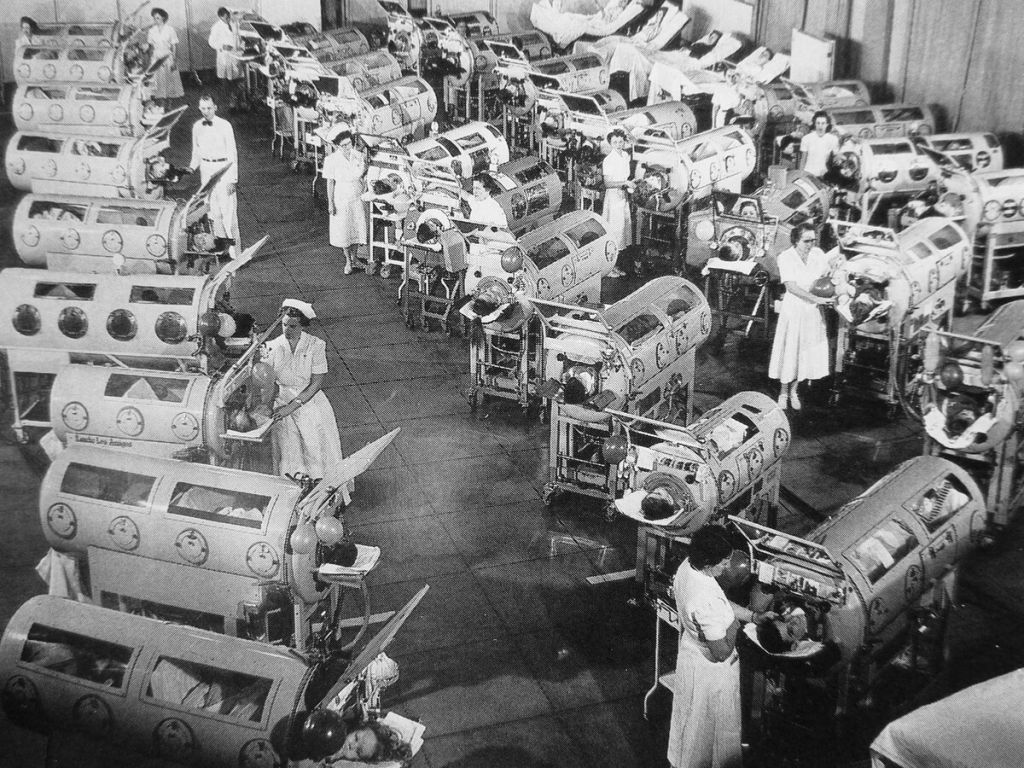
Пациенты, пораженные полиомиелитом, в аппаратах Энгстрёма, 1953 г. Фото: wikimedia.org
Как это часто бывает в медицине, ее развитию способствуют нерадостные события. Так, толчком для создания первого поколения современных аппаратов ИВЛ стали эпидемия полиомиелита 1940-50 гг. и Вторая мировая война, когда военные технологии активно использовались гражданскими медиками. В 1960-70-е годы компактные экспираторные приборы становятся основным типом аппаратов для ИВЛ. В это время в СССР начат выпуск серии аппаратов ИВЛ «РО». Они выпускались как с ручным, так и с автоматическим приводом, были просты в работе и эффективны.
Второе поколение аппаратов ИВЛ отличалось расширенными функциями мониторинга дыхания и появлением новых режимов работы. Для третьего поколения характерно широкое использование микропроцессоров, которые помогли эффективнее управлять устройствами. Сегодня медики имеют дело с аппаратами ИВЛ четвертого поколения. Кроме большого спектра режимов работы и широкого арсенала мониторинга параметров, их системы отклика отличаются высокой чувствительностью на дыхательную попытку пациента, то есть внимательно следят за тем, когда больной начнет дышать самостоятельно.
Последний шанс на спасение
Аппарат работает следующим образом. С помощью компрессора под давлением в легкие подается воздух, в обратном направлении – из легких − выводится углекислый газ. Специальные устройства увлажняют входящую смесь и корректируют ее температуру. Также при наличии жидкости в легких она откачивается.
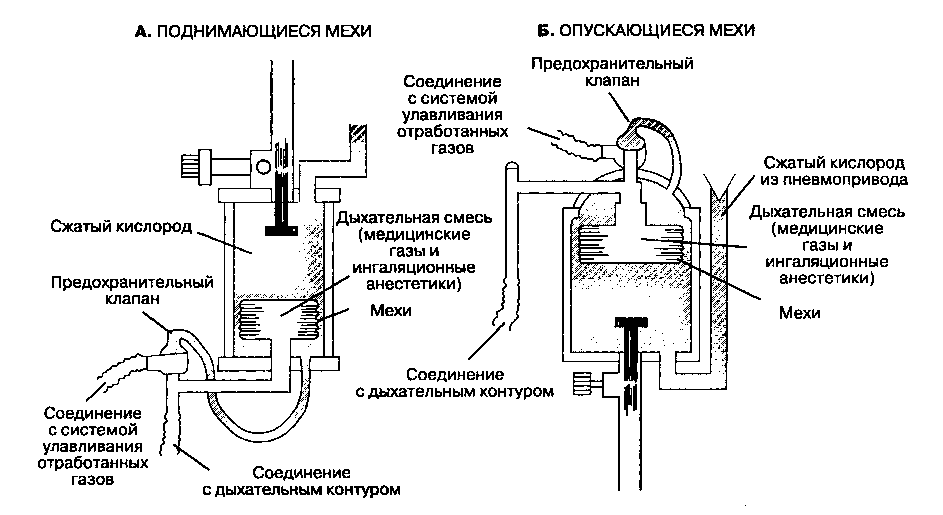
Общая схема работы аппарата ИВЛ
Вентиляция может выполняться двумя способами: неинвазивным и инвазивным. В первом случае воздух подается через плотно прилегающую маску. Такая вентиляция показана пациентам с более легкими симптомами. При инвазивном способе в трахею через рот или нос вводится интубационная трубка. Это довольно болезненная процедура, поэтому часто она сопровождается анестезией. Кроме того, пациент, подключенный к респиратору, не может ни есть, ни пить, ни разговаривать. Питание при этом подается через специальную трубку.
Несмотря на кажущуюся простоту процесса и возможности современных приборов работать в автоматическом режиме, аппарат ИВЛ может использоваться только квалифицированным медперсоналом. Поэтому покупка аппарата ИВЛ в личное пользование – довольно бессмысленная затея. Его обладателю придется также нанимать соответствующий штат медиков. И нужно понимать, что сам по себе аппарат не лечит. Он лишь дает возможность пройти тяжелый этап болезни, чтобы время и лекарственная терапия восстановили естественное дыхание.
Таким образом, основная функция аппарата ИВЛ — закачка насыщенного кислородом воздуха в легкие и выведение углекислого газа. Это и есть вентиляция, или, как еще говорят, воздухообмен.
Один из основных и самых простых типов аппаратов ИВЛ — мешок Амбу. Это незаменимый ручной инструмент для бригад скорой помощи, экстренных служб и отделений интенсивной терапии. Мешок Амбу легкий, компактный и простой в использовании. Изобретен в 50-х годах датским профессором Хеннингом Рубеном и немецким инженером Хольгером Хессе. С помощью мешка Амбу они хотели предотвратить эпидемию полиомиелита.
В тяжелых случаях, когда необходим стабильный и контролируемый воздухообмен, медики используют механические и автоматизированные аппараты ИВЛ.
Они состоят из компьютеризированной коробки, расположенной на верхней части передвижной тележки. У аппарата множество экранов, циферблатов, кабелей для передачи данных, шнуров питания и газовых трубок.
Воздух для аппарата ИВЛ может подаваться из центральной системы газоснабжения медицинского учреждения, баллона сжатого воздуха, индивидуального мини-компрессора или кислородного концентратора.
Современные аппараты ИВЛ — сложное и высокотехнологичное оборудование, которое позволяет обеспечить превосходный уровень ухода за пациентом. Они регулируют следующие функции:
Один из самых современных методов синхронизации аппарата ИВЛ с дыханием пациента — нейроконтролируемая респираторная поддержка (NAVA — Neurally Adjusted Ventilatory Assist). Технологию разработали в 2007 году.
Принцип работы следующий: датчик устройства устанавливается в желудочный зонд и вводится в организм, аппарат фиксирует нервные импульсы, идущие от дыхательного центра головного мозга по диафрагмальному нерву к диафрагме.
Таким образом оборудование синхронизируется с дыхательным центром мозга, подавая кислород, когда легкие получают из него соответствующую команду. То есть аппарат полностью ориентируется на импульсы, подаваемые мозгом: когда нужно дышать, когда — не дышать.
Постоянный прирост пациентов с COVID-19 приводит к острой нехватке аппаратов ИВЛ по всему миру. Врачам приходится буквально делить один аппарат на несколько больных. Одна из нью-йоркских больниц, например, подключила к одному аппарату ИВЛ сразу двух пациентов.
Исследования показывают, что такая методика может быть опасной для пациентов. Поэтому часть распределителей, которые сейчас массово печатают владельцы 3D-принтеров, может оказаться не только бесполезной, но и вредной.
Для создания настоящих аппаратов ИВЛ необходим огромный опыт в исследованиях, проектировании и производстве такого оборудования. Нужна гарантия надежности, исправности и соответствия строгим нормативным требованиям.
Все это жизненно важно, потому что аппараты ИВЛ часто используются в критических ситуациях, когда ошибка или отказ оборудования может привести к смерти пациента. Поэтому механические аппараты ИВЛ стоят достаточно дорого.
В то же время, одно из серьезных осложнений от вируса COVID-19, с которым столкнулся весь мир – это быстрое развитие тяжелой пневмонии, при котором возникает острая дыхательная недостаточность. Такого больного нужно как можно быстрее подключить к аппарату искусственной вентиляции легких, иначе существует риск летального исхода. Еще раз повторим: подключение к аппарату ИВЛ требуется только самым тяжелым больным, находящимся на грани жизни и смерти.
Аппараты ИВЛ не являются чем-то уникальным и сегодня достаточно распространены. Ими оснащаются отделения интенсивной терапии, реанимационные, машины и вертолеты скорой помощи. Но в условиях пандемии резкий рост количества больных с острыми формами пневмонии привел к тому, что во всем мире возникла нехватка и аппаратов ИВЛ, и специалистов по работе с ними.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Кому и зачем нужен аппарат ИВЛ: 7 ответов анестезиолога-реаниматолога
Что такое аппарат ИВЛ?
Это высокотехнологичное медицинское оборудование, которое подает в легкие дыхательную смесь, насыщает кровь кислородом и удаляет из легких углекислый газ.
Искусственная вентиляция легких применяется в практике врача — анестезиолога-реаниматолога в различных ситуациях. Современный аппарат ИВЛ анализирует множество параметров, у него много датчиков, которые обеспечивают эффективность и безопасность проведения процедуры. Это позволяет настроить индивидуальный режим для каждого реанимационного пациента.
Проведение искусственной вентиляции легких можно сравнить с полетом на самолете. Здесь есть свой взлет, своя посадка и зоны турбулентности.
Где применяются аппараты ИВЛ?
Аппараты для проведения ИВЛ используются при общей анестезии, особенно при длительных и сложных хирургических вмешательствах. В этом случае пациент переводится на ИВЛ в операционной в процессе проведения наркоза.
Это делает хирургическое вмешательство более удобным для хирурга и безопасным для пациента, а наркоз — более управляемым. Тем самым улучшаются результаты хирургических вмешательств. После окончания операции пациент просыпается и снимается с искусственного дыхания.
Также ИВЛ используют при острой дыхательной недостаточности для спасения жизни человека. Причем неважно, чем обусловлена дыхательная недостаточность.
Пациентов переводят на искусственное дыхание при травмах, инсультах, отравлениях, при повреждениях головного мозга, чтобы предотвратить гипоксию (кислородное голодание). Она может возникнуть и при повреждении легких бактериальной или вирусной пневмонией, коронавирусной инфекцией.
После ИВЛ человек сможет дышать сам?
Среди людей бытует мнение, что если человек попал на ИВЛ, то снять его уже невозможно. Это не так. Искусственная вентиляция позволяет пациенту пережить критическое состояние, минимизировать его энергетические затраты. Тогда человек может направить все силы организма на борьбу с болезнью.
Аппарат ИВЛ защищает центральную нервную систему от кислородного голодания. Когда болезнь отступает, человека снимают с аппарата.
Современные аппараты обладают различными режимами, которые способны учитывать дыхательные попытки пациента и помогать ему дышать самостоятельно.
Как врачи понимают, что пациента нужно переводить на ИВЛ?
В каждой ситуации анестезиолог-реаниматолог принимает решение индивидуально. Он основывает его на лабораторных показателях, на клинической картине и согласует с различными протоколами ведения дыхательной недостаточности.
Есть определенные критерии, по которым врач оценивает состояние человека и масштаб поражения легочной ткани.
У пациента проверяют уровень кислорода и углекислого газа в крови, определяют кислотность крови, частоту дыхания, цвет кожных покровов, сатурацию кислорода (это доля насыщенного кислородом гемоглобина относительно общего гемоглобина в крови. — прим. ред.).
Как работает аппарат ИВЛ?
Аппарат вдувает в человека определенный объем воздуха, а человек выдыхает его. Грудная клетка у человека ригидна. Это можно сравнить с тем, как мы надуваем воздушный шар. Для того чтобы он сдулся, нужно лишь открыть клапан, дополнительных усилий не нужно. Так и в случае с выдохом при искусственной вентиляции легких.
При аппаратном дыхании врач задает многие параметры: поток воздуха, содержание кислорода во вдыхаемой смеси, давление, под которым осуществляется дыхание, давление в конце выдоха, частота дыхания. Критериев очень много.
Когда у человека восстанавливается дыхание, можно активировать режим, при котором аппарат лишь помогает ему сделать эффективный вдох. Он как бы предугадывает желание человека вдохнуть. Это помогает человеку адаптироваться к самостоятельному дыханию.
Когда дыхание человека становится эффективным, его можно отключить от аппарата.
Как аппарат ИВЛ помогает при COVID-19?
Абсолютно так же, как и при другой дыхательной недостаточности. При коронавирусной инфекции у человека нарушается газообмен в легких, их физические свойства, способность насыщать кровь кислородом.
При коронавирусной инфекции у пациента возникает одышка, истощаются мышцы, которые обеспечивают дыхание. В результате на каждый акт вдоха человек начинает тратить слишком много энергии. Перевод на ИВЛ помогает пациенту экономить силы и направить их на борьбу с болезнью. Кроме того, это позволяет бороться с кислородным голоданием.
Если состояние легких улучшается и человек может дышать сам, то его снимают с искусственной вентиляции. Таким образом, ИВЛ — это метод, который помогает пациенту пережить критическое состояние. Это дыхательный кокон аппарата ИВЛ, через который пациенту доставляется дыхательная смесь
Как долго человек может быть на ИВЛ?
В моей практике были люди, которые находились на искусственном дыхании по несколько месяцев. Все это время врач оценивал их состояние и менял вспомогательные режимы аппарата. И после у людей получалось или не получалось восстановить свое дыхание.
Есть много способов тренировки самостоятельного дыхания у пациентов. Это искусство реаниматолога «отлучить» человека от аппарата.
Сложно сказать, сколько времени пациенту с диагнозом COVID-19 потребуется для восстановления собственного дыхания, если он подключен к аппарату.
Пока клинические показания требуют ИВЛ, анестезиологи-реаниматологи его проводят. И неважно, чем вызвана патология, — коронавирусом, пневмококком, вирусом гриппа или другой болезнью.
_MAQUET_SERVO-i.jpg/im194-289px-%D0%90%D0%BF%D0%BF%D0%B0%D1%80%D0%B0%D1%82_%D0%B8%D1%81%D0%BA%D1%83%D1%81%D1%81%D1%82%D0%B2%D0%B5%D0%BD%D0%BD%D0%BE%D0%B9_%D0%B2%D0%B5%D0%BD%D1%82%D0%B8%D0%BB%D1%8F%D1%86%D0%B8%D0%B8_(%D0%98%D0%92%D0%9B)_MAQUET_SERVO-i.jpg)