Как называют биологические катализаторы белковой природы
Катализаторы биологические
Смотреть что такое «Катализаторы биологические» в других словарях:
КАТАЛИЗАТОРЫ — вещества, ускоряющие химические реакции. Вещества, замедляющие реакции, называются ингибиторами. Биологические катализаторы называются ферментами. Катализаторами служат синтетические алюмосиликаты, металлы платиновой группы, серебро, никель и др … Большой Энциклопедический словарь
Катализаторы — вещества, ускоряющие химические реакции (ср.: ингибиторы замедлители реакций). Биологические К. называются ферментами. Наиболее распространенными К. являются: синтетические алюмосиликаты, металлы платиновой группы, серебро, никель и др … Российская энциклопедия по охране труда
катализаторы — вещества, ускоряющие химические реакции. Вещества, замедляющие реакции, называются ингибиторами. Биологические катализаторы называются ферментами. Катализаторами служат синтетические алюмосиликаты, металлы платиновой группы, серебро, никель и др … Энциклопедический словарь
Катализаторы — (см. Катализ) вещества, как правило, ускоряющие (в противоположность ингибиторам) скорость химических реакций. Катализаторы не смещают равновесие, а изменяют скорости прямой и обратной реакций, способствуют скорейшему достижению равновесия.… … Начала современного естествознания
ПОЛИМЕРЫ БИОЛОГИЧЕСКИЕ — (биополимеры) природные макромолекулы, играющие осн. роль в биол. процессах. К П. б. относятся белки, нуклеиновые кислоты (НК) и полисахариды. П. б. образуют структурную основу всех живых организмов; все процессы в клетке связаны с… … Физическая энциклопедия
Катализатор — (Catalyst) Определение катализатора, механизм действия катализатора Определение катализатора, механизм действия катализатора, применение катализатора Содержание Содержание 1. в химии Виды катализаторов Механизм действия катализаторов Требования,… … Энциклопедия инвестора
КАТАЛИЗ — ускорение химических реакций под действием малых количеств веществ (катализаторов), которые сами в ходе реакции не изменяются. Каталитические процессы играют огромную роль в нашей жизни. Биологические катализаторы, называемые ферментами,… … Энциклопедия Кольера
Катализ — (от греч. katálysis разрушение) изменение скорости химических реакций в присутствии веществ (катализаторов (См. Катализаторы)), вступающих в промежуточное химическое взаимодействие с реагирующими веществами, но восстанавливающих после… … Большая советская энциклопедия
фермент — Термин фермент Термин на английском enzyme Синонимы Аббревиатуры Связанные термины активный центр катализатора, белки, биологические моторы, биологические нанообъекты, биосенсор, генная инженерия, иммобилизация, кинезин, клетка, лаборатория на… … Энциклопедический словарь нанотехнологий
Биотехнологии — Биотехнология интеграция естественных и инженерных наук, позволяющая наиболее полно реализовать возможности живых организмов или их производные для создания и модификации продуктов или процессов различного назначения. Чаще всего применяется в… … Википедия
Характеристики биологического катализатора и примеры
катализ
Химические реакции включают энергию: исходные молекулы, участвующие в реакции, или реагенты начинаются с определенной степени энергии. Дополнительное количество энергии поглощается для достижения «переходного состояния». Впоследствии энергия высвобождается с продуктами.
Разница энергий между реагентами и продуктами выражается как ΔG. Если уровни энергии продуктов выше, чем у реагентов, реакция является эндергонической, а не спонтанной. Напротив, если энергия продуктов ниже, реакция является экзергонной и спонтанной.
Однако, если реакция является спонтанной, это не значит, что она будет происходить с заметной скоростью. Скорость реакции зависит от ΔG * (звездочка обозначает энергию активации).
Читатель должен помнить об этих понятиях, чтобы понять, как происходит функционирование ферментов..
ферменты
Что такое фермент?
Характеристики ферментов
Ферменты существуют в нескольких формах. Некоторые состоят исключительно из белков, в то время как другие имеют небелковые области, называемые кофакторами (металлы, ионы, органические молекулы и т. Д.).
Таким образом, апофермент представляет собой фермент без его кофактора, и комбинация апофермента и его кофактора называется голоферментом..
Это молекулы значительно большего размера. Однако только небольшой сайт фермента непосредственно участвует в реакции с субстратом, и этот регион является активным сайтом.
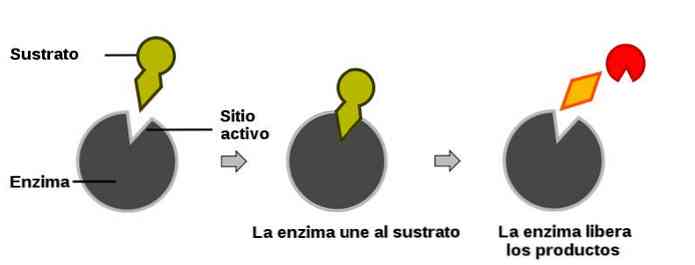
Когда реакция начинается, фермент связывается со своим субстратом, поскольку ключ связан со своим замком (эта модель является упрощением реального биологического процесса, но служит для иллюстрации процесса).
Все химические реакции, которые происходят в нашем организме, катализируются ферментами. На самом деле, если бы этих молекул не существовало, нам пришлось бы ждать сотни или тысячи лет, чтобы реакции завершились. Следовательно, регуляция ферментативной активности должна контролироваться очень специфическим образом..
Номенклатура и классификация ферментов
Существует шесть основных типов ферментов: оксидоредуктазы, трансферазы, гидролазы, лиазы, изомеразы и лигазы; отвечает за: окислительно-восстановительные реакции, перенос атомов, гидролиз, присоединение двойных связей, изомеризацию и связывание молекул соответственно.
Как работают ферменты?
Разница между продуктами и реагентами остается одинаковой (фермент на нее не влияет), так же как и распределение. Фермент облегчает формирование переходного состояния.
Ферментные ингибиторы
Обычно процесс ингибирования является обратимым, хотя некоторые ингибиторы могут оставаться связанными с ферментом почти постоянно.
примеров
В наших клетках и в клетках всех живых существ содержится большое количество ферментов. Однако наиболее известны те, которые участвуют в метаболических путях, таких как гликолиз, цикл Кребса, цепь переноса электронов и другие..
Сукцинатдегидрогеназа является ферментом типа оксидоредуктазы, который катализирует окисление сукцината. В этом случае реакция включает потерю двух атомов водорода..
Разница между биологическими катализаторами (ферментами) и химическими катализаторами
Есть катализаторы химической природы, которые, подобно биологическим, увеличивают скорость реакций. Однако есть заметные различия между молекулами обоих типов..
Ферментативные реакции происходят быстрее
Большинство ферментов работают в физиологических условиях
Поскольку биологические реакции проводятся внутри живых существ, их оптимальные условия окружают физиологические значения температуры и pH. Химикам, с другой стороны, нужны резкие условия температуры, давления и кислотности.
специфичность
Ферменты очень специфичны в реакциях, которые они катализируют. В большинстве случаев они работают только с одним субстратом или с несколькими. Специфика также относится к типу продукции, которую они производят. Ассортимент субстратов химических катализаторов значительно шире.
Силы, которые определяют специфичность взаимодействия между ферментом и его субстратом, являются такими же, которые определяют конформацию одного и того же белка (взаимодействия Ван-дер-Ваальса, электростатические, водородные и гидрофобные связи).
Ферментативная регуляция является точной
Наконец, ферменты обладают большей способностью регуляции, и их активность варьируется в зависимости от концентрации различных веществ в клетке..
Среди регуляторных механизмов мы находим аллостерический контроль, ковалентную модификацию ферментов и изменение количества синтезируемого фермента..
Ферменты. Понятие о ферментах как о биологических катализаторах белковой природы
В природе существуют особые вещества белковой природы, одинаково успешно функционирующие как в живой клетке, так и за её пределами. Это ферменты. С их помощью организм переваривает пищу, выращивает и разрушает клетки, благодаря им эффективно работают все системы нашего организма и, в первую очередь, центральная нервная система. Без ферментов в мире не существовало бы йогурта, кефира, сыра, брынзы, кваса, готовых каш, детского питания. Из чего состоят и как устроены эти биокатализаторы, недавно ставшие верными помощниками биотехнологов, как их отличают друг от друга, как они облегчают нашу жизнь, об этом вы узнаете из этого урока.
Ферменты – это белковые молекулы, которые синтезируются живыми клетками. В каждой клетке насчитывается более сотни различных ферментов. Роль ферментов в клетке колоссальна. С их помощью химические реакции идут с высокой скоростью, при температуре, подходящей для данного организма.
То есть ферменты – это биологические катализаторы, которые облегчают протекание химической реакции и за счет этого увеличивают её скорость. Как катализаторы они не изменяют направление реакции и не расходуются в процессе реакции.
Ферменты—биокатализаторы– вещества, увеличивающие скорость химических реакций.
Без ферментов все реакции в живых организмах протекали бы очень медленно и не могли бы поддерживать его жизнеспособность.
Наглядный пример работы ферментов – сладковатый вкус во рту, который появляется при пережевывании продуктов, содержащих крахмал (например, риса или картофеля). Появление сладкого вкуса связано с работой фермента амилазы, которая присутствует в слюне и расщепляет крахмал (рис. 1). Крахмал является полисахаридом, и сам по себе безвкусный, но продукты расщепления крахмала (моносахариды) с меньшей молекулярной массой (декстрины, мальтоза, глюкоза) сладкие на вкус.
Рис. 1. Механизм действия амилазы
Все ферменты –глобулярные белки с третичной или четвертичной структурой. Ферменты могут быть простыми, состоящими только из белка, и сложными.
Сложные ферменты состоят из белковой и небелковой части (белковая часть – апофермент, а добавочная небелковая – кофермент). В качестве кофермента могут выступать витамины – E, K, B групп (рис. 2).
Рис. 2. Классификация ферментов по их составу
Фермент взаимодействует с субстратом, не всей молекулой, а отдельной её частью – т. н. активным центром.
Механизм действия ферментов
Фермент взаимодействует с субстратом и образует короткоживущий фермент-субстратный комплекс. По завершении реакции, фермент-субстратный комплекс распадается на продукты и фермент. Фермент в итоге не изменяется: по окончании реакции он остается таким же, каким был до неё, и может теперь взаимодействовать с новой молекулой субстрата (рис. 3).
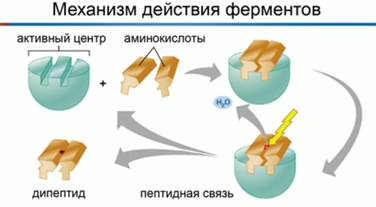
Рис. 3. Механизм взаимодействия фермента и субстрата
На рисунке 3 представлен механизм работы фермента, в частности, образования пептидной связи между молекулами аминокислот. Две аминокислоты взаимодействуют между собой в активном центре фермента, между ними образуется пептидная связь. Новое вещество (дипептид) покидает активный центр фермента, поскольку оно по своей структуре не соответствует этому центру.
Особенностью ферментов является то, что они обладают высокой специфичностью, т. е. могут ускорять только одну реакцию или реакции одного типа.
В 1890 году Э. Г. Фишер предположил, что эта специфичность обусловлена особой формой молекулы фермента, которая точно соответствует форме молекулы субстрата. Эта гипотеза получила название «ключа и замка», где ключ сравнивается с субстратом, а замок – с ферментом. Гипотеза гласит: субстрат подходит к ферменту, как ключ подходит к замку. Избирательность действия фермента связана со строением его активного центра (рис. 4).
Рис. 4. Гипотеза взаимодействия фермента и субстрата по принципу ключ-замок Э. Г. Фишера
В первую очередь, на активность фермента влияет температура. С повышением температуры скорость химической реакции возрастает. Увеличивается скорость молекул, у них появляется больше шансов столкнуться друг с другом. Следовательно, увеличивается вероятность того, что реакция между ними произойдет. Температура, обеспечивающая наибольшую активность фермента – оптимальная.
За пределами оптимальной температуры скорость реакции снижается вследствие денатурации белков. Когда температура снижается, скорость химической реакции тоже падает. В тот момент, когда температура достигает точки замерзания, фермент инактивируется, но при этом не денатурирует (см. видео).
В наше время для длительного хранения продуктов широко используют способ быстрого замораживания. Оно останавливает рост и развитие микроорганизмов, а также инактивирует ферменты, находящиеся внутри микроорганизмов, и предотвращает разложение продуктов питания.
Кроме этого, активность ферментов зависит ещё от pH среды (кислотности – то есть показателя концентрации ионов водорода).
В большинстве случаев, ферменты работают при нейтральном pH, т. е. при pH около 7. Но существуют ферменты, которые работают либо в кислой и сильнокислой, либо в щелочной и сильнощелочной среде. Например, один из таких ферментов – пепсин, он находится у нас с вами в желудке, работает в сильнокислой среде и расщепляет белки. Поскольку в желудке среда достаточно кислая, 1,5 – 2 pH, то этот фермент работает при сильнокислой среде.
Ферменты подвержены действию активаторов и ингибиторов. Некоторые ионы, например, ионы металлов Mg, Mn, Zn активируют ферменты. Другие же ионы (к ним относятся ионы тяжелых металлов, а именно Hg, Pb, Cd), наоборот, подавляют активность ферментов, денатурируют их белки.
В 1961 году была предложена систематическая классификация ферментов на 6 групп. Но названия ферментов оказались очень длинными и трудными в произношении, поэтому ферменты принято сейчас именовать с помощью рабочих названий. Рабочее название состоит из названия субстрата, на который действует фермент, и окончания «аза» (рис. 5). Например, если вещество — лактоза, то есть молочный сахар, то лактаза – это фермент который его преобразует. Если сахароза (обыкновенный сахар), то фермент, который его расщепляет, – сахараза. Соответственно, ферменты, которые расщепляют протеины, носят название протеиназы.
Ферменты применяются практически во всех областях человеческой деятельности, и такое широкое применение, в первую очередь, связано с тем, что они сохраняют свои уникальные свойства вне живых клеток.
Ферменты групп амилаз, протеаз и липаз применяются в медицине. Они расщепляют крахмал, белки и жиры. Все эти ферменты, как правило, входят в состав комбинированных препаратов, таких как фестал и панзинорм, и используются, в первую очередь, для лечения заболеваний желудочно-кишечного тракта (рис. 6).
Ферменты применяют для растворения тромбов в кровеносных сосудах, при лечении гнойных ран.
Особое место занимает энзимотерапия при лечении онкологических заболеваний.
Такие ферменты как амилаза расщепляют крахмал и поэтому широко используются в пищевой промышленности. В пищевой промышленности используется протеиназа, расщепляющая белки, и липазы, расщепляющие жиры. Ферменты амилазы используются в хлебопечении, виноделии и пивоварении (см. видео).
Протеазы используются для смягчения мяса и при изготовлении готовых каш.
Липазы используются в производстве сыра.
Ферменты широко используются в косметической промышленности, входят в состав кремов, некоторые ферменты входят в состав стиральных порошков.
Энзимопатология
Энзимопатология – область энзимологии, которая изучает связь между болезнью и недостаточным синтезом, или отсутствием синтеза какого-либо фермента.
Например, причиной наследственного заболевания – фенилкетонурии, которое сопровождается расстройством психической деятельности, является потеря клетками печени способности синтезировать фермент, катализирующий превращение фенилаланина в тирозин.
В результате в организме накапливаются токсические вещества. Новорожденный ребенок выглядит здоровым, а первые симптомы фенилкетонурии проявляются в возрасте от двух до шести месяцев. Это выраженная вялость, отсутствие интереса к окружающему миру, повышенная раздражительность, а также беспокойство и рвота.
Во втором полугодии жизни у ребенка выражено отставание в психическом развитии. Менее чем в 10% случаев – это слабая степень олигофрении, а у 60% развивается идиотия.
При своевременной диагностике патологических изменений можно избежать, если с момента рождения до наступления полового созревания ограничить поступление фенилаланина с пищей.
Вопрос 1. Какие вещества называются катализаторами?
Вещества, которые изменяют скорость химической реакции, оставаясь к концу ее неизменными, называются катализаторами.
Вопрос 2. Какую роль играют ферменты в клетке?
Ферменты – это белковые катализаторы, синтезируемые клетками. Они регулируют скорость и специфичность тысяч химических реакций, протекающих в клетке. Ферменты могут действовать в качестве катализатора не только в клетке, где они образовались, но и за её пределами, например, пищеварительные ферменты работают в полости желудочно-кишечного тракта. Многие ферменты просто растворены в цитоплазме. Молекулы одних ферментов состоят только из белков, другие включают белок и соединение небелковой природы (органическое — кофермент или неорганическое — ионы различных металлов). Ферменты строго специфичны: каждый фермент катализирует определенный тип реакций, в которых участвуют определенные виды молекул субстратов.
Вопрос 4. Почему большинство ферментов при высокой температуре теряет каталитические свойства?
Высокая температура среды, как правило, вызывает денатурацию белка, т. е. нарушение его природной структуры. Поэтому при высокой температуре большинство ферментов утрачивает свои каталитические свойства.
Вопрос 5. Почему недостаток витаминов может вызвать нарушения в процессах жизнедеятельности организма?
Многие витамины входят в состав ферментов. Поэтому недостаток в организме витаминов ведет к ослаблению активности ферментов в клетках, а следовательно, может вызвать нарушения в процессах жизнедеятельности.
Ферменты – биологические катализаторы.
«Управление общеобразовательной организацией:
новые тенденции и современные технологии»
Свидетельство и скидка на обучение каждому участнику
Глава 1. Что такое ферменты?
1.1. Ферменты – биологические катализаторы…….…………………….2-3
1.2. Типы ферментов……………………………………………………..…3
1.3. Структура ферментов………………………………………………..…3
1.4. Специфичность ферментов и условия их активности. ………….… 4
Глава 2. Значение ферментов в живых организмах.
2.1. Роль ферментов в организме ……………………………………. 4-5
Глава 3. Исследовательская работа.
3.1. Химические результаты исследования ………………………. 5-6
3.2. Механизм работы ферментов…………. ………………………………6
3.3. Исследовательский опрос…………………………………………. 6-7
Глава 4. Заключение.
Актуальность: Известно, ферменты играют важнейшую роль в регуляции химических превращений обмена веществ. Ферменты обнаружены у всех живых существ, начиная от самых примитивных микроорганизмов. Получено около 600 ферментов. Ферменты способны управлять сложнейшими процессами разрушения и сотворения новых веществ в организме. В настоящее время знания о работе ферментов человек поставил себе на службу в медицине, промышленности, сельском хозяйстве и других сферах жизни.
Цель проекта: Провести исследование по обнаружению ферментов в живых организмах, рассмотреть их значение.
Что такое ферменты?
Ферменты – это биологические катализаторы белковой природы, ускоряющие химические реакции в живых организмах и вне их.
Ферменты присутствуют во всех живых клетках и способствуют превращению одних веществ (субстратов) в другие (продукты). Ферменты выступают в роли катализаторов практически во всех биохимических реакциях, протекающих в живых организмах. К 2013 году было описано более 5000 разных ферментов. Они играют важнейшую роль во всех процессах жизнедеятельности, направляя и регулируя обмен веществ организма.
Подобно всем катализаторам, ферменты ускоряют как прямую, так и обратную реакцию, понижая энергию активации процесса. Химическое равновесие при этом не смещается ни в прямую, ни в обратную сторону. Каждая молекула фермента способна выполнять от нескольких тысяч до нескольких миллионов «операций» в секунду.
При этом эффективность ферментов значительно выше эффективности небелковых катализаторов — ферменты ускоряют реакцию в миллионы и миллиарды раз, небелковые катализаторы — в сотни и тысячи раз.
Фермент амилаза необходим для переработки углеводов. Под воздействием амилазы углеводы разрушаются и легко всасываются в кровь. Амилаза присутствует как в слюне, так и в кишечнике. Амилаза тоже бывает разной. Для каждого вида сахаров существует собственный вид этого фермента.
Липаза – это ферменты, которые присутствуют в желудочном соке и вырабатываются поджелудочной железой. Липаза необходима для усвоения организмом жиров.
Протеаза – это группа ферментов, которые присутствуют в желудочном соке и тоже вырабатываются поджелудочной железой. Кроме этого, протеаза присутствует и в кишечнике. Протеаза необходима для расщепления белков.
Активность ферментов определяется их трёхмерной структурой.
Как и все белки, ферменты синтезируются в виде линейной цепочки аминокислот, которая сворачивается определённым образом. Каждая последовательность аминокислот сворачивается особым образом, и получающаяся молекула (белковая глобула) обладает уникальными свойствами. Несколько белковых цепей могут объединяться в белковый комплекс. Третичная структура белков разрушается при нагревании или воздействии некоторых химических веществ.
Ферменты обычно проявляют высокую специфичность по отношению к своим субстратам (субстратная специфичность). Это достигается частичной комплементарностью формы, распределения зарядов и гидрофобных областей на молекуле субстрата и в центре связывания субстрата на ферменте. Ферменты обычно демонстрируют также высокий уровень стереоспецифичности (образуют в качестве продукта только один из возможных стереоизомеров или используют в качестве субстрата только один стереоизомер), региоселективности (образуют или разрывают химическую связь только в одном из возможных положений субстрата) и хемоселективности (катализируют только одну химическую реакцию из нескольких возможных для данных условий). Несмотря на общий высокий уровень специфичности, степень субстратной и реакционной специфичности ферментов может быть различной. Например, эндопептидаза трипсин разрывает пептидную связь только после аргинина или лизина, если за ними не следует пролин, а пепсин гораздо менее специфичен и может разрывать пептидную связь, следующую за многими аминокислотами.
Влияние условий среды на активность ферментов
Активность ферментов зависит от условий в клетке или организме — давления, кислотности среды, температуры, концентрации растворённых солей (ионной силы раствора) и др.
Роль ферментов в организме
Ферменты участвуют в осуществлении всех процессов обмена веществ, в реализации генетической информации. Переваривание и усвоение пищевых веществ, синтез и распад белков, нуклеиновых кислот, жиров, углеводов и других соединений в клетках и тканях всех организмов — все эти процессы невозможны без участия ферментов. Любое проявление функций живого организма — дыхание, мышечное сокращение, нервно-психическая деятельность, размножение и др. — обеспечивается действием ферментов. Индивидуальные особенности клеток, выполняющих определенные функции, в значительной мере определяются уникальным набором ферментов, производство которых генетически запрограммировано. Отсутствие даже одного фермента или какой-нибудь его дефект могут привести к серьезным отрицательным последствиям для организма.
Местонахождение ферментов в организме
В клетке часть ферментов находится в цитоплазме, но в основном ферменты связаны с определенными клеточными структурами, где и проявляют свое действие. В ядре, например, находятся ферменты, ответственные за репликацию — синтез ДНК(ДНК-полимеразы), за ее транскрипцию — образование РНК (РНК-полимеразы). В митохондриях присутствуют ферменты, ответственные за накопление энергии, в лизосомах — большинство гидролитических ферментов, участвующих в распаде нуклеиновых кислот и белков.
Химические результаты исследования
Нами был проведен опыт по изучению механизма действия ферментов на примере вареного куриного филе и сырого.
1. Активность фермента проявилась в пробирке с живыми тканями и не проявилась в пробирке с мёртвыми тканями, потому что в результате денатурации белка, нарушается структура молекулы фермента, её активность снижается, затем прекращается.
2. Измельчение ткани влияет на активность фермента из-за увеличения площади прикосновения, таким образом скорость протекания реакции увеличивается.
Важные отличия ферментов и неорганических катализаторов в том, что реакции с участием неорганических катализаторов протекают, как правило, при высоких давлениях, а ферменты работают при нормальном давлении. Самое главное отличие в том, что скорости реакций, катализируемых ферментами, во много раз больше.
Механизм работы ферментов
Мы провели опрос, среди учащихся МАОУ СШ №55 «Лингвист» по следующим вопросам:
Что такое ферменты?
Какова их роль в организме?
Что влияет на активность ферментов?
Какова химическая природа ферментов?
Чьи работы положили начало ферментологии, как самостоятельному разделу биологической химии?
Из 20 человек лишь 3 ответили правильно на все вопросы. 4 и 5 вопросы оказались самыми трудными для ребят.
Ферменты являются посредниками между организмом и окружающей средой, обеспечивают адаптацию организма к изменяющимся условиям (авторегуляторы).
Ферменты участвуют в осуществлении всех процессов обмена веществ, в реализации генетической информации. Переваривание и усвоение пищевых веществ, синтез и распад белков, нуклеиновых кислот, жиров, углеводов и других соединений в клетках и тканях всех организмов — все эти процессы невозможны без участия ферментов. Любое проявление функций живого организма — дыхание, мышечное сокращение, нервно-психическая деятельность, размножение и др. — обеспечивается действием ферментов. Индивидуальные особенности клеток, выполняющих определенные функции, в значительной мере определяются уникальным набором ферментов, производство которых генетически запрограммировано. Отсутствие даже одного фермента или какой-нибудь его дефект могут привести к серьезным отрицательным последствиям для организма.
Обычно ферменты выделяют из тканей животных, растений, клеток и культуральных жидкостей микроорганизмов, биологических жидкостей (кровь, лимфа и др.). Для получения некоторых труднодоступных ферментов используются методы генетической инженерии. Из исходных материалов ферменты экстрагируют солевыми растворами. Затем их разделяют на фракции, осаждая солями [обычно (NH 4 ) 2 SO 4 ] или, реже, органическими растворителями, и очищают методами гельпроникающей и ионообменной хроматографии. На заключительных этапах очистки часто используют методы аффинной хроматографии. Контроль за ходом очистки ферментов и характеристику чистых препаратов осуществляют, измеряя каталитическую активность ферментов с применением специфических (обычно дающих цветные реакции) субстратов. За единицу количества фермента принимают такое его количество, которое катализирует превращение 1 мк моля субстрата в 1 мин в стандартных условиях. Число единиц фермента, отнесенное к 1 мг белка, называется удельной активностью.
В мире производится около 20 ферментов в объеме 65 тыс. тонн (а существует, как предполагают 25000 ферментов). Например, промышленным способом производят такие ферменты как амилаза, глюкоамилаза, протеаза, инвертаза, пектиназа, каталаза, стрептокиназа, целлюлаза и другие.
Амилазы и протеазы используют в текстильной, хлебопекарной и кожевенной промышленности. Пектолитические ферменты могут быть использованы для мацерации тканей при переработке растительного сырья, например при получении льноволокна. Щелочные протеазы, особенно иммобилизованные, очень эффективно используются в составе моющих средств. Кроме протеолитических ферментов в состав моющих средств вводят липазу, целлюлазу, оксидазу и амилазу для удаления загрязнений крахмального происхождения. Использование иммобилизованной глюкозоизомеразы для непрерывного получения глюкозы является наиболее крупным процессом такого рода в мире.
Микробные ферменты активно используют в клинической диагностике при определении уровня холестерина в крови и мочевой кислоты. Ферменты предлагают использовать для очистки канализационных и водопроводных труб и т.д. и т.п. Ферменты для медицинских или аналитических целей должны быть высокоочищенными.
Иммобилизация и получение связанных ферментных препаратов стало возможным благодаря детальному изучению строения многих ферментов. Раскрыт аминокислотный состав ряда ферментных белков, их пространственная конфигурация, выявлены активные центры, значение различных функциональных групп в проявлении каталитической активности фермента и так далее.
Болезни, связанные с нарушением выработки ферментов
Отсутствие или снижение активности какого-либо фермента (нередко и избыточная активность) у человека приводит к развитию заболеваний (энзимопатий) или гибели организма. Так, передаваемое по наследству заболевание детей — галактоземия (приводит к умственной отсталости) — развивается вследствие нарушения синтеза фермента, ответственного за превращение галактозыв легко усваиваемую глюкозу. Причиной другого наследственного заболевания — фенилкетонурии, сопровождающегося расстройством психической деятельности, является потеря клетками печени способности синтезировать фермент, катализирующий превращение аминокислоты фенилаланинав тирозин. Определение активности многих ферментов в крови, моче, спинно-мозговой, семенной и других жидкостях организма используется для диагностики ряда заболеваний. С помощью такого анализа сыворотки крови возможно обнаружение на ранней стадии инфаркта миокарда, вирусного гепатита, панкреатита, нефрита и других заболеваний.
Если происходит мутация в гене, кодирующем определенный фермент, может измениться аминокислотная последовательность фермента. При этом в результате большинства мутаций его каталитическая активность снижается или полностью пропадает. Если организм получает два таких мутантных гена (по одному от каждого из родителей), в организме перестает идти химическая реакция, которую катализирует данный фермент. Например, появление альбиносов связано с прекращением выработки фермента тирозиназы, отвечающего за одну из стадий синтеза темного пигмента меланина. Фенилкетонурия связана с пониженной или отсутствующей активностью фермента фенилаланин-4-гидроксилазы в печени.
В настоящее время известны сотни наследственных заболеваний, связанные с дефектами ферментов. Разработаны методы лечения и профилактики многих из таких болезней.
1. Тарханов И. Р., Ферменты, в физиологии // Энциклопедический словарь Брокгауза и Ефрона: В 86 томах (82 т. и 4 доп.). — СПб., 1890—1907.
2. Энзимы // Энциклопедический словарь Брокгауза и Ефрона: В 86 томах (82 т. и 4 доп.).
3. Фершт Э. Структура и механизм действия ферментов. М., 1980.
5. Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохомия человека. Т. 1. М., 1993.
13. Березов Т.Т., Коровкин Б.Ф. Биологическая химия. М.: «Медицина», 2004, с. 114-116, 118-120, 129-134, 139-143, 159-163, 165-168.
14. Кушманова О.Д., Ивченко Г.М. Руководство к лабораторным занятиям по биологической химии. М.: М. Медицина, 1983, раб 24 (п. 1), 25.
15. Учебник Химии 11 класс, Кузнецова Н.Е., Литвинова Т.Н., Лёвкин А.Н. с.132.