Providencia rettgeri что это
Providencia rettgeri что это
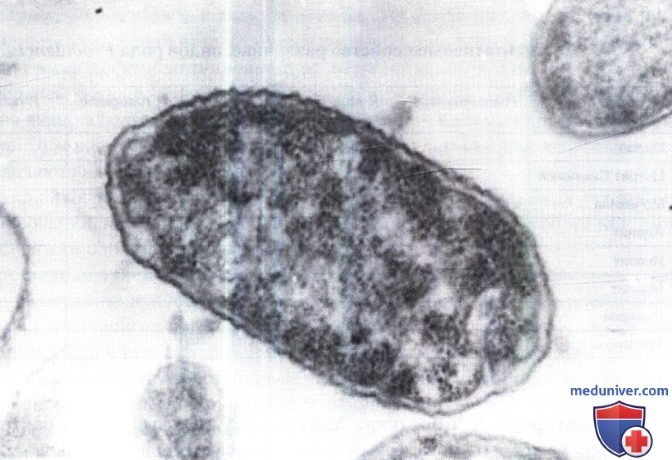
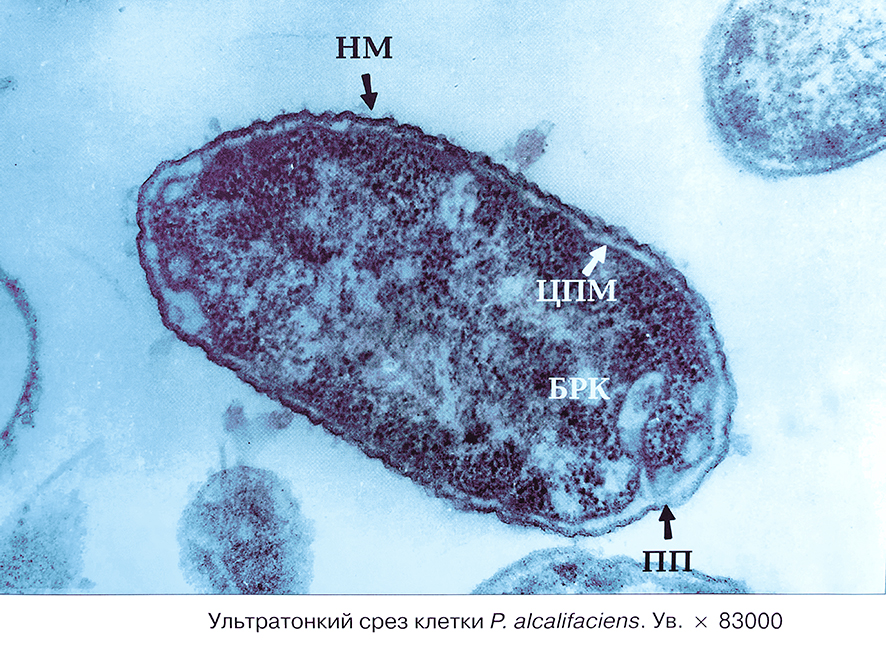
а) Таксономия. Бактерии Providencia — самостоятельный род в семействе Enterobacteriaceae. Город Providence, где они впервые были выделены, — столица штата Род-Айленд, расположенного в северо-восточной части США. В прошлом эти бактерии относили к роду Proteus в качестве отдельного вида Р. inconstans. В настоящее время результаты изучения биохимических, антигенных свойств, данные геносистематики позволили рассматривать бактерии Providencia как самостоятельный род в семействе Enterobacteriaceae, включающий в себя также следующие виды: Providencia alcalifaciens, Р. stuartii, Р. rettgeri, Р. rustigianii, Р. heimbachae. Ультратонкий срез Р. alcalifaciens представлен на рисунке ниже.
Провиденции входят в состав транзиторной нормальной микрофлоры кишечника человека и животных, и могут присутствовать в окружающей среде в качестве сапрофитной микрофлоры. Бактерии рода Providencia могут вызывать тяжелые осложнения у больных с ожогами, после операций, явиться причиной пневмонии, бактериемии, острых гастроэнтеритов. Р. stuartii и Р. rettgeri нередко обнаруживали в моче госпитализированных больных после катетеризации мочевого пузыря. Эти виды часто оказываются причиной внутрибольничных инфекций.
б) Морфология и биохимические свойства. Провиденщш — грамотрицательные палочки; спор и капсул не образуют; как правило, подвижны; обладают способностью дезаминировать аминокислоты; не содержат декабоксилаз лизина и орнитина, не образуют сероводорода; мочевину гидролизуют только Р. rettgeri и некоторые представители Р. stuartii. Внутриродовая дифференциация возможна по признакам, представленным в таблице ниже.
Детальное изучение ферментативных свойств штаммов Providencia, выделенных из различных источников, позволило разным авторам дифференцировать исследованные штаммы на биотипы, что важно с эпидемиологической точки зрения. Так, в зависимости от способности образовывать газ из глюкозы и ферментировать адонит и инозит было определено два биотипа у Р. alcalifaciens и три у Р. stuartii. Неодинаковое отношение к салицину и рамнозе привело к выделению четырех биотипов Р. rettgeri.
Было показано, например, что штаммы Р. rettgeri, полученные от больных с хирургической, урологической патологией, дисфункцией желудочно-кишечного тракта, принадлежали главным образом к 4-му биотипу — не ферментировали ни салицин, ни рамнозу.
в) Факторы патогенности. Как и все энтеробактерии, провиденции обладают эндотоксином (ЛПС). Некоторые штаммы способны синтезировать фимбриальные адге-зины, различного тина энтеротоксины, разнообразные протеолитические ферменты, ДНК-азы, РНК-азы и др..
г) Лабораторная диагностика. Материалом для выделения бактерий рода Providencia может быть моча, фекалии, рвотные массы, пищевые продукты, кровь, отделяемое ран, генитального тракта и др. Исследуемый материал (кроме стерильных в норме жидкостей организма) сеют количественным методом, для чего после гомогенизации проб готовят десятикратные разведения в буферном фосфатном растворе. Бактериологическое исследование соответствует стандартной схеме.
Второй день. Просматривают чашки, засеянные накануне. Подсчитывают число выросших колоний каждого вида. Отбирают подозрительные колонии для дальнейшего изучения. На среде Эндо Providencia образуют небольшие бледно-розовые прозрачные колонии, на агаре Плоскирева — колонии прозрачные с желтоватым оттенком. Для исследования отбирают не менее 3 однородных но виду колоний или 2-3 колонии каждого вида, если на чашках обнаружен разновидный рост.
Отобранные колонии (каждую отдельно) засевают петлей в полужидкий агар, под пробку пробирки помещают полоску индикаторной бумаги на индол; агар Клиглера (не забыть проткнуть столбик среды!), цитратный агар Симмонса, среду с мочевиной (посевы производят бактериологической петлей из одной пробирки в другую в указанном порядке, не прожигая петли). Посевы инкубируют в термостате при 37°С в течение 18-24 ч.
Третий день. Учитывают результаты ферментативной активности. Культуры, не ферментирующие лактозу, не продуцирующие сероводорода, образующие индол (индол-отрицательны только Р. heimbachae), не гидролизующие мочевину (уреазой обладают только Р. rettgeri и некоторые представители Р. stuartii), утилизирующие или не утилизирующие цитрат в качестве единственного источника углерода, подозрительны на принадлежность к роду Providencia. Для подтверждения родовой принадлежности и определения вида требуется провести дополнительные тесты: в первую очередь посев на фенилаланиновый агар и другие.
Четвертый день. Учитывают полученные результаты. При положительной реакции на фенилаланиновом агаре (появление темно-зеленого окрашивания при добавлении 10%-ного водного раствора FeCl3) и по результатам дополнительных тестов определяют вид выделенных бактерий.
Как и при лабораторном исследовании других условно-патогенных энтеробактерий, при обнаружении бактерий одного вида в концентрации 10 5 и более КОЕ/мл, они могут быть заподозрены в качестве этиологического агента.
д) Лекарственная чувствительность. Провиденции обычно чувствительны к канамицину и гентамицину, устойчивы ко многим антибактериальным препаратом, в частности, к полимиксину, цефалотину, тетрациклину. Приобретенная резистентность формируется в процессе лечения и зависит от тактики выбора и назначения препаратов. Полиантибиотикоустойчивые штаммы провиденций нередко являются причиной оппортунистических инфекций у иммунокомпрометированных больных. Чувствительность к антибиотикам определяют общепринятыми методами, чаще используют диско-диффузионный метод на среде АГВ или агаре Мюллера-Хинтона.
Редактор: Искандер Милевски. Дата публикации: 6.4.2020
PROVIDENCIA
Providencia — род грамотрицательных бактерий, относящихся к трибе Proteae семейства Enterobacteriaceae.
В роде Providencia различают два биохимических вида: Providencia alcalifaciens и Providencia stuartii. В определителе бактерий Берджи (1974) род Providencia представлен как вид Proteus inconstans, разделенный на две подгруппы — А и В. Providencia — грамотрицательные, не образующие спор и капсул, подвижные (или неподвижные) палочки, расположенные единично или короткими цепочками, размером 0,4—0,6 х 1,0—3,0 мкм. Они являются факультативными анаэробами, хорошо растут при t 37° на обычных питательных средах, на слабощелочном агаре образуют изолированные колонии без склонности к роению.
Providencia не ферментируют лактозу, из углеводов постоянно сбраживают только глюкозу, иногда со слабым газообразованием, утилизируют цитрат, не гидролизуют мочевину, дают отрицательную реакцию Фогеса — Проскауэра (см. Фогеса-Проскауэра реакция) и положительную реакцию с метиловым красным, не разжижают желатину, не образуют сероводорода, образуют индол, растут на среде с цианистым калием, восстанавливают нитраты в нитриты, обладают ферментом фенилаланиндезаминазой, но не имеют лизин-, орнитин-декарбоксилазы, аргининдегидролазы и цитохромоксидазы. К виду Р. alcalifaciens относят штаммы, образующие газ при ферментации глюкозы, ферментирующие адонит и не ферментирующие трегалозу; к виду P. stuartii — штаммы, не обладающие этими свойствами и ферментирующие трегалозу и инозит.
Providencia имеют О- и H-антигены; у отдельных штаммов описаны a-, ß- и К-антигены. По антигенной структуре род Р. включает 63 серологические О-группы и 30 различных Н-антигенов, сочетания к-рых образуют более 150 серологических вариантов.
Providencia описаны как возбудители групповых или спорадических острых кишечных заболеваний у детей и взрослых, при этом отдельные серологические варианты Providencia. рассматриваются как энтеропатогенные, другие же могут быть выделены и от здоровых людей. Они являются частым этиол. фактором в возникновении урологических инфекционных заболеваний. Возросло их этиол. значение и в развитии тяжелых септических осложнений у больных с ожогами и после оперативных вмешательств. Одной из причин повышения этиологического значения Providencia в развитии различных заболеваний считают распространение патогенных разновидностей микроорганизмов с высокой устойчивостью к большинству антибиотиков.
Микробиологическая диагностика заболеваний, вызываемых Providencia, основывается на выделении чистой культуры при посеве исследуемого материала на дифференциально-диагностические и элективные среды для бактерий кишечной группы и дальнейшей дифференциации ее от других представителей семейства Enterobacteriaceae по основным дифференциальнодиагностическим тестам: отсутствие гидролиза мочевины, образования сероводорода и разжижения желатины, а также продукция фенилаланиндезаминазы и утилизация цитрата. Выделенная по этим признакам культура идентифицируется диагностическими О- и Н-сыворотками до определения серологического варианта.
Библиогр.: Батуро А. П. и др. Значение условно патогенных кишечных бактерий в хирургии, Хирургия, № 12, с. 93, 1976; Холодкова Е. В. и Рагинская В. П. Бактерии рода Providencia, Журн. микр., эпид. и иммун., № 5, с. 56, 1972; Bergey’s manual of determinative bacteriology, ed. by R. E. Buchanan a. N. E. Gibbons, p. 327, Baltimore, 1975; Edwards P. R. a. Ewing W. H. Identification of enterobacteriaceae, p. 331, Minneapolis, 1972; Penner J. L. a. o. Reconstitution of the somatic (O-) antigenic scheme for Providencia and preparation of O-typing antisera, J. infect. Dis., v. 133, p. 283, 1976; Penner J. L. а. о. О serotyping of Providencia stuartii isolates collected from twelve hospitals, J. clin. Microbiol., v. 9, p. 11, 1979.
Инфекции, вызываемые возбудителями рода PROTEUS (Протей)
В последние годы инфекционисты отмечают рост заболеваний, обусловленных нетрадиционными микроорганизмами. Особое место занимает протейная инфекция. Ее кишечная форма, вызванная бакетриями рода Протей — P. vulgaris протекает тяжелее у детей раннего возраста. Не менее опасны гнойно-воспалительные заболевания мочевыводящей системы, вызываемые P. mirabilis, P. rettgeri и P. morganii.
В греческой мифологии Протей – божество, способное менять облик. Отсюда название полиморфных, мелких, нитевидных палочек, отличающихся активной подвижностью. Размеры клеток составляют 0,5 — 3 мкм. P. morganii, P. rettgeri — менее полиморфны и малоподвижны.
Протейная инфекция: причины, развитие, опасность для организма
Возбудителями протейной инфекции являются грамотрицательные условно-патогенные микроорганизмы семейства энтеробактерий, которые присутствуют в нормальной микрофлоре кишечника, а также повсеместно распространены в воздухе, почве и воде. Бактерии рода Proteus в течение долгого времени не причислялись к возбудителям серьезных инфекционно-воспалительных заболеваний. Однако в связи с последними достижениями в области диагностики было обнаружено, что эти микроорганизмы способны вызывать трудно поддающиеся лечению патологии (протеозы), поражающие преимущественно ЖКТ и мочеполовую систему.
Протей – факультативный анаэроб, палочковидная, неспороносная, подвижная, грамотрицательная бактерия. В микробиологическом анализе кала протей встречается в комплексе с другими условно-патогенными бактериями семейства энтеробактерий. Кроме протея, в составе нормальной микрофлоры кишечника человека определяются: клебсиелла, энтеробактер, гафния, серратия, морганелла, провиденция, цитробактер. В 1 г кала должно быть меньше 10 4 общего количества этих бактерий. Большее количество перечисленных бактерий является признаком дисбактериоза.
В природе бактерии рода Proteus обнаруживаются: в сточных водах, в земле, в водоемах, на овощах, в разлагающихся органических веществах. Эти микроорганизмы — сапрофиты, они живут на слизистых оболочках, на коже, в кишечнике человека и животных. Протеи устойчивы во внешней среде и сохраняют жизнедеятельность в слабых растворах фенола и других средств. Выявлена также резистентность ко многим антибиотикам.
Причины протейной инфекции
Протейная палочка, присутствующая в кишечной микрофлоре в небольших количествах, не причиняет организму никакого вреда. При определенных обстоятельствах (снижение иммунитета, неправильное питание, длительный прием антибиотиков) она может активизироваться и начать интенсивно размножаться. Также инфицирующее количество этих бактерий способно проникнуть в организм из внешней среды.
Основными путями передачи инфекции являются пищевой и контактно-бытовой. Чаще всего заражение происходит при употреблении белковых продуктов (мяса, рыбы, молока, колбасы), которые хранились с нарушением надлежащих сроков и условий. Значительно реже инфицирование осуществляется через немытые руки, во время купания или при употреблении зараженной воды.
Инфицирование протеем может произойти через полуфабрикаты, сырые продукты или готовые блюда из мяса, рыбы, молока, колбасы, студня. В них происходит быстрое размножение бактерий с образованием токсинов. Реже отмечают водный путь передачи: при купании в загрязненных водоемах или употреблении инфицированной воды. Возможен и контактный путь передачи на инфицированных руках зараженного человека.
Развитие патологии
При непосредственном попадании протея в ЖКТ вместе с продуктами питания инфекционное заболевание развивается очень стремительно. Первые симптомы ярко выражены, а общая клиническая картина совпадает с проявлениями сильного пищевого отравления. При контактно-бытовом способе заражения развитие признаков инфекции обычно происходит медленнее.
Если инфекционный процесс протекает в легкой форме, больной испытывает слабость, у него отмечаются повышение температуры, рвота, боль в животе, частый водянистый стул, в котором могут обнаруживаться слизь и зеленые включения. При тяжелом течении заболевания приступы рвоты случаются около 10 раз за сутки и более, а температура обычно поднимается до 40°С.
При условии своевременного и адекватного лечения вся острая симптоматика протеоза легкой или средней степени тяжести исчезает спустя несколько дней, после чего больной быстро идет на поправку.
Протеи выделяют токсические вещества — эндотоксины с гемолитическими свойствами и с различной степенью биохимической активности. У штаммов P. vulgaris обнаружена лецитиназная активность. Протеи обладают способностью адгезии к уротелию при помощи ресничек. Отмечают, что резистентность к антибиотикам связана с адгезивной способностью уропатогенных протеев.
Острой кишечной протейной инфекцией, протекающей по типу гастроэнтерита, гастрита и колиэнтерита часто болеют дети раннего возраста с пониженным иммунитетом и после бесконтрольного назначения антибиотиков. Заболевание сопровождается симптомами токсикоза — повышением температуры, рвотой, метеоризмом, схваткообразными болями в животе, нарушением аппетита, кратковременными судорогами, появлением водянистого, зловонного, учащенного стула.
В тяжелых случаях могут развиться осложнения: гемолитико-уремический синдром, а также симптомы острой гемолитической тромбопении, анемии или острой почечной недостаточности.
Клинические проявления внутрибольничной инфекции протейной этиологии весьма разнообразны: поражения мочевыводящей системы, отиты, холециститы, нагноения ран и септические состояния. Попадание протеев в пупочную ранку новорожденного может привести к бактериемии или развитию менингита.
Данные заболевания могут развиться: при передаче возбудителя контактно-бытовым или воздушно-капельным путями, при заносе с катетером, другими урологическими инструментами.
Если в мазках исследуемого материала (участки ожоговой ткани, гной, раневое отделяемое, испражнения) обнаруживаются грамотрицательные палочки, то бактериоскопический метод позволяет сделать предварительное заключение. Бактериологическим методом на средах определяют колонии протея в виде тонкого стелющегося налета. Активно размножаются протеи на белковой питательной среде вызывают гниение мяса, рыбы, других белковых продуктов.
Важнейшие профилактические меры — это соблюдение санитарного режима в детских учреждениях и стационарах, проведение общесанитарных мероприятий. Для профилактики протея каждому необходимо соблюдать правила личной гигиены, исключить потребление подозрительных продуктов в питании, избегать контактов с больными детьми и взрослыми.
При лечении протейной инфекции следует придерживаться лечебной щадящей диеты с исключением жареных, острых блюд, белковых продуктов. В острый период протейного инфицирования, при поражении желудочно-кишечного тракта — необходимо обеспечить восполнение потерянной жидкости. Полезно употреблять отвары трав – тысячелистника, алтея, зверобоя, ромашки, календулы; морсы, компоты с клюквой, черной смородиной, абрикосами, черникой, яблоками. Применять антибиотики можно только по назначению врача, в соответствии с данными анализов чувствительности бактерии протея к ним.
Обязательно нужно принимать препараты – пробиотики, пребиотики, синбиотики для восстановления нормальной флоры кишечника.
Синбиотические комплексы Нормофлорины, содержащий живые активные лакто- и бифидобактерии, секретирующие молочную, уксусную, масляную, пропионовую кислоты, оказывающие защитное, антисептическое, противовоспалительное, сорбционное действие – уменьшает интоксикацию, улучшает моторику кишечника, функцию печени, повышает иммунную реактивность. Это помогает в борьбе с протейной инфекцией, восстанавливает работу желудочно-кишечного тракта, общее самочувствие, повышает иммунитет.
Схема (возрастные дозировки для детей или взрослых): (взрослый) нормофлорин Л – 20 мл (при диарее) – 40 (при запорах) мл утром перед едой, Д — 40 мл вечером за 20 мин до еды, Б – 20-30 мл на ночь в клизме. При диарее в обед можно добавить Д – 30-40 мл, при запорах в обед + Л – 30-40 мл.
Курс приема нормофлоринов — 1 — 1,5 месяца, для выведения токсинов, патогенной микрофлоры, восстановления полезных собственных бактерий. Уникальный состав нормофлоринов, не содержащих белков коровьего молока, молочного сахара, консервантов позволяет при протейной инфекции успешно применять его у детей с первых дней жизни, беременных, кормящих, больных сахарным диабетом, аллергическими заболеваниями, т.е. у взрослых при любой сопутствующей патологии.
Опасность протейной инфекции

Тяжелые формы патологии могут осложняться состояниями, требующими срочной госпитализации больного, такими как сильное обезвоживание, судороги, инфекционно-токсический шок.
protey_mirabilis
Помимо острых инфекций пищеварительной системы бактерии Proteus способны поражать другие органы, распространяясь через кровь или по лимфатическим сосудам. Очаг воспаления может локализоваться в мочеполовой системе, глазах, ушах, легких и даже в костной ткани или мозговых оболочках. Данные патологии достаточно часто переходят в хроническую форму с упорным рецидивирующим течением, которая тяжело поддается терапии.
Если протейная инфекция заносится на незажившие поверхности кожи и слизистых оболочек (послеоперационные раны, ожоги), вызванный ею воспалительный процесс значительно замедляет регенерацию тканей и снижает эффективность лечебных мероприятий.
Следует отметить, что даже незначительное превышение нормального количества протейной палочки в кишечной микрофлоре может негативно отразиться на состоянии здоровья. Так, если у человека имеются аутоиммунные болезни, существует высокий риск их обострения из-за возросшей активности протейной палочки. Атопический дерматит, астма, аллергические заболевания и другие иммунозависимые патологии могут впервые развиться или обостриться под воздействием бактерий Proteus.
Инфекции, вызванные Proteus, Morganella и Providencia
Этиология
Род Proteus семейства Enterobacteriaceae включает грамотрицательные бактерии, не ферментирующие лактозу и характеризующиеся активной подвижностью и ползучим распространяющимся ростом на поверхности плотных питательных сред. Микроорганизмы, которые ранее были классифицированы и отнесены к роду Proteus, после недавно проведенного детального изучения ДНК получили новые названия. Р. morganii был классифицирован как Morganella morganii, тогда как некоторые биогруппы В. rettgeri были реклассифицированы как Providencia stuartii и Providencia rettgeri. P. mirabilis и Р. vulgaris сохранили свою номенклатуру. Р. mirabilis вызывает 75—90% инфекций человека и отличается от других упомянутых микроорганизмов тем, что не обладает способностью образовывать индол. Все четыре вида расщепляют мочевину с образованием аммония. Некоторые штаммы Р. vulgaris имеют общий антиген с определенными риккетсиями, за счет которого объясняется появление антител к протеям (реакция Вейля — Феликса) при тифе, японской речной лихорадке (цуцугамуши) и лихорадке Скалистых гор. Микроорганизмы, объединяемые в группу Providencia, очень тесно примыкают к представителям рода протеев, отличаясь от них только некоторыми биохимическими свойствами.
Эпидемиология и патогенез
Эти микроорганизмы в норме обнаруживаются в почве, воде и сточных водах и входят в состав нормальной флоры кишечника. Иногда им приписывают этиологическую роль при диареях детей раннего возраста, но это не получило достаточных подтверждений. Их часто обнаруживают в посеве из отделяемого поверхностных ран, дренированных полостей среднего уха и из мокроты, особенно у больных, получавших антибиотики. В подобных условиях они замещают более чувствительную флору, погибающую под действием этих препаратов.
Проявления
Указанные микроорганизмы редко служат причиной первичного поражения. Обычно они вызывают заболевание в участках, ранее инфицированных другими возбудителями: на коже, в ушах, сосцевидном отростке, синусах, глазах, брюшной полости, костях, мочевом тракте, мозговых оболочках, легких, кровяном русле.
Кожные инфекции. Эти микроорганизмы присутствуют в отделяемом хирургических ран, особенно после антимикробной терапии, но никогда не присоединяются к нормальной раневой микрофлоре, если происходит нормальное заживление, ткани жизнеспособны и нет инородных тел. Часто в ассоциации с другими грамотрицательными бактериями или стафилакокками они могут инфицировать ожоговые поверхности, варикозные раны, язвы, образующиеся при пролежнях.
Инфекции уха и сосцевидного синуса. Воспаление среднего уха и мастоидит, особенно вызванные Р. mirabilis, могут привести к обширной деструкции среднего уха и сосцевидного синуса. Зловонные выделения, холестеатома и грануляционная ткань составляют хронический фокус инфекции в среднем и внутреннем ухе и в сосцевидном отростке, в результате чего развивается глухота. В качестве случайного осложнения возможно развитие паралича лицевого нерва. Основная опасность этих инфекций заключается в возможности их распространения в полость черепа, что ведет к тромбозу бокового синуса, менингиту, абсцессу мозга и бактериемии.
Инфекции глаз. Эти микроорганизмы могут вызывать язвы роговицы, обычно возникающие в результате травмы глаз, заканчивающиеся панофтальмитом и деструкцией глазного яблока.
Перитонит. Будучи составной частью нормальной микрофлоры кишечника, представители этих родов могут выделяться из брюшной полости после перфорации внутренних органов или инфаркта кишечника.
Инфекции мочевого тракта. Эти микроорганизмы служат основной причиной инфекционных поражений мочевого тракта, особенно у больных с хронической бактериурией, многие из которых страдают обструктивной уропатией, имеют в анамнезе сведения об инструментальном вмешательстве на мочевом пузыре и повторных курсах химиотерапии. Их часто выделяют от больных с калькулезными поражениями почек или мочевого пузыря, сопровождающимися бактериурией. Это можно объяснить уреазной активностью этих микроорганизмов, обусловливающей щелочную реакцию мочи и обеспечивающей благоприятную среду для формирования аммонийно-магниево-фосфатных камней.
Бактериемия
Внедрение в кровоток—это наиболее серьезное проявление инфекции, вызванной представителями родов Proteus, Morganella и Providencia. В 75% случаев входными воротами инфекции служит мочевой тракт; в остальных случаях первичным фокусом являются желчные протоки, желудочно-кишечный тракт, уши, синусы, кожа. Развитию бактериемии часто предшествуют такие процедуры, как цистоскопия, катетеризация мочеточника, трансуретральная резекция предстательной железы или другие оперативные вмешательства. Клинические признаки, симптомы и лабораторные показатели сепсиса — повышение температуры тела, озноб, шок, метастатические абсцессы, лейкоцитоз и иногда тромбоцитопения — сходны с аналогичными признаками бактериемии, вызванной кишечной палочкой, клебсиеллами или другими грамотрицательными бактериями.
Диагностика
Диагноз инфекции, вызванной Proteus, Morganella или Providencia, зависит от результатов культурального выделения этих микроорганизмов из крови, мочи или экссудата и их идентификации с помощью соответствующих биохимических тестов. Особенно важно отделить Р. mirabilis, индол-отрицательный вид, от индол-положительных микроорганизмов, так как Р. mirabilis чувствителен к действию пенициллина и многих других антибиотиков. Представители рода протеев часто обнаруживаются в ассоциации с другими возбудителями. Особое внимание было обращено на выделение микроорганизмов, не относящихся к Р. mirabilis или Р. vulgaris, но растущих на тех же питательных средах, чтобы они не были за маски рованы ползучим ростом протея. Распространенный ползучий характер роста этих бактерий затрудняет также интерпретацию результатов определения их лекарственной чувствительности.
Лечение
Большинство штаммов Р. mirabilis чувствительны к пенициллину в высоких концентрациях (10 ЕД в 1 мл или больше), к ампициллину, карбенициллина динатриевой соли, гентамицину, тобрамицину или амикацину, а также к цефалоспориновым антибиотикам. Бактериурия, вызванная Р. mirabilis, может быть быстро ликвидирована с помощью любого из перечисленных антибиотиков. Наиболее эффективен при этой форме инфекции ампициллин в дозе 0,5 г каждые 4—6 ч. При тяжелой инфекции лечение следует проводить парентерально: от 6 до 12 г ампициллина или 20000000 ЕД пенициллина G в-сочетании с тобрамицином или гентамицином в дробных дозах по 5 мг/кг в сутки, если не повреждена функция почек. Существуют некоторые данные, что при инфекциях, вызванных
P. mirabilis, аминогликозиды обладают синергическим действием с ампициллином и пенициллином G. В связи с наличием большого числа более эффективных препаратов при инфекциях, обусловленных Р. mirabilis, нет необходимости применять левомицетин. Все штаммы Р. mirabilis устойчивы к тетрациклину. Большинство же штаммов, не относящихся к Р. mirabilis, чувствительны только к аминогликозидам и цефалоспоринам третьего поколения. Карбенициллин, тикарциллин и новые уреидопенициллины эффективны в отношении штаммов, выделенных из клинического материала. В идеале терапия должна основываться на результатах определения лекарственной чувствительности in vitro, а при отсутствии их — на знании характерных образцов. Так же как и в отношении других инфекций, вызванных грамотрицательными микроорганизмами, соответствующее внимание должно быть уделено дренированию гноя, поддержанию баланса жидкости и электролитов и при наличии эндотоксического шока — лечению циркуляторного коллапса.