Staphylococcus haemolyticus у мужчин в секрете простаты что это
Стафилококк: как выявить и вылечить
Это особая категория бактериальных культур, многие виды которой опасны для человеческого здоровья. Стафилококки принято называть условно-патогенными микробами. Обитая в организме постоянно, они находятся под контролем иммунитета. Но при ослаблении защиты могут спровоцировать воспалительный процесс. Некоторые бактерии чрезвычайно устойчивы к антимикробным средствам и нередко становятся причиной суперинфекций.
Что такое стафилококк
Это неподвижный грамположительный микроорганизм шаровидной формы, образующий многочисленные колонии. Стафилококки анаэробны — могут существовать и размножаться без участия кислорода, в закрытой среде. Штаммов бактерий насчитывается более двадцати. Некоторые из них довольно безобидны, а другие вызывают мощные патологические реакции в человеческом организме. Части тела и органы, наиболее уязвимые перед стафилококками:
Поражая их, микробы вырабатывают токсичные вещества, провоцируют воспаления, в тяжелых случаях приводящие к сепсису, необратимым изменениям структур или стойким нарушениям функций.
Виды патогенных стафилококков
Для человека опасны несколько разновидностей бактерий. Самые распространенные:
Staphylococcus aureus: золотистый. Название получил из-за характерного желтого пигмента на поверхности. Проникая в организм, синтезирует фермент коагулазу, может вызывать гнойные воспаления почти любых внутренних органов. Этот вид патогена быстро приспосабливается к воздействию антибиотиков, образуя резистентные формы.
Staphylococcus epidermidis: эпидермальный. Поражает обычно кожные покровы слизистые оболочки. Часто становится фактором воспаления повреждений, послеоперационных швов, развития гнойного конъюнктивита, инфекций дыхательных путей.
Staphylococcus saprophyticus: сапрофитный. Его специфика: поражать слизистые мочевыводящих органов, провоцировать цистит, уретрит, почечные воспаления.
Staphylococcus haemolyticus: гемолитический. Опасен для слизистых и тканей внутренних органов. Становится провокатором развития эндокардита, пневмоний, нефритов и других тяж елых патологий.
Практически все типы патогенных стафилококков склонны к мутациям в результате неправильного или недостаточно продолжительного лечения.
Как проявляется стафилококковая инфекция
Симптоматика, ее длительность и интенсивность зависят от штамма возбудителя, общего физического состояния больного и особенностей его иммунитета. Два характерных признака поражения стафилококком: воспаления различной локализации и интоксикация.
При пиодермии воспаляются потовые, сальные железы, волосяные фолликулы, из-за чего на коже образуются болезненные выпуклые узелки, наполняемые гноем. Фурункулы и карбункулы обычно окружены участками покрасневшей отекшей кожи. При интенсивном воспалении вероятно появление лихорадки, набухание близко расположенных к очагам воспаления лимфоузлов.
Поражение пазух носа стафилококком проявляется банальным насморком с вязкими желтоватыми или зел еными выделениями. Проникновение инфекции глубже вызывает развитие синуситов. Их симптомы характерны:
заложенность в области переносицы;
ощущение тяжести, распирания с пораженной стороны;
густые гнойные выделения из носа;
повышение температуры тела выше +37°С.
Нередко инфекция распространяется на среднее ухо, вызывая отит: резкие стреляющие боли, снижение слуха. При поражении слизистых глаз развивается нагноение конъюнктивы, склеры краснеют и отекают.
При атаке стафилококком верхних дыхательных путей неизбежны гнойные фарингиты или ларингиты. Их признаки:
сильная отечность, покраснение глотки;
затрудненное болезненное глотание;
сухой навязчивый кашель, дискомфорт в горле.
Часто стафилококковые фарингиты поражают детей младше 12 лет. У взрослых эта патология контролируется иммунитетом.
При развитии воспалений в нижних отделах дыхательных путей «актуальны» бронхит и пневмония с характерным лающим или мокрым кашлем, высокой температурой температурой и физической слабостью.
Менее распространенные признаки поражений стафилококком:
воспаления суставных тканей, мышц;
нарушения работы сердца.
Среди грозных осложнений, вызываемых стафилококком: менингит, абсцессы л егких, остеомиелит, синдром токсического шока, генерализованный сепсис.
Как лечить стафилококк
Точный диагноз — виновен ли микроб в патологии, можно установить только после лабораторного анализа. Обнаружить и идентифицировать его в пробах мочи, мазках и соскобах с кожных покровов и слизистых не составляет труда. А вот избавиться от заразы намного тяжелее. Печально известный стафилококк аурум (золотистый) чрезвычайно устойчив к воздействию дезинфекторов, в том числе к хлорке и «зеленке». Почти 15%всех случаев заражения им происходят внутри больниц.
Применение антибиотиков тоже не всегда оправдано. К пенициллинам, например, стафилококки приспосабливаются очень быстро. А золотистый давно к ним устойчив, как ко многим другим медикаментам. Для быстрого подавления активности патогенов применяют комбинации различных групп препаратов. Относительно новые и эффективные: макролиды и фторхинолоны. Лекарства этих категорий разрушают и уничтожают белковые оболочки бактерий, не давая им времени для развития резистентности.
Чтобы терапия оказалась действенной, важно применять антимикробным средства только по назначению врача, четко следовать указанной схеме. Запрещено прерывать курс по своему разумению, менять без разрешения один препарат на другой, корректировать дозировку.
В качестве профилактики заражения необходимо соблюдать общие правила гигиены. Важно избегать употребления непроверенных продуктов, вовремя санировать полость рта, лечить насморк. Полезно закаляться, принимать иммуномодуляторы. А главное — не применять антимикробные средства без веских причин.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Стафилакокк в простате 36,77см
Добрый день. Сделал узи предстательной железы и мошонки, в результате было выявлено увеличение предстат.железы(36.77) и варикоциле мошонки(прикрепил фото). По назначению уролога, сделал посев секрета простаты на условно-патогенную микрофлору, в результате был выявлен Staphylococcus haemolyticus. На данный момент продолжают беспокоить неприятные ощущения при мочеиспускании.
———————————————————————————————————————————————————————————————————————————————————————————————————————————————————————————————————————Предыдущий вопрос от 23 января https://sprosivracha.com/questions/108897-neznachitelnoe-zhzhenie-v-polovom-chlene——————————————
Здравствуйте, в декабре был случайный незащищенный половой акт, после этого спустя некоторое время, появилось жжение при мочеиспускании. Сдал анализы на половые инфекции(+общий мочи,крови),результаты анализа прикрепил к вопросу. В результате была обнаружена уреаплазма.
С уреаплазмой сталкиваюсь не в первый раз, до этого принимал Юнидок Солютаб в декабре 2017 года и марте 2018 года. Позже опять заражался от партнера.
В декабре, опять пропил Юнидокс Солютаб курсом. 10 дней по 2 таблетки каждые 12 часов. Во время приема антибиотика-жжения не было, по прекращению-жжение появилось.
Сейчас незначительное жжение в половом члене появляющиеся время от времени.
Уважаемые посетители сайта СпросиВрача! Рекомендуем Вам перейти на страницу консультации и узнать, что лечит уролог для того, чтобы решить Вашу проблему индивидуально. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос врачу и получите ответ сразу же!
Современные подходы к терапии хронического бактериального простатита
Хронический простатит (ХП) принадлежит к числу самых распространенных урологических заболеваний. По данным Н. А. Лопаткина (1998), в России на долю ХП приходится до 35% всех обращений к врачу по поводу
Хронический простатит (ХП) принадлежит к числу самых распространенных урологических заболеваний. По данным Н. А. Лопаткина (1998), в России на долю ХП приходится до 35% всех обращений к врачу по поводу урологических проблем среди мужчин в возрасте от 20 до 50 лет. Для получения данных о частоте встречаемости симптомов простатита с оценкой распространенности дизурии, дискомфорта в промежности и в области полового члена было проведено международное (Англия, Франция, Голландия, Корея) эпидемиологическое исследование Urepik. Анализ, проводившийся на основании шкалы симптомов Nickel и Sorensen (1996), дал возможность выявить признаки простатита у 4800 мужчин в возрасте от 40 до 79 лет. У 35% мужчин за последний год наблюдался как минимум один из симптомов простатита, и для 8% мужчин это представляло, по меньшей мере, неудобство [1].
На долю хронического бактериального простатита (ХБП) приходится 5–15% случаев заболевания [6]. Наиболее распространенными, по мнению большинства исследователей, этиологическими агентами ХБП являются такие грамотрицательные бактерии семейства Enterobacteriaceae, как Escherichia coli, которые обнаруживаются в 65–80% случаев инфекций. Различные виды Serratia, Klebsiella, Enterobacter, Acinetobacter выявляются у 10–15% больных. Большинство исследователей полагают, что на долю таких грамположительных бактерий, как Enterococcus faecalis, приходится от 5 до 10% случаев подтвержденных инфекций простаты [5].
В настоящее время обсуждается роль грамположительных бактерий — коагулазо-негативных стафилококков и стрептококков в развитии ХБП [5, 6, 7]. По нашим данным (Е. Б. Мазо и соавт., 2003, 2004) [1], основанным на результатах микробиологического исследования, которое проводилось в виде четырехстаканного теста Meares–Stamey у 70 больных с ХБП с 2002 г., именно коагулазо-негативные стафилококки играют ведущую роль (66%), если говорить об этиологии ХБП. Между тем на долю грамотрицательных патогенов приходится 19% случаев ХБП, а 15% составляют больные с Enterococcus faecalis. Аналогичными данными располагают М. Ф. Трапезникова и соавторы (2004), суммировавшие результаты идентификации 662 штаммов микроорганизмов у 264 больных ХБП, за которыми велось наблюдение в течение последних 13 лет. При этом выявлена ведущая роль грамположительных кокков в этиологии ХБП: за последние 3 года частота распространения коагулазо-негативных стафилококков составила 87,5% [3]. В то же время удельный вес грамотрицательных палочек — «общепризнанных» возбудителей ХБП — за предыдущие 7 лет неуклонно снижался (с 13,3 до 4,2%). С. Н. Калинина, В. П. Александров, О. Л. Тиктинский (2003) при обследовании 174 больных ХБП также выявили преобладание (82%) грамположительной флоры. Инфекция простаты может быть следствием бактериальной колонизации мочеиспускательного канала. Нормальная флора мочеиспускательного канала у мужчин состоит главным образом из дифтероидов и грамположительных кокков. Сексуальная активность может способствовать колонизации мочеиспускательного канала потенциальными уропатогенами. Blacklock (1974) и Stamey (1980) отметили, что секрет простаты у некоторых мужчин с ХБП содержал те же уропатогены, которые присутствовали в вагинальной флоре их сексуальных партнерш. Бактериальная колонизация может также вызвать персистенцию бактерий в простате. Отличительной чертой этого состояния является персистенция бактерий внутри простаты, несмотря на лечение антибиотиками, что связано с хроническим воспалением и склонностью к обострению инфекции мочевыводящего тракта тем же самым патогеном.
К предрасполагающим факторам развития ХБП относятся: уретропростатический рефлюкс; фимоз; анально-генитальные сношения без предохранения; инфекции мочевых путей; острый эпидидимит; постоянные уретральные катетеры и проведение трансуретральных операций у мужчин с инфицированной мочой без предшествующей антимикробной терапии [1]. У пациентов с ХП может быть выявлено нарушение секреторной функции простаты, характеризующееся изменением состава секрета, т. е. снижением уровней фруктозы, лимонной кислоты, кислой фосфатазы, катионов цинка, магния и кальция; цинксодержащего антибактериального фактора простаты. При этом увеличиваются такие показатели, как рН, отношения изоферментов лактатдегидрогеназы-5 к лактатдегидрогеназе-1, белков воспаления — церулоплазмина и компонента комплемента С3. Эти изменения в секреторной функции простаты также обусловливают неблагоприятное воздействие на антибактериальную природу секрета простаты. Уменьшение действия антибактериального фактора простаты способно снижать врожденную противобактериальную активность секрета, тогда как щелочной показатель рН может препятствовать диффузии в ткань и в секрет простаты основных антимикробных препаратов.
Симптомами ХП являются боли в тазовой области, расстройства мочеиспускания и эякуляции (см. табл. 1).
| Таблица 1 Симптомы хронического простатита | ||
| Локализация боли в тазовой области | Расстройство мочеиспускания | Расстройство эякуляции |
| В промежности В половом члене В яичках В паховой области Над лоном В прямой кишке В крестце | Учащенное мочеиспускание Неполное опорожнение мочевого пузыря Слабая или прерывистая струя мочи Боль или ее усиление во время мочеиспускания | Боли во время или после эякуляции Гемоспермия |
Ведущее место в лабораторной диагностике ХБП принадлежит микробиологическому исследованию — четырехстаканному локализационному тесту, предложенному в 1968 г. Meares и Stamey [8]. Он состоит в получении, после тщательного туалета наружных половых органов (во избежание контаминации поверхностными бактериями), первой (10 мл) и второй (средней) порций мочи для бактериологического исследования, массажа предстательной железы (ПЖ) со взятием секрета для микроскопии и посева, а также третьей порции мочи (после взятия секрета) для посева (рис. 1). Количественные посевы первой и второй порций мочи выявляют бактерии в уретре и мочевом пузыре, в то время как при посевах секрета простаты и порции мочи после взятия секрета (третьей порции мочи) выявляют флору простаты. ХБП характеризуется воспалительной реакцией в секрете (при микроскопии определяется более 10 лейкоцитов в поле зрения при большом увеличении). После инкубации посевов подсчитывают количество колониеобразующих единиц (КОЕ).
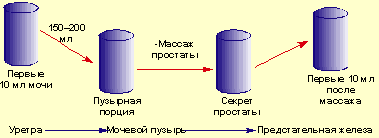 |
| Рисунок 1. Четырехстаканный локализационный тест Meares–Stamey |
Бактериологическое подтверждение ХБП мы проводим на основании, по крайней мере, одного из следующих критериев, предложенных K. G. Naber (2003):
Характерное для ХБП содержание патогенов в образцах примерно следующее:
первая порция мочи 3 КОЕ/мл;
вторая порция мочи 3 КОЕ/мл;
секрет простаты ≥ 10 4 КОЕ/мл;
третья порция мочи ≥ 10 3 КОЕ/мл.
Четкое соблюдение правил микробиологической диагностики и вышеуказанных критериев интерпретации результатов локализационного теста Meares — Stamey на большом количестве наблюдений позволят более точно определить частоту встречаемости истинных патогенов ХБП.
Антимикробная терапия. После идентификации этиологического агента и определения антибиотикорезистентности возникает необходимость назначения больному с ХБП антимикробной терапии. К факторам, оказывающим влияние на выбор антимикробного препарата для лечения ХБП, относятся: чувствительность идентифицированного микроорганизма к антибиотику, его способность в достаточной концентрации проникать через гематопростатический барьер и накапливаться в ткани и секрете простаты, сперме, а также способность препарата преодолевать экстрацеллюлярную полисахаридную оболочку, формируемую микроколониями бактерий, и хорошая переносимость при длительном пероральном приеме. Идеальный антибактериальный препарат для лечения ХБП должен быть жирорастворимым, слабощелочным, с коэффициентом диссоциации, способствующим максимальной концентрации препарата в простате [2]. Антимикробные средства из группы фторхинолонов на сегодняшний день отвечают вышеперечисленным требованиям и являются препаратами выбора для лечения ХБП. Особенностью антибактериального действия фторхинолонов является наличие двух мишеней действия в бактериальной клетке, каковыми являются ферменты (топоизомеразы II типа), ответственные за изменения пространственной конфигурации бактериальной ДНК: ДНК-гираза и топоизомераза IV. ДНК-гираза осуществляет суперспирализацию бактериальной ДНК, а топоизомераза IV — разделение дочерних хромосом в процессе репликации. Ключевым моментом в действии фторхинолонов является образование трехкомпонентного комплекса (бактериальная ДНК–фермент–фторхинолон). Указанный комплекс предотвращает репликацию бактериальной ДНК. Благодаря тому, что топоизомеразы обладают расщепляющей активностью, происходит разрушение молекулы ДНК (С. В. Сидоренко, 2002).
 |
| Рисунок 2. Классификация фторхинолонов (по K.G. Naber,1998) |
В настоящее время в практическое здравоохранение внедрены новые антимикробные препараты из группы фторхинолонов III и IV поколений, которые проявляют активность в отношении как грамотрицательных и грамположительных бактерий, так и атипичных внутриклеточных микроорганизмов, а также обладают способностью воздействовать на бактерии в биологических пленках (см. рис. 2). Антимикробная активность in vitro фторхинолонов III поколения — спарфлоксацина и левофлоксацина, а также фторхинолона IV поколения — моксифлоксацина наглядно представлена в таблице 2.
| Таблица 2 Антимикробная активность in vitro спарфлоксацина, левофлоксацина и моксифлоксацина (МПК90, мкг/мл) [4] | |||
| Микроорганизмы | Спарфлоксацин | Левофлоксацин | Моксифлоксацин |
| Acinetobacter spp. | 0,25 | 16 | 0,5 |
| Citrobacter freundii | 0,25 | 0,5 | 0,5 |
| Enterobacter cloacae | 0,5 | 0,5 | 0,5 |
| Escherichia coli | 0,12 | 0,12 | 0,5 |
| Klebsiella pneumoniae | 0,25 | 0,25 | 0,5 |
| Proteus mirabilis | 0,5 | 0,25 | 0,12 |
| Pseudomonas aeruginosa | 8 | 4 | 16 |
| Staphylococcus epidermidis | 1 | 1 | 2 |
| Staphylococcus saprophyticus | 0,25 | — | 0,5 |
| Enterococcus faecalis | 2 | 16 | 4 |
В 2004 г. мы сравнили чувствительность 25 различных штаммов коагулазо-негативных стафилококков — наиболее распространенных, по нашим данным (Е. Б. Мазо и соавт., 2003, 2004), этиологических агентов ХБП — к левофлоксацину, спарфлоксацину и моксифлоксацину. Бактериологическое исследование проводили классическим методом: выполняли посев мочи и секрета простаты на питательные среды с выделением чистой культуры и идентификацией выделенных штаммов при помощи полуавтоматического микробиологического анализатора Sceptor (Becton Dickinson, USA). Чувствительность выделенных микроорганизмов к левофлоксацину, спарфлоксацину и моксифлоксацину определяли дискодиффузионным методом на среде Мюллера–Хинтона. Результаты оценивали по значениям диаметров зон задержки роста. Всего было изучено 25 штаммов коагулазо-негативных стафилококков (21 — Staphylococcus haemolyticus, 3 — Staphylococcus epidermidis, 1 — Staphylococcus warnerii), выделенных в диагностическом титре из секрета простаты и мочи у больных ХБП при четырехстаканном тесте Meares–Stamey. Проведенный нами анализ чувствительности коагулазо-негативных стафилококков к фторхинолонам III и IV поколений показал наиболее высокую чувствительность этих бактерий к моксифлоксацину — у 24 (96%) штаммов. К левофлоксацину оказались чувствительны 21 (84%), а к спарфлоксацину 20 (80%) штаммов коагулазо-негативных стафилококков. Пять резистентных к спарфлоксацину штаммов были выделены нами у больных после длительной антимикробной терапии этим препаратом. Был выделен также штамм гемолитического стафилококка, резистентный ко всем фторхинолонам III и IV поколений у больного, ранее принимавшего в течение 6 нед моксифлоксацин. Проведенное исследование продемонстрировало высокую чувствительность коагулазо-негативных стафилококков, выделенных от больных ХБП, к фторхинолонам III и IV поколений. Чувствительность исследованных бактерий к моксифлоксацину оказалась наиболее высокой, в то время как к левофлоксацину и спарфлоксацину была практически одинаково ниже. Таким образом, длительная антимикробная терапия моксифлоксацином может привести к селекции устойчивых штаммов и развитию перекрестной резистентности к фторхинолонам III и IV поколений.
На сегодняшний день проведено ограниченное количество клинических исследований применения фторхинолонов в лечении ХБП. Результаты таких исследований, с периодом наблюдения не менее 6 мес, представлены в таблице 3.
Как видно из данных, приведенных в таблице 3, несмотря на существенные различия в количестве больных, принимавших участие в исследованиях, бактериальная эрадикация при различной длительности терапии фторхинолонами, наблюдалась более чем у 60% пациентов. Проведение подобных исследований в будущем, с соблюдением стандартов микробиологической диагностики, позволит выработать единый подход к рациональной антимикробной терапии ХБП.
Согласно актуальным на сегодняшний день рекомендациям Европейской ассоциации урологов по лечению инфекций мочевыводящих путей и инфекций репродуктивной системы у мужчин, принятым в 2001 г., длительность антимикробной терапии ХБП фторхинолонами или триметопримом должна составлять 2 нед (после установления предварительного диагноза). После повторного обследования больного антимикробную терапию рекомендуют продолжать суммарно в течение 4–6 нед только при положительном результате микробиологического исследования секрета простаты, взятого до начала лечения, или в случае, если у больного улучшилось состояние после приема антимикробных препаратов [2].
Антимикробные препараты, используемые для лечения ХБП, а также способы их применения приведены в таблице 4.
| Таблица 4 Способы применения антимикробных препаратов для лечения хронического бактериального простатита | ||
| Группа препаратов | Препараты | Способ применения |
| Фторхинолоны | Ципрофлоксацин (сифлокс, ципролет, цифран) | По 500 мг 2 раза в сутки |
| Офлоксацин (джеофлокс, заноцин, офлоксин 200) | По 400 мг 2 раза в сутки | |
| Ломефлоксацин (ксенаквин, ломфлокс, максаквин) | По 400 мг 1 раз в сутки | |
| Левофлоксацин (таваник) | По 500 мг 1 раз в сутки | |
| Спарфлоксацин (спарфло) | Первый прием 400 мг, затем по 200 мг 1 раз в сутки | |
| Моксифлоксацин (авелокс) | По 400 мг 1 раз в сутки | |
| Триметоприм/ сульфаметоксазол | Ко-тримоксазол (бикотрим, бисептол) | По 960 мг 2 раза в сутки |
Следует отметить, что больные с ХБП должны принимать антибиотик фторхинолонового ряда в течение длительного периода (от 4 до 6 нед) для предотвращения рецидива инфекции нижних мочевых путей. Продолжительная терапия антибиотиками в низких профилактических дозах или супрессивная антимикробная терапия могут применяться в случаях рецидивирующего или невосприимчивого к лечению простатита.
Литература
С. В. Попов
А. К. Чепуров, доктор медицинских наук, профессор
В. И. Карабак, кандидат медицинских наук
РГМУ, Москва
Микрофлора урогенитального тракта у мужчин, обследованных по поводу хронического простатита
Лечение хронической воспалительной патологии урогенитального тракта у мужчин всегда было непростой задачей в урологии. Лечение по поводу этих заболеваний, особенно осложненных нарушением фертильности, сексуальной дисфункцией, синдромом тазовых болей, может быть успешным, если производится индивидуально и базируется на знании этиологии воспалительного процесса, иммунореактивности на данный воспалительный процесс и морфо-функциональные изменений в тазовых органах.
В широкой врачебной практике в настоящее время при диагностике этиологического фактора воспалительной патологии урогенитального тракта акцент делается на выявление инфекций передаваемых половым путем. Целью данного исследования является демонстрация значимости других, не менее важных, этиологических факторов, а также места ИППП в патогенезе данной группы воспалительных заболеваний. Инфекционный воспалительный процесс в урогенитальном тракте возникает по двум механизмам.
В первом случае вирулентная ИППП вызывает клинически и лабораторно идентифицируемый уретрит, который в дальнейшем приводит к возникновению восходящего воспалительного процесса. Патогенетическая роль инфекции передаваемой половым путем в данном случае очевидна: при исследовании отделяемого из уретры, секрета предстательной железы, семенной жидкости выявляется достоверное увеличение количества лейкоцитов и ИППП; первично воспалительный процесс начинается с клиники уретрита. Пациенты с воспалительным процессом такого характера чаще всего находятся на лечении в кожно-венерологических диспансерах, когда помимо острого венерического заболевания имеется клиника простатита.
Второй механизм более сложный. Возникновению инфекционного воспалительного процесса в урогенитальном тракте в данном случае предшествуют определенные предрасполагающие факторы.
Выделим несколько основных групп:
При развитии инфекционного процесса в урогенитальном тракте по данному механизму отсутствует какая-либо клиника уретрита, в исследованиях отделяемого из уретры будет отсутствовать достоверное увеличение количества лейкоцитов, в соскобах из уретры будет значительно реже выявляться ИППП, однако у пациентов будет присутствовать клинически и лабораторно идентифицируемый воспалительный процесс в простато-везикулярном комплексе или в органах мошонки.
При наличии вышеуказанных предрасполагающих факторов инфицирование урогенитального тракта банальной бактериальной микрофлорой принципиально возможно двумя путями: трансуретральным и гематогенным.
Гематогенным путем инфицирование чаще всего происходит из очагов хронической инфекции при сопутствующей ЛОР- патологии, заболеваниях, имеющих широчайшее распространение у населения; при заболеваниях прямой кишки с хроническими запорами, геморрое ( особенно при частых обострениях). Инфицирование по данному пути чаще всего происходит тогда, когда в предстательной железе уже имеются выраженные структурные изменения ( конгестия, кальцинаты, ДГПЖ ).
Более значим трансуретральный путь инфицирования вторичной бактериальной микрофлорой.Следует выделить 4 основных источника бактериального инфицирования.
Таблица микроорганизмов, наиболее часто встречающихся в половых органах у женщин при воспалительных заболеваниях, вызванных влагалищной гарднареллой и неспорообразующими бактериями. ( сборник трудов УрНИИДВиИ, 1985 год )
Виды микроорганизмов.
Морфологические особенности.
Коккобациллы одиночные, парные, полиморфные

