Staphylococcus pseudintermedius что это
Стафилококк: как выявить и вылечить
Это особая категория бактериальных культур, многие виды которой опасны для человеческого здоровья. Стафилококки принято называть условно-патогенными микробами. Обитая в организме постоянно, они находятся под контролем иммунитета. Но при ослаблении защиты могут спровоцировать воспалительный процесс. Некоторые бактерии чрезвычайно устойчивы к антимикробным средствам и нередко становятся причиной суперинфекций.
Что такое стафилококк
Это неподвижный грамположительный микроорганизм шаровидной формы, образующий многочисленные колонии. Стафилококки анаэробны — могут существовать и размножаться без участия кислорода, в закрытой среде. Штаммов бактерий насчитывается более двадцати. Некоторые из них довольно безобидны, а другие вызывают мощные патологические реакции в человеческом организме. Части тела и органы, наиболее уязвимые перед стафилококками:
Поражая их, микробы вырабатывают токсичные вещества, провоцируют воспаления, в тяжелых случаях приводящие к сепсису, необратимым изменениям структур или стойким нарушениям функций.
Виды патогенных стафилококков
Для человека опасны несколько разновидностей бактерий. Самые распространенные:
Staphylococcus aureus: золотистый. Название получил из-за характерного желтого пигмента на поверхности. Проникая в организм, синтезирует фермент коагулазу, может вызывать гнойные воспаления почти любых внутренних органов. Этот вид патогена быстро приспосабливается к воздействию антибиотиков, образуя резистентные формы.
Staphylococcus epidermidis: эпидермальный. Поражает обычно кожные покровы слизистые оболочки. Часто становится фактором воспаления повреждений, послеоперационных швов, развития гнойного конъюнктивита, инфекций дыхательных путей.
Staphylococcus saprophyticus: сапрофитный. Его специфика: поражать слизистые мочевыводящих органов, провоцировать цистит, уретрит, почечные воспаления.
Staphylococcus haemolyticus: гемолитический. Опасен для слизистых и тканей внутренних органов. Становится провокатором развития эндокардита, пневмоний, нефритов и других тяж елых патологий.
Практически все типы патогенных стафилококков склонны к мутациям в результате неправильного или недостаточно продолжительного лечения.
Как проявляется стафилококковая инфекция
Симптоматика, ее длительность и интенсивность зависят от штамма возбудителя, общего физического состояния больного и особенностей его иммунитета. Два характерных признака поражения стафилококком: воспаления различной локализации и интоксикация.
При пиодермии воспаляются потовые, сальные железы, волосяные фолликулы, из-за чего на коже образуются болезненные выпуклые узелки, наполняемые гноем. Фурункулы и карбункулы обычно окружены участками покрасневшей отекшей кожи. При интенсивном воспалении вероятно появление лихорадки, набухание близко расположенных к очагам воспаления лимфоузлов.
Поражение пазух носа стафилококком проявляется банальным насморком с вязкими желтоватыми или зел еными выделениями. Проникновение инфекции глубже вызывает развитие синуситов. Их симптомы характерны:
заложенность в области переносицы;
ощущение тяжести, распирания с пораженной стороны;
густые гнойные выделения из носа;
повышение температуры тела выше +37°С.
Нередко инфекция распространяется на среднее ухо, вызывая отит: резкие стреляющие боли, снижение слуха. При поражении слизистых глаз развивается нагноение конъюнктивы, склеры краснеют и отекают.
При атаке стафилококком верхних дыхательных путей неизбежны гнойные фарингиты или ларингиты. Их признаки:
сильная отечность, покраснение глотки;
затрудненное болезненное глотание;
сухой навязчивый кашель, дискомфорт в горле.
Часто стафилококковые фарингиты поражают детей младше 12 лет. У взрослых эта патология контролируется иммунитетом.
При развитии воспалений в нижних отделах дыхательных путей «актуальны» бронхит и пневмония с характерным лающим или мокрым кашлем, высокой температурой температурой и физической слабостью.
Менее распространенные признаки поражений стафилококком:
воспаления суставных тканей, мышц;
нарушения работы сердца.
Среди грозных осложнений, вызываемых стафилококком: менингит, абсцессы л егких, остеомиелит, синдром токсического шока, генерализованный сепсис.
Как лечить стафилококк
Точный диагноз — виновен ли микроб в патологии, можно установить только после лабораторного анализа. Обнаружить и идентифицировать его в пробах мочи, мазках и соскобах с кожных покровов и слизистых не составляет труда. А вот избавиться от заразы намного тяжелее. Печально известный стафилококк аурум (золотистый) чрезвычайно устойчив к воздействию дезинфекторов, в том числе к хлорке и «зеленке». Почти 15%всех случаев заражения им происходят внутри больниц.
Применение антибиотиков тоже не всегда оправдано. К пенициллинам, например, стафилококки приспосабливаются очень быстро. А золотистый давно к ним устойчив, как ко многим другим медикаментам. Для быстрого подавления активности патогенов применяют комбинации различных групп препаратов. Относительно новые и эффективные: макролиды и фторхинолоны. Лекарства этих категорий разрушают и уничтожают белковые оболочки бактерий, не давая им времени для развития резистентности.
Чтобы терапия оказалась действенной, важно применять антимикробным средства только по назначению врача, четко следовать указанной схеме. Запрещено прерывать курс по своему разумению, менять без разрешения один препарат на другой, корректировать дозировку.
В качестве профилактики заражения необходимо соблюдать общие правила гигиены. Важно избегать употребления непроверенных продуктов, вовремя санировать полость рта, лечить насморк. Полезно закаляться, принимать иммуномодуляторы. А главное — не применять антимикробные средства без веских причин.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Кожный стафилококк — симптомы, лечение, исследование. Что такое Staphylococcus epidermidis?
Кожный стафилококк — симптомы, лечение, исследование. Что такое Staphylococcus epidermidis
Кожный стафилококк (Staphylococcus epidermidis) является потенциально смертельной бактерией, которая обычно встречается на коже, слизистой оболочке полости рта и в мочеполовых путях. Кто подвергается риску заражения кожным стафилококком? Какие заболевания вызывает кожный стафилококк? Как лечить инфекцию Staphylococcus epidermidis?
Бактерии кишечной палочки и метициллинрезистентный золотистый стафилококк (бактерии MRSA) являются опасными и очень быстро распространяющимися бактериями. Инфекция Staphylococcus aureus может вызывать такие заболевания, как пневмония, миокардит, флебит и менингит. В свою очередь, бактерия Escherichia coli (кишечная палочка), причина для инфекций мочевыводящих путей, уретрита, цистита. Последствия инфекции E.coli в значительной степени зависят от штамма бактерий.
Бактерия Escherichia coli
Бактерия Escherichia coli
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Бактерия-Escherichia-coli.jpg?fit=400%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Бактерия-Escherichia-coli.jpg?fit=733%2C550&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/%D0%91%D0%B0%D0%BA%D1%82%D0%B5%D1%80%D0%B8%D1%8F-Escherichia-coli.jpg?resize=900%2C675&ssl=1″ alt=»Бактерия Escherichia coli» width=»900″ height=»675″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Бактерия-Escherichia-coli.jpg?w=900&ssl=1 900w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Бактерия-Escherichia-coli.jpg?resize=400%2C300&ssl=1 400w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Бактерия-Escherichia-coli.jpg?resize=733%2C550&ssl=1 733w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Бактерия-Escherichia-coli.jpg?resize=768%2C576&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″ /> Бактерия Escherichia coli
Между тем оказывается, что Staphylococcus epidermidis, то есть кожный стафилококк, является гораздо более опасной бактерией. Эта бактерия становится все более устойчивой к антибиотикам и вызывает опасные для жизни инфекции после операции.
Что такое кожный стафилококк?
Этот тип стафилококка часто игнорируется в клинических испытаниях, и из-за его повсеместного распространения он может очень быстро эволюционировать и генетически мутировать между бактериями.
Проблема с кожным стафилококком возникает, когда снижается иммунитет — тогда инфекция Staphylococcus epidermidis может вызвать ряд осложнений и стать фактором риска для многих заболеваний. Кожный стафилококк особенно опасен для людей, прошедших инвазивные процедуры.
Кожный стафилокок — симптомы
Симптомы активации стафилококковой инфекции :
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Стафилококковая-инфекция.jpg?fit=440%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Стафилококковая-инфекция.jpg?fit=806%2C550&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/%D0%A1%D1%82%D0%B0%D1%84%D0%B8%D0%BB%D0%BE%D0%BA%D0%BE%D0%BA%D0%BA%D0%BE%D0%B2%D0%B0%D1%8F-%D0%B8%D0%BD%D1%84%D0%B5%D0%BA%D1%86%D0%B8%D1%8F.jpg?resize=900%2C614&ssl=1″ alt=»Стафилококковая инфекция» width=»900″ height=»614″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Стафилококковая-инфекция.jpg?w=900&ssl=1 900w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Стафилококковая-инфекция.jpg?resize=440%2C300&ssl=1 440w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Стафилококковая-инфекция.jpg?resize=806%2C550&ssl=1 806w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Стафилококковая-инфекция.jpg?resize=768%2C524&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″ /> Стафилококковая инфекция
Симптомы кожного стафилококка неспецифичны — каждый случай кожного стафилококка может иметь немного разные симптомы в зависимости от того, какая часть тела поражена. Люди, которым предстоит операция, должны обратить внимание на симптомы кожного стафилококка.
Кожный стафилококк у ребенка
Иммунная система ребенка более чувствительна, чем у взрослого, поэтому кожный стафилококк может быть опасным даже для самых маленьких. Если у ребенка есть повреждения кожи — его следует тщательно обработать, одеть и защитить от внешних факторов, чтобы избежать инфекции. Если у вашего ребенка изменения кожи без причины — обратитесь к врачу.
Стафилококки у ребенка могут вызвать фолликулит, стафилококковый сикоз, множественные абсцессы. Такие заболевания, как буллезное импетиго, буллезное воспаление и шелушение кожи, могут возникать в результате стафилококковой инфекции у новорожденных.
Кожный стафилококк — как можно заразиться?
Кожная стафилококковая инфекция возникает у пациентов с ослабленным иммунитетом,например, после тяжелой инфекции, после операции, после химиотерапии, у реципиентов органов и костного мозга. Бактерия попадает в кровоток и приводит к генерализованной инфекции, то есть к стафилококковой бактериемии.
Кожный стафилококк — какие заболевания может вызывать Staphylococcus epidermidis?
Проникнув в организм, стафилококк вызывает:
Кожный стафилококк — диагностика
Как выявить инфекцию Staphylococcus epidermidis? Для этого проводятся анализы крови, мочи и ткани из зараженной области кожи.
» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Диагостика-стафилококка.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Диагостика-стафилококка.jpg?fit=825%2C550&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/%D0%94%D0%B8%D0%B0%D0%B3%D0%BE%D1%81%D1%82%D0%B8%D0%BA%D0%B0-%D1%81%D1%82%D0%B0%D1%84%D0%B8%D0%BB%D0%BE%D0%BA%D0%BE%D0%BA%D0%BA%D0%B0.jpg?resize=900%2C600&ssl=1″ alt=»Диагностика стафилококка» width=»900″ height=»600″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Диагостика-стафилококка.jpg?w=900&ssl=1 900w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Диагостика-стафилококка.jpg?resize=450%2C300&ssl=1 450w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Диагостика-стафилококка.jpg?resize=825%2C550&ssl=1 825w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2020/07/Диагостика-стафилококка.jpg?resize=768%2C512&ssl=1 768w» sizes=»(max-width: 900px) 100vw, 900px» data-recalc-dims=»1″ /> Диагностика стафилококка
Кожный стафилококк — лечение
Ученые из Центра эволюции Милнера при Университете Бата определили в стафилококковых бактериях кожи 61 ген, которые могут вызывать смертельные заболевания. Пробы были взяты у пациентов, перенесших инфекции после операции по замене тазобедренного или коленного сустава и фиксации перелома, и были сопоставлены с образцами мазков кожи от здоровых добровольцев.
Удивительно, что у некоторых здоровых людей, принявших участие в исследовании, были обнаружены еще более смертельные формы бактерий. Также было обнаружено, что Staphylococcus epidermidis образует биопленки, которые повышают сопротивляемость организма к антибиотикам.
Лечение кожного стафилококка предполагает использование антибиотиков. К сожалению, некоторые антибиотики не действуют против некоторых типов кожного стафилококка — лекарственная устойчивость кожного стафилококка аналогична таковой у золотистого стафилококка.
В случае штаммов с высокой лекарственной устойчивостью используются ванкомицин или тейкопланин, эффективные против стафилококков, включая штаммы, устойчивые к метициллину.
Staphylococcus pseudintermedius что это
ОСТАВЬТЕ О НАС ОТЗЫВ НА ЯНДЕКСЕ!
МЫ НА YOUTUBE

СТАФИЛОКОККИ. ВВЕДЕНИЕ
Описано 54 видов и 24 подвида, из которых наибольшее значение в ветеринарной медицине имеют Staphylococcus aureus и Staphylococcus intermedius. Однако после недавних таксономических изменений, описанных ниже, все штаммы, выделенные от собак (и, возможно, от кошек), ранее относившиеся к S. intermedius, в настоящее время следует относить к Staphylococcus pseudintermedius. В настоящем обзоре термин “S. pseudintermedius» относится к штаммам, в более старых источниках классифицируемых как S. intermedius (это относится к штаммам, выделенным от собак и кошек).
ЭКОЛОГИЯ
Стафилококки, коагулазоположительные (Ко+) и ко-агулазоотрицательные (Ко-), являются нормальными обитателями кожи и слизистых оболочек животных и человека. Отмечена тенденция к предпочтительному заселению кожи и слизистых оболочек млекопитающих и птиц определенными видами стафилококков. Стафилококки, попавшие в окружающую среду с кожи и шерсти, способны сохранять жизнеспособность в течение нескольких месяцев [53, 79]. У людей более 80 % больничных инфекций S. aureus вызываются эндогенными штаммами, обитающими в носовой полости пациента [78]. Сходным образом Pinchbeck and others [58] показали, что более 94 % штаммов S. pseudinterme-dius, выделенных из пораженных участков кожи собак с пиодермой, были генетически идентичны штаммам, обитающим на нормальных покровах этой же собаки.
У собак преобладающим видом является S. pseudin-termedius, который выделяется с кожи и слизистых оболочек здоровых собак в 20-90 % случаев [2, 14, 17, 28, 32]. Частота выделения отдельных Ко+ стафилококков с кожи и шерсти здоровых кошек составляет приблизительно 10 % для S. aureus и 45 % для S. pse-udintermedius [1, 12, 41].
ПОСЛЕДНИЙ ПЕРЕСМОТР ТАКСОНОМИЧЕСКОЙ КЛАССИФИКАЦИИ “S. INTERMEDIUM
В обзоре таксономической классификации от 1992 г. Noble ссылается на работу 1962 г. под названием “An introduction to chaos: or the classification of micrococci and staphylococci» (Введение в хаос: классификация микрококков и стафилококков); на момент написания этой работы было известно всего три вида стафилококков, а именно S. aureus, S. epidermidis и Staphylococcus saprop-hyticus. Появление молекулярно-биологических методов стало основой для обширного пересмотра классификации стафилококков. В настоящее время род включает 45 видов и 24 подвида, которые можно отнести к 11 кластерам по результатам секвенирования гена 16S РНК и 4 кластерам по результатам секвенирования gap-гена [24].
Все эти наблюдения указывают, что штаммы с традиционными фенотипическими характеристиками “S. intermedius» должны идентифицироваться как S. pseudintermedius, если они выделены от собак. Штаммы с такими свойствами, выделенные от других видов, лучше всего идентифицировать как «бактерии группы S. intermedius», если нет результатов оценки молекулярно-биологическими методами [33]. Хотя молекулярнобиологические методы позволили прояснить таксономию бактерий группы S. intermedius, фенотипическая классификация в диагностических лабораториях все еще пребывает в состоянии хаоса из-за различий в экспрессии биохимических свойств как в пределах одного вида, так и между видами, относящимися к группе S. intermedius. Например, сообщается, что S. pseudintermedius в культуре образует ацетоин (реакция Фогеса-Проскауэра) при анализе с помощью набора API STAPH (Био Мерье) [19]. В противоположность этому, по данным Sasaki and others [65], 28 из 83 штаммов S. pseudintermedius, идентифицированные молекулярно-биологическими методами, не образуют ацетоин при исследовании стандартными методами, и исследование с помощью набора API STAPH не показывает образование ацетоина. Кроме того, сообщается, что данная культура не образует фактор агглютинации при исследовании с плазмой кролика, в то время как, по данным Cox and others [13], 55 из 105 выделенных от собак штаммов “S. intermedius» (и, вероятно, S. pseudinterme-dius) экспрессировали фактор агглютинации, что согласуется с общепринятым представлением, которого придерживаются многие ветеринарные микробиологи. Описанные ранее данные, касающиеся S. intermedius, нуждаются в переоценке, так как некоторые штаммы, ранее классифицировавшиеся как S. intermedius, могут с высокой вероятностью принадлежать к S. pseudin-termedius или S. delphini [20].
УСТОЙЧИВОСТЬ К АНТИБИОТИКАМ
ШТАММЫ S. PSEUDINTERMEDIUS, УСТОЙЧИВЫЕ К МЕТИЦИЛЛИНУ (MRSP)
Метициллин, полусинтетический антибиотик из группы пенициллинов, был введен в 1959 г. для борьбы со стафилококками, образующими р-лактамазу и устойчивыми к пенициллину. Вскоре после этого были выделены штаммы S. aureus, устойчивые к метициллину (MRSA), преимущественно в условиях стационара. В основе устойчивости к метициллину лежит экспрессия гена mecA, кодирующего модифицированный белок клеточной стенки, связывающий пенициллин (PBP2a), низкое сродство которого к р-лактамным антибиотикам делает пенициллины и цефалоспорины неэффективными. Ген mecA располагается в стафилококковой хромосомной кассете mec (SCCmec), крупном мобильном генетическом элементе, при этом дополнительные генетические детерминанты часто придают микроорганизму дополнительную устойчивость к другим антибиотикам, использующимся в клинической практике.
Встраивание элемента SCCmec в геном штаммов S. pseudintermedius привело к резкому росту распространенности устойчивых к метициллину штаммов по Европе, главным образом в период с 2005 по 2006 г [45, 57, 62, 66]. В отчете об исследовании S. intermedius в Северной Америке сообщается, что в период с 2003 по 2004 г. устойчивостью к метициллину обладали 57 из 336 выделенных штаммов (17 %) [50], в то время как за период с 1995 по 1998 г. лишь один штамм стафилококков из 25 обладал устойчивостью к метициллину [26]. В Европе устойчивостью к метициллину обладало 23 % штаммов S. pseudintermedius, выделенных в дерматологической клинике на севере Германии за 2006 г [45]. Частота выделения устойчивых к метициллину стафилококков (n = 61, 7,4 % MRSP) была более чем в 4 раза выше, чем MRSA (n = 15, 18,75 % выделенных штаммов S. aureus), по данным обзора, 901 Ко+ штамма стафилококков, выделенных от собак в Германии за 2007 г [62]. По результатам обзора 590 образцов от собак, представленных в диагностическую ветеринарную лабораторию в Италии за двухмесячный период в 2008 г., на MRSP приходилось 10 из 48 выделенных штаммов из группы 5. intermedius (21 %); все эти штаммы, устойчивые к метициллину, были также устойчивы к фторхинолонам, гентамицину, линкозамидам, тетрациклинам и потенцированы [15], что отражает приобретение дополнительных генов, обусловливающих устойчивость.
По-видимому, данные о распространенности в Великобритании не публиковались в реферируемых журналах, хотя коммерческая лаборатория в Девоне, Великобритания, недавно сообщила, что на MRSP приходится 14 % из 125 Ко+ штаммов, выделенных за 12-месячный период вплоть до июля 2008 г. [68]. Эти штаммы были устойчивы к большему числу антибиотиков, чем штаммы MRSA, выделенные за этот же период.
МЕТОДЫ МОЛЕКУЛЯРНОГО ТИПИРОВАНИЯ ДЛЯ ИССЛЕДОВАНИЯ ЭПИЗООТОЛОГИИ MRSP
Для эффективного и точного типирования клонов S. pseudintermedius был разработан ряд молекулярных методов. Эти методы показали выраженное генетическое разнообразие среди штаммов S. pseudintermedius, чувствительных к метициллину [63]. Метод муль-тилокусного секвенирования-типирования позволяет типировать выделенные штаммы путем секвенирова-ния внутренних фрагментов многочисленных конститутивных генов (пять в случае S. pseudintermedius в настоящее время). При исследовании каждого конституционного гена разные последовательности, имеющиеся у бактерий определенных видов, относятся к определенным аллелям, и аллели в каждом из пяти локусов каждого штамма определяют аллельный профиль типа последовательности (ТП); профили легко сравнить с хранящимися в интернет-базах данных. Типирование белка А S. aureus включает амплификацию, секвени-рование и анализ различных областей Х гена белка А. Метод импульсного гель-электрофореза заключается в гидролизе геномной ДНК эндонуклеазой SmaI и последующем электрофоретическом разделении фрагментов ДНК в агарозном геле. Вставка элемента SCCmec в хромосому чувствительных видов является причиной возникновения линий стафилококков, устойчивых к метициллину При типировании SCCmec определяются типы генов рекомбиназы (ссг) вместе с классом гена :таес и связанные регуляторные последовательности. В отличие от наблюдаемой генетической вариабельности MSSP исследование штаммов MRSP показало, что у собак и кошек в Европе преобладает один клон, в частности с типом последовательности ST71 (MLST)-J(PGFE)-t02(spa)-II-III(SCCmec). Этот клон был выделен в Германии, Швейцарии, Нидерландах, Дании, Швеции и Италии и, спорадически, в Северной Америке и Гонконге [4, 7, 37, 57, 63]. В Северной Америке также обнаружен один преобладающий клон, в частности ST68-C-t06-V [57, 63]. Наблюдающееся в настоящее время отсутствие штаммов ST71 5. pseudinterme-dius, чувствительных к метициллину, не подтверждает одновременное и быстрое приобретение SCCmec широко распространенной и успешно развивающейся линией 5. pseudintermedius, а скорее свидетельствует о быстром распространении этого конкретного клона. Эти молекулярные эпизоотологические данные позволяют предположить, что при выделении микроорганизмов и обнаружении инфекции у животных необходимы тщательные гигиенические меры, чтобы ограничить дальнейшее распространение.
ЗООАНТРОПОНОЗНЫЙ ПОТЕНЦИАЛ.
Staphylococcus pseudintermedius редко обнаруживается на коже человека, хотя частота его передачи среди людей, регулярно соприкасающихся с собаками, растет [25, 29, 32]. Из 3397 штаммов, выделенных от пациентов больниц общего профиля, 3357 относились к S. aureus, и только два принадлежали к S. pseudinter-medius [48], хотя описаны случаи ошибочной идентификации S. pseudintermedius как S. aureus в медицинских лабораториях, для которых последний вид был привычнее [39, 59, 67, 72, 76]. Исследование на 56 здоровых добровольцах не показало наличия S. pseudinter-medius на слизистой оболочке носа, хотя у 89 % этот микроорганизм был обнаружен в слюне и зубном налете [55]. В исследовании персонала ветеринарного колледжа частота выделения микроорганизма со слизистой оболочки ротоглотки составила менее 1,5 % [44, 71], однако результаты более поздних исследований владельцев собак показывают большие цифры. Исследование наружных носовых ходов 16 владельцев собак с атопическим дерматитом и 13 сотрудников ветеринарной клиники, постоянно контактирующих с собаками, на стафилококков выявило одного постоянного и четырех временных носителей Staphylococcus “interme-dius» [32]; штаммы, выделенные от людей, обычно соответствовали штаммам, выделенным от собак, с которыми они контактировали [25]. В исследовании 242 владельцев собак и кошек в Онтарио S. pseudintermedius был выделен от девяти людей, а неотличимые от него штаммы выделены от собак в четырех из девяти случаев носительства [31]. Guardabassi and others [29] показали, что носительство S. pseudintermedius на слизистой оболочке носовой полости среди владельцев собак с глубокой пиодермой встречалось чаще (7 из 13), чем у людей без ежедневного контакта с собаками (1 из 13), и что у 6 из 13 владельцев обнаружены штаммы, идентичные выделенным от их собак по результатам электрофореза.
Появление штаммов MRSP привело к выяснению но-сительства у людей, контактирующх с собаками, а также спорадических случаев инфекции у людей [8, 23, 39, 69]. MRSP были выделены от пяти собак и одной кошки с инфицированными хирургическими ранами в лаборатории в Нидерландах [74]. В ходе дальнейших исследований из носовой полости ветеринарного врача и 3 из 6 ассистентов, из 4 из 22 образцов из среды, а также из носовой полости здоровой собаки, принадлежащей сотруднику, регулярно присутствовавшему в клинике, были выделены MRSP с такой же картиной устойчивости. MRSP и MRSA были выделены из 3 и 8 из 34 образцов соответственно, взятых у ветеринарных врачей из университетской ветеринарной клиники в Японии, при этом все 36 образцов от сотрудников неклинических лабораторий оказались отрицательными [36]. Обзор по результатам исследования 171 сотрудника ветеринарных дерматологических клиник и их животных в Северной Америке показал наличие MRSP у девяти человек и MRSA у шести [51]. Соответствующие штаммы MRSP были выделены от животных, содержащихся в доме, где жили три человека-носите-ля. По данным другого исследования в Северной Америке, носительство MRSP на слизистой оболочке носовой полости было обнаружено у 2 из 15 владельцев собак, инфицированных MRSP с тем же типом SCCmec и картиной восприимчивости к антибиотикам; при повторном отборе проб через два месяца после лечения эти штаммы отсутствовали, что позволяет предположить временное носительство MRSP людьми [21]. В сходном исследовании, проведенном в Нидерландах, результат анализа проб со слизистой оболочки носа людей оказался положительным в 2 из 45 случаев, в то время как MRSP были выделены из примерно трети образцов от собак и кошек, находившихся в контакте, и 44 % образцов из окружающей среды [75]. Эти наблюдения очевидно свидетельствуют о возможности передачи стафилококков от людей к собакам и наоборот. Хотя контакт человека с 5. pseudintermedíus от собаки, скорее всего, приведет лишь к временному неочевидному носительству, в редких случаях возможно развитие инфекции, сложно поддающейся лечению в случае MRSP [69]. Кроме того, собачьи штаммы MRSP должны рассматриваться как потенциальный источник переноса SCCmec и, возможно, других мобильных детерминант устойчивости стафилококков, обитающих на коже и слизистых оболочках человека, к антибиотикам [29].
ЗНАЧЕНИЕ ДЛЯ ЛАБОРАТОРНОЙ ИДЕНТИФИКАЦИИ
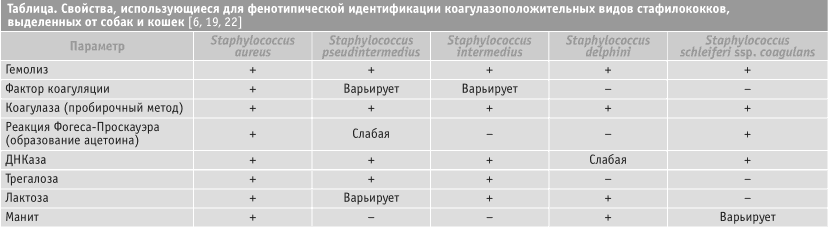
Видовая дифференциация патогенных стафилококков сложнее, чем предполагают стандартные микробиологические тесты [59, 73]. Перед появлением MRSA как патогена собак видовая идентификация Ко+ стафилококков, выделенных от собак, имела минимальное клиническое значение. Однако в настоящее время точная видовая идентификация и дифференциация MRSA и MRSP необходима в связи со значительным различием в зооантропонозном потенциале этих двух видов, и пограничные значения при исследовании восприимчивости in vitro могут различаться. Начальная идентификация стафилококков с точностью до рода возможна по морфологии колоний (гладкие, выпуклые, слегка блестящие, от белого до желтого цвета, диаметром от 1 до 2 мм после 24-часовой инкубации на кровяном или другом питательном агаре при 37 °C [6]); результатам микроскопии (грамположительные кокки) и образованию каталазы (этот признак позволяет дифференцировать их от стрептококков и энтерококков; обзор Freney and others [22]).
Таблица.
ЛЕЧЕНИЕ ИНФЕКЦИЙ, ВЫЗВАННЫХ MRSP
Хотя устойчивость стафилококков к метициллину не всегда связана с полирезистентностью, большинство штаммов MRSP, описанных в литературе, устойчивы к большинству препаратов, использующихся в ветеринарии. Клон MRSP, преобладающий в Европе, обычно устойчив к р-лактамным антибиотикам, ами-ногликозидам, макролидам, линкозамидам, тетрацик-линам, хлорамфениколу, триметоприму и фторхино-лонам и чувствителен только к амикацину, фусидовой кислоте, рифампицину, ванкомицину, тейкопланину и линезолиду, однако ни один из этих последних препаратов не лицензирован для системного лечения мелких домашних животных [16, 57]. В 2009 г. консультативная группа Всемирной организации здравоохранения по объединенному надзору за резистентностью к антибиотикам (AGISAR) выпустила стандартный документ, призванный помочь сформулировать и определить приоритеты оценки риска и стратегий управления рисками, связанными с устойчивостью к антибиотикам. Согласно их классификации антимикробные препараты делятся на критически важные, очень важные и важные на основании их роли как единственного лечебного средства или одной из немногих альтернатив для лечения серьезных заболеваний у человека, или заболеваний, вызванных микроорганизмами, передающимися из других источников (не от человека), или микроорганизмами, способными приобретать детерминанты устойчивости из других источников [81].
Иногда поверхностные кожные инфекции и некоторые раневые инфекции хорошо поддаются лечению местными средствами в сочетании с коррекцией первопричины либо после удаления инородного материала, например швов или имплантатов. Loeffler and others [45] описали разрешение поверхностной пио-дермы, вызванной MRSP, у пяти из семи собак после местного применения препаратов фусидовой кислоты и хлоргексидина, а также шампуня, содержащего этиллактат.
Для лечения глубокой пиодермы или других серьезных инфекций может потребоваться назначение системных антибактериальных препаратов, не соответствующее утвержденным показаниям, хотя данных об оптимальной дозировке и частоте применения та-
ких препаратов часто недостаточно. Амикацин не всасывается из пищеварительного тракта и должен вводиться в инъекционной форме. Рифампицин можно давать внутрь, однако при этом существует риск развития устойчивости, особенно при применении в форме монотерапии [38], а риск гепатотоксичности требует регулярного контрольного биохимического исследования крови. Описаны отдельные штаммы MRSP с устойчивостью к рифампицину [57]. В то время как 54 из 57 штаммов MRSP из Северной Америки были чувствительными [50], среди 25 европейских штаммов чувствительностью обладали всего 30-40 % [15, 16]. Такое географическое различие подчеркивает важность выбора препарата для лечения MRSP по результатам определения чувствительности отдельных штаммов in vitro.
Случаи устойчивости MRSP к ванкомицину, тей-копланину и линезолиду до настоящего времени неизвестны [57, 62], хотя Perreten and others высказали сомнения в целесообразности применения этих антибиотиков для лечения животных. Ввиду статуса этих препаратов в медицине в качестве резервных для лечения бактериемии, вызванной MRSA, и активного изучения использования антибиотиков в ветеринарии Европейским агентством по лекарственным средствам (ЕМЕА) авторы придерживаются мнения, что применение ванкомицина, тейкопланина и линезолида в ветеринарии не оправдано.
ПРОФИЛАКТИКА И КОНТРОЛЬ СТАФИЛОКОККОВЫХ ИНФЕКЦИЙ, ВЫЗВАННЫХ ПОЛИРЕЗИСТЕНТНЫМИ ШТАММАМИ
Распространение 5. pseudintermedius с кожи собак и кошек ответственно за частое обнаружение этого микроорганизма в среде ветеринарных клиник [74]. При обнаружении или подозрении на инфекцию или
носительство MRSP у животных необходимо принять тщательные меры предосторожности во избежание больничных инфекций и дальнейшего распространения этой полирезистентной бактерии [42]. Эти меры должны включать личную гигиену (мытье рук, использование масок, халатов и перчаток при хирургических вмешательствах) и гигиену окружающей среды (регулярную очистку и дезинфекцию всех поверхностей в клинике для уничтожения MRSA [52] и других контагиозных микроорганизмов [9] согласно рекомендациям).
До настоящего времени среди полирезистентных стафилококков не было обнаружено штаммов, устойчивых к моющим средствам и дезинфектантам; показано, что распространенные в ветеринарной практике дезинфицирующие средства обладают ингибирующим действием MRSP даже в низких концентрациях [3].
ВЫВОДЫ
Выделенные от собак штаммы, ранее классифицировавшиеся как S. intermedins, в настоящее время следует относить к S. psendintermedins. Термин “группа S. intermedins” следует использовать для обозначения штаммов, выделенных от других хозяев, при отсутствии результатов молекулярного исследования. Быстрое появление и широкое распространение MRSP в Европе и Северной Америке, как прогнозировал Waller [80], представляет значительную проблему как для ветеринарии, так и для медицины. Ввиду распространенности стафилококковой инфекции у собак MRSP способны значительно ухудшить возможности эффективного лечения распространенных инфекций кожи и мягких тканей у животных. Фенотипическая вариабельность группы S. intermedins и необходимость точной дифференциации между MRSP и MRSA представляет собой сложную задачу для ветеринарных диагностических лабораторий, для решения которой может потребоваться пересмотр и обновление повседневных лабораторных методик. Ветеринарным клиникам следует внедрить меры строгого контроля инфекций, рекомендуемые при обнаружении MRSA, для предотвращения дальнейшего распространения MRSP, играющего большую роль патогена для животных и являющегося потенциально зооантропонозным микроорганизмом и новым резервуаром генов устойчивости. Возникновение MRSP подчеркивает важность благоразумного использования антибиотиков в ветеринарной практике.
Текст научной работы на тему «Что произошло со Staphylococcus intermedius? Пересмотр таксономической классификации и развитие лекарственной полирезистентности».
Авторы: R. Bond, A. Loeffler