таваник какое поколение антибиотиков
Таваник (500 мг)
Инструкция
Торговое название
Международное непатентованное название
Лекарственная форма
Таблетки, покрытые пленочной оболочкой, 250 мг, 500 мг
Состав
Одна таблетка, покрытая пленочной оболочкой, содержит
активное вещество — левофлоксацина гемигидрат 256,230 мг (эквивалентно левофлоксацину 250,00 мг) или левофлоксацина гемигидрат 512,460 мг (эквивалентно левофлоксацину 500,00 мг),
вспомогательные вещества: гипромеллоза (метилгидроксипропилцеллюлоза), кросповидон, целлюлоза микрокристаллическая, натрия стеарилфумарат,
Описание
Таблетки продолговатой формы, двояковыпуклые, покрытые пленочной оболочкой, от бледно-желтовато-белого до красновато-белого цвета, с риской для разлома (для дозировок 250 мг и 500 мг).
Фармакотерапевтическая группа
Фармакологические свойства
Фармакокинетика
Пища не оказывает значительного эффекта на всасывание левофлоксацина.
Устойчивая концентрация препарата достигается в течение 48 ч после приема по схеме в дозировке 500 мг 1 или 2 раза в сутки.
Средний объем распределения левофлоксацина составляет приблизительно 100 л после введения однократной и повторной дозы 500 мг, что указывает на обширное распределение в тканях организма.
Проникновение в ткани и жидкости организма
Было показано, что левофлоксацин проникает в слизистую оболочку бронхов, жидкость эпителиальной выстилки, альвеолярные макрофаги, ткань легких, кожу (интерстициальная жидкость), ткань простаты и мочу. Однако левофлоксацин плохо проникает в спинномозговую жидкость.
Левофлоксацин метаболизируется незначительно, метаболитами являются дезметил-левофлоксацин и N-оксид левофлоксацина. Данные метаболиты содержат 85% введенной дозы).
Средний кажущийся общий клиренс левофлоксацина после введения однократной дозы 500 мг составил 175 +/- 29,2 мл/мин.
Не существует значительных различий в фармакокинетике левофлоксацина при внутривенном и пероральном способе применения, что подтверждает их взаимозаменяемость.
Фармакокинетика левофлоксацина является линейной в диапазоне доз от 50 до 1000 мг.
Особые группы пациентов
Пациенты с почечной недостаточностью
На фармакокинетику левофлоксацина оказывает влияние почечная недостаточность. При снижении функции почек снижается выведение препарата почками и почечный клиренс, увеличивается период полувыведения, как показано в нижеприведенной таблице.
Фармакокинетика при почечной недостаточности после перорального приема однократной дозы 500 мг.
Streptococcus A, B, C, G
Пограничные значения, не связанные с видом микроорганизмов4
Пограничные значения для левофлоксацина имеют отношение к терапии с применением высоких доз препарата.
Может наблюдаться низкий уровень резистентности к фторхинолонам (МИК препарата ципрофлоксацин 0,12-0,5 мг/л), однако нет доказательств того, что данная резистентность имеет клиническую значимость при инфекциях дыхательных путей палочкой H. influenzae.
Штаммы, у которых значения МИК выше пограничных значений чувствительности встречаются очень редко, или о них еще не сообщалось. Анализы на идентификацию и чувствительность к антимикробным препаратам с использованием любого подобного изолята следует повторить, и если результат подтверждается, нужно отправить изолят в справочную лабораторию. Пока не будут получены данные по клиническому ответу для подтвержденных изолятов с МИК выше уровня пограничных значений резистентности в настоящий момент, такие изоляты должны считаться резистентными.
Пограничные значения применимы для дозы 500 мг x 1 до 500 мг x 2 для перорального приема и 500 мг x 1 до 500 мг x 2 для в/в введения.
Распространение резистентности может варьироваться географически и с течением времени (для отдельных видов), желательно получить информацию по локальной резистентности, особенно при лечении тяжелых инфекций. При необходимости следует обратиться за советом эксперта, если локальная резистентность настолько распространена, что ставится под сомнение польза от применения препарата, по крайней мере, при некоторых типах инфекций.
Обычно восприимчивые виды микроорганизмов
Аэробные грамположительные бактерии
Метициллинчувствительный Staphylococcus aureus
Аэробные грамотрицательные бактерии
НОВЫЕ ФТОРХИНОЛОНЫ: новые возможности лечения внебольничной пневмонии
Инфекции дыхательных путей по частоте возникновения занимают первое место среди инфекционных заболеваний человека. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов разных классов, в последние годы наблюдается отчетлив
Инфекции дыхательных путей по частоте возникновения занимают первое место среди инфекционных заболеваний человека. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов разных классов, в последние годы наблюдается отчетливая тенденция к увеличению смертности от пневмонии во всех развитых странах мира. Причина может быть связана прежде всего с ростом резистентности основных возбудителей внебольничных инфекций дыхательных путей ко многим антибактериальным препаратам. Этим объясняется интерес клиницистов к новым антибактериальным средствам, к которым отмечается меньший уровень резистентности бактерий.
Этиология внебольничной пневмонии непосредственно связана с нормальной микрофлорой «нестерильных» верхних отделов дыхательных путей (полости рта, носа, рото- и носоглотки). Из множества видов микроорганизмов, колонизующих верхние отделы дыхательных путей, лишь некоторые, обладающие повышенной вирулентностью, проникая в нижние дыхательные пути, способны вызывать воспалительную реакцию даже при минимальных нарушениях защитных механизмов. Такими типичными бактериальными возбудителями внебольничной пневмонии являются следующие перечисленные ниже микроорганизмы.
Streptococcus pneumoniae — самый частый возбудитель внебольничной пневмонии у лиц всех возрастных групп (30-50%). Наиболее остро в настоящее время стоит проблема распространения среди пневмококков пенициллинрезистентных штаммов. В некоторых странах частота устойчивости пневмококков к пенициллину может достигать 60%. Масштабных исследований распространения резистентности пневмококков к пенициллину в нашей стране не проводилось. По данным локальных исследований в Москве, частота устойчивых штаммов составляет 2%, штаммов с промежуточной чувствительностью — около 20%. Устойчивость пневмококков к пенициллину связана не с продукцией β-лактамаз, а с модификацией мишени действия антибиотика в микробной клетке — пенициллинсвязывающих белков, поэтому ингибитор-защищенные пенициллины в отношении этих пневмококков также неактивны. Устойчивость пневмококков к пенициллину обычно ассоциируется с устойчивостью к цефалоспоринам I-II поколений, макролидам, тетрациклинам, ко-тримоксазолу.
Haemophilus influenzae — второй по частоте возбудитель (10-20%), особенно у лиц, страдающих хроническими обструктивными болезнями легких, а также у курильщиков; высокой природной активностью в отношении гемофильной палочки обладают аминопенициллины, амоксициллин/клавуланат, цефалоспорины II-IV поколений, карбапенемы, фторхинолоны. Основной механизм резистентности H. influenzae связан с продукцией β-лактамаз.
Staphylococcus aureus — нечастый возбудитель пневмонии (около 5%), наиболее опасен для пожилых людей, наркоманов, алкоголиков, после перенесенного гриппа. Препаратами выбора при стафилококковых пневмониях являются оксациллин, также активны амоксициллин/клавуланат, цефалоспорины, фторхинолоны.
Klebsiella pneumoniae — редкий возбудитель внебольничной пневмонии (менее 5%), встречается, как правило, у больных с тяжелыми сопутствующими заболеваниями (сахарный диабет, застойная сердечная недостаточность, цирроз печени и др.). Наиболее высокой природной активностью в отношении этого возбудителя обладают цефалоспорины III-IV поколений, карбапенемы, фторхинолоны.
Определенное значение в этиологии пневмонии имеют также два других микроорганизма, характеризующихся особыми биологическими свойствами и внутриклеточной локализацией в макроорганизме — Micoplasma pneumoniae и Chlamidia pneumoniae. В отношении этих микроорганизмов клинически неэффективны все β-лактамные антибиотики. Наибольшей природной активностью обладают макролиды и тетрациклины, несколько менее активны ранние фторхинолоны.
В настоящее время в качестве основных средств стартовой терапии внебольничной пневмонии в амбулаторной практике обычно рекомендуются аминопенициллины (ампициллин, амоксициллин), защищенные аминопенициллины (амоксициллин/клавуланат), пероральные цефалоспорины II поколения (цефуроксим аксетил), макролиды (эритромицин, кларитромицин, рокситромицин, азитромицин, спирамицин, мидекамицин). При тяжелом течении пневмонии у госпитализированных больных целесообразно применение парентеральных цефалоспоринов III поколения или фторхинолонов. Клиническая эффективность всех указанных препаратов примерно одинакова, однако при лечении внебольничной пневмонии ни один из этих антибиотиков не может считаться идеальным.
Аминопенициллины характеризуются высокой природной активностью в отношении S. pneumoniae (амоксициллин более высокой, чем ампициллин), однако о проблемах, связанных с возрастающим распространением пенициллинрезистентных пневмококков, упоминалось выше. Имеются данные, что амоксициллин пока сохраняет клиническую эффективность в отношении штаммов пневмококка с промежуточной чувствительностью, а также в отношении устойчивых штаммов. Однако можно предположить снижение клинической эффективности амоксициллина при выделении штаммов пневмококка с высоким уровнем резистентности. Аминопенициллины неэффективны при пневмонии, вызванной S. aureus и K. pneumoniae.
Назначение амоксициллина/клавуланата и цефуроксима аксетила предусмотрено большинством международных и отечественных стандартов лечения внебольничной пневмонии ввиду высокой активности против пневмококков, гемофильной палочки, стафилококков. Однако в отношении пенициллинрезистентных пневмококков мы сталкиваемся с теми же проблемами, что и у аминопенициллинов.
Следует подчеркнуть, что все пенициллины и цефалоспорины неактивны в отношении микоплазм, а также хламидий, и поэтому клинически неэффективны при атипичных пневмониях.
Макролидные антибиотики проявляют высокую природную активность в отношении пневмококков, стафилококков, микоплазм, хламидий и низкую — в отношении гемофильной палочки. Однако в последние годы во всех регионах мира, в том числе и в нашей стране, отмечается неуклонная тенденция повышения устойчивости пневмококков к макролидам. Резистентность пневмококков обычно ассоциируется с неуспехом терапии макролидами. Следует отметить, что новые полусинтетические макролиды не имеют преимуществ перед эритромицином, когда речь идет об устойчивых штаммах пневмококков. В последние годы значение макролидов при внебольничной пневмонии пересматривается. По всей видимости, эти препараты могут быть рекомендованы только в случае нетяжелой пневмонии при подозрении на атипичную этиологию.
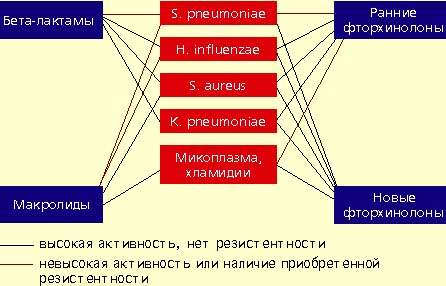 |
| Антимикробная активность бета-лактамов, макролидов и фторхинолонов в отношении наиболее значимых возбудителей внебольничной пневмонии |
Фторхинолоны обладают широким спектром антимикробной активности. Эти препараты проявляют природную активность в отношении практически всех потенциальных возбудителей внебольничной пневмонии. Однако применение ранних фторхинолонов (ципрофлоксацин, офлоксацин, пефлоксацин) при внебольничной пневмонии было ограничено из-за их слабой природной активности в отношении основного возбудителя пневмонии — S. pneumoniae. Значения минимальных подавляющих концентраций (МПК) ранних фторхинолонов в отношении пневмококков составляют от 4 до 8 мкг/мл, а их концентрация в бронхолегочной ткани значительно ниже, что недостаточно для успешной терапии. Описаны случаи, когда терапия фторхинолонами при пневмококковой пневмонии не приносила успеха.
Определенные перспективы лечения внебольничной пневмонии связаны с появлением в последние годы препаратов нового поколения фторхинолонов, которые характеризуются более высокой активностью в отношении S. pneumoniae. Современная классификация фторхинолонов представлена в таблице.
Первым препаратом нового поколения фторхинолонов является левофлоксацин, представляющий собой левовращающий изомер офлоксацина. Левофлоксацин характеризуется более высокой активностью против пневмококков (МПК = 2 мкг/мл) по сравнению с офлоксацином и ципрофлоксацином, причем препарат сохраняет активность и в отношении пенициллинрезистентных штаммов S. pneumoniae. Левофлоксацин — это первый и пока единственный антибактериальный препарат, который официально рекомендован в США для лечения пневмонии, вызванной пенициллинрезистентными пневмококками. Среди новых фторхинолонов только левофлоксацин выпускается в двух лекарственных формах — для приема внутрь и для внутривенного введения. Поэтому левофлоксацин может применяться не только в амбулаторной практике, но и при тяжелых пневмониях у госпитализированных больных. В большом количестве клинических исследований показана высокая эффективность левофлоксацина при внебольничной пневмонии в дозе 500 мг, вводимой однократно в сутки. К несомненным достоинствам левофлоксацина можно отнести его хорошую переносимость.
Вторым препаратом нового поколения фторхинолонов, внедренным в клиническую практику, был спарфлоксацин. Он зарегистрирован в нашей стране и выпускается только в пероральной форме. Однако наряду с доказанной высокой клинической эффективностью следует отметить ряд нежелательных эффектов, отмеченных при его применении. Прежде всего речь идет о существенной фототоксичности спарфлоксацина (т. е. повышенной чувствительности кожи к ультрафиолету); по некоторым данным, частота возникновения этого нежелательного явления составляет более 10%. Фототоксичность характерна для всех препаратов класса фторхинолонов, однако при использовании других препаратов этой группы (например, левофлоксацина, офлоксацина, ципрофлоксацина) это побочное явление возникает гораздо реже. К другим достаточно серьезным нежелательным явлениям, связанным с приемом спарфлоксацина, относится удлинение интервала QT на ЭКГ, что может сопровождаться появлением желудочковых аритмий, иногда опасных для жизни. Клиническое значение этого феномена до конца не ясно, однако известен факт отзыва с рынка препарата этого класса (грепафлоксацина) именно по данной причине. Таким образом, спарфлоксацин, по всей видимости, не может быть рекомендован для рутинного применения в амбулаторной практике при пневмонии, учитывая наличие других, более безопасных препаратов этой группы.
Последним зарегистрированным в нашей стране новым фторхинолоном является моксифлоксацин. Пока он существует только для перорального приема, однако в следующем году ожидается появление в клинической практике парентеральной лекарственной формы. Моксифлоксацин характеризуется очень высокой природной активностью в отношении пневмококков (МПК = 0,25 мкг/мл), в том числе пенициллинрезистентных штаммов, а также более высокой активностью (по сравнению с ранними фторхинолонами) в отношении микоплазм и хламидий. Моксифлоксацин в суточной дозе 400 мг (однократно) показал высокую клиническую эффективность и хорошую переносимость при внебольничной пневмонии. В контролируемых исследованиях не отмечено клинически значимого удлинения интервала QT и существенной фототоксичности.
Ряд перспективных препаратов нового поколения фторхинолонов в настоящее время проходят стадию клинического изучения. В 2001 году ожидается разрешение клинического применения в России еще двух препаратов этой группы — гемифлоксацина и гатифлоксацина.
Антибиотики нового поколения: за и против
Антибиотики – это вещества биологического или полусинтетического происхождения. Применяются в лечебной практике для борьбы с болезнетворными микробами, вирусами. До появления этих медпрепаратов статус неизлечимых болезней был у брюшного тифа, дизентерии, пневмонии, туберкулеза. Сегодня лечение заболеваний инфекционного характера возможно с применением 1-6 поколения антибиотиков.
На этот момент фармакологическая индустрия выпускает более 2000 разновидностей лекарственных средств подобного типа. Медики описали действие около 600 позиций, а во врачебной практике используются порядка 120-160 препаратов.
Важно! При любом заболевании принимать антибиотики рекомендуется после консультации с врачом. В противном случае может развиться антибиотикорезистентность (снижение чувствительности патогенных микроорганизмов к антибактериальным средствам).
Классификация антибиотиков
Все антибактериальные средства можно разделить на 5 категорий по характеристикам и спектру применения. Рассмотрим эту классификацию подробнее:
Спектр действия
Различают антибактериальные средства:
По составу
Антибактериальные препараты делят на 6 групп:
Поколения препаратов. У передовых антимикробных препаратов насчитывается уже шесть генераций. Например, пенициллин был первым средством природного происхождения, тогда как третья или шестая генерация – это уже улучшенная версия, которая включает в состав сильнейшие ингибиторы. Зависимость прямая: чем новее генерация, тем эффективнее воздействие препаратов на патогенную микрофлору.
По способу приема. Пероральные – принимают через рот. Это различные сиропы, таблетки, растворимые капсулы, суспензии. Парентеральные – вводятся внутривенно или внутримышечно. Они быстрее дают эффект, чем пероральные лекарства. Ректальные препараты вводятся в прямую кишку.
Важно! Принимать антибиотики допускается только после консультации с врачом, иначе разовьется антибиотикорезистентность.
Антибактериальные средства нового поколения
Отличие последних генераций антибиотиков от их ранних версий в более совершенной формуле действующего вещества. Активные компоненты точечно устраняют только патологические реакции в клетке. Например, кишечные антибиотики нового поколения не нарушают микрофлору ЖКТ. При этом они борются с целой «армией» возбудителей инфекций.
Новейшие антибактериальные препараты делятся на пять групп:
Рассмотрим несколько известных противомикробных средств импортного и российского производства.
Амоксициллин – импортный противомикробный препарат из группы пенициллинов. Используется во врачебной практике для лечения бактериальной инфекции. Эффективен при кишечных инфекциях, гайморите, ангине, болезни Лайма, дизентерии, сепсисе.
Авелокс – медпрепарат последней генерации из группы фторхинолонов. Отличается сильнейшим воздействием на бактериальные и атипичные возбудители. Не вредит почкам и ЖКТ. Используется при острых, хронических заболеваниях.
Цефалоспорины – антибиотики третьего поколения. К этой группе относят Цефтибутен, Цефтриаксон и другие. Используются для лечения пиелонефрита, пневмонии. В целом это безопасные средства с малым количеством побочных действий. Однако их нужно принимать только после консультации с врачом. Медпрепаратов много, а какой именно выбрать – порекомендует специалист.
Дорипрекс – импортный противомикробный препарат синтетического происхождения. Показал хорошие результаты при лечении пневмонии, запущенных интраабдоминальных инфекций, пиелонефритах.
Инваз – антибактериальное средство из группы карбапенемов. Выпускается в ампулах для парентерального способа применения. Показывает быстрый эффект при лечении бактериальных расстройств кожи, мягких тканей, инфекциях мочевыводящих путей, пневмонии, септицемиях.
Аугметин – полусинтетический пенициллин третьей генерации с добавлением усиливающих ингибиторов. Педиатрами признается лучшим комплексным медпрепаратом для лечения детских гайморита, бронхита, тонзиллита и других инфекций дыхательных путей.
Цефамандол – антибактериальное средство российского производства. Относится к группе цефалоспоринов третьего поколения. Используется для лечения кишечных инфекций, возбудителей инфекций половых органов. Как противомикробное средство обширного диапазона воздействия применяется при простудных заболеваниях.
Лучшие антибактериальные препараты широкого диапазона действия
Противомикробные средства новой генерации обычно синтезируют из природного сырья и стабилизируют в лабораториях. Это помогает усилить эффект лекарства на патогенную микрофлору.
Какие препараты самые сильные? Врачи относят к таким антибактериальные средства широкого спектра воздействия. Приведем ниже краткий список препаратов по названиям:
Резюме
Мы рассмотрели российские и импортные антибиотики широкого спектра действия, кратко описали классификацию препаратов. Ответим на вопрос: какие антибактериальные средства выбрать?
Важно понимать, противомикробные лекарства для обширного применения обладают токсичностью, поэтому негативно влияют на микрофлору. Кроме того, бактерии мутируют, а значит препараты теряют свою эффективность. Поэтому антибактериальные средства с новейшей структурой будут в приоритете, чем их ранние аналоги.
Самолечение антибиотиками опасно для здоровья. При инфекционном заболевании первым делом нужно обратиться к врачу. Специалист установит причину болезни и назначит эффективные антибактериальные средства. Самолечение «наугад» приводит к развитию антибиотикорезистентности.
Таваник какое поколение антибиотиков
Течение и исход пневмоний во многом определяются выбором антибактериального средства для исходной терапии. Для того чтобы антибактериальная терапия (АБТ) была эффективной и рациональной идеальным является назначение в качестве препарата первого ряда антибактериального средства, наиболее активного в отношении возбудителя.
Даже в условиях современного клинического стационара лишь у половины больных пневмонией удается достоверно установить этиологию, причем этиологическая диагностика может длиться до 10–14 дней (максимальные сроки выделения гемокультуры или определение антител в парных сыворотках). В связи с этим почти всегда выбор антибиотика первого ряда осуществляется эмпирически. Врач принимает решение, основываясь на клиническом опыте, знании аллергологического анамнеза, эпидемиологической и клинической ситуации, спектра действия антибиотика.
Трудности диагностики и лечения пневмоний во многом обусловлены тем, что на этапе диагностики врач, зная спектр действия антибиотиков, должен принять практически немедленное решение о препарате первого ряда, не располагая при этом доказательными данными об этиологическом агенте. Оптимальный выбор исходной эмпирической терапии возможен при квалифицированном анализе анамнеза, клинических и рентгенологических данных в сопоставлении с эпидемиологической ситуацией.
Объективной реальностью является возрастание эпидемиологической значимости ранее малоизвестных возбудителей пневмонии, таких как легионелла, микоплазма, хламидия, пневмоцисты, различные вирусы и микобактерии. Серьезной проблемой является приобретенная резистентность к антибиотикам многих микроорганизмов. Наконец к реалиям современной жизни следует отнести увеличение численности лиц, страдающих серьезными хроническими заболеваниями: больных новообразованиями, диабетом, заболеваниями почек и печени, получающих кортикостероиды и иммунодепрессанты; алкоголиков и наркоманов.
Принятие решения о выборе антибактериального препарата
Установление диагноза пневмонии является абсолютным показанием для назначения АБТ. При этом необходимо учитывать следующие факторы:
• достоверность диагноза пневмонии (клинические и рентгенологические данные, оценка лейкоцитарной формулы);
• предположительный этиологический агент (особенности клинических, рентгенологических и лабора-
торных данных, анализ эпидемиологической ситуации);
• аллергологический анамнез;
• адекватность выбора антибактериального препарата и режима лечения;
• определение критериев эффективности антибактериальной терапии.
У лиц молодого возраста без вредных привычек пневмонии обычно вызываются микоплазмой, хламидией, пневмококками. У лиц старше 60 лет более частыми этиологическими агентами являются пневмококки и гемофильные палочки, а нередко ассоциации грамположительных и грамотрицательных микроорганизмов. При предшествующем хроническом бронхите возбудителем пневмонии могут быть гемофильные палочки и моракселла. Те же возбудители характерны и при привычке к курению, которая
Внутрибольничные пневмонии чаще вызываются резистентными штаммами стафилококков, грамотрицательными (нередко полирезистентными) палочками, анаэробами.
Клиническая диагностика пневмоний
Обычно начало заболевания острое, реже постепенное, иногда развитию пневмонии предшествует эпизод острой респираторной вирусной инфекции или трахеобронхит. Клиническая диагностика пневмонии обычно [5] основывается на таких признаках, как повышение температуры до фебрильных и субфебрильных цифр, кашель (чаще с отделением мокроты). У части больных отмечаются озноб, боль в груди, одышка. При долевых пневмониях выявляют признаки консолидации легочной ткани – укорочение перкуторного звука, бронхиальное дыхание, усиление голосового дрожания. Характерен феномен крепитации, хотя наиболее часто при аускультации выявляются локальные мелкопузырчатые хрипы.
Пневмонии тяжелого течения характеризуют следующие клинические признаки [3–5]:
• двусторонняя, многодолевая локализация или абсцедирование;
• быстрое прогрессирование процесса (увеличение зоны инфильтрации на 50 % и более за 48 часов наблюдения);
• тяжелая дыхательная недостаточность;
• тяжелая сосудистая недостаточность, требующая применения прессорных аминов;
• лейкопения менее 4 или гиперлейкоцитоз более 20 × 1000/мкл с числом незрелых нейтрофилов
более 10 %;
• олигурия или проявления острой почечной недостаточности.
При тяжелом течении пневмонии нередко диагностируют такие жизненно опасные проявления, как инфекционно-токсический шок, дистресс-синдром, ДВС-синдром, полиорганная недостаточность. Тяжелое течение пневмонии констатируют при наличии 2–3 и более из перечисленных признаков.
У лиц пожилого и старческого возраста может не быть классических проявлений пневмонии, возможны лихорадка, гипотермия, спутанность сознания, одышка (или сочетание этих симптомов).
При осмотре больного следует внимательно фиксировать опасные симптомы: одышку, гипотонию, олигурию, тяжелые брадикардию/тахикардию, спутанность сознания. Из возможных осложнений наиболее часто встречается плеврит, реже – абсцедирование. Однако не следует забывать и о
более редких и тяжелых осложнениях: менингите, абсцессе мозга, артрите, перикардите, эндокардите, перитоните, эмпиеме плевры.
Для пневмоний микоплазменной природы характерны признаки фаринго-ларинго-трахеобронхита в начале заболевания, миалгии, обильная потливость (даже при невысоком субфебрилитете), навязчивый сухой “коклюшеподобный” кашель необычно низкого тембра (проявления трахеобронхиальной дискинезии). Те же особенности (кроме миалгий и обильного потоотделения) часты при хламидийных пневмониях.
Доказательные критерии диагноза
Доказательным является рентгенологическое исследование [5], при котором выявленная патология может быть характерной для тех или иных возбудителей. Инфильтративные изменения могут быть долевыми и многодолевыми, что характерно для бактериальных пневмоний (в т. ч. для пневмококковых, легионеллезных, вызванных анаэробами, грибами) и микобактериозов, включая туберкулез легких. Диффузные двусторонние инфильтрации типичны для таких возбудителей, как вирус гриппа, пневмококк, стафилококк, легионелла. Очаговая и многоочаговая инфильтрация может быть гомогенной (пневмококк, легионелла) или негомогенной (стафилококк, вирусы, микоплазма). Сочетание инфильтративных и интерстициальных изменений типично для пневмоний вирусной, микоплазменной и пневмоцистной природы. Интерстициальные изменения могут быть милиарными (микобактерия туберкулеза, сальмонелла, грибы) или сетчатыми (вирусы, пневмоцисты, микоплазма, хламидия). Сочетание инфильтративных или интерстициальных изменений на фоне лимфоаденопатии достаточно типично для туберкулеза легких и пневмоний, вызванных грибами, микоплазмой, хламидиями, вирусами кори и ветряной оспы. Наконец при пневмониях рентгенологические изменения могут отсутствовать. Это бывает в самом начале болезни, при дегидратации, тяжелой нейтропении, а также при пневмоцистной этиологии заболевания.
Рентгенография легких выявляет такие осложнения, как абсцедирование, экссудативный плеврит.Компьютерная томография легких оправданна лишь при проведении дифференциальной диагностики, если обычная рентгенограмма малоинформативна, а также для более точной оценки возможных осложнений. Компьютерная томография позволяет выявлять ранние инфильтративные и интерстициальные изменения в тех случаях, когда стандартная рентгенография еще не демонстративна. Четко определяются полости, лимфоаденопатии, плевральный выпот и многоочаговые изменения.
При исследовании лейкоцитарной формулы типичны лейкоцитоз более 10 × 1000/мкл, сдвиг лейкоцитарной формулы влево (более 10 % палочкоядерных нейтрофилов), токсическая зернистость нейтрофилов. При т. н. атипичных пневмониях (микоплазменных и хламидийных) лейкоцитарная формула нередко не изменена, обычно наблюдается умеренный лейкоцитоз без нейтрофилеза.
Для установления возбудителя традиционно проводят бактериологическое исследование мокроты. Количественная оценка микрофлоры считается необходимой, т. к. диагностически значимыми являются концентрации более 1 млн микробных тел в 1 мл мокроты. Наиболее убедительны данные посевов мокроты, полученной до начала лечения, пока результаты бактериологического исследования не искажены предшествующей АБТ.
Определение чувствительности микрофлоры, выделенной из мокроты (крови, плевральной жидкости), к антибиотикам может быть хорошим подспорьем клиницисту, особенно в случаях, когда исходная терапия оказалась неэффективной. Для этиологической расшифровки хламидийных, микоплазменных, легионеллезных пневмоний обычно применяют серотипирование. Специфические антитела к этим возбудителям определяют с помощью реакции непрямой иммунофлюоресценции (РНИФ) или более современных методик – теста ELISA (антитела классов IgM и IgG к микоплазме и хламидиям) и определения антигена в моче (легионелла).
Следует отметить, что ныне действующая классификация пневмоний привела врачей к упрощенным диагнозам типа “внебольничная пневмония”, “домашняя пневмония” и т. д. Следует учитывать, что такие диагнозы не соответствуют Международной классификации болезней 10-го пересмотра, по которой ведется статистический учет. Правомочно требование Росздравнадзора о статистической шифровке пневмоний по этиологическому принципу.
Антибактериальная химиотерапия
При установлении диагноза пневмонии практический врач должен сразу же определить программу АБТ, что означает выбор антибиотика первого ряда, его суточной дозы, способа применения и кратности введения препарата. В последующие дни решаются вопросы о целесообразности коррекции АБТ и оптимальных сроках ее применения. Немаловажно, что в нашей стране разрешено медицинское применение многочисленных генериков. Так, например, в США разрешено применение бренда ципрофлоксацина и трех генериков. В Российской Федерации (РФ) кроме бренда разрешено медицинское применение более 60 генериков ципрофлоксацина. Брендом является защищенный патентом препарат, разработанный и произведенный компанией. Бренды проходят тщательную клиническую апробацию, их применение разрешается только после успешного доказательства высокой эффективности и хорошей переносимости препарата. Бренды, естественно, дороже генериков, которые разрешаются к медицинскому применению без проведения клинической апробации. Стоимость генериков значительно ниже, иногда за счет использования более дешевых наполнителей. В некоторых научных исследованиях, сравнивающих бренды и генерики, доказано, что эффективность и переносимость антибиотиков-брендов лучше.
В нашей стране основную часть больных пневмониями госпитализируют. Отечественные формуляры лечения пневмонии во многом соответствуют международным, предусматривающим лечение пневмоний как на дому, так и в условиях стационара. Оптимальное антибактериальное лечение подразумевает правильный выбор антибиотика, его дозировок и продолжительности лечения. Федеральным стандартом терапии пневмоний предусмотрено лечение в течение 7 дней. Это приемлемо для неосложненных пневмоний легкой и средней тяжести течения. Существенно, что терапия должна быть пролонгирована не только при абсцедировании или развитии эмпиемы плевры, но и в зависимости от этиологических агентов. Так, при микоплазменных и хламидийных пневмониях длительность антибактериальной терапии составляет 14 дней, а при легионеллезных – до 21 дня. Во всех формулярах для лечения пневмоний в качестве важного антибактериального средства приводятся т. н. респираторные фторхинолоны: левофлоксацин (Таваник) и моксифлоксацин.
Таваник (бренд левофлоксацина) хорошо подавляет грамположительные микроорганизмы: стрептококки, пневмококки, стафилококки, листерии, коринебактерии и в меньшей степени – энтерококки. Он обладает высокой активностью в отношении большинства грамотрицательных бактерий – гемофильной палочки, моракселлы, ацинетобактера, энтеробактера, цитробактера и несколько меньшей – в отношении синегнойной и кишечной палочек, клебсиеллы. Левофлоксацин высокоактивен в отношении легионеллы, микоплазмы и хламидий, он также подавляет микобактерии туберкулеза и некоторые анаэробы.
Левофлоксацин хорошо всасывается и характеризуется высокой биодоступностью (до 99 %). При этом создаются высокие концентрации препарата в слизистой оболочке бронхов, альвеолярных макрофагах, легочной паренхиме, превышающие таковые в сыворотке крови. Существенно, что особенности фармакокинетики позволяют применять левофлоксацин 1 раз в сутки (что обусловливает хорошую приверженность терапии) в дозе 500 мг. Левофлоксацин обычно хорошо переносится [1–4]. Препарату в меньшей степени, чем другим фторхинолонам, свойственны гепато- и фототоксичность, удлинение QT-интервала на электрокардиограмме. Препарат не следует назначать лицам с аллергией к любым хинолонам, а также детям, беременным и кормящим матерям.
Широкий спектр антибактериальной активности, высокая биодоступность, особенности фармакокинетики и распределения в органах дыхания, хорошая переносимость определяют возможность использования левофлоксацина в качестве препарата первого ряда при лечении внебольничных пневмоний (уровень доказательности А) [6, 7]. Доказана его высокая эффективность при инфекциях респираторного тракта, внебольничных и госпитальных пневмониях, инфекциях мочевыводящих путей. Таваник разрешен к медицинскому применению в РФ в двух лекарственных формах: таблетках по 500 и 250 мг для перорального приема и растворе для внутривенного введения во флаконах по 100 мл, содержащих 500 мг препарата. Перорально Таваник принимают до еды или в интервале между приемами пищи. Внутривенная инфузия препарата должна быть продолжительной (не менее 60 минут). Во время лечения Таваником следует избегать инсоляции и ультрафиолетового облучения. При развитии тендинита левофлоксацин немедленно отменяют. В стационаре для лечения внебольничных пневмоний, особенно тяжелых и при подозрении на возможность инфицирования внутриклеточными агентами, назначают β-лактамные антибиотики в сочетании с макролидами [1–4]. Также вместо комбинации двух антибактериальных средств возможна монотерапия респираторными фторхинолонами (левофлоксацином, моксифлоксацином).
В случае тяжелого течения пневмонии антибиотики необходимо применять внутривенно в возможно более ранние сроки (немедленная АБТ подразумевает первое введение антибиотика в пределах двух часов с момента установления диагноза).
В отделении пульмонологии ФГУ “Центральная клиническая больница с поликлиникой” УД Президента РФ из числа респираторных фторхинолонов широко применяется Таваник, который за последние годы использовался для лечения более 400 больных пневмонией.
Основные критерии для решения о назначении Таваника пациентам с диагностированной внебольничной пневмонией среднетяжелого и тяжелого течения:
• поздняя диагностика пневмонии (на 5–10-й день от начала заболевания) без догоспитальной антибактериальной терапии;
• безуспешное применение β-лактамных антибиотиков (в эффективных дозах) на догоспитальном этапе.
Другими основаниями для назначения Таваника были:
• долевые и многодолевые пневмонии у пациентов с аллергией к β-лактамным антибиотикам;
• пневмонии в эпидемиологических очагах (вспышки респираторных инфекций в семье или в коллективе).
• в отсутствие эффекта от первоначальной АБТ цефалоспоринами 3-го поколения в сочетании с макролидами.
Естественно, в условиях пульмонологического отделения применение Таваника начиналось с внутривенных инфузий по 500 мг один раз в сутки. При долевых и многодолевых пневмониях в первые сутки лечения суточная доза составляла 1000 мг, что позволяло получать отчетливый клинический эффект уже в течение 24 часов. В последующие дни применяли обычные дозировки препарата – 500 мг каждые 24 часа внутривенно. При тяжелом течении или у лиц с резецированным желудком препарат применялся только внутривенно. Средняя продолжительность лечения составляла 10–12 дней. Стремление обеспечить высокую эффективность лечения при уменьшении его стоимости и сокращении числа инъекций оправдало широкое применение в отделении программ ступенчатой (stepdown) терапии, внедренной в практику работы отделения с 1994 г. При использовании этой методики лечение начинается с парентерального применения антибиотика. При достижении клинического эффекта, через 2–3 дня от начала терапии, внутривенное применение препарата заменяется пероральным приемом антибиотика. Средняя продолжительность лечения при ступенчатой терапии составляла 10 дней. Такая терапия легче переносится пациентами и реже сопровождается побочными эффектами.
Анализ показал, что наиболее широко применявшаяся схема ступенчатой монотерапии левофлоксацином по 500 мг внутривенно каждые 24 часа в течение 2–3 суток с последующим переходом на пероральный прием по 500 мг каждые 24 часа оказалась эффективной при лечении внебольничных пневмоний среднетяжелого течения у большинства больных. Исходная суточная дозировка 1000 мг применялась ограниченно – примерно у 10 % наиболее тяжелых больных. Побочные эффекты со стороны желудочно-кишечного тракта, отмеченные у нескольких обследованных (ранее лечившихся по поводу хронического колита), были кратковременными и регрессировали после применения эубиотиков, спазмолитиков и завершения терапии респираторным фторхинолоном.
В течение последних четырех лет было необычно много больных многодолевыми пневмониями с крайне тяжелым септическим течением, нуждающихся в интенсивной терапии с использованием искусственной вентиляции легких (ИВЛ). Практически во всех подобных клинических ситуациях мы использовали сочетанную АБТ, состоявшую из Таваника 500 мг внутривенно каждые 24 часа и меропенема по 1000 мг внутривенно каждые 8 часов. Эта терапия была достаточно эффективной, о чем свидетельствовало выздоровление пациентов пожилого возраста, находившихся на ИВЛ в течение 52 и 74 суток.
Несколько лет назад было проведено многоцентровое международное исследование, в котором Таваник использовали для лечения внутрибольничных пневмоний в дозировке 750 мг внутривенно один раз в сутки. По результатам этого исследования высокие дозы Таваника эффективны и при лечении внутрибольничных пневмоний.
Заключение
Таким образом, Таваник является препаратом выбора для лечения пневмоний. Препарат проявляет высокую активность в отношении большинства микроорганизмов, вызывающих инфекции нижних отделов дыхательных путей. При пневмониях тяжелого течения Таваник должен применяться внутривенно. С позиций фармакоэкономики оптимальной представляется ступенчатая монотерапия Таваником. Перорально применение Таваника возможно при пневмониях легкой и средней тяжести течения. Высокая эффективность и хорошая переносимость препарата обеспечивают отличные результаты при лечении пневмоний.
Литература
1. Практическое руководство по антиинфекционной химиотерапии / Под ред. Л.С. Страчунского, Ю.Б. Белоусова, С.Н. Козлова. Смоленск, 2007. C. 464.
2. Справочник лекарственных средств формулярного комитета / Под ред. П.А. Воробьева. М., 2010. C. 536.
3. Бартлетт Д. Антимикробная химиотерапия. М., 2007. C. 440.
4. Гилберт Д, Моллеринг Р-младший, Элиопулос Д и др. Сэнфордский справочник – антимикробная терапия. М., 2009. С. 288.
5. Zackon H. Pulmonary Differential Diagnosis. 2000;885.


